HEMOGLOBINA Y MIOGLOBINA PROTEINAS GLOBULARES HEMOGLOBINA Y MIOGLOBINA

HEMOGLOBINA Y MIOGLOBINA PROTEINAS GLOBULARES
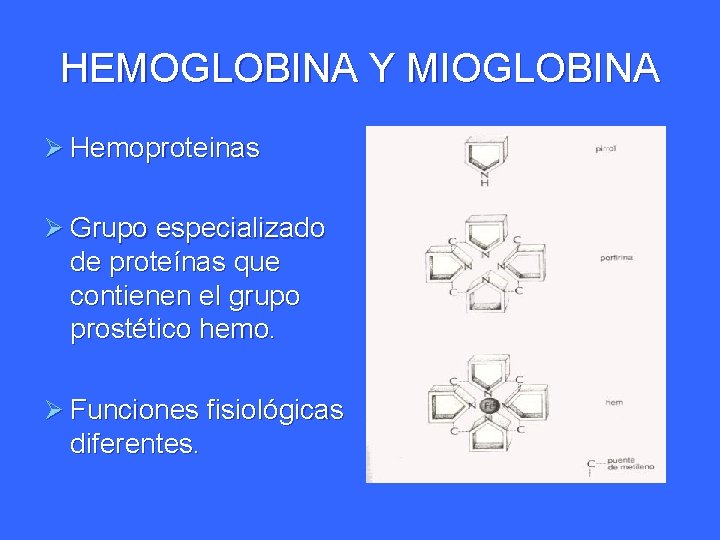
HEMOGLOBINA Y MIOGLOBINA Ø Hemoproteinas Ø Grupo especializado de proteínas que contienen el grupo prostético hemo. Ø Funciones fisiológicas diferentes.
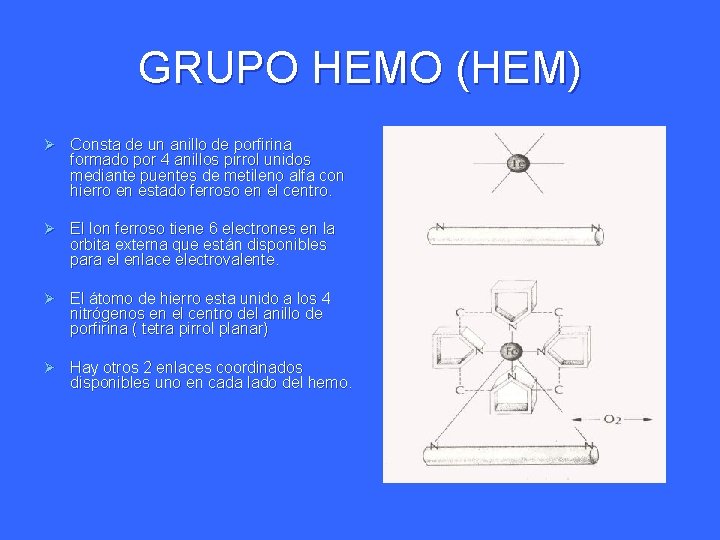
GRUPO HEMO (HEM) Ø Consta de un anillo de porfirina formado por 4 anillos pirrol unidos mediante puentes de metileno alfa con hierro en estado ferroso en el centro. Ø El Ion ferroso tiene 6 electrones en la orbita externa que están disponibles para el enlace electrovalente. Ø El átomo de hierro esta unido a los 4 nitrógenos en el centro del anillo de porfirina ( tetra pirrol planar) Ø Hay otros 2 enlaces coordinados disponibles uno en cada lado del hemo.
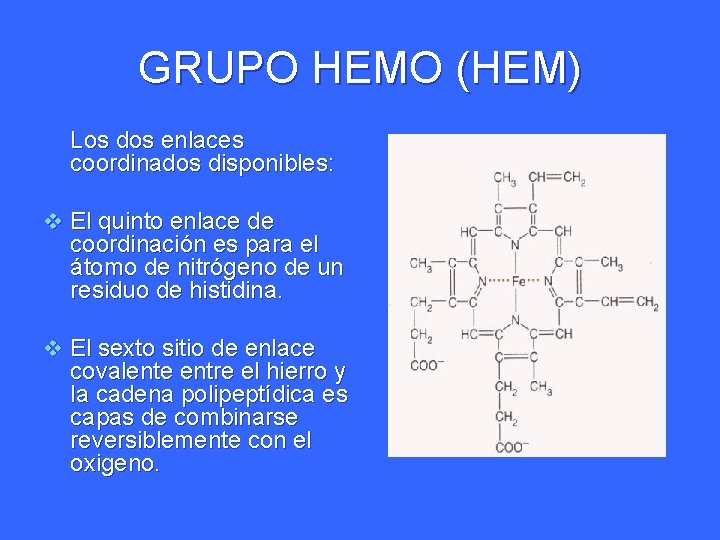
GRUPO HEMO (HEM) Los dos enlaces coordinados disponibles: v El quinto enlace de coordinación es para el átomo de nitrógeno de un residuo de histidina. v El sexto sitio de enlace covalente entre el hierro y la cadena polipeptídica es capas de combinarse reversiblemente con el oxigeno.

HEM v Todos los aminoácidos que interactúan con el hem son apolares. v La quinta posición de coordinación del hierro se une a un anillo de histidina ( histidina proximal ) v La sexta posición (histidina distal) estabiliza el lugar de unión del O 2.

MIOGLOBINA v Concentración elevada en el músculo esquelético y cardiaco ( color rojizo) v El O 2 almacenado se libera durante la falta de O 2, útil en mitocondrias ( síntesis aeróbicas de ATP v Componente proteico globina: Cadena única polipeptídica. 8 secciones de hélice alfa (A-H). Forma hendidura que sierra casi completo al grupo hem. v El hemo libre afinidad elevada por el O 2 se oxida de forma irreversible para formar hematina (Fe 3+).

HEMOGLOBINA v Molécula esférica en los eritrocitos v Transporta O 2 desde los pulmones a los tejidos del cuerpo. v Cuatro moléculas de hem y una molécula de globina forman una molécula. v La globina contiene 4 sub. unidades denominadas alfa y beta ( 4 cadenas polipeptídicas). v Cada sub. unidad contiene un grupo hem que se une reversiblemente con el O 2. v Una molécula se combina de modo reversible con 4 moléculas de O 2

HEMOGLOBINA v A. B. Hemoglobina del adulto (Hb. A): Hb. A: dos cadenas alfa dos cadenas beta Hb. A 2: dos cadenas delta (2%) dos cadenas alfa Hemoglobina fetal (Hb. F): Hb. E (vida embrionaria): dos cadenas epsilon. dos cadenas alfa. Hb. F: dos cadenas gamma dos cadenas alfa
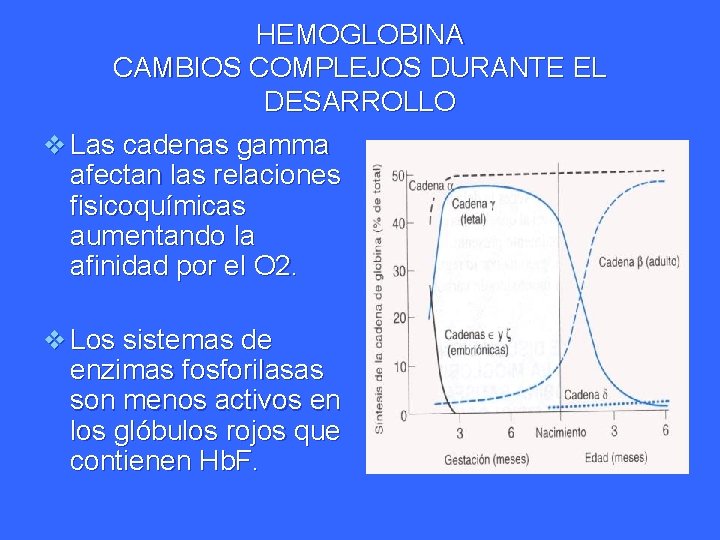
HEMOGLOBINA CAMBIOS COMPLEJOS DURANTE EL DESARROLLO v Las cadenas gamma afectan las relaciones fisicoquímicas aumentando la afinidad por el O 2. v Los sistemas de enzimas fosforilasas son menos activos en los glóbulos rojos que contienen Hb. F.
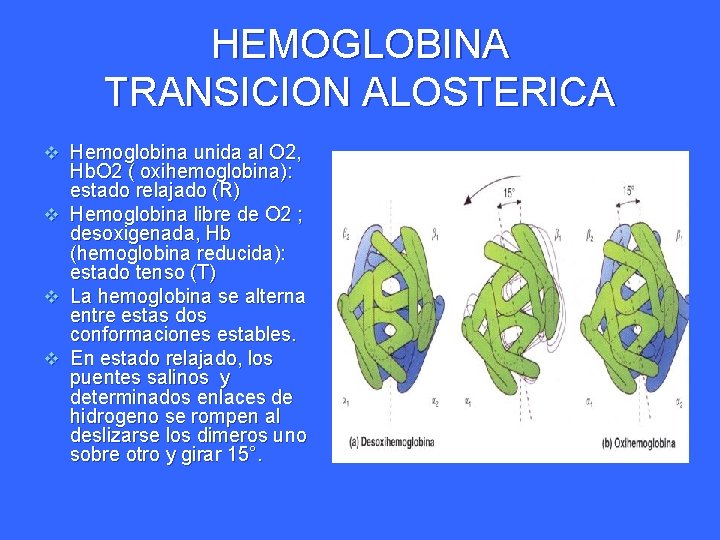
HEMOGLOBINA TRANSICION ALOSTERICA v Hemoglobina unida al O 2, Hb. O 2 ( oxihemoglobina): estado relajado (R) v Hemoglobina libre de O 2 ; desoxigenada, Hb (hemoglobina reducida): estado tenso (T) v La hemoglobina se alterna entre estas dos conformaciones estables. v En estado relajado, los puentes salinos y determinados enlaces de hidrogeno se rompen al deslizarse los dimeros uno sobre otro y girar 15°.
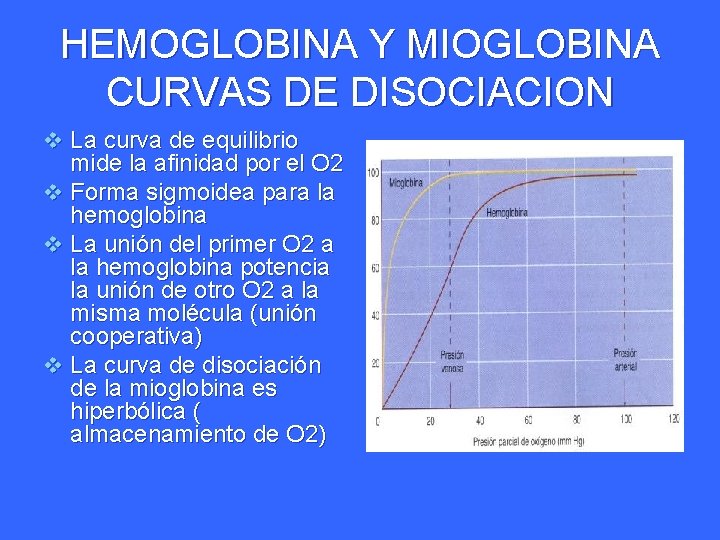
HEMOGLOBINA Y MIOGLOBINA CURVAS DE DISOCIACION v La curva de equilibrio mide la afinidad por el O 2 v Forma sigmoidea para la hemoglobina v La unión del primer O 2 a la hemoglobina potencia la unión de otro O 2 a la misma molécula (unión cooperativa) v La curva de disociación de la mioglobina es hiperbólica ( almacenamiento de O 2)
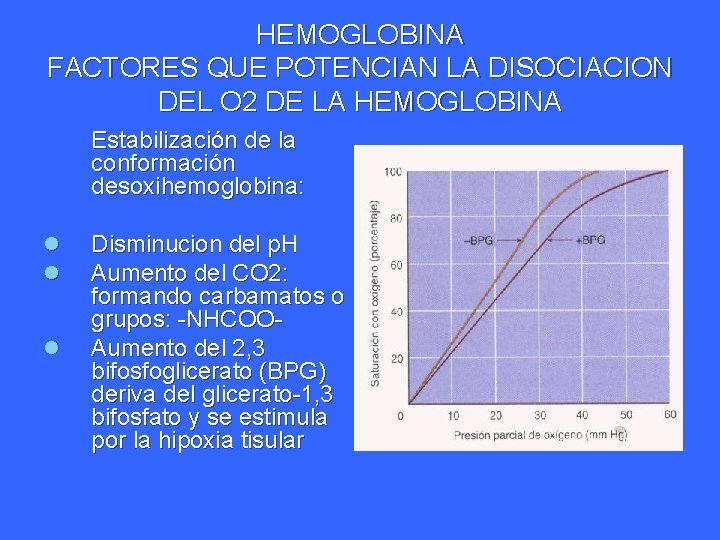
HEMOGLOBINA FACTORES QUE POTENCIAN LA DISOCIACION DEL O 2 DE LA HEMOGLOBINA Estabilización de la conformación desoxihemoglobina: l l l Disminucion del p. H Aumento del CO 2: formando carbamatos o grupos: -NHCOOAumento del 2, 3 bifosfoglicerato (BPG) deriva del glicerato-1, 3 bifosfato y se estimula por la hipoxia tisular
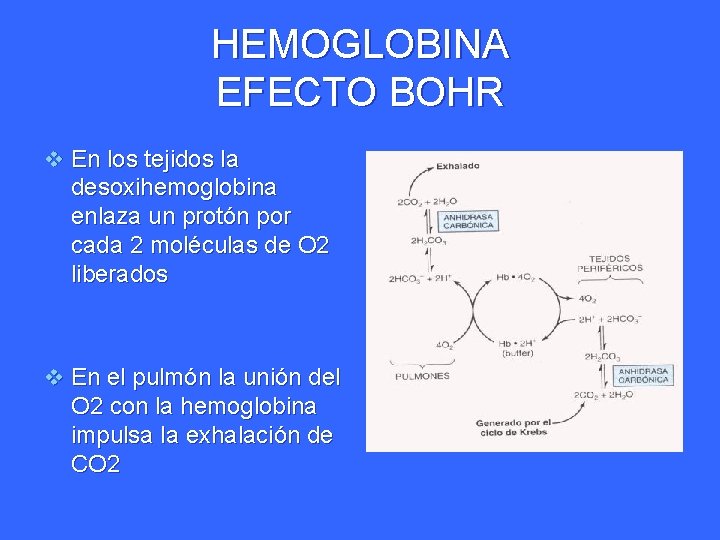
HEMOGLOBINA EFECTO BOHR v En los tejidos la desoxihemoglobina enlaza un protón por cada 2 moléculas de O 2 liberados v En el pulmón la unión del O 2 con la hemoglobina impulsa la exhalación de CO 2
HEMOGLOBINA TRANSPORTE DE CO 2 1. Carbamatos: CO 2+Hb-NH 3+ = 2 H+Hb-NH-COO 2. Bicarbonato: CO 2+H 2 O === H 2 CO 3 === HCO 3 -+H+

1. • • • HEMOGLOBINAS MUTANTES HEMOGLOBINOPATIAS Metahemoglobina El hierro hemo es ferrico No puede enlazar ni transportar O 2 Surge por la oxidación del FE 2+ a FE 3+ (sulfonamidas , hemoglobina M hereditaria, actividad reducida de la reductasa de metahemoglobina) 2. • • • Hemoglobina M La histidina es sustituida por la tirosina El equilibrio R- T favorece el estado T Esta reducida la afinidad por el oxigeno 3. • • Hemoglobina S El aminoácido no polar valina ha sustituido residuo superficial polar Glu 6 de la subunidad beta formando un parche adhesivo A Pa. O 2 bajas , la desoxi. HBS puede polimerizarse en fibras insolubles largas Forma de hoz característico del eritrocito Vulnerable a la lisis en el bazo 4. • • • Talasemias Resultan de la ausencia parcial o total de una o mas cadenas alfa o beta Mas de 750 mutaciones distintas Comunes ; talasemias alfa , talasemias beta ,
- Slides: 15