HEMOGLOBINA MIOGLOBINA Describir funciones no cataliticas de las

HEMOGLOBINA MIOGLOBINA

�Describir funciones no cataliticas de las proteinas de las �Comprender el funcionamiento proteinas con union reversible a ligandos (Hb y Mb)

Las funciones de muchas proteinas involucran la union reversible con otras moleculas. Ligando: Cualquier molecula unida reversiblemente a una proteina

Un ligando puede ser cualquier tipo de molecula incluyendo otra proteina. Permiten a un organismo responder rapida y reversiblemente a circunstancias metabolicas y ambientales cambiantes.

Sitio de union: Una misma proteina puede tener varios sitios de union para diferentes ligandos. Estas interacciones moleculares especificas son cruciales para el mantenimiento del alto grado de orden necesario en un sistema vivo

Hemoglobina y Mioglobina, Proteinas captadoras de Oxigeno y CO 2.

�Ambas son miembros de una familia de proteínas denominadas colectivamente globinas (Globulares) �Estas desempeñan funciones especiales en uno de los aspectos mas importantes del metabolismo animal: la adquisición y utilización del oxigeno.
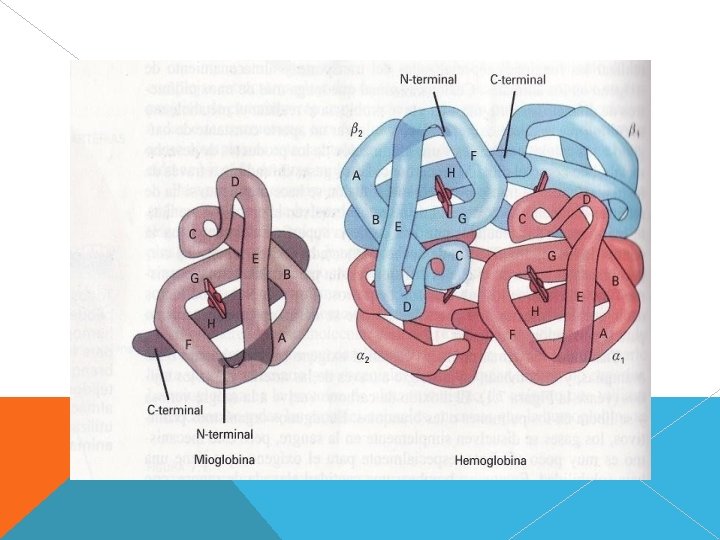
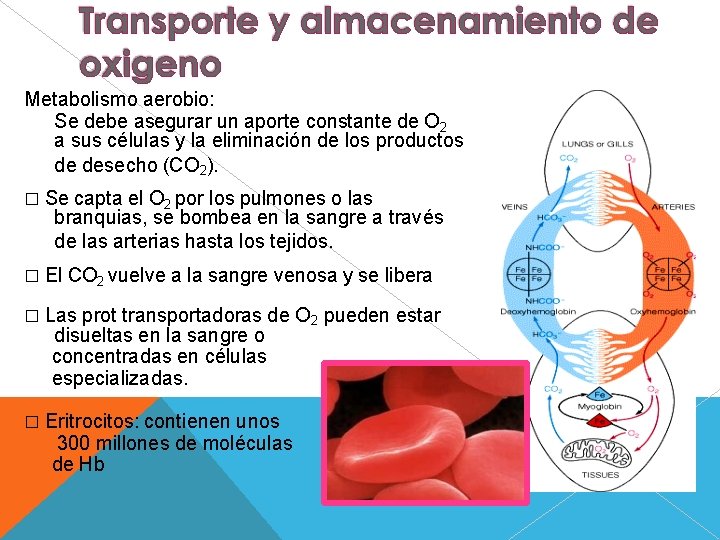
Metabolismo aerobio: Se debe asegurar un aporte constante de O 2 a sus células y la eliminación de los productos de desecho (CO 2). � Se capta el O 2 por los pulmones o las branquias, se bombea en la sangre a través de las arterias hasta los tejidos. � El CO 2 vuelve a la sangre venosa y se libera � Las prot transportadoras de O 2 pueden estar disueltas en la sangre o concentradas en células especializadas. � Eritrocitos: contienen unos 300 millones de moléculas de Hb

Algunos tejidos, como el musculo (mm) necesitan reservas de oxigeno elevadas durante periodos de altas demandas energeticas. � � La Mb es utilizada para almacenar este oxigeno en musculo En la Mb una sola cadena polipeptídica se pliega sobre un grupo prostetico (HEMO), que contiene el lugar de unión del oxigeno.
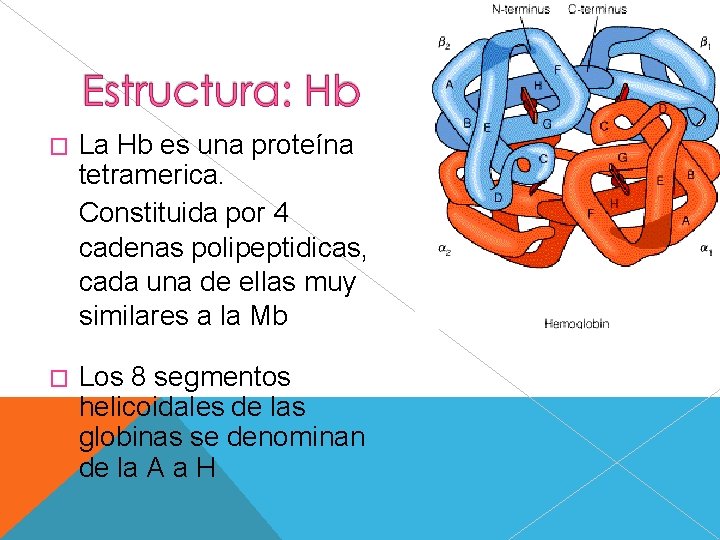
� La Hb es una proteína tetramerica. Constituida por 4 cadenas polipeptidicas, cada una de ellas muy similares a la Mb � Los 8 segmentos helicoidales de las globinas se denominan de la A a H

Un quelante, se une con iones de metales pesados �El hierro esta quelado por un sistema de anillo tetrapirrolico: protoporfirina IX. � Las porfirinas son intensamente coloreadas: de ahí se explica el color rojo intenso de la sangre � HEMO: es el complejo formado por la protoporfirina IX con el Fe (II). Fe: Esta unido de forma no covalente en una hendidura hidrófoba en la molécula de Mb o de Hb
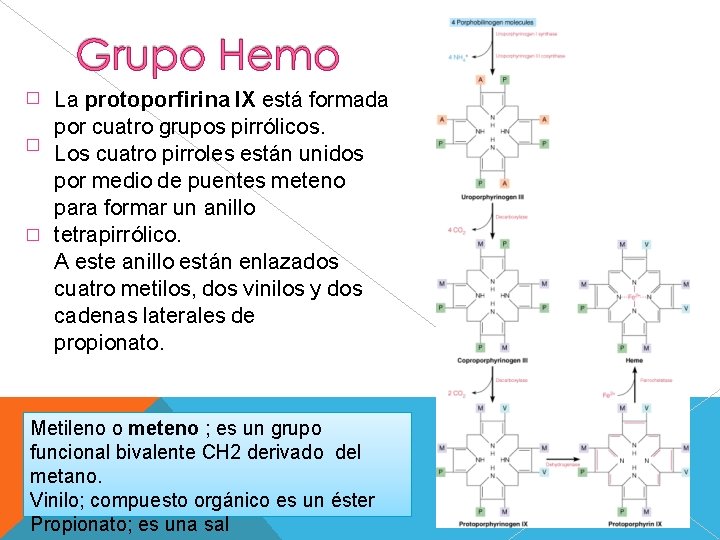
� � � La protoporfirina IX está formada por cuatro grupos pirrólicos. Los cuatro pirroles están unidos por medio de puentes meteno para formar un anillo tetrapirrólico. A este anillo están enlazados cuatro metilos, dos vinilos y dos cadenas laterales de propionato. Metileno o meteno ; es un grupo funcional bivalente CH 2 derivado del metano. Vinilo; compuesto orgánico es un éster Propionato; es una sal

� � Fuera del ambiente celular el hierro se oxida lentamente formando lo que se denomina metamioglobina. Cuando se produce esta oxidación el lugar de unión se inactiva. La protección de un metal que une oxigeno frente a la oxidación irreversible es la razón fundamental de la existencia de la mioglobina y la hemoglobina. El hemo esta adaptado para contener una molécula de O 2, también acepta algunas otras moléculas pequeñas.

La mas importante de ellas desde el punto de vista fisiológico es el monóxido de carbono. El CO se fija a la mioglobina y a la hemoglobina con mucha mayor afinidad que el oxigeno. El CO es un gas muy toxico ocupa los lugares de unión del oxigeno y bloquea la respiración.
![En los pulmones: � La [O 2 ] elevada de favorece la oxigenación �Forma En los pulmones: � La [O 2 ] elevada de favorece la oxigenación �Forma](http://slidetodoc.com/presentation_image/02e43998a672d4b162702c603bf901fb/image-16.jpg)
En los pulmones: � La [O 2 ] elevada de favorece la oxigenación �Forma OXI de la molécula �Por tanto, se reduce la estabilidad de los Nterminales carbamados y se expulsa CO 2. En la circulación arterial, en capilares: � p. H menor �Elevado [CO 2] �Forma DESOXI �Facilita la liberación de O 2 y la unión de CO 2.

Formas Fisiológicas de la Hemoglobina Desoxihemoglobina (estado T): hemoglobina descargada de oxígeno. Oxihemoglobina (estado R): Representa la hemoglobina que se encuentra unida al oxígeno normalmente ( Hb+O 2) dando el aspecto rojo o escarlata intenso característico de la sangre arterial.

Carboxihemoglobina: Hemoglobina resultante de la unión con el CO 2, este presenta una afinidad 200 veces mayor que el Oxígeno por la Hb desplazándolo fácilmente. Carbaminohemoglobina: Se refiere a la hemoglobina unida al CO. Hemoglobina glucosilada: resulta de la unión de la Hb con carbohidratos libres unidos a cadenas carbonadas con funciones ácidas en el carbono 3 y 4.

Metahemoglobinemia: Metahemoglobina: Hemoglobina con grupo hemo con hierro en estado fèrrico, Fe (III). Una clase de variantes denominadas hemoglobinas M tienden a oxidase con facilidad para dar metahemoglobina, que no puede unirse al oxigeno. Los individuos que portan esta mutación presentan dificultades par el transporte de oxigeno suficiente a los tejidos.
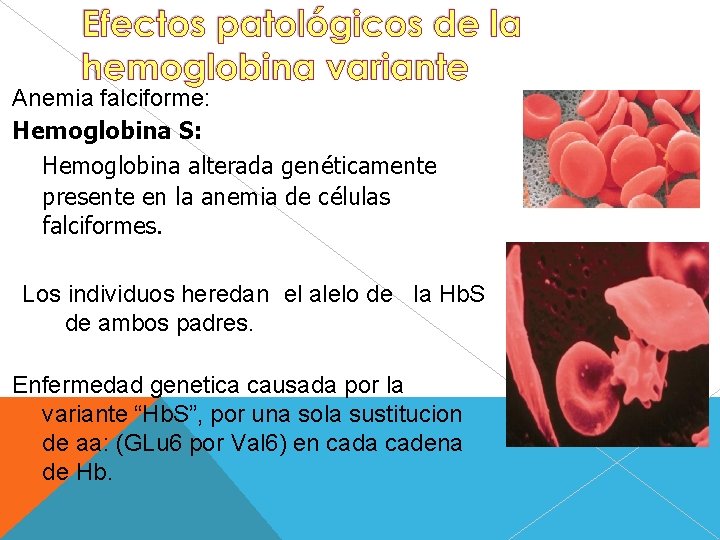
Anemia falciforme: Hemoglobina S: Hemoglobina alterada genéticamente presente en la anemia de células falciformes. Los individuos heredan el alelo de la Hb. S de ambos padres. Enfermedad genetica causada por la variante “Hb. S”, por una sola sustitucion de aa: (GLu 6 por Val 6) en cada cadena de Hb.
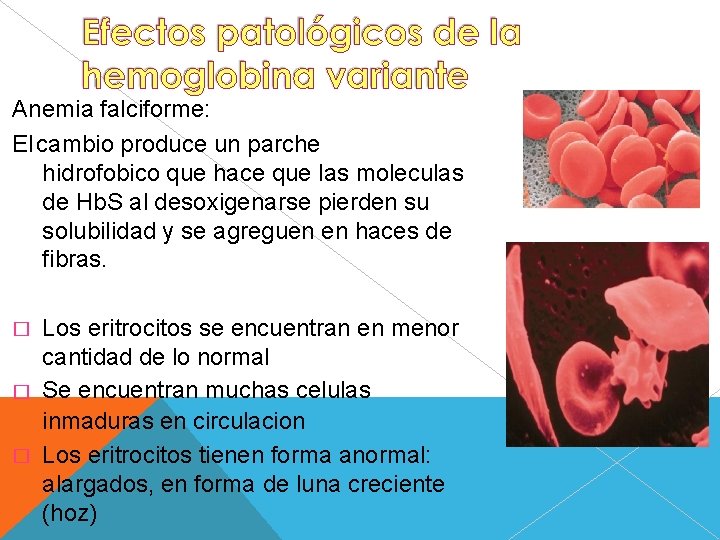
Anemia falciforme: El cambio produce un parche hidrofobico que hace que las moleculas de Hb. S al desoxigenarse pierden su solubilidad y se agreguen en haces de fibras. � � � Los eritrocitos se encuentran en menor cantidad de lo normal Se encuentran muchas celulas inmaduras en circulacion Los eritrocitos tienen forma anormal: alargados, en forma de luna creciente (hoz)

ά talasemia: las talasemias que afectan la cadena alfa presentan una situación más complicada. Hay dos copias del gen (ά 1 ά 2 ) una junta a la otra en el cromosoma humano sus cadenas ά 1 ά 2 difieren en un tan solo aminoácido.

Los individuos afectados por el trastorno nacen invariablemente muertos ya que solamente pueden formar la hemoglobina γ 4 y puesto que la producción de estas cadenas disminuye al aproximarse al momento del nacimiento no disponen de la hemoglobina suficiente para mantener laconcentracion necesaria de Hb fetal.

- Slides: 24