HEMOGLOBINA Es el principal componente de los eritrocitos

HEMOGLOBINA • Es el principal componente de los eritrocitos. • Es la proteína responsable del transporte eficaz de los gases O 2 y CO 2 • La concentración de Hemoglobina se define como la cantidad del pigmento presente en 100 ml de sangre. • Valor de referencia es: - en el hombre: 15. 4 gr% - en la mujer: 13. 8 gr% • A concentraciones normales de Hb, el total del volumen sanguíneo transporta 210 ml de O 2, es decir que cada gramo de Hb es capaz de transportar 1. 34 ml de O 2. • Sus variaciones fisiológicas concuerdan más o menos con las descriptas para el número de eritocitos.

ESTRUCTURA DE LA HEMOGLOBINA • Estructura común a todos los mamíferos. • Lugar de síntesis: eritrocitos. • Es una proteína conjugada oligomérica constituida por 4 subunidades. • PM aproximado: 68. 000. • Formada por dos componentes: 1. Grupo HEMO: derivado porfirínico que contiene el átomo de Fe indispensable para el transporte de O 2, constituye el núcleo prostético. 2. GLOBINA: proteína conjugada oligomérica formada por 4 subunidades, cada unida a un grupo HEMO.

COMPONENTES DE LA HEMOGLOBINA 1. GRUPO HEMO: es un derivado porfirínico que contiene un átomo de Fe (elemento clave en el transporte de O 2). Este grupo constituye el núcleo prostético (porción no proteica sin la cual la proteína no tendría actividad) 2. GLOBINA: proteína conjugada oligomérica constituida por 4 subunidades, cada subunidad contiene un grupo HEMO unida a la cadena polipeptídica.

CARACTERÍSTICAS DEL GRUPO HEMO: • Constituye el 4% de la molécula de Hemoglobina. • Es una estructura heterocíclica llamada protoporfirina IX (por ser la 9º de una serie de estructuras isoméricas) • Contiene un átomo de Fe ligado por uniones covalentes a sus átomos de N centrales, es decir que es una metalo-porfirina o ferro-porfirina. • Cada molécula de Hb contiene 4 grupos HEMO unidos cada uno a una diferente cadena polipeptídica de la globina.

GRUPO HEMO: es una ferro-porfirina (combinación del Fe con la PORFIRINA) PORFIRINA: • Compuesto cíclico tetrapirrólico con 4 núcleos pirrólicos unidos entre sí por puentes de meteno ( =CH -) que se designan como a, b, d, g. • Los núcleos pirrólicos se denominan I, III y IV. • Los H de sustitución en los núcleos se numeran del 1 al 8. M V I M M IV • Si los H 1 al 8 de los núcleos se reemplazan: - 4 metilos (CH 3) en 1, 2, 5, 8. - 2 vinilos (-CH=CH 2 -) en 3, 4 - 2 ac. Propiónicos (CH 2 -COOH) en 6, 7 II V P III P M

Transparencia 1 Estructura química del grupo HEMO donde se muestra la unión con el O 2 y la globina. Fig 22 -9. Ganong. Pag 456

CARACTERISTICAS DE LA PORCIÓN GLOBINA • • Es una proteína conjugada oligomérica. Representa el 96% de la molécula de Hb. Está formada por 4 subunidades de PM cercano a 17. 000. Cada subunidad está constituida por un grupo HEMO y una cadena polipeptídica. • En todas las especies las cadenas polipeptídicas aparecen como dos pares idénticos, dos alfa y dos no-alfa (β, γ o δ). - En el hombre adulto normal predomina la Hb A que tiene 2 cadenas polipeptídicas alfa y dos beta (a 2, b 2). - Existen normalmente otras Hb en menor cantidad como la Hb. A 2 con dos cadenas alfa y dos delta (a 2, d 2). - La Hb fetal presenta dos alfa y dos gama (a 2, γ 2). - La Hb glicosilada es un derivado de la Hb. A que presenta glucosa fijada al AA Valina terminal en cada cadena beta (marcador para el seguimiento de los diabéticos)
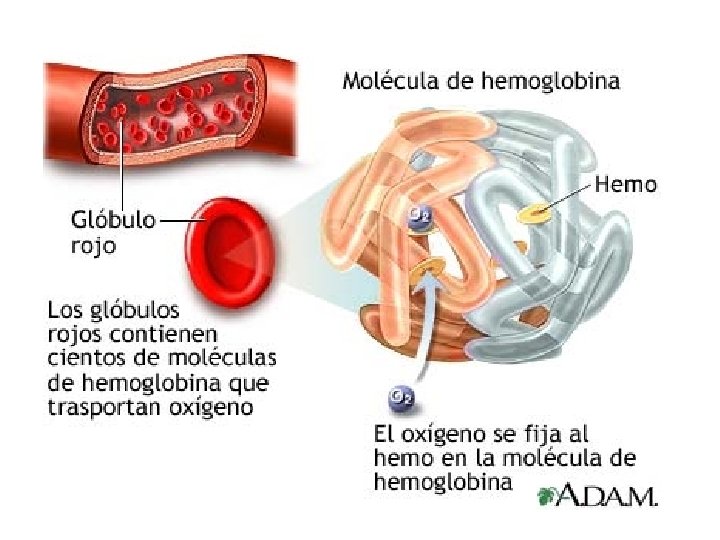

ESTRUCTURA DE LA HEMOGLOBINA Transparencia 2 Fig. 22 -1. Estructura de la Hemoglobina Best y Taylor (pag. 323)

EFECTO COOPERATIVO DE LA MOLÉCULA DE Hb • Cuando el O 2 se une a un grupo Hemo se produce en la molécula de Hb un cambio conformacional que facilitará la unión del O 2 a los 3 grupos hemo restantes o a la inversa: en los tejidos, la liberación de una molécula de O 2 de uno de los grupos hemo facilita la liberación de los restantes. • La molécula de Hb pasa por dos conformaciones espaciales diferentes con distinta afinidad por el O 2: - Conformación tensa (T): la Hb desoxigenada presenta unión electrostática firme entre las cadenas de la globina, - Conformación relajada (R): la unión de una molécula de O 2 a uno de los hemo rompe esas uniones electrostáticas aumentando la afinidad por el O 2 unas 500 veces. • La mioglobina siempre presenta gran afinidad por el O 2 lo que determina su avidez por el mismo cuando está presente.

EFECTO COOPERATIVO DE LA HEMOGLOBINA Transparencia 3 Fig. 22 -2. A. Curva de disociación de la oxihemoglobina B. Estados tenso (T) y relajado ® de la estructura cuaternaria de la Hb. Best y Taylor. (pag. 323)

REACCIONES DE LA HEMOGLOBINA: • Con O 2 (oxígeno): oxihemoglobina • Oxidación de la Hemoglobina: metahemoglobina • Con CO (monóxido de carbono): Carboxihemoglobina • Con CO 2 (dióxido de carbono): carbo hemoglobina

REACCIÓN CON O 2 → Oxihemoglobina • El Fe de la molécula de Hb se encuentra en estado Fe+2 (ferroso) y no cambia por unión al O 2. Se produce oxigenación pero no oxidación de la Hb. • Si se produjera oxidación el Fe+2 (ferroso) pasaría al estado Fe+3 (férrico), en esas condiciones la molécula de Hb es incapaz de transportar O 2. • En condiciones normales cada átomo de Fe puede fijar una molécula de O 2: cada molécula de Hb. puede transportar 4 moléculas de O 2. • La formación de oxihemoglobina es una reacción reversible lo que permite la captación y liberación de O 2 según la presión parcial de O 2. • Esta reacción depende de: el p. H, la temperatura y la concentración de 2, 3 difosfoglicerato.

REACCIÓN CO 2 → Carbo hemoglobina • Esta unión no se lleva a cabo con el grupo HEMO sino con la globina de la molécula de Hemoglobina. • Se producen compuestos carbámicos (carbamatos). • De esta manera, una vez que la Hb ha liberado el O 2 en los tejidos es capaz de captar el CO 2 producido por el metabolismo celular y transportarlo a los pulmones para su eliminación al exterior. • Reacción: Hb. NH 2 + CO 2 → Hb. NH. COO- + H+

OXIDACIÓN DE LA HB → Metahemoglobina • El Fe+2 de la Hb sufre normalmente procesos de oxidación a Fe+3 (metahemoglobina) que no transporta O 2 afectando diariamente a un 3% del total de la Hb. • El GR precisa de un mecanismo que reconvierta la meta. Hb en Hb: sistema enzimático NADH-metalohemoglobina reductasa. • Alteraciones: - falla congénita de este sistema enzimático metalohemoglobinemia hereditaria. - alteraciones genéticas en la molécula de Hb. - drogas vasodilatadorasdel tipo del nitroprusiato de sodio. • Cantidades de methemoglobina mayores del 15% producen una coloración azulada de la piel y mucosas.

REACCIÓN CO → Carboxihemoglobina • La Hb también puede combinarse con el monóxido de carbono (CO), resultante de procesos de combustión incompleta, ya que tiene por él mayor afinidad que por el mismo O 2 de modo que lo desplaza de su unión con el Fe. • Peligro de intoxicación con CO: - Si el porcentaje de carboxihemoglobina es del 30% aparecen cefaleas y vómitos, - Si es de 50% hay peligro de vida, - Si es de 60 -70% se produce muerte por asfixia.

SÍNTESIS DE HEMOGLOBINA v LOCALIZACIÓN: orgános eritropoyéticos en células eritrocíticas principalmente y escasamente en reticulocitos circulantes. v SÍNTESIS DEL HEMO: se necesita no solo para Hb sino para citocromos, catalasas y peroxidasas. • sustrato: glicina y succinil-Co. A. • Fe+2 llega desde el plasma (transferrina), atraviesa la membrana del GR en desarrollo y es captado la sideroglobulina. Es incorporado al HEMO ya sintetizado. • Los GR nucleados tienen depósitos Fe+2 en gránulos de ferritina. v SÍNTESIS DE GLOBINA: retículo endoplásmico rugoso de células de los tejidos eritropoyéticos

METABOLISMO DEL HIERRO • Cada gramo de Hemoglobina contiene 3, 4 mg de Fe la reserva sanguínea es de 50 mg. • Las pérdidas renales, por sudoración y digestivas son menores que 1 mg el déficit de Fe se genera más por pérdidas sanguíneas que por problemas nutricionales. • Sin embargo en los niños pequeños y en las embrazadas la ingestión adicional de Fe es fundamental para cubrir las necesidades de síntesis. • La absorción de Fe estará regulada por la magnitud de la eritropoyesis, el estado de los depósitos de reserva y la cantidad de Fe de la dieta. • Fe+2 necesario para sintetizar la Hemoglobina nueva es aprox. de 20 mg diarios. El requerimiento diario de un adulto es de 1 mg/día. no viene de la dieta sino que proviene de la destrucción de GR.

ABSORCIÓN DEL Fe • Se absorbe en intestino delgado en estado de Fe+2 aunque en los alimentos se encuentra como Fe+3. Es reducido antes de la absorción al p. H estomacal y en presencia de ácido ascórbico. • La capacidad absortiva máxima del intestino es de 3 -4 mg diarios que se aseguran con una ingesta diaria de 12 -15 mg diarios ya que la absorción es de aproximadamente el 8% de lo ingerido. • El % de absorción puede aumentar cuando el contenido de Fe del organismo es bajo: infancia, adolescencia, segunda mitad del embarazo, después de una pérdida sanguínea importante.

CONCENTRACIÓN PLASMÁTICA DE Fe+2 LA CANTIDAD DE Fe+2 PLASMÁTICO ES MANTENIDA EN UN EQUILIBRIO DINÁMICO ENTRE: • lo que se absorbe a nivel intestinal • lo que llega desde el sistema retículo endotelial por catabolismo de la Hb eritrocitaria. • Lo que abandona el plasma para dirigirse a los lugares de síntesis. • intercanbio con los depósitos de reserva. • lo que proviene de otros compuestos que contienen el grupo Hemo (citocromos, mioglobina y algunas enzimas). • lo que proviene del pool de Fe+2 lábil eritropoyético ubicado principalmente en médula ósea.

CAUSAS DE DISMINUCIÓN DE LA FERREMIA • Cuando los depósitos son bajos o ausentes (anemia por deficiencia de Fe). • Si la eritropoyesis es muy activa (hemorragia aguda). • Cuando aumentan las necesidades (embarazo y crecimiento). • Cuando disminuye la transferrina circulante.

OTROS ELEMENTOS NUTRICIONALES IMPORTANTES PARA LA PROLIFERACIÓN Y MADURACIÓN DE GR: q Ácido Fólico: - Afecta los procesos de síntesis de ADN alterando la maduración nuclear de precursores eritroides, leucocitos y megacariocitos. - Presente en verduras de hoja, frutas frescas y secas, legumbres hígado. - En las mujeres embarazadas se recomienda un refuerzo adicional de folatos debido a los requerimientos del feto. q Vitamina B 12: - Produce las mismas alteraciones hemáticas pero también afecta el desarrollo del SNC. - Su principal aporte proviene de las proteínas animales.
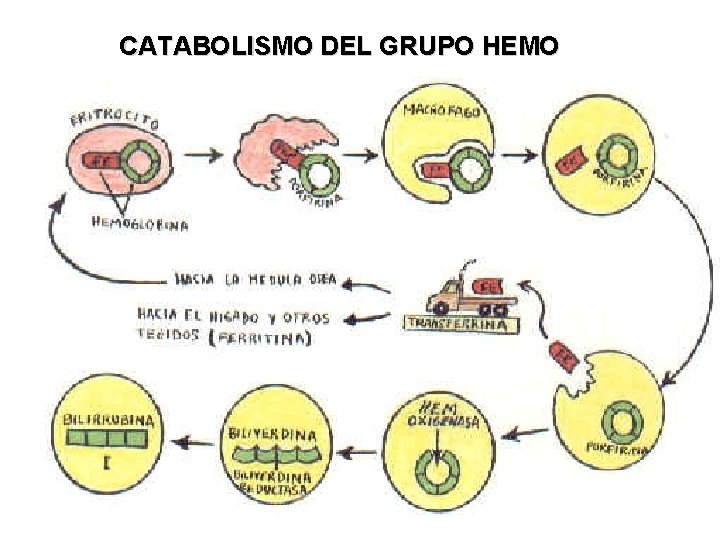
CATABOLISMO DEL GRUPO HEMO
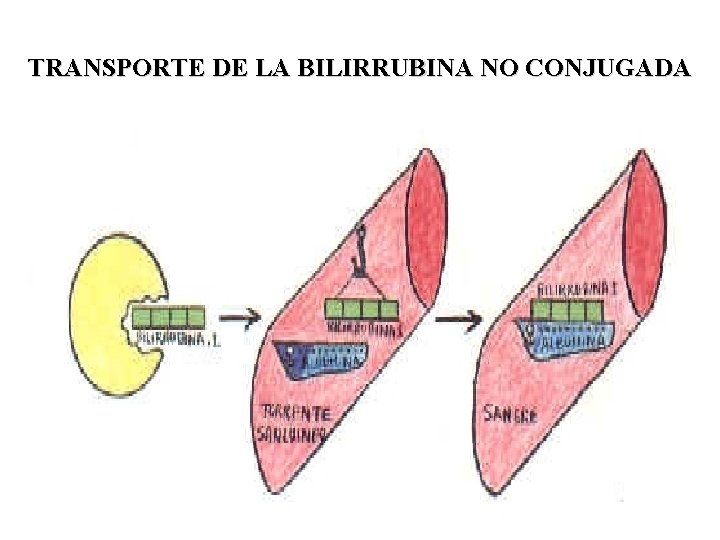
TRANSPORTE DE LA BILIRRUBINA NO CONJUGADA
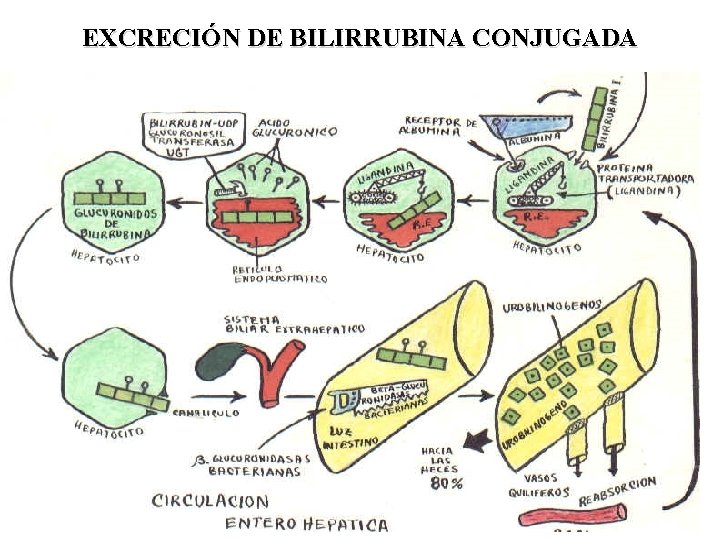
EXCRECIÓN DE BILIRRUBINA CONJUGADA

CATABOLISMO DE LA HEMOGLOBINA • Los GR envejecidos son destruidos en el SISTEMA RETICULOENDOTELIAL (SER): - la GLOBINA se separa de la molécula de Hemoglobina. - el grupo HEMO es transformado en BILIVERDINA. • La BILIVERDINA es convertida en BILIRRUBINA y se excreta por bilis. • El Fe del HEMO es reutilizado en la síntesis de nueva Hemoglobina.

DESTINO DE LA BILIRRUBINA • La Bilirrubina liberada por el SER (BILIRRUBINA NO CONJUGADA) es un pigmento amarillo soluble en solventes orgánicos pero muy poco soluble en solventes acuosos a p. H fisiológico, de modo que podría difundir a través de membranas y pasar a la célula donde su acumulación resulta tóxica. Para prevenirlo circula en plasma unida a la albúmina • El hígado posee una capacidad selectiva para remover la Bilirrubina no conjugada del plasma por acción de la enzima glucuroniltransferasa del retículo endoplásmico que transfiere el ácido glucurónico a la bilirrubina, formando BILIRRUBINA CONJUGADA que es más soluble en agua y puede excretarse por bilis y orina. • La Bilirrubina Conjugada pasa a sangre y de allí a la bilis que la transporta al intestino donde la flora bacteriana la reduce a compuestos que reciben el nombre de UROBILINOGENO. • Una parte de la Bilirrubina Conjugada unida a la albúmina puede ser eliminada por orina. • CONCLUSIÓN: la mayor parte de la Bilirrubina se excreta por heces mientras una pequeña fracción lo hace por orina.
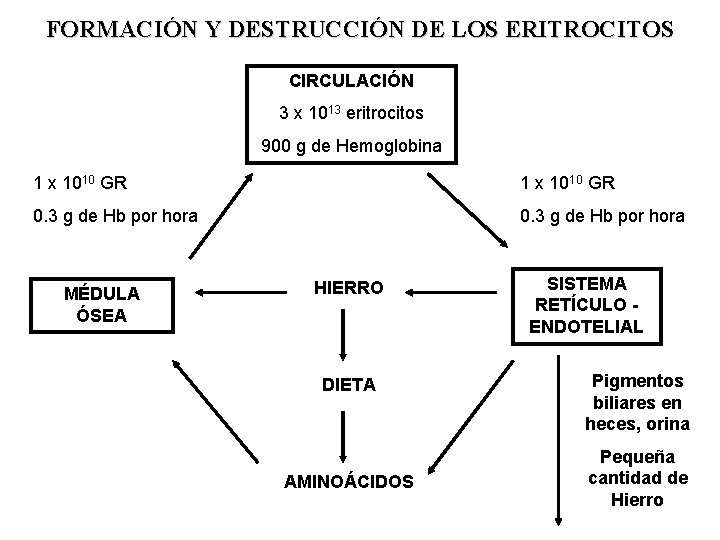
FORMACIÓN Y DESTRUCCIÓN DE LOS ERITROCITOS CIRCULACIÓN 3 x 1013 eritrocitos 900 g de Hemoglobina 1 x 1010 GR 0. 3 g de Hb por hora MÉDULA ÓSEA HIERRO DIETA AMINOÁCIDOS SISTEMA RETÍCULO ENDOTELIAL Pigmentos biliares en heces, orina Pequeña cantidad de Hierro
- Slides: 28