Hemijske osobine toksinih supstanci Literatura Danilo Popovi Toksikologija

Hemijske osobine toksičnih supstanci Literatura: Danilo Popović, Toksikologija – Izvodi sa predavanja, Niš, 2018, str. 60 -72.

Osobine toksičnih supstanci n n Osobina – eksperimentalno izmerena ili matematički izračunata kvantitativna karakteristika proučavane supstance. Podaci o supstanci koje je neophodno znati: n n n Osnovni podaci (naziv, proizvođač, godina proizvodnje, kvalitet, čistoća) Fizičke osobine Hemijske osobine Toksične osobine Štetne osobine

Hemijske osobine toksičnih supstanci n n Hemijske osobine dolaze do izražaja pri hemijskim reakcijama. Poznavanje hemijskih osobina toksičnih supstanci je neophodno radi: n n n predviđanja ponašanja toksične supstance pre ulaska u organizam (pri proizvodnji, transportu, čuvanju); predviđanja ponašanja toksične supstance u organizmu predviđanja toksičnog efekta). Najznačajnije hemijske osobine toksičnih supstanci su: n n hemijske veze, hemijska reaktivnost, hemijska struktura, hidroliza. (tj

Hemijske osobine toksičnih supstanci Hemijske veze

Hemijske veze n n Hemijske veze – sile koje drže zajedno atome u molekulu Stvaraju se sudarom čestica (atoma, atomskih grupa, molekula) Prilikom građenja hemijskih veza uvek se oslobađa energija Prilikom raskidanja hemijskih veza uvek je neophodno dovesti energiju

Hemijske veze n Teorije hemijske veze: n n Teorija valentne veze – Lewis-ova teorija Molekulsko-orbitalna teorija

Hemijske veze n n n Atomi teže da postignu stabilnu elektronsku konfiguraciju najbližeg plemenitog gasa Atomi otpuštaju, primaju ili dele elektrone u cilju postizanja elektronske konfiguracije plemenitih gasova U formiranju hemijskih veza učestvuju valentni elektroni (elektroni iz poslednjeg energetskog nivoa)

Hemijske veze n Intramolekulske (u molekulu): n n jonska kovalentna n n n Intermolekulske (između molekula): n n polarna nepolarna koordinativno-kovalentna metalna vodonična Van der Valsove sile n n dipol-dipol jon-dipol-indukovani dipol Londonove sile n n n trenutni dipol-trenutni dipol-permanentni dipol trenutni dipol-indukovani dipol

Jonska veza n n Jonska veza – elektrostatičko privlačenje između suprotno naelektrisanih jona Nastaje između metala koji u potpunosti otpušta elektrone i postaje pozitivno naelektrisani jon (katjon) i nemetala koji prima elektrone i postaje negativno naelektrisani jon (anjon)
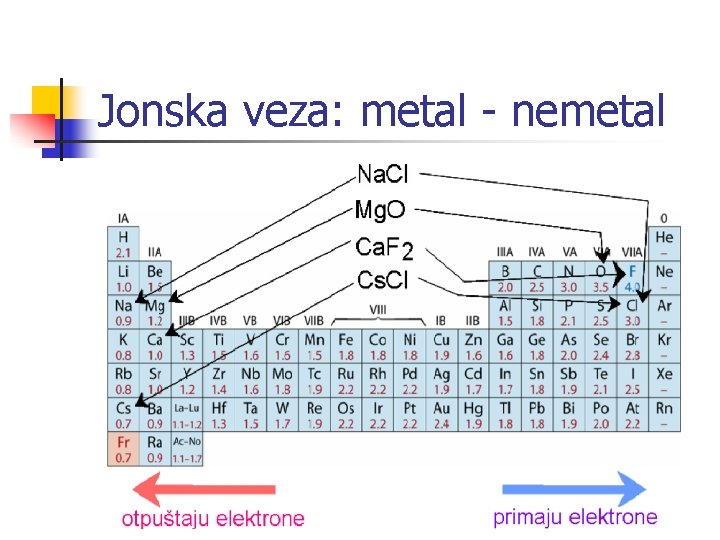
Jonska veza: metal - nemetal

Jonska veza – građenje Na. Cl 11 Na: 1 s 2 2 p 6 3 s 1 Na(g) → Na+(g) + e- Ei=+5, 14 e. V 17 Cl: 1 s 2 2 p 6 3 s 2 3 p 5 Cl(g) + e- → Cl-(g) Ea=-3, 61 e. V Na(g) + Cl(g) → Na+(g) + Cl-(g) ΔE=+1, 53 e. V Međutim ΔE=-3, 8 e. V Na(g) + Cl(g) → Na+Cl-(g) ΔE=-3, 8 e. V Jonski par Na+Cl-(g) se formira usled elektrostatičkog privlačenja između katjona Na+ i anjona Cl- pri čemu se gubi energija (ΔE=-5, 3 e. V) => Pri interakciji atoma koja vodi formiranju jona i građenju jonske veze energja se smanjuje što uzrokuje veliku stabilnost ove veze.
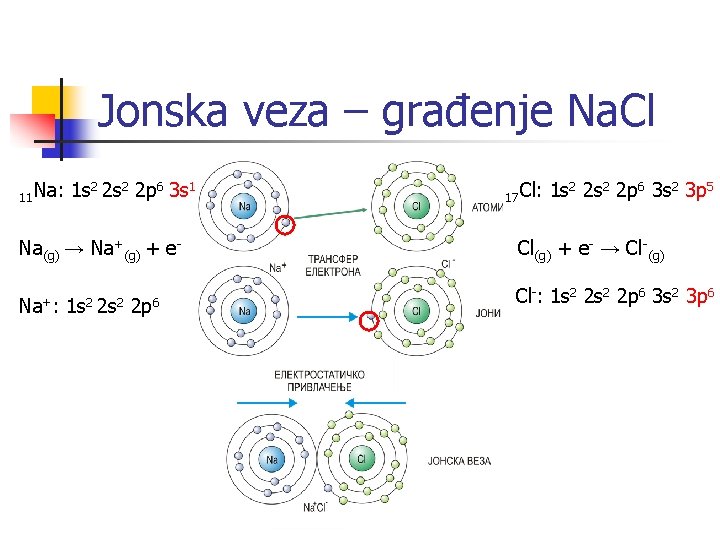
Jonska veza – građenje Na. Cl 11 Na: 1 s 2 2 p 6 3 s 1 17 Cl: 1 s 2 2 p 6 3 s 2 3 p 5 Na(g) → Na+(g) + e- Cl(g) + e- → Cl-(g) Na+: Cl-: 1 s 2 2 p 6 3 s 2 3 p 6 1 s 2 2 p 6

Osobine jedinjenja sa jonskom vezom n n n n Nije usmerena u prostoru (elektrostatičko privlačenje prostire se na sve jone u okolini); Jonski parovi postoje samo na visokim temperaturama; Na običnoj temperaturi su čvrste, kistalne supstance pravilnih geometrijskih oblika; Visoka tačka topljenja; Visoka tačka ključanja; Rastvaraju se u polarnim rastvaračima (voda); Vodeni rastvori i rastopi provode električnu struju.

Kovalentna veza n n Kovalentna veza nastaje udruživanjem elektrona u zajedničke elektronske parove Svaki atom daje jedan ili više elektrona za građenje zajedničkog elektronskog para Svaki zajednički elektronski par čini oktet svakog od atoma koji učestvuje u građenju veze Nastaje između atoma nemetala
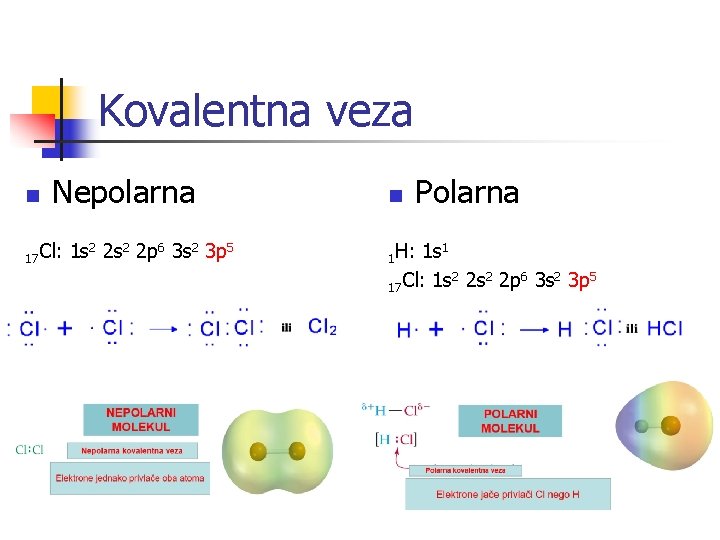
Kovalentna veza n Nepolarna 17 Cl: 1 s 2 2 p 6 3 s 2 3 p 5 n Polarna 1 H: 1 s 1 2 2 6 2 5 17 Cl: 1 s 2 s 2 p 3 s 3 p

Kovalentno vezivanje i toksičnost n n n Mnoge toksične supstance se vezuju za konstituente ćelija kovalentnom vezom i na taj način ispoljavaju svoj toksični efekat Kovalentno vezivanje toksičnih supstanci za sulfhidrilne (-SH) grupe enzima dovodi do inaktivacije enzima Npr. arsenova i živina jedinjenja se vezuju za sulfhidrilne grupe enzima kovalentnom vezom
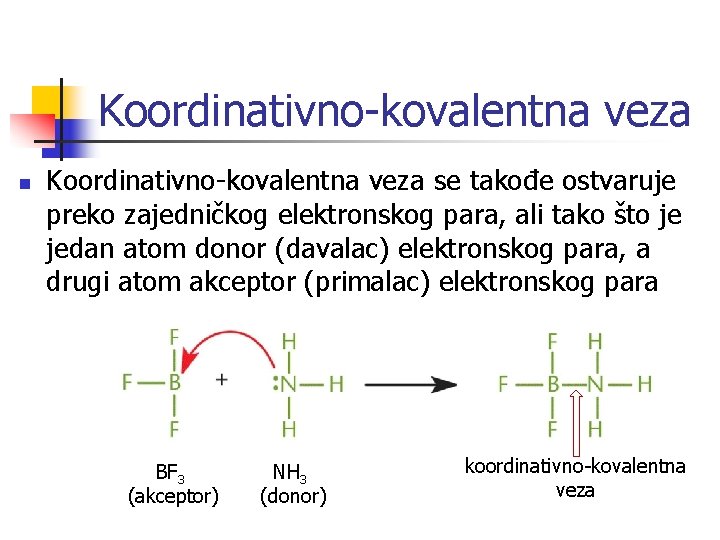
Koordinativno-kovalentna veza n Koordinativno-kovalentna veza se takođe ostvaruje preko zajedničkog elektronskog para, ali tako što je jedan atom donor (davalac) elektronskog para, a drugi atom akceptor (primalac) elektronskog para BF 3 (akceptor) NH 3 (donor) koordinativno-kovalentna veza

Metalna veza n Metali su hemijski elementi sledećih osobina: n n n u čvrstom su agregatnom stanju na sobnoj temperaturi (samo je živa tečna); poseduju metalni sjaj; dobri su provodnici toplote i elektriciteta; imaju visoke tačke ključanja i topljenja; lako se kuju i izvlače u žice. Ove osobine posledica su unutrašnje strukture metala, tj. metalne veze.

Metalna veza

Metalna veza n n U čvorovima kristalne rešetke nalaze se katjoni metala oko kojih se nalaze slobodni elektroni koji su lako pokretni i kreću se kroz metal => objašnjenje provodljivosti Metalna hemijska veza obezbeđuje kompaktnu strukturu metala; postoji elektrostatičko privlačenje između slobodno pokretnih elektrona i pozitivnih jona metala => građenje metalne kristalne rešetke
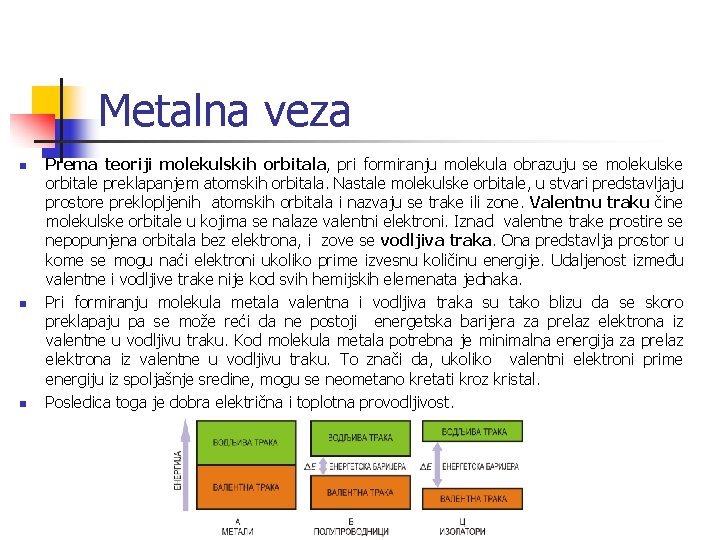
Metalna veza n n n Prema teoriji molekulskih orbitala, pri formiranju molekula obrazuju se molekulske orbitale preklapanjem atomskih orbitala. Nastale molekulske orbitale, u stvari predstavljaju prostore preklopljenih atomskih orbitala i nazvaju se trake ili zone. Valentnu traku čine molekulske orbitale u kojima se nalaze valentni elektroni. Iznad valentne trake prostire se nepopunjena orbitala bez elektrona, i zove se vodljiva traka. Ona predstavlja prostor u kome se mogu naći elektroni ukoliko prime izvesnu količinu energije. Udaljenost između valentne i vodljive trake nije kod svih hemijskih elemenata jednaka. Pri formiranju molekula metala valentna i vodljiva traka su tako blizu da se skoro preklapaju pa se može reći da ne postoji energetska barijera za prelaz elektrona iz valentne u vodljivu traku. Kod molekula metala potrebna je minimalna energija za prelaz elektrona iz valentne u vodljivu traku. To znači da, ukoliko valentni elektroni prime energiju iz spoljašnje sredine, mogu se neometano kretati kroz kristal. Posledica toga je dobra električna i toplotna provodljivost.

Intermolekulske veze n n Intermolekulske veze (između molekula) su slabije od intramolekulskuh (unutar molekula) U osnovi su elektrostatičke prirode Značajne su za supstance u tečnom i čvrstom agregatnom stanju (drže molekule na okupu) Intermolekulske veze: n n n vodonične veze, Van der Valsove sile, Londonove sile.

Vodonične veze n n Vodonična veza se javlja između molekula kod kojih je vodonikov atom kovalentno vezan za atom velike elektronegativnosti (imeđu molekula HF, H 2 O, NH 3. . . ) Element veće elektronegativnosti privlači ka sebi zajednički elektronski par kovalentne veze što dovodi do pojave parcijalno negativnog naelektrisanja (δ-) na tom elementu i pojave parcijalno pozitivnog naelektrisanja na vodoniku (δ+) Kada se ovako nagrađeni polarizovani molekuli međusobno približe, dolazi do elektrostatičkog privlačnja između parcijalno pozitivnog kraja jednog molekula i parcijalno negativnog kraja dugog molekula U organizmu vodonična veza je značajna za privlačenje antigena i antitela
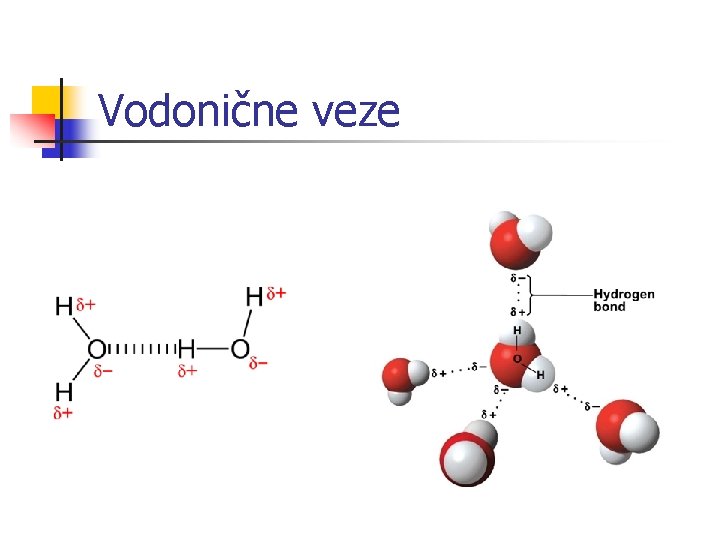
Vodonične veze

Van der Valsove sile n Van der Valsove sile – slabe, elektrostatičke interakcije između molekula: n n n n permanenni dipol – permanentni dipol – jon permanentni dipol – indukovani dipol Dipol – molekul u kome dolazi do razdvajanja naelektrisanja Permanentni dipol – javlja se kada se atomi kovalentne veze značajno razlikuju po elektronegativnosti. Atom veće elektronegativnosti privlači ka sebi zajednički elektronski par kovalentne veze što dovodi do pojave parcijalno negativnog naelektrisanja (δ-) na tom elementu i pojave parcijalno pozitivnog naelektrisanja na atomu manje elektronegativnosti (δ+). Trenutni dipol – kada se elektroni više skoncentrišu na jednom mestu u molekulu. Indukovani dipol – kada se raspored naelektrisanja u nepolarnom molekulu menja pod dejstvom nekog spoljašnjeg uticaja.

Dipol-dipol interakcije n n Dipol-dipol interakcije se javljaju kada se molekuli sa permanentnim dipolom (HF, H 2 O, NH 3. . . ) dovoljno približe jedan drugom pri čemu dolazi do orjentacije dipola tako da se suprotno naelektrisani polovi privlače. Zastupljene su u supstancama svih agregatnih stanja.

Dipol-jon interakcije n n Dipol-jon interakcije se javljaju kada se molekuli sa permanentnim dipolom (HF, H 2 O, NH 3, etanol, kiseline. . . ) dovoljno približe nekom jonu. Dipol se orjentiše ka jonu svojim krajem koji je suprotnog naelektrisanja u odnosu na jon. Ove interakcije su zastupljene prilikom rastvaranja jonskih jedinjenja (solvatacija). Ukoliko je reč o rastvaranju u vodi reč je o hidrataciji.
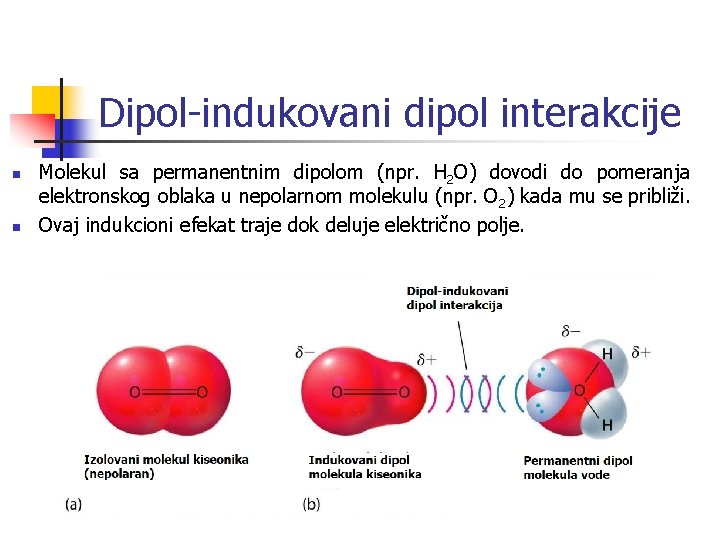
Dipol-indukovani dipol interakcije n n Molekul sa permanentnim dipolom (npr. H 2 O) dovodi do pomeranja elektronskog oblaka u nepolarnom molekulu (npr. O 2) kada mu se približi. Ovaj indukcioni efekat traje dok deluje električno polje.

Van der Valsove sile n n Kada su toksična supstanca i receptor sličnog stereo oblika onda se omogućava bolje približavanje molekula koje se pojačava delovanjem Van der Valsovih sila. Van der Valsove sile su odgovorne za fizičku adsorpciju na graničnim površinama.

Londonove (disperzione) sile n n Nastaju kao posledica neprestanog kretanja elektrona u molekulskim i atomskim orbitalama i oscilatornog kretanja jezgra atoma jer dolazi do trenutnih poremećaja ravnoteže u raspodeli naelektrisanja. Te trenutne neravnoteže u naelektrisanjima kod nepolarnih molekula i atoma sa zasićenim orbitalama (inertni gasovi) dovode do pojave trenutnih dipola. Do interakcije trenutni dipol-trenutni dipol dolazi ako se dovoljno približe takva dva trenutna dipola. Energija koja omogućava to privlačenje zove se disperziona energija.

Londonove (disperzione) sile n n n Do interakcije trenutni dipol-indukovani dipol dolazi kada trenutni dipol indukuje električno polje kod neutralnog molekula ili atoma. Disperziona energija kod molekula sa permanentnim dipolom doprinosi jačanju trenutnog dipola i tako dolazi do interakcije trenutni dipol-permanentni dipol. Disperzione sile uslovljavaju fizičke osobine i reaktivnost mnogih supstanci.

Hemijske osobine toksičnih supstanci Hemijska reaktivnost

Hemijska reaktivnost toksičnih supstanci n Toksične supstance mogu reagovati sa molekulima u našem organizmu pri čemu nastaju supstance koje mogu biti iste, manje ili veće toksičnosti od polaznih supstanci.

Hemijske reakcije neorganskih toksičnih supstanci n n n n n Redoks Kiselinsko-bazne Protolitičke Jono-izmenjivačke Kompleksne Disocijacije i asocijacije Fotohemijske Taloženja Složene

Redoks rekcije n n n n Redoks (oksido-redukcione) reakcije su reakcije u kojima dolazi do razmene perifernih elektrona, zbog čega dolazi do promene oksidacionih brojeva učesnika reakcije Oksidacioni broj predstalja stvarno ili formalno naelektrisanje atoma Oksidacija je proces otpuštanja elektrona (oksidacioni broj se povećava) Redukcija je proces primanja elektrona (oksidacioni broj se smanjuje) Reakcije oksidacije i redukcije se vrše istovremeno i međusobno su zavisne, pa se proces naziva oksido-redukcija Oksidaciono sredstvo je supstanca koja oksiduje druge supstance, ali se pri tom sama redukuje (prima elektrone, tj. to je akceptor elektrona) Redukciono sredstvo je supstanca koja redukuje druge supstance, ali se pri tom sama oksiduje (otpušta elektrone, tj. to je donor elektrona)
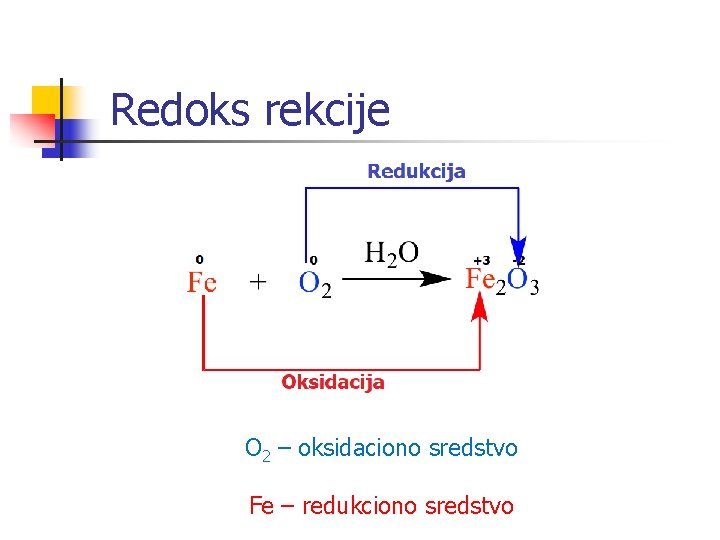
Redoks rekcije O 2 – oksidaciono sredstvo Fe – redukciono sredstvo

Kiselinsko-bazne reakcije n n Kiselinsko-bazne reakcije su reakcije između kiselina i baza. Neutralizacione reakcije su kiselinsko-bazne reakcije između ekvivalentnih količina jake kiseline i jake baze jer je ekvivalentna tačka u neutralnoj sredini (p. H=7). HA + MOH → MA + H 2 O Kiselina + Baza → so + voda

Protolitičke reakcije n n n Protolitičke reakcije su reakcije razmene protona (H+ jona). Kiselina je donor (davalac) protona (H+ jona). Baza je akceptor (primalac) protona (H+ jona). HA + H 2 O B + H 2 O Kiselina H 3 O+ + ABH+ + OHH+ + Baza Kiselinsko-bazni par

Jono-izmenjivačke reakcije n n n Jono-izmenjivačke reakcije su reverzibilne (povratne) reakcije u kojima se joni istog predznaka izmenjuju između čvrste supstance i rastvora. Čvrsta supstanca mora da ima jone koje može izmenjivati sa rastvorom i propusnu strukturu kroz koju joni i molekuli rastvarača mogu da difunduju. Ove osobine ispunjava glina.
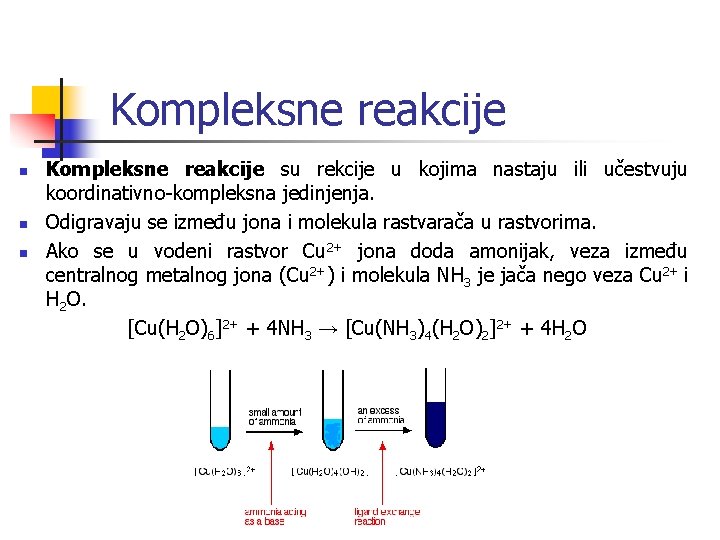
Kompleksne reakcije n n n Kompleksne reakcije su rekcije u kojima nastaju ili učestvuju koordinativno-kompleksna jedinjenja. Odigravaju se između jona i molekula rastvarača u rastvorima. Ako se u vodeni rastvor Cu 2+ jona doda amonijak, veza između centralnog metalnog jona (Cu 2+) i molekula NH 3 je jača nego veza Cu 2+ i H 2 O. [Cu(H 2 O)6]2+ + 4 NH 3 → [Cu(NH 3)4(H 2 O)2]2+ + 4 H 2 O

Reakcije jonizacije i asocijacije n Reakcije jonizacije i asocijacije se odigravaju u sva tri agregatna stanja i u rastvorima. N 2 O 4 ↔ 2 NO 2 I 2 ↔ 2 I Hg 22+ ↔ 2 Hg+ n n Toksičnost mnogih supstaci zavisi od njihove jonizacije u rastvoru jer se takve supstance za receptore u našem organizmu vezuju jonskom vezom. Neke supstance su toksične u nejonizovanom obliku.

Fotohemijske reakcije n n Fotohemijske reakcije se odigravaju pod dejstvom svetlosti (hν). Apsorpcijom svetlosti atom ili molekul prelazi iz osnovnog u pobuđeno (ekscitovano) stanje. Iz ekscitovanog stanja oni mogu: n n da da se vrate u osnovno stanje, pređu u drugo ekscitovano stanje, se razlože, podlegnu intramolekulskom premeštanju dajući fotoproizvode. Hg(g) + hν ↔ Hg*(g) + H 2 ↔ Hg(g) + 2 H(g)

Reakcije taloženja n n n n Reakcije taloženja se odigravaju onda kada su u rastvoru joni teško rastvorne soli prisutni u većoj koncentraciji od rastvorljivosti supstance. Do taloženja dolazi kada se prekorači proizvod rastvorljivosti. Ako je proizvod koncetracija jona manji od proizvoda rastvorljivosti jedinjenja ne dolazi do taloženja. Mnogi katjoni se talože u obliku hidroksida pri određenoj vrednosti p. H. Nastajanje hidroksida i koloida zavisi od proizvoda rastvorljivosti i p. H sredine. U organizmu radioaktivne supstance su prisutne u malim količinama, proizvod koncentracije jona ne premašuje proizvod rastvorljivosti hidrokisda, odnosno nastaje pravi rastvor. Taloženjem hidroksida se stvaraju uslovi za polimerizaciju, odnosno dolazi do stvaranja hidroksida.

Složene reakcije n n n Složene reakcije su sastavljene od niza jednostavnih reakcija. Do hemijske reakcije dolazi kada se čestice sudare. Prvo nastaju međuproizvodi, koji daljim reagovanjem daju sve složenije konačne proizvode.

Podela hemijskih reakcija organskih toksičnih supstanci n Na osnovu načina raskidanja (formiranja) veze n n n Prema tipu reakcije n n n homolitičke heterolitičke supstitucija adicija eliminacija premeštanje redoks Prema tipu reagensa n nukleofilne elektrofilne slobodno-radikalske

Hemijske reakcije organskih toksičnih supstanci n n Organski molekuli su izgrađeni iz C i H atoma, a mogu sadržati i heteroatome (N, O, S, P. . . ), koji su međusobno povezani kovalentnim vezama. Raskidanje veza u organskim molekulima može biti: n Homolitičko n Heterolitičko

Hemijske reakcije organskih toksičnih supstanci n n Homolitičko (simetrično, nepolarno) raskidanje kovalentne veze vrši se tako što svaki atom ili atomska grupa zadržava jedan elektron zajediničkog elektronskog para. Homolitičkim raskidanjem nastaju slobodni radikali – čestice sa nesparenim elektronom. Suprotan proces od homolize se naziva rekombinacija. Karakteristično je za reakcije koje se odigravaju u: n n n gasnoj fazi, nepolarnoj sredini, termički, fotohemijski, pod dejstvom slobodnog radikala.

Hemijske reakcije organskih toksičnih supstanci n n Slobodni radikali su vrlo reaktivne čestice Učestvuju u lančanim reakcijama

Hemijske reakcije organskih toksičnih supstanci n n Heterolitičko (asimetrično, polarno, jonsko) raskidanje kovalentne veze vrši se tako što zajednički elektronski par pripadne jednom atomu (grupi atoma) koji postaje negativan jon (karbanjon), a drugi atom (grupa atoma) postaje pozitivan jon (karbkatjon). Suprotan proces se naziva koordinacija.

Hemijske reakcije organskih toksičnih supstanci n n Polarni reagensi vrše heterolitičko raskidanje veza. Polarni reagensi su: n n n Nukleofili (Nu: , vole jezgro (nukleus)) – daju elektrone; Elektrofili (E+, vole elektrone) – primaju elektrone. Heterolitičke reakcije: n n odigravaju se u rastvorima, polarnost rastvarača utiče na brzinu i tok reakcije, kiseline i baze su katalizatori u ovim reakcijama, nisu lančane.

Hemijske reakcije organskih toksičnih supstanci n Podela prema tipu reakcije: n n supstitucija (zamena) – atom ili grupa atoma se zamenjuje drugim atomom ili grupom atoma; adicija – karakteristična za nezasićena jedinjenja (sa dvostrukim i trostrukim vezama); dva ili više reaktanta se kombinuju da se dobije jedan proizvod; eliminacija – iz jednog reaktanta dobijaju se dva proizvoda; u ravnoteži je sa adicijom i često je povratan proces; redoks – promene oksidacionog broja su promene koje se javljaju uz supstituciju, adiciju, eliminaciju; kod neorganskih supstanci redoks promena podrazumeva potpuni prelazak elektrona sa jedne vrste na drugu; kod organskih redoks reakcija prelaz nije potpun, tada nastaju promene u kovalentnom vezivanju među atomima različite elektronegativnosti.
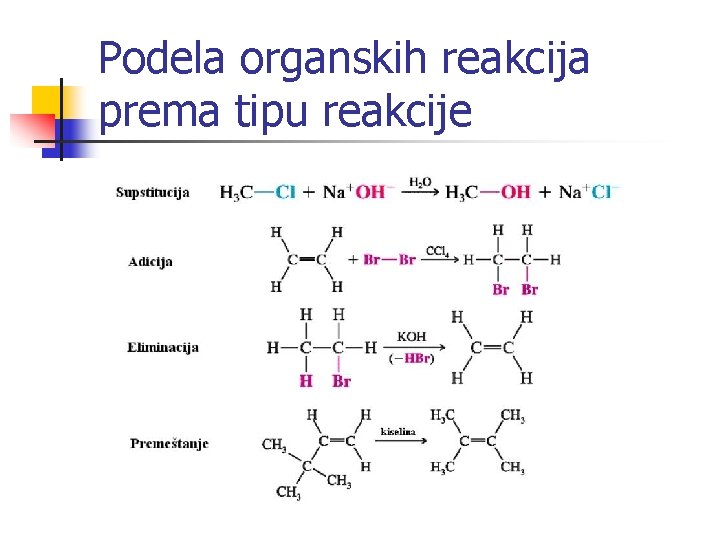
Podela organskih reakcija prema tipu reakcije

Hemijske osobine toksičnih supstanci Hemijska struktura

Hemijska struktura i toksičnost n n n Postoji veza između hemijske strukture i toksičnosti. Toksikofora – deo molekula koji je zaslužan za toksični efekat. Kod uvođenja novih supstanci u tehnološke procese unapred bi se mogla znati toksičnost supstance na osnovu hemijske strukture. Članovi homologih redova bi trebalo da imaju slične toksične osobine i sličan mehanizam dejstva. Međutim, moguće je i da supstance slične strukture postignu isti efekat pomoću različitih mehanizama ili da jedna supstanca ima više različitih efekata. Supstance koje imaju različitu strukturu, a slično delovanje menjaju fizičko-hemijske uslove u ćelijama verovatno zahvaljujući fizičkim osobinama, a ne funkcionalnim grupama.

Hemijska struktura i toksičnost n Alifatični ugljovodonici n n n Toksičnost raste od C 1 do C 9, a opada od C 10 jer se smanjuje isparljivost Račvanje smanjuje toksičnost Povećanje broja nezasićenih veza povećava toksičnost (etan<eten <etin)

Hemijska struktura i toksičnost n Alkoholi n n n Metanol (CH 3 OH) je toksičniji od etanola (C 2 H 5 OH) Toksičnost raste od etanola (C 2 H 5 OH) do pentanola (C 5 H 11 OH) Od pentanola se sa porastom broja C atoma toksičnost smanjuje zbog slabe rastvorljivosti u telesnim tečnostima

Hemijska struktura i toksičnost n Hlorovani ugljovodonici - alifatični n n n Generalno, toksičnost raste sa porastom broja atoma hlora Međutim, hloroform (CHCl 3) je manje toksičan i od dihlormetana (CH 2 Cl 2) i od ugljentetrahlorida (CCl 4) CH 3 Cl < CH 2 Cl 2 > CHCl 3 < CCl 4 Hlorovani ugljovodonici - aromatični n benzen je toksičniji od hlorbenzena
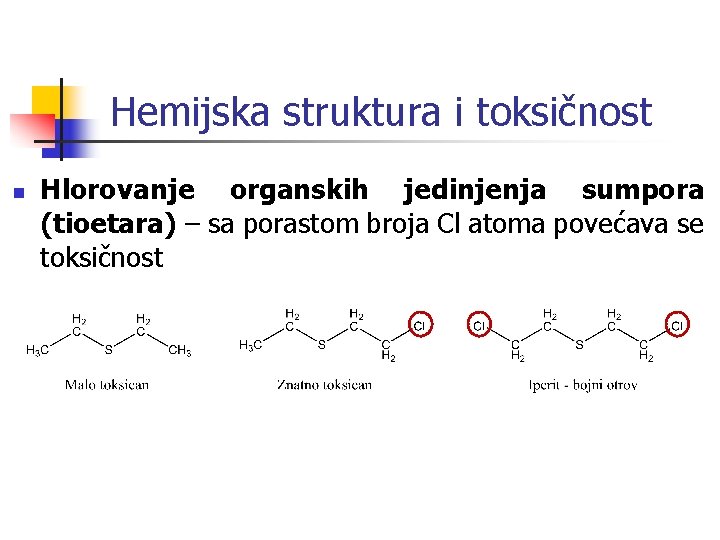
Hemijska struktura i toksičnost n Hlorovanje organskih jedinjenja sumpora (tioetara) – sa porastom broja Cl atoma povećava se toksičnost

Hemijske osobine toksičnih supstanci Hidroliza

Hidroliza n n u širem smislu – razlaganje složenih jedinjenja jednostavnija pod dejstvom vode u užem smislu – razlaganje soli pod dejstvom vode neutralizacija МOH + HA ⇄ hidroliza MA + H 2 O u

Hidroliza n Soli jake kiseline i jake baze ne podležu hidrolizi – sredina je neutralna Na+ + Cl- + H 2 O → Na+ + OH- + H+ + Cl. H 2 O → OH- + H+
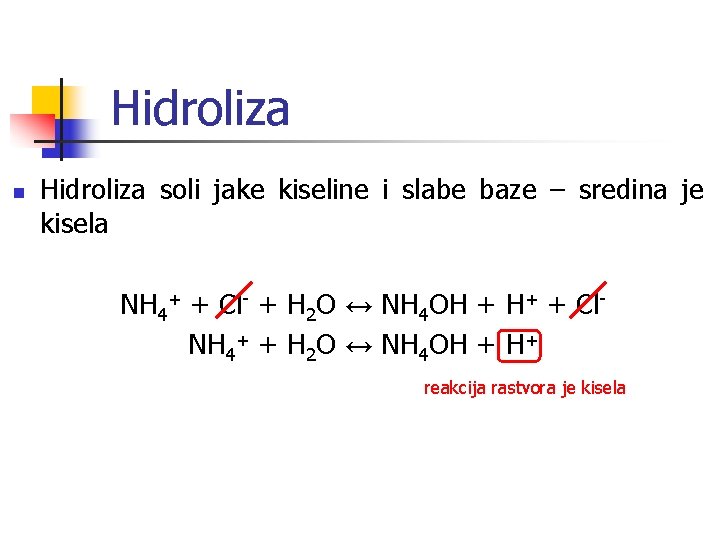
Hidroliza n Hidroliza soli jake kiseline i slabe baze – sredina je kisela NH 4+ + Cl- + H 2 O ↔ NH 4 OH + H+ + Cl. NH 4+ + H 2 O ↔ NH 4 OH + H+ reakcija rastvora je kisela
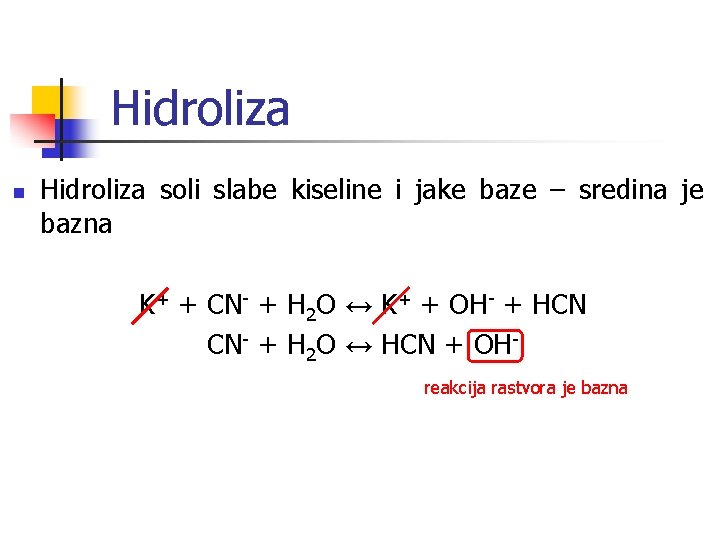
Hidroliza n Hidroliza soli slabe kiseline i jake baze – sredina je bazna K+ + CN- + H 2 O ↔ K+ + OH- + HCN CN- + H 2 O ↔ HCN + OHreakcija rastvora je bazna

Hidroliza n Hidroliza soli slabe kiseline i slabe baze – sredina je približno neutralna NH 4+ + CN- + H 2 O ↔ NH 4 OH + HCN
- Slides: 64