Hematolgiai norml rtkek Hb 13 0 18 0

Hematológiai normál értékek Hb: 13. 0– 18. 0 g/d. L (ffi) ill. 11. 5– 16. 5 g/d. L (nő) hematokrit: 0. 40– 0. 52 (ffi) ill. 0. 36– 0. 47 (nő) RCC: 4. 5– 6. 5 × 1012/L (ffi) ill. 3. 8– 5. 8 × 1012/L (nő) MCV: 77– 95 f. L MCH: 27. 0– 32. 0 pg MCHC: 32. 0– 36. 0 g/d. L retikulocita: 0. 5– 2. 5% (vagy 50– 100× 109/L)

Az anémia okai kinetika alapján

Az anémia okai vörösvérsejt morfológia alapján

A transzfúzió indikációja anémiában akut vérzés hemodinamikai megingással (hemorrágiás sokk) • akut vérzés inadekvát oxigénszállító kapacitással (izovolémiás = normovolémiás anémia mellett) • szervek oxigénhiány okozta funkciózavara (élettani jelek, regionális és globális - az anémiára legérzékenyebben azok a szervek jeleznek, ahol magas a nyugalmi oxigén extrakció (SN_XIV_1_5_tablazat)) - zárt periféria, megnyúlt kapilláris telődés, perifériás vazokonstrikció - EKG: ST eltérések (szív O 2 extrakció artériás vér oxigéntartalomból: 60%) - zavartság, nyugtalanság (agyi O 2 extrakció: 30%) - oliguria és anuria: a vese a hipoperfúzióra sokkal érzékenyebb, mint az anémiára (O 2 extrakció: <10%) - laktátacidózis • oxigén extrakció >0, 3 (SN_XIV_1_6_tablazat) • oxigén szállítás <10 -12 ml/kg/min nem akut vérzés esetén, ha Hb <7 g/dl kivétel bizonyos kardiorespiratorikus betegségekben például akut infarktusban, instabil angina esetén <10 g/dl Hb szint is lehet indikáció forrás: Transfusion Requirements in Critical Care (TRICC - 1999)
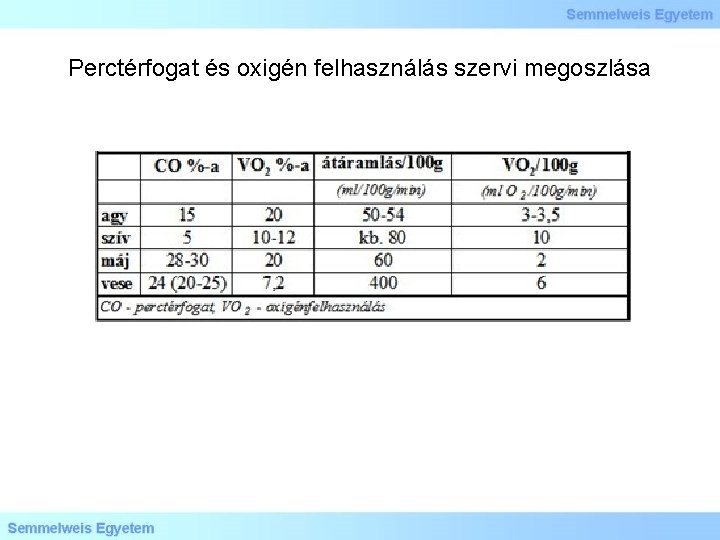
Perctérfogat és oxigén felhasználás szervi megoszlása
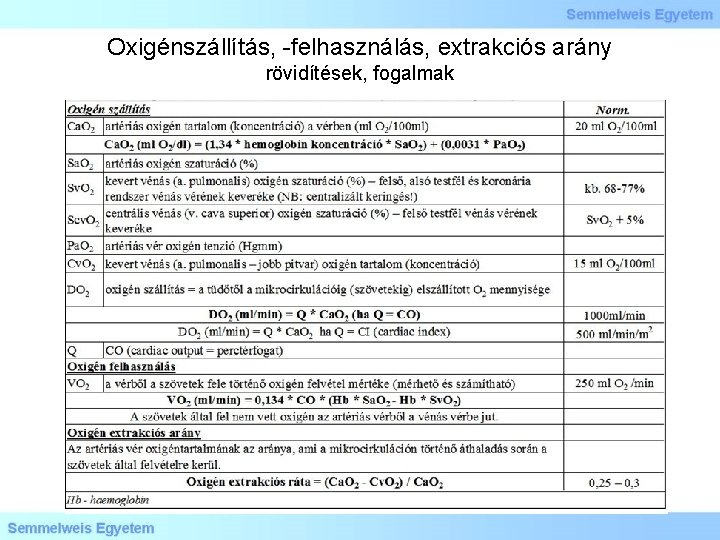
Oxigénszállítás, -felhasználás, extrakciós arány rövidítések, fogalmak
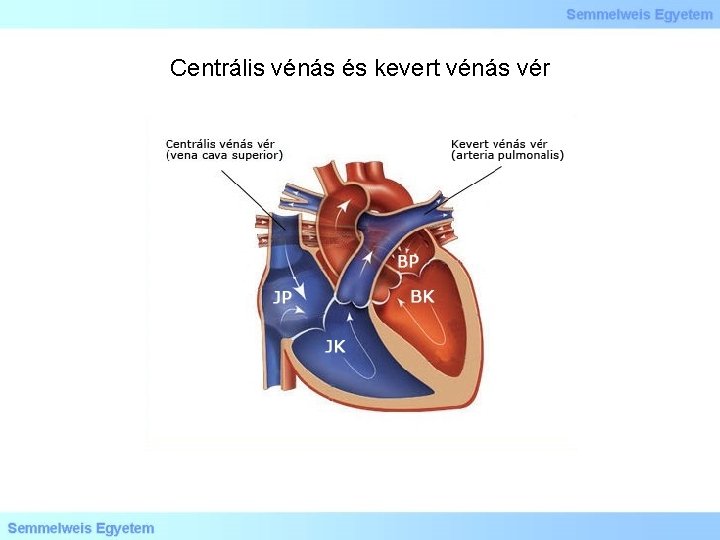
Centrális vénás és kevert vénás vér

A DIC kiváltó okai fertőzések • baktérium (elsősorban Gram-negatív szepszis) • gomba • vírus terhesség során • magzatvíz embólia • preeklampszia, eklampszia • visszamaradt lepény transzfúziós, transzplantációs komplikáció malignus alapbetegség kiterjedt trauma, égés kihűlés májelégtelenség

A trombocita aktiváció mediátorai aktivátor eredet kollagén sérült subendotelium TXA 2 aktivált trombocita 5 -HT aktivált trombocita adrenalin aktivált trombocita, vér trombin vér PAF gyulladásos szövetek fehérvérsejtjei
A trombocitopénia etiológiája csökkent csontvelői termelődés • kongenitalis (Fanconi-szindróma) • csontvelő károsodás (gyógyszerek, vegyi anyagok, sugár, kemoterápia, vírusfertőzések, megakariociták elleni antitest) • csontvelő infiltráció (leukémia, karcinóma, limfóma) • B 12 vagy folsav hiány (megakariocita érési zavar) • alkohol toxicitás fokozott perifériás trombocita pusztulás miközben a trombociták élettartama néhány órára csökken, megakariocitózis alakul ki fokozott trombin hatás DIC, bizonyos infekciók, malignus betegségek immun trombocitopéniák ITP, SLE, limfóma, gyógyszer indukálta trombocitopénia, HIT-II, posztranszfúziós TTP HUS dilúciós trombocitopénia nagy vérvesztés esetén, ha a volumenterápia során trombocita készítmény nem kerül beadásra disztribucionális trombocitopénia: splenomegália pszeudo-trombocitopénia • aggregáció és agglutináció (vérvételi hiba, EDTA-függő agglutininek) • trombocita és fehérvérsejt közötti szatellita képződés • óriás trombociták jelenléte trombocita képzés és pusztulás egyidejű zavara: pl. májcirrhosis egyes eseteiben

A gyógyszer-indukálta trombocitopéniák kritériumrendszere, jellemző gyógyszerek

Trombolízis A trombolitikumok közül Streptokináz esetén 250 000 NE bolus adandó 20 perc alatt, majd 100 000 NE/óra dózisban max. 4 napig folytatható. Streptokináz tartós adása során észlelt magasabb vérzéses szövődmények miatt, amennyiben elérhető úgy a korszerűbb urokináz vagy rt-PA választandó. Urokináz használatakor 250 000 -600 000 NE, 10 -20 perc alatt. Az rt-PA (rekombináns szöveti plazminogén aktivátor) jelenleg a legkorszerűbb. Javasolt 100 mg adása 2 óra alatt, vagy 0, 6 mg/ttkg egyszeri bólusban. Rt-PA és Urokináz használata esetén terápiás szintű LMWH (alacsony molekulasúlyú heparin) vagy UFH (hagyományos, frakcionáltalan heparin) kezelést kell indítani a trombolízissel párhuzamosan.
Antikoaguláns terápia LMWH sc alkalmazásakor a választott készítmény leiratában szereplő ajánlás értelmében, antikoaguláns dózisban használjuk, általánosságban 100 NE/kg 12 óránként (enoxaparin, dalteparin) 4 -5 napig. A második napon az oralis antikoaguláns kezelés indítható kumarin származékkal. Monitorozása rutinszerűen nem szükséges, de terhességben, veseelégtelenségben, obezitás esetén javasolt. Terápiánk akkor tekinthető hatásosnak, amennyiben sc. beadást követően 4 órával az anti-Xa aktivitás 0, 6 -1, 0 NE/ml. UFH intravénás használatakor Na-Heparint adunk 5000 NE bólusban, majd 1000 -1500 NE/óra folyamatos infúziót indítunk. Monitorozása APTI kontrollal 6 óránként (az APTI legyen a kontroll 1, 5 -2, 5 -szerese). A célértéket elérve napi egyszeri kontroll is elég. Igazán kívánatos UFH esetén is az Anti-Xa aktivitás meghatározás lenne. Oralis antikoagulánst indíthatjuk szintén a második napon. Heparint addig adjuk, míg az INR érték 2 egymást követő napon 2, 0 értéket eléri. LMWH és UFH alkalmazásakor kötelező a trombocitaszám ellenőrzése a 0 -3 -5 napon, tartósabb kezelés estén a 14. napig hetente kétszer, a heparin indukálta trombocitopénia (HIT) veszélye miatt.

A trombózis klinikai manifesztációi • • • purpura fulminans (neonatális/felnőtt) felületes vénatrombózis vénás tromboembólia: mélyvénás trombózis, tüdőembólia a legjellemzőbb manifesztáció • „szokatlan” lokalizációjú vénás trombózis pl. : agyi, máj, mezenteriális, vese, felső végtag, portális vénák • warfarin-indukált bőrnekrózis • egyes esetekben artériás trombózis pl. sztrók, miokardialis infarktus • ismétlődő vetélés • terhesség során jelentkező komplikációk pl. intrauterin retardáció, preeklampszia, placenta abrupció

Hiperkoagulabilitással járó defektusok öröklött trombofíliák szerzett trombofíliák Aktivált protein C rezisztencia V. faktor Leyden mutációja malignitás Protrombin G 20210 A mutáció kemoterápia l-aszparagináz, thalidomide, antiangiogenezis terápia Protein C defektus Protein S defektus mieloproliferatív megbetegedések heparin-indukált trombocitopénia Antitrombin III defektus nefrózis-szindróma homocisztinúria orális fogamzásgátlók hiperhomociszteinémia ösztrogén terápia diszplazminogénémia terhesség, posztpartum időszak hipo-, diszfibrinogénémia szelektív ösztrogén receptor modulátorok tamoxifen, raloxifen csökkent szöveti faktor út inhibítor antifoszfolipid-szindróma eritropoezist stimuláló gyógyszerek hiperhomociszteinémia

A hemolítikus anémiák felosztása

A hemolítikus anémiák epidemiológiája • A szferocitózis Európában a leggyakoribb öröklődő hemolítikus anémia. Autoszomális, domináns öröklődést mutat, incidenciája 2/10000 fő. • A leggyakoribb enzimopátia a glükóz-6 -foszfát-dehidrogenáz-hiány (favizmus), amely nemhez kötötten, recesszív módon öröklődik, ezért jellemzően férfiakban manifesztálódik. Az afrikai színes bőrű lakosság kb. 10%-a érintett. Geográfiai elterjedése nagyjából a malária elterjedését követi, hasonlóan a sarlósejtes anémiához. • A leggyakoribb hemoglobinopátia a sarlósejtes anémia elsősorban az afrikai származású fekete bőrű, az arab és a dél-indiai populáció körében fordul elő. Szintén autoszomális, domináns módon öröklődik. • Az akutan jelentkező autoimmun hemolítikus anémia (AIHA) ritka, nőknél valamivel gyakoribb előfordulású, incidenciája 1 -3/10000/év. Az AIHA kb. 80%-át meleg antitest okozza.

Elsődleges laborvizsgálatok hemolízisben • • perifériás vérkenetben módosult, sérült morfológiájú vörösvértestek megjelenése szérum laktát dehidrogenáz (LDH, 1 és 2 típusú) emelkedés szérum vas emelkedés szérum haptoglobin csökkenés szérum indirekt bilirubin emelkedés direkt, indirekt antiglobulin teszt (Coombs teszt) pozitivitás a legtöbb AIHA-ban teljes vérképben az abszolút ill. korrigált retikulocita-szám növekedés, szferocitózis a legjellemzőbb (MCHC↑, MCV↑) A hirtelen induló hemolízisben, a csontvelőt illetve az eritropoezist is érintő folyamatokban a retikulocitózis elmarad. • hideg agglutinin kimutatása: hideg típusú AIHA-ban (1: 1000 feletti titer).

Intravaszkuláris hemolízist megerősítő vizsgálatok • plazma szabad hemoglobin jelenléte (hemoglobinémia) • vizeletben szabad hemoglobin megjelenése (hemoglobinuria) • a vizeletben hemosziderin tartalmú tubulushám sejtek megjelenése a hemolízist követő > 7 nap múlva (hemosziderinuria)

Akut hematológiai prognózist befolyásoló faktorok • • • invazív lélegeztetés igénye invazív gombafertőzés csontvelő transzplantáció utáni állapot többszervi elégtelenség foka (MODS score) az intenzív ellátást megelőző kórház kezelés hossza

Az intenzív osztályos felvétel indikációja hematiológiai betegnél

Empírikus terápia hematológiai betegségekben • • empírikus terápia: Pseudomonas ellenes β-laktám monoterápia Az empírikus terápia kiegészíthető a klinikai kép alapján (sokk, pneumonia stb. ) vagy rezisztens kórokozó által kiváltott fertőzés gyanúja esetén. Rutin vancomycin terápia nem javasolt. Vancomycin adása elsősorban katéter-szepszis, bőr-, és lágyrészfertőzés, sokk, illetve pneumónia esetén ajánlott A kezdeti terápia módosítása a klinikai kép és tenyésztési eredmények alapján történjen. Instabil állapot indokolja a terápiás spektrum szélesítését. Klinikailag illetve mikrobiológiailag igazolt fertőzés esetén a klinikai kép illetve a kórokozó alapján javasolt megválasztani a terápia hosszát, de a legalább a neutropenia rendeződéséig (ANC > 500/mm 3). Ismeretlen eredetű láznál a terápia folytatása a neutropenia rendeződéséig (ANC > 500/mm 3) javasolt. Gombaellenes kezelés elindítása 4 -7 napos antibiotikus kezelés ellenére perzisztáló/rekurráló láz esetén megfontolandó. Szintén megfontolandó olyan betegeknél, ahol a neutropénia időtartama előreláthatólag meghaladja a 7 napot.

Terápiás aferezissel eltávolítható anyagok

A terápiás aferezis indikációi

A vérkészítmények felosztása típus készítmény vörösvérsejt koncentrátum sejtes készítmények trombocita koncentrátum fehérvérsejt koncentrátum sejtszegény vagy sejtmentes készítmények plazma (elsősorban friss fagyasztott) véralvadási faktorkészítmények stabil (humán plazmából készített) vérkészítmények* albumin *alkalmazásuk nem tartozik szigorúan a hemoterápia csoportba, így jelen fejezet nem tér ki rájuk részletesen immunglobulin készítmények

Speciális technikával előállított vérkészítmények mosott/közegcserélt/helyreállított Fehérjementesített, minimális plazmafehérjét tartalmazó, izotóniás nátrium-klorid oldatban, vagy speciális tároló oldatban reszuszpendált sejtes vérkészítmény. fehérvérsejt-mentesített/szűrt Szűréssel vagy aferezissel állítják elő. Csökkenti a lázas, nem hemolítikus transzfúziós reakciót; a HLA allo-immunizációt, CMV átvitelt, transzfúzió asszociált immunmodulációt, a tüdőkárosodás mértékét kardiopulmonális bypass alatt és után. besugarazott Limfocita osztódás megakadályozására 25– 50 Gray sugárdózissal kezelt vérkészítmény. Csökkenti a transzfúzió-asszociált GVH reakciót. Csökkent celluláris immunitás esetén javasolt.

Vörösvérsejt transzfúzió indikációja: A vér oxigénszállító kapacitásának növelése. (ld. : SN_XIV_1_fejezet) Vörösvérsejt transzfúzió kontraindikációja: Minden olyan esetben, amikor az anaemia gyógyszeres kezeléssel rendezhető. Vörösvérsejt transzfúzió alternatívái: • anaemia okának tisztázása, annak megfelelő oki terápia • Erithropoetin: a gyógyszer-előirat kizárólag a krónikus veseelégtelenség illetve kemoterápia következtében kialakult csontvelő depresszió miatti anémiát jelöli meg az indikációs körben. Transzfúziós válaszkészség: Egy egység vörösvérsejt koncentrátumtól várható haematokrit-emelkedés 3%, hemoglobinemelkedés 1 g/dl.

Kompatibilis vérkészítmény kiválasztása

Plazma készítmények FFP – friss fagyasztott plazma A vérdonáció során a frissen levett vérből nyerik a vörösvérsejt, a fehérvérsejt és a trombocita elkülönítésével (buffy-coat) vagy aferezissel. Fagyasztva tárolják, és beadás előtt olvasztják fel. Felolvasztás után 24 órán belül szükséges beadni, különben az V. és VIII. faktor szintje csökken. A leggyakrabban használt plazmakészítmény, mivel feljavítja az összes alvadási faktor szintjét. AB 0 kompatibilitás szükséges, de keresztpróba és Rh azonosság nem szükséges. Az alap-vérkészítményből speciális technikával kombinációban is előállítható vérkészítmények: sejtszegény, osztott, besugarazott. Krioprecipitátum Kiolvasztott FFP készítményből 4 0 C-on eltávolítják a felülúszót (csapadékot). Gazdag von Willebrand, VIII és XIII faktorban valamint fibrinogénben. Előnye, hogy a fenti alvadási faktorokat kisebb volumenterheléssel lehet bejuttatni, mintha azokat FFPvel pótolnánk. AB 0 kompatibilitás nem feltétlenül szükséges, de ha van rá mód, kompatibilis készítmény adandó. Faktor koncentrátum Nagy mennyiségű speciális faktortartalmú készítmény, amit vagy rekombináns technológiával vagy sok donortól gyűjtött vérkészítményből állítanak elő. Stabil, vírusinaktivált gyógyszerkészítmények, plazmafrakcionáló-eljárással készülnek az FFPből gyógyszergyári körülmények között. A rekombináns technológiával előállított készítmény virális kontaminációtól mentes. • PCC Prothrombin komplex koncentrátum. II, VII, IX és X faktor, valamint protein C és S tartalom. • APCC Aktivált protrombin komplex koncentrátum. In vitro aktivált PCC, magas koncentrációban tartalmaz aktivált és precursor K vitamin dependens alvadási faktorokat. • Fibrinogén Humán plazmából előállított, nagy tisztaságú fibrinogen (I faktor) koncentrátum. Human albumin (5% és 20%-os oldat): humán plazmafehérje. Intravénás immunglobulin (Iv. Ig) Sok donortól vett vérből előállított, tisztított immunglobulin-készítmény.

Friss fagyasztott plazma adása • • Klinikai tünetekkel járó (aktív vérzés), nem izolált alvadási faktor-hiány, amennyiben megfelelő véralvadási-faktorkoncentrátum nem áll rendelkezésre (pl. májbetegek szerzett, szekunder hemostasis zavara). Masszív transzfúzió (vörösvérsejt koncentrátum), koagulációs faktorok várható dilúciója miatt. Orális antikoaguláns túladagolása miatti vérzés (SN_XIV_10_7_tablazat) K-vitaminhiányos beteg súlyos vérzése, illetve akut műtéti beavatkozás esetén, Kvitaminpótlással együtt. Vérzésveszéllyel járó sebészeti beavatkozás (mellkasi, hasi, spinalis, intracranialis, bizonyos urológiai műtétek), amennyiben a betegnek véralvadási zavara van (INR, PTT). Alacsony vérzésveszéllyel járó invazív beavatkozások előtt (endoszkópia, szívkatéterezés, centrális kanül bevezetés, stb. ), amennyiben a beteg véralvadási zavara súlyos (INR >2, PTT >2* a kontrollnak). V és XI faktorhiány, amennyiben nincs elérhető speciális faktorkoncentrátum. Plazmapótlás plazmaferezisnél (pl. TTP, HUS).

FFP és PCC adag számítása

FFP kompatibilitás AB 0 egyező plazma A recipiens és a plazma (donor) vércsoportja azonos. AB 0 kompatibilitás Nem feltétlenül azonos a recipiens és a plazma (donor) vércsoportja (anti. A és anti. B antitestek jelenléte). • AB recipiens csak AB plazmát • A recipiens A és AB plazmát • B recipiens B és AB plazmát • 0 recipiens 0, A, B és AB plazmát kaphat.

Trombocita készítmények trombocita koncentrátum Teljes véregységek feldolgozásából vagy aferezis útján előállított trombocita-szuszpenzió. poolozott koncentrátum (többegységes) Olyan trombocita készítmény, amely legalább négy egység egyedi trombocita koncentrátum egyesítésével keletkezik, vagy amelyet legalább négy egység egyesített határrétegből (buffycoat) állítanak elő. egyedi trombocita koncentrátum Aferezissel nyert (fehérvérsejt-mentesített) trombocita készítmény.

Transzfúzió okozta fertőzésveszély

A vírusfertőzés becsült kockázata
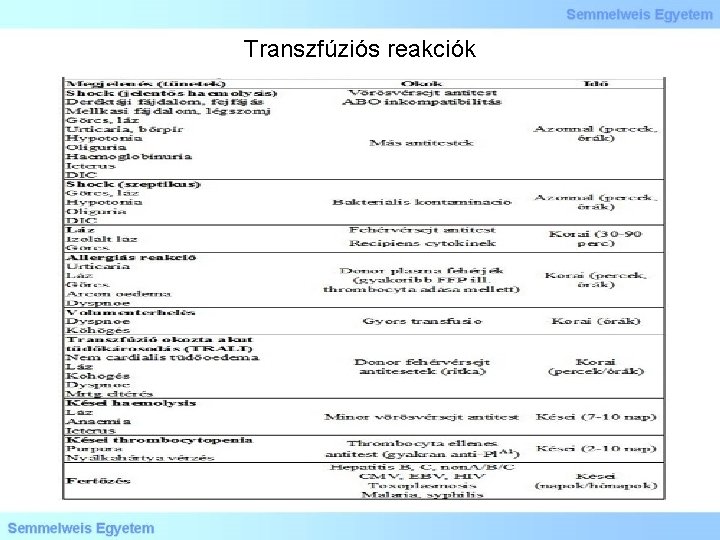
Transzfúziós reakciók

A transzfúziós reakciók kezelése
- Slides: 37