Heiluftballon Der aufsteigende Heiluftballon nutzt Wrme um Hubarbeit

Heißluftballon Der aufsteigende Heißluftballon nutzt Wärme, um Hubarbeit zu verrichten Das Volumen des Ballons beträgt etwa 4000 m 3. Ein Teil der erwärmten Luft entweicht, wobei die Auftriebskraft gleich der Gewichtskraft der verdrängten Luft ist.

Aggregatzustände Beschreibung durch mikroskopisches Modell Wärme spielt auch bei den Aggregatzuständen eine wichtige Rolle
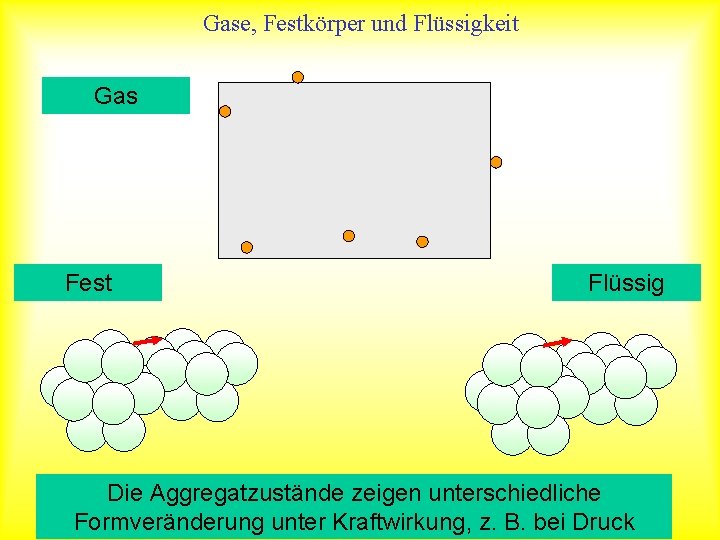
Gase, Festkörper und Flüssigkeit Gas Fest Flüssig Die Aggregatzustände zeigen unterschiedliche Formveränderung unter Kraftwirkung, z. B. bei Druck
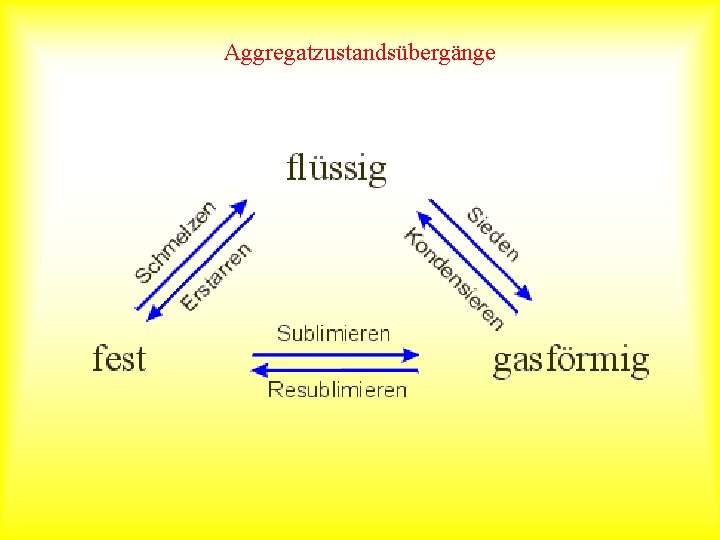
Aggregatzustandsübergänge

Aggregatzustände Wärme spielt auch bei den Aggregatzuständen eine Rolle. Wasser existiert als Eis, in flüssiger Form und als Wasserdampf. Für Übergänge zwischen zwei Aggregatzuständen gibt es Fachbegriffe wie ‘schmelzen’ und ‘erstarren’ Kohlendioxid zeigt einen direkten Übergang von gasförmig nach fest (Trockeneis: -650 C aus Druckflasche)

Spezifische Übergangswärme Normaler Weise ändert sich bei Zuführung oder Entzug von Wärme die Temperatur des Materials. Beim Übergang von Aggregatzuständen wird Energie zugeführt aber die Temperatur bleibt konstant. Erst wenn alles Eis geschmolzen ist, steigt die Temperatur wieder. qs=spezifische Schmelzwärme
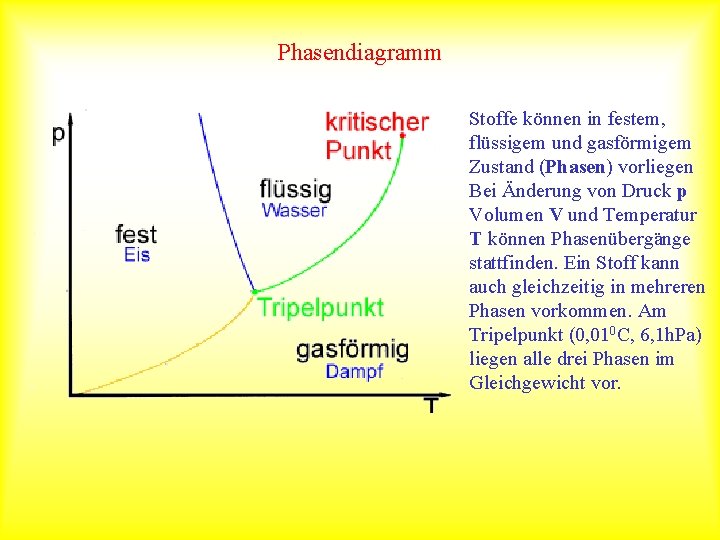
Phasendiagramm Stoffe können in festem, flüssigem und gasförmigem Zustand (Phasen) vorliegen Bei Änderung von Druck p Volumen V und Temperatur T können Phasenübergänge stattfinden. Ein Stoff kann auch gleichzeitig in mehreren Phasen vorkommen. Am Tripelpunkt (0, 010 C, 6, 1 h. Pa) liegen alle drei Phasen im Gleichgewicht vor.
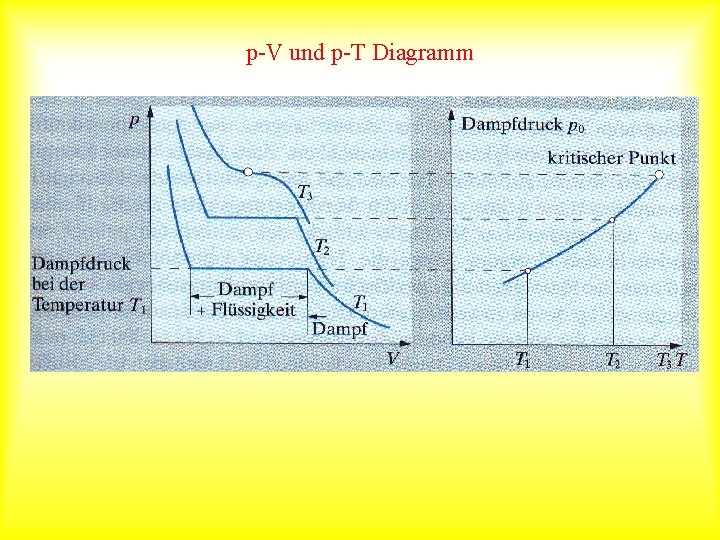
p-V und p-T Diagramm

Spezifische Wärmekapazität Einzelner Aggregatzustand Zufuhr von Wärme bewirkt eine proportionale Temperaturerhöhung. Die Materialkonstante c wird spezifische Wärmekapazität genannt. Beispiel: Nachtspeicheröfen mit Magnesitsteinen
![Wärmemenge Stoff c in [J K-1 kg-1] Aluminium 897 Eisen 452 Beton 922 Wasser Wärmemenge Stoff c in [J K-1 kg-1] Aluminium 897 Eisen 452 Beton 922 Wasser](http://slidetodoc.com/presentation_image_h2/19f508c64418667a25f2e0f478c86480/image-10.jpg)
Wärmemenge Stoff c in [J K-1 kg-1] Aluminium 897 Eisen 452 Beton 922 Wasser 4180 Eis 2100 Wasserdampf 1390 Luft Wasserstoff 716 10100 Da Wasser eine sehr hohe spezifische Wärmekapazität hat, eignet es sich gut als Wärmespeicher. Beispiel: Welche Menge an Wärmeenergie ist nötig, um 220 Liter Badewasser von T 1=180 C auf eine Temperatur von T 2=320 C zu erwärmen?

Bestimmung der spezifischen Wärmekapazität Man erwärmt zunächst den Körper der Masse m. K z. B. in einem Wasserbad auf eine genau definierte Ausgangstemperatur TK. Anschließend bringt man den warmen (trockenen!) Körper in ein mit Wasser (Masse m. W) gefülltes Kalorimeter mit der Ausgangstemperatur TW. Nach dem Temperaturausgleich mißt man die Endtemperatur TE des Wassers, die mit dem Körper identisch ist. Man vernachlässigt evtl. auftretende Wärmezugänge bzw. –abgänge.

1. Hauptsatz der Wärmelehre Wärme erhöht die Temperatur des Kesselwassers (innere Energie) und verrichtet Arbeit. Die mittlere Geschwindigkeit der Gasmoleküle ist ein Maß für die Temperatur des Gases. Die zugehörige Energie heißt innere Energie U. Wird das Gas erhitzt, dann verschiebt sich der Kolben nach außen und es wird Arbeit verrichtet. Innere Energie = Arbeit + Wärme
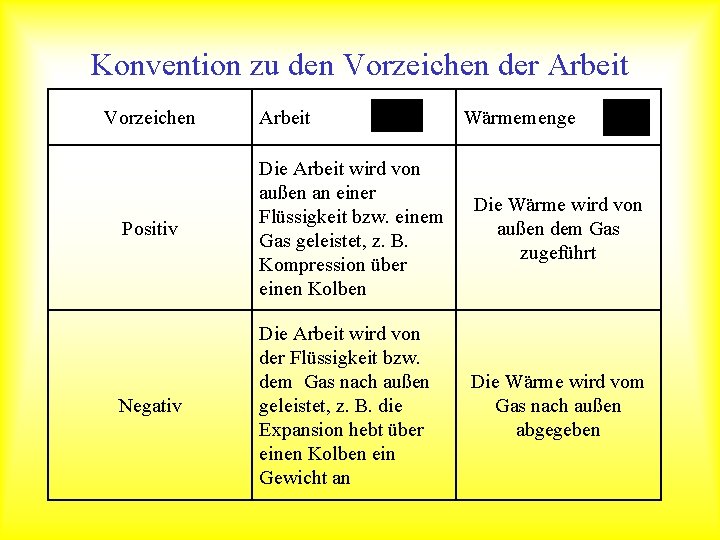
Konvention zu den Vorzeichen der Arbeit Vorzeichen Arbeit Wärmemenge Positiv Die Arbeit wird von außen an einer Flüssigkeit bzw. einem Gas geleistet, z. B. Kompression über einen Kolben Die Wärme wird von außen dem Gas zugeführt Negativ Die Arbeit wird von der Flüssigkeit bzw. dem Gas nach außen geleistet, z. B. die Expansion hebt über einen Kolben ein Gewicht an Die Wärme wird vom Gas nach außen abgegeben
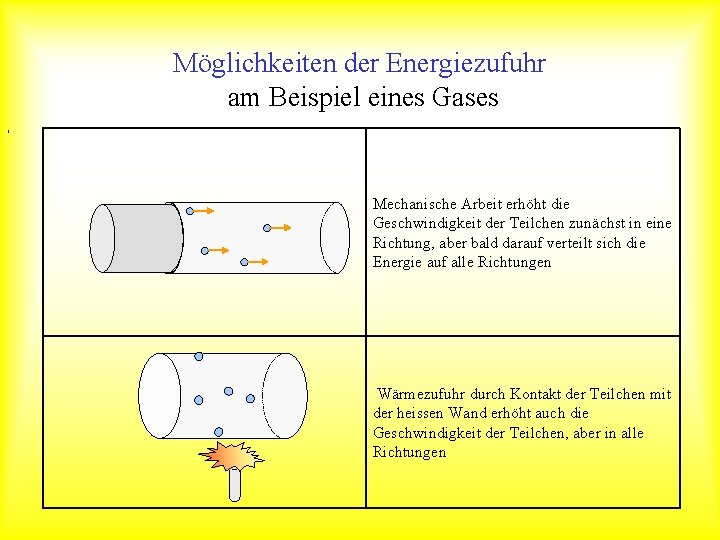
Möglichkeiten der Energiezufuhr am Beispiel eines Gases , Mechanische Arbeit erhöht die Geschwindigkeit der Teilchen zunächst in eine Richtung, aber bald darauf verteilt sich die Energie auf alle Richtungen Wärmezufuhr durch Kontakt der Teilchen mit der heissen Wand erhöht auch die Geschwindigkeit der Teilchen, aber in alle Richtungen
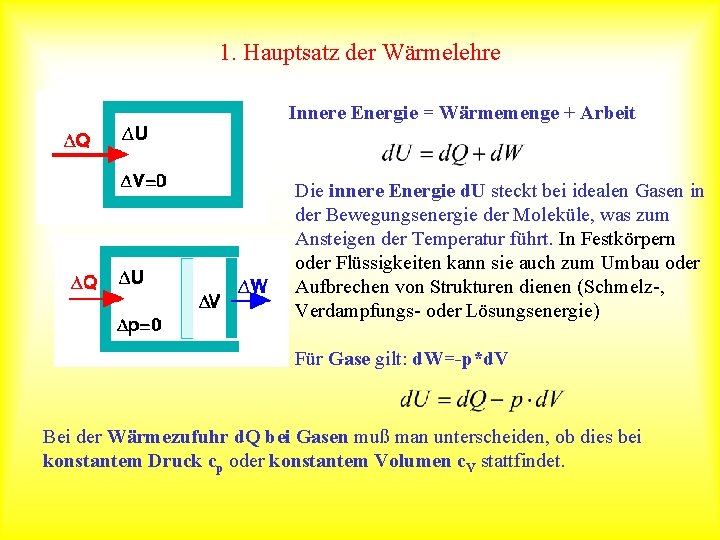
1. Hauptsatz der Wärmelehre Innere Energie = Wärmemenge + Arbeit Die innere Energie d. U steckt bei idealen Gasen in der Bewegungsenergie der Moleküle, was zum Ansteigen der Temperatur führt. In Festkörpern oder Flüssigkeiten kann sie auch zum Umbau oder Aufbrechen von Strukturen dienen (Schmelz-, Verdampfungs- oder Lösungsenergie) Für Gase gilt: d. W=-p*d. V Bei der Wärmezufuhr d. Q bei Gasen muß man unterscheiden, ob dies bei konstantem Druck cp oder konstantem Volumen c. V stattfindet.
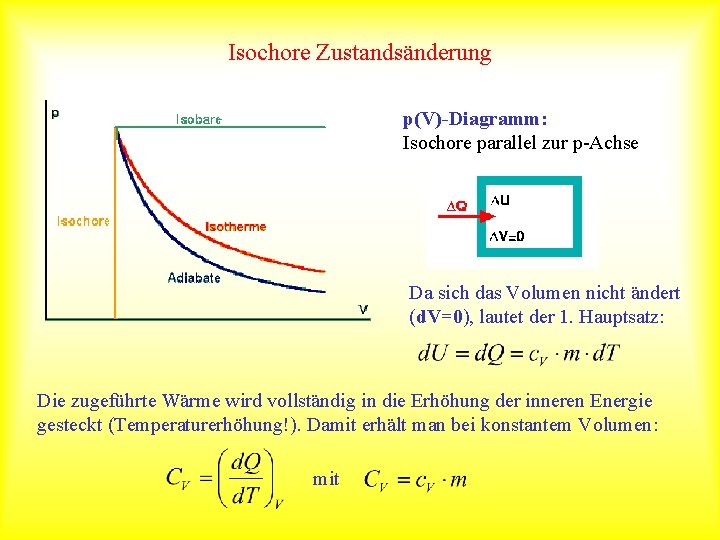
Isochore Zustandsänderung p(V)-Diagramm: Isochore parallel zur p-Achse Da sich das Volumen nicht ändert (d. V=0), lautet der 1. Hauptsatz: Die zugeführte Wärme wird vollständig in die Erhöhung der inneren Energie gesteckt (Temperaturerhöhung!). Damit erhält man bei konstantem Volumen: mit
Isobare Zustandsänderung , Zusätzlich zur Erwärmung wird bei der zur Erhaltung des konstanten Drucks erforderlichen Volumenvergrößerung auch noch Arbeit gegen den Druck verrichtet
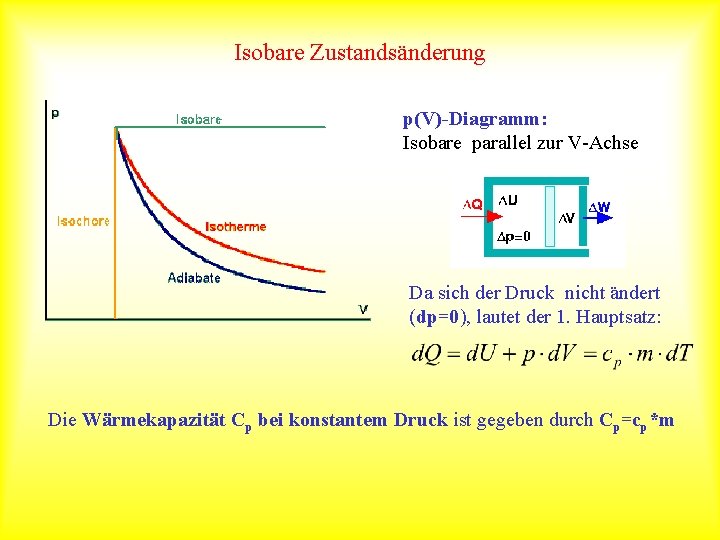
Isobare Zustandsänderung p(V)-Diagramm: Isobare parallel zur V-Achse Da sich der Druck nicht ändert (dp=0), lautet der 1. Hauptsatz: Die Wärmekapazität Cp bei konstantem Druck ist gegeben durch Cp=cp*m
![Zusammenhang zwischen Cp und CV Druckarbeit wegen cp [J K-1 kg-1] c. V [J Zusammenhang zwischen Cp und CV Druckarbeit wegen cp [J K-1 kg-1] c. V [J](http://slidetodoc.com/presentation_image_h2/19f508c64418667a25f2e0f478c86480/image-19.jpg)
Zusammenhang zwischen Cp und CV Druckarbeit wegen cp [J K-1 kg-1] c. V [J K-1 kg-1] Cp [J K-1 mol-1] CV [J K-1 mol-1] Cp-CV [J K-1 mol-1] 40 Ar 0, 523 0, 318 20, 898 12, 703 8, 195 20 Ne 1, 021 0, 624 20, 614 12, 586 8, 028 4 He 5, 232 3, 210 20, 944 12, 849 8, 095
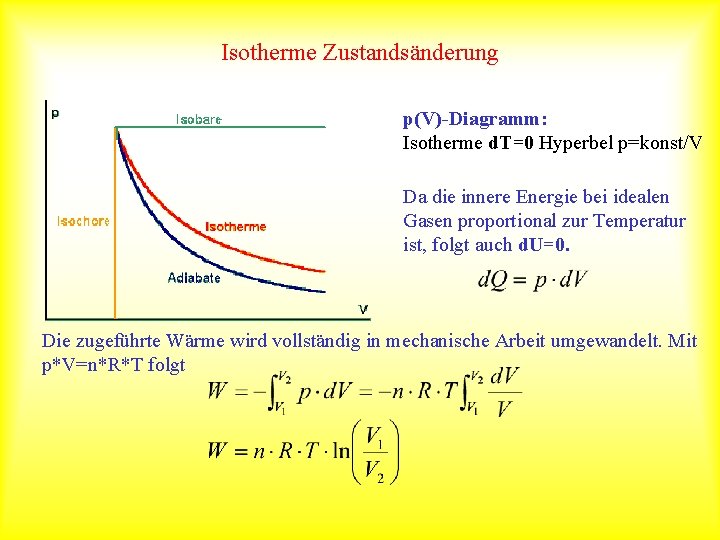
Isotherme Zustandsänderung p(V)-Diagramm: Isotherme d. T=0 Hyperbel p=konst/V Da die innere Energie bei idealen Gasen proportional zur Temperatur ist, folgt auch d. U=0. Die zugeführte Wärme wird vollständig in mechanische Arbeit umgewandelt. Mit p*V=n*R*T folgt
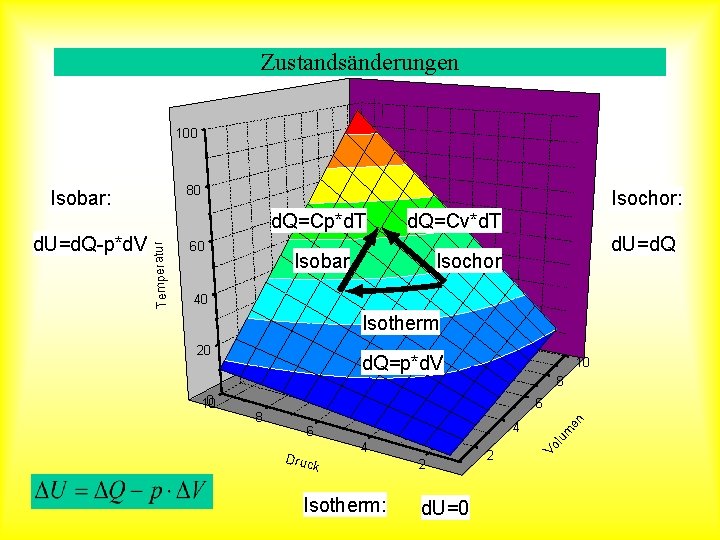
Zustandsänderungen 100 80 Isochor: 60 d. Q=Cv*d. T Isobar d. U=d. Q Isochor 40 Isotherm 20 d. Q=p*d. V 10 8 4 6 Druc k 4 Isotherm: en 6 8 m 0 10 lu d. U=d. Q-p*d. V Temperatur d. Q=Cp*d. T 2 d. U=0 2 Vo Isobar:
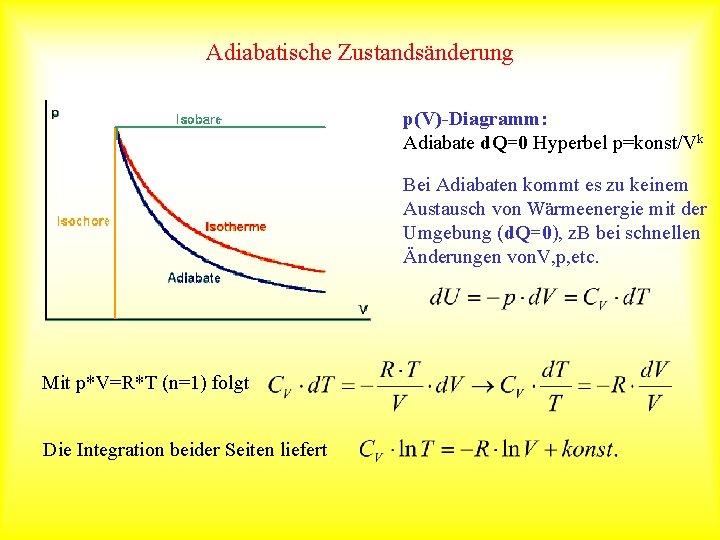
Adiabatische Zustandsänderung p(V)-Diagramm: Adiabate d. Q=0 Hyperbel p=konst/Vk Bei Adiabaten kommt es zu keinem Austausch von Wärmeenergie mit der Umgebung (d. Q=0), z. B bei schnellen Änderungen von. V, p, etc. Mit p*V=R*T (n=1) folgt Die Integration beider Seiten liefert
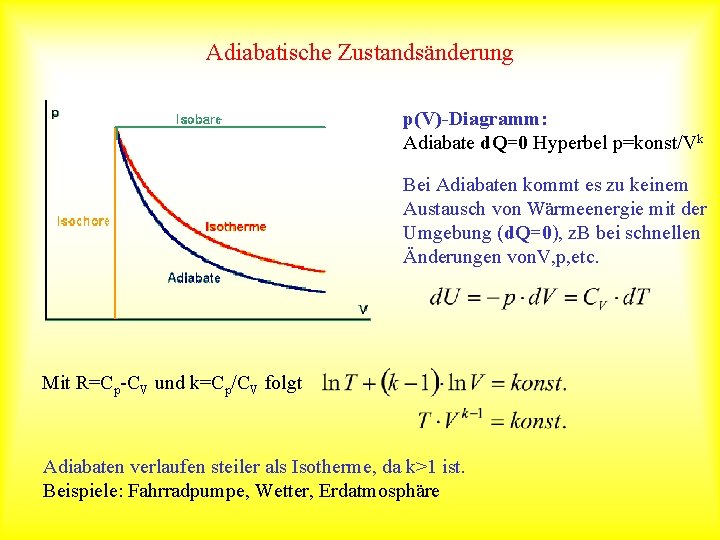
Adiabatische Zustandsänderung p(V)-Diagramm: Adiabate d. Q=0 Hyperbel p=konst/Vk Bei Adiabaten kommt es zu keinem Austausch von Wärmeenergie mit der Umgebung (d. Q=0), z. B bei schnellen Änderungen von. V, p, etc. Mit R=Cp-CV und k=Cp/CV folgt Adiabaten verlaufen steiler als Isotherme, da k>1 ist. Beispiele: Fahrradpumpe, Wetter, Erdatmosphäre

Beispiel adiabatischer Zustandsänderung Bei diesem Vorgang wird dem Gas weder Wärme zugeführt noch entzogen (d. Q=0) Beispiel: schnelle Komprimierung der Luft. Es gilt eines Gases sind. mit wobei f die Freiheitsgrade 2 -atomige Moleküle N 2 und O 2 (2 Rotationsfreiheitsgrade): f=5, dh. k=7/5 Volumenkompression bei Zimmertemperatur um Faktor 10:

2. Hauptsatz der Thermodynamik Der 2. Hauptsatz beschäftigt sich mit der Umwandlung von Wärme in Arbeit. Er beantwortet die Fragen: • In welcher Richtung laufen Umwandlungsprozesse von mechanischer Energie und Wärmeenergie ab? • Kann Wärmeenergie vollständig in mechanische Arbeit umgewandelt werden? • Kann mechanische Arbeit vollständig in Wärmeenergie umgewandelt werden? Aus Beobachtungen ist bekannt, daß Umwandlungsprozesse nicht-umkehrbar (irreversibel) ablaufen: • Wärme fließt immer vom wärmeren zum kälteren Körper • Reibung wandelt kinetische Energie in Wärmeenergie um

2. Hauptsatz der Thermodynamik Der 2. Hauptsatz beschreibt wie der erste eine Erfahrungstatsache und läßt sich wie folgt zusammenfassen: • Wärme fließt von selbst stets vom wärmeren zum kälteren Körper, nie umgekehrt. • Es gibt keine periodisch arbeitende Maschine, die einem Reservoir Wärme entzieht und diese ohne Energiezufuhr von außen vollständig in mechanische Arbeit umwandelt. • Es gibt kein perpetuum mobile zweiter Art.
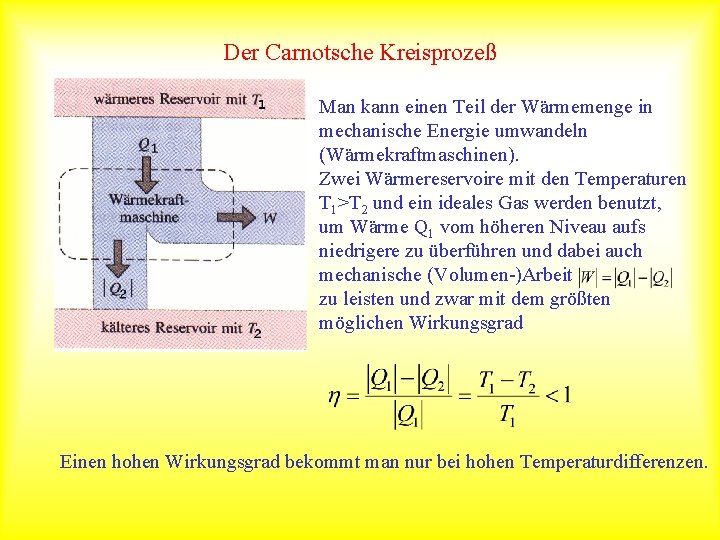
Der Carnotsche Kreisprozeß Man kann einen Teil der Wärmemenge in mechanische Energie umwandeln (Wärmekraftmaschinen). Zwei Wärmereservoire mit den Temperaturen T 1>T 2 und ein ideales Gas werden benutzt, um Wärme Q 1 vom höheren Niveau aufs niedrigere zu überführen und dabei auch mechanische (Volumen-)Arbeit zu leisten und zwar mit dem größten möglichen Wirkungsgrad Einen hohen Wirkungsgrad bekommt man nur bei hohen Temperaturdifferenzen.

Entropie Die Entropie S ist eine thermodynamische Zustandsgröße, die wie die Temperatur T, Volumen V und Druck p den Zustand eines Systems beschreibt. Sie ist auch ein Maß für die Ordnung bzw. Unordnung eines Systems. Makroskopische Betrachtung Analog zur inneren Energie U interessiert man sich vor allem für die Änderung der Entropie bei thermodynamischen Prozessen. Man definiert Dabei bezeichnet d. Qrev die Wärmemenge, die bei einem reversiblen Prozeß mit der Umgebung ausgetauscht wird. Der Quotient wird auch reduzierte Wärmemenge genannt. Die Änderung der Entropie ist unabhängig vom Weg beim Wechsel eines thermodynamischen Zustands und hängt nur von dessen Anfangs- und Endzustand ab.

Wärmekontakt zweier Körper Beide Körper haben die gleiche Masse m und die gleiche spezifische Wärmekapazität c. Beim Wärmeausgleich wird vom Körper 1 die Wärmemenge abgegeben, die vom Körper 2 aufgenommen wird Mit folgt für die Mischtemperatur des Körpers 1 ist damit Die Entropieänderung Analog für Körper 2 Da T 2<TM<T 1 folgt für die Änderung der Entropie des Gesamtsystems Da nimmt auch die Entropie zu.
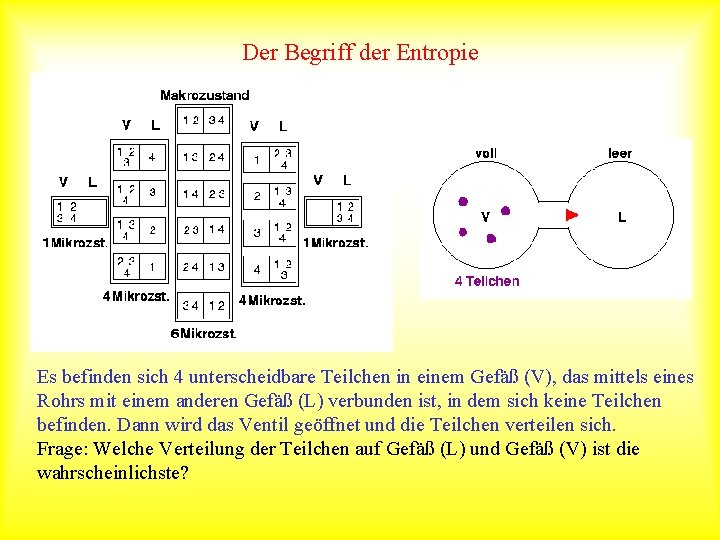
Der Begriff der Entropie Es befinden sich 4 unterscheidbare Teilchen in einem Gefäß (V), das mittels eines Rohrs mit einem anderen Gefäß (L) verbunden ist, in dem sich keine Teilchen befinden. Dann wird das Ventil geöffnet und die Teilchen verteilen sich. Frage: Welche Verteilung der Teilchen auf Gefäß (L) und Gefäß (V) ist die wahrscheinlichste?

Entropie (mikroskopisch) Einen anderen Zugang zur Entropie erschließt die Statistik. Dazu betrachtet man zum Beispiel die freie Expansion eines Gases vom Volumen V 0 auf 2*V 0. Wie groß ist nach der Expansion die Wahrscheinlichkeit W 10 daß sich 10 Teilchen wieder in V 0 befinden? Wie groß ist nach der Expansion die Wahrscheinlichkeit W 50 daß sich 50 Teilchen wieder in V 0 befinden? Nun verallgemeinern wir die Betrachtung und gehen von der freien Expansion eines Gases vom Volumen V 1 in ein Volumen V 2 aus.

Entropie (mikroskopisch) Die Wahrscheinlichkeit W 1, daß sich nach der freien Expansion wieder alle N Moleküle des Gases im Volumen V 1 befinden und damit der Ausgangszustand wieder hergestellt ist, beträgt Im Endzustand müssen sich alle Teilchen im Volumen V 2 aufhalten und die Wahrscheinlichkeit ist damit W 2=1. Es gilt nun für das Verhältnis der Ausgangswahrscheinlichkeit W 1 und der Wahrscheinlichkeit im Endzustand W 2 (thermodynamisches Wahrscheinlichkeitsverhältnis):

Entropie (mikroskopisch) Um bei Teilchenzahlen von Zahlen vernünftiger Größenordnung zu erhalten, logarithmiert man die Gleichung und erhält Mit Hilfe eines reversiblen Ersatzprozesses, bei dem das ideale Gas in einem Zylinder mit beweglichem Kolben isotherm vom Volumen V 1 auf das Endvolumen V 2 entspannt wird, kann die Entropieänderung berechnet werden. Dazu verwendet man den 1. Hauptsatz und die Beziehung

Entropie (mikroskopisch) Der Vergleich beider Gleichungen zeigt den von Ludwig Boltzmann gefundenen Zusammenhang zwischen der Änderung der Entropie und dem thermodynamischen Wahrscheinlichkeitsverhältnis: Dabei bezeichnet k den Boltzmann-Faktor. Für die Entropie selbst gilt wobei W die Wahrscheinlichkeit angibt, mit der ein thermodynamischer Zustand realisiert ist. Die Entropie ist ein Maß für die Wahrscheinlichkeit eines Zustands oder den Grad der Unordnung.

Entropie und der 2. Hauptsatz Jedes isolierte System strebt nach einem Zustand, in dem die Anzahl realisierbarer Zustände größer ist als zu Beginn (Entropiezunahme). Da ein System von selbst nie in einen bedeutend unwahrscheinlicheren Zustand übergeht, wie es der 2. Hauptsatz formuliert, ergeben sich folgende Regeln für die Entropieänderung: 1. Bei beliebigen Prozessen, in denen ein thermisch isoliertes System von einem Makrozustand in einen anderen übergeht, ist die Änderung der Entropie stets größer gleich Null. Damit ist bei Systemen, die sich nicht im Gleichgewicht befinden, die Richtung definiert, in der eine Zustandsänderung abläuft. 2. Bei reversiblen Kreisprozessen bleibt die Entropie konstant.

Beispiele 1. Reversibler Kreisprozess (Carnot’scher Kreisprozess) Die reduzierte Wärmemengen ändern sich nur auf den Isothermen, da es auf den Adiabaten zu keinerlei Wärmeaustausch kommt Bei der Betrachtung des Carnot’schen Kreisprozesses wurde gezeigt: Damit ergibt sich sofort: 2. Isotherme freie Expansion eines Gases (Diffusion) Öffnet man den Deckel eines mit Gas gefüllten Behälters in einem Raum (V 2), dann entweicht das gas und diffundiert in der Umgebung. Für die Entropieänderung des Systems gilt bei der Expansion von V 1 nach V 2

Fragen zur Wärmeenergie 1. 2. 3. 4. 5. 6. Welche Wärmemenge Q ist nötig, um einen Kochtopf aus Eisen (m=0, 6 kg) von 200 C auf 1000 C zu erhitzen (c. Fe=452 JK-1 kg-1) ? Eine Stahlkugel der Masse m 1=2 kg fällt aus einer Höhe von 10 m auf einen Aluminiumklotz der Masse m 2=0, 1 kg. Wie groß ist die Temperaturzunahme des Aluminiumklotzes (c. Al=897 JK-1 kg-1) ? Welche Leistung muß ein Tauchsieder haben, um 5 Liter Wasser von 150 C in 6 Minuten auf 800 C zu erwärmen (c. Wasser=4180 JK-1 kg-1) ? Welche Wärmemenge Q muß 5 Liter Wasser zugeführt werden, um es von -180 C auf 600 C zu erwärmen (c. Eis=2100 JK-1 kg-1, c. Wasser=4180 JK-1 kg-1 und qs=3, 33*105 J/kg) ? Um welchen Betrag steigt die Temperatur eines künstlichen Erdsatelliten im Mittel, wenn er beim Eintauchen in die Atmosphäre von v 1=5000 m/s auf v 2=1000 m/s abgebremst wird (spez. Wärmekapazität des Satelliten c=900[J/kg. K], 80% der Wärme wird an die umgebende Luft abgegeben)? Welche Wärmemenge entsteht beim Abbremsen eines Pkw’s der Masse m=800 kg aus v 0=72 km/h zum Stillstand?
- Slides: 37