HAYVANCILIKTA BYOTEKNOLOJ Do Dr Uur EN nvitro Embriyo

HAYVANCILIKTA BİYOTEKNOLOJİ Doç. Dr. Uğur ŞEN

İn-vitro Embriyo Üretimi (IVEP) üGünümüzde hayvan ıslahı ile ilgili olarak çok sayıda biyoteknolojik yöntem kullanılmaktadır. üBunlardan başlıcası, suni tohumlama ve süperovulasyonla birlikte gerçekleştirilen embriyo transferidir. üAncak 1980’li yıllardan itibaren in-vitro fertilizasyon tekniği de bu konuda uygulama alanı bulmuştur. üGünümüzde, dünyada üretilen embriyoların %15 kadarını in-vitro koşullarda üretilen embriyolar oluşturmaktadır. üIslah çalışmalarının yanı sıra, konuyla ilgili bilimsel çalışmalarda da çok sayıda embriyo kullanılmaktadır. üDolayısıyla embriyo üretiminin artırılması açısından biyoteknolojik yöntemler geliştirilmesinin önemi ortaya çıkmaktadır. üİn vitro embriyo üretim teknikleri sayesinde mezbahada kesilen hayvanlardan veya üstün genetik karakterli hayvanlardan çok sayıda oosit toplanarak laboratuvarda embriyo elde edilebilmektedir. Bu metotlar sayesinde prepubertal hayvanlardan, gebe ve genital kanallarında fizyolojik bozukluklara sahip hayvanlardan da yararlanmak olasıdır. ü

üHayvansal biyoteknoloji konusunda sağladığı büyük avantaja rağmen pek çok laboratuarda in-vitro sığır embriyosu elde etme oranı %25 -50 arasında kalmaktadır. Bunun başlıca nedeni kültür koşullarının ve in-vitro oosit maturasyonunun önündeki problemlerin tam olarak aşılamamış olması ve in vivo şartların tam olarak bilinememesinden kaynaklanmaktadır. Henüz başarı düzeyi tatmin edici olmasa da in-vitro embriyo üretimi gelişmiş ülkelerin pek çoğunda hayvan ıslahındaki yerini çoktan almıştır. Hayvansal gıdalardan yararlanma oranının gelişmiş ülkelere kıyasla oldukça düşük kaldığı ülkemizde, hayvansal protein açığını kapatmak için bu gibi tekniklerin hayvancılığa verebileceği katkılar göz ardı edilmemelidir. ü ü ü

İn-vitro Embriyo Üretimi; ØOosit (COCs) toplanma (canlı veya kesilmiş hayvandan) ØIVM; İn vitro maturasyon (olgunlaşma) ØFertilizasyonda kullanılacak spermanın hazırlanması ØSwim-up ØPercoll Gradient ØIVF; İn vitro fertilizasyon (dölleme) ØIVC; İn vitro kültür (embriyo gelişimi)

üİn-vitro embriyo üretiminde Kumulus Oosit Komleksleri (COCs) şekilde toplanmaktadır ovaryumlardan iki 1. Mezbahanede kesilmiş hayvanların ovaryumları alınarak üzerlerindeki folliküllerin şırınga ile aspire edilerek COCs toplama 2. Canlı hayvanda süper ovulasyon sonrası veya normal kızgınlık döngüsünde COCs toplama ovum pick-up yöntemiyle

üMezbahada kesilen hayvanlardan alınan ovaryumlar termos içersindeki 32– 35 °C sıcaklıktaki serum fizyolojik (0. 9% w/v Na. Cl) içersine konulur üLaboratuara ulaştırılan ovaryumların üzerindeki 2– 6 mm çapındaki folliküllerin içerisindeki COCs’lar içersinde bir miktar doku kültür medyumu (TCM 199 -Hepes tamponlu) bulunan şırınga (10 ml’lik ve 18

üCanlı hayvanlarda ise çeşitli hormon muameleleri ile (özellikle FSH) süperovulasyon yapılmış hayvanlara oviduct yıkaması (flush) yapılarak oositler toplanır üYada, ultrason cihazı kullanılarak ovum pick -up yöntemiyle ovaryumlardaki 2 -10 mm çapındaki follliküller aspire edilir.

Ovum pick-up yönteminde, üOvaryumu gözlemek, follikülleri tespit etmek ve oosit aspirasyonunu gerçekleştirmek için ultrason cihazı (Pie med. /Aquila) kullanılmaktadır. üUltrason cihazına 7. 5 MHz dalga boyunda çalışan, konveks prob (R 10, endocavity 150 o), bu probun ve aspirasyon iğnesinin yerleştirildiği özel prob ataçmanı (Resim 1), vakum pompası ve oositleri toplayıp işlem bitene dek korumak amacıyla su banyosu düzeneğinden oluşan bir sistem eklenmektedir (Resim 2).
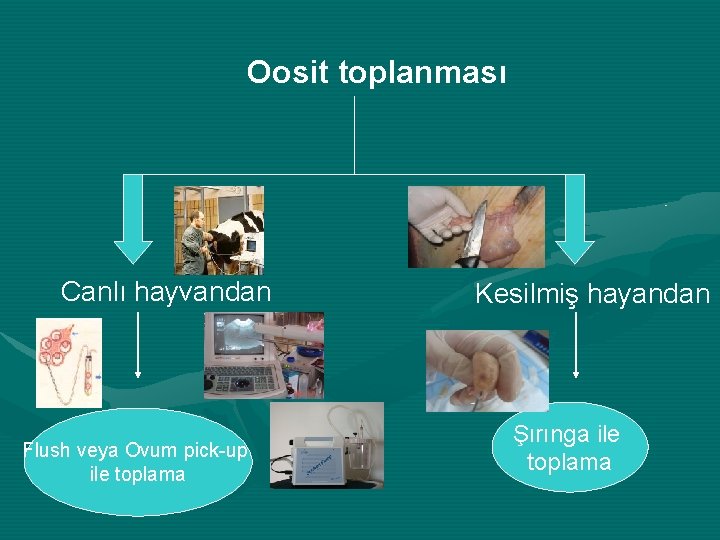
Oosit toplanması Canlı hayvandan Flush veya Ovum pick-up ile toplama Kesilmiş hayandan Şırınga ile toplama
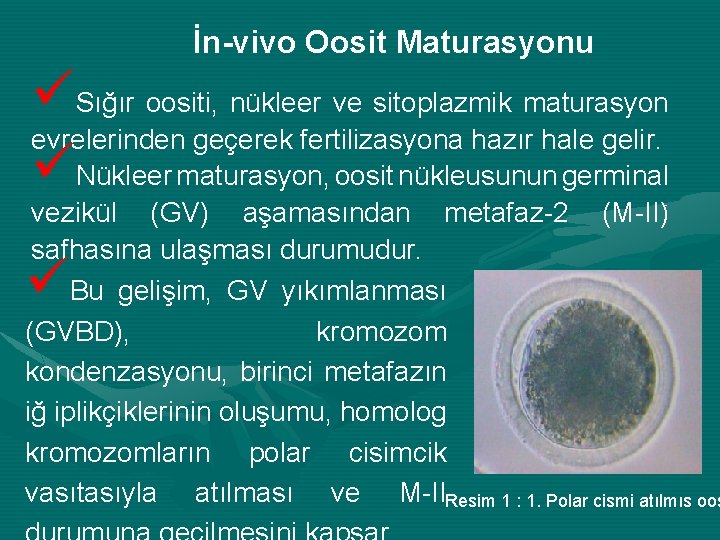
İn-vivo Oosit Maturasyonu üSığır oositi, nükleer ve sitoplazmik maturasyon evrelerinden geçerek fertilizasyona hazır hale gelir. üNükleer maturasyon, oosit nükleusunun germinal vezikül (GV) aşamasından metafaz-2 (M-II) safhasına ulaşması durumudur. Bu gelişim, GV yıkımlanması (GVBD), kromozom kondenzasyonu, birinci metafazın iğ iplikçiklerinin oluşumu, homolog kromozomların polar cisimcik vasıtasıyla atılması ve M-IIResim 1 : 1. Polar cismi atılmıs oos ü

İn-vivo Oosit Maturasyonu üSitoplazmik maturasyon ise, oositin GV safhasından M-II safhasına, olgun bir oosit oluncaya kadar geçirmiş olduğu değişimleri ifade eder. Bu değişimler, oositin normal fertilizasyonu, bölünmeye başlaması ve blastosist safhasına kadar ulaşmasında indirekt olarak etkilidir. Maturasyonu destekleyici faktör (Maturation Promotion Factor-MPF), mayoz kilitlenmesi (Meiotic Arrest), foliküler apoptozis, inhibitörler, foliküler sıvı oositin in vivo maturasyonunu az ya da çok etkileyen faktörler arasındadır. ü ü

İn-vitro Oosit Maturasyon Tekniği (IVM) üÇeşitli yöntemler ile elde edilen COCs’lar en az 3 defa TCM 199 -Hepes tamponlu ile yıkanır üDaha sonra, COCs’lar 4 kuyulu kültür petrisinin her bir kuyusunda yaklaşık 30– 40 adet olacak şekilde üzeri mineral yağ ile kaplanmış 500 µl maturasyon medyumuna aktarılır. üMaturasyon medyumu; sodyum bikarbonat tamponlu (2. 2 g/l) TCM 199’a 10% Fötal bovine serum, 5. 5 µg/ml sodyum pürivat ve 1% penisilinstreptomisin (10. 000 U/ml penisilin G, 10. 000 µg/ml

İn-vitro Oosit Maturasyonu üMaturasyon medyumuna aktarılan COCs’lar 38. 5 o. C’de, %5 CO 2 içeren ve %95 oranında neme doyurulmuş inkübatörde 22 -24 saat olgunlaştırmaya bırakılır.
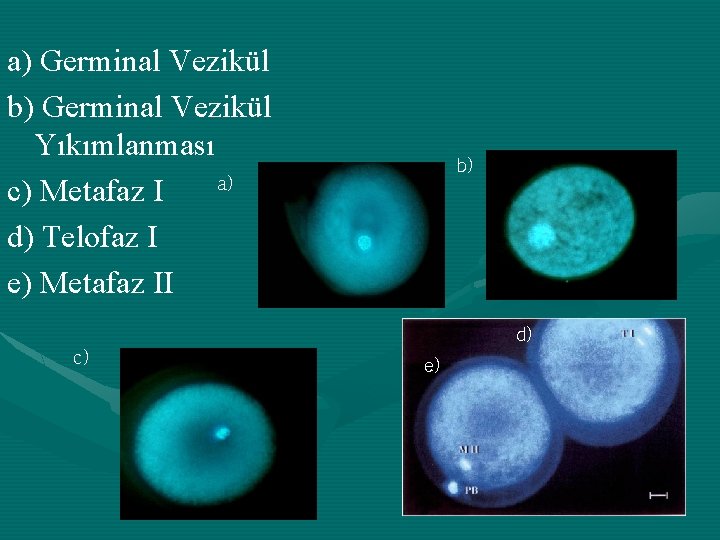
a) Germinal Vezikül b) Germinal Vezikül Yıkımlanması a) c) Metafaz I d) Telofaz I e) Metafaz II c) b) d) e)
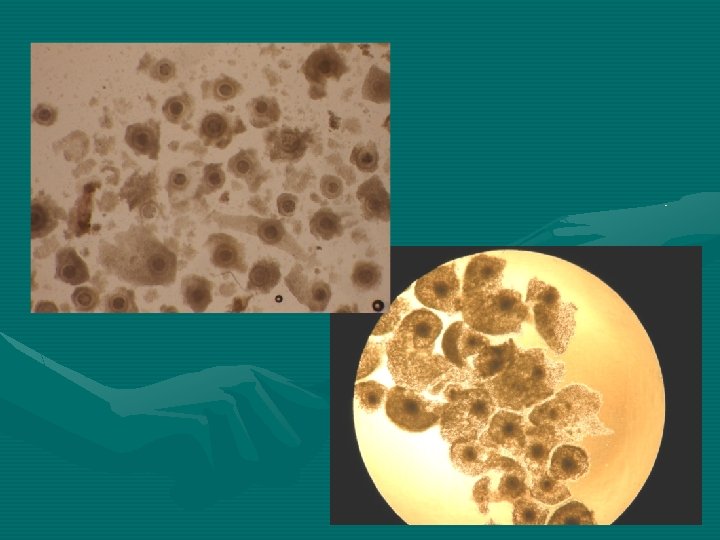

İn-vitro Fertilizasyon (IVF) üIVF, dişi genital organların dışında (laboratuar şartlarında) olgunlaştırılan oositlerin, kapasite olmuş spermatozoitlerle dölenip embriyoların oluşmasıdır üBu tekniğin ilk uygulanışı 1959' da tavşanlarda uygulamış ve başarı sağlanarak ilk yavru elde edilmiştir. Bu tarihden itibaren in vitro fertilizasyon teknigi, fare, rat, hamster, kedi, köpek, koyun, inek ve insanda uygulanmaktadır

Fertilizasyonda kullanılacak spermanın hazırlanması üFertilizasyonda kullanılacak spermadaki ölü canlı sperm hücrelerini ayırmak için ØPercoll Gradient ØSwim up yöntemleri kullanılır. üElde edilen sperm hücrelerinin yoğunluğu tespit edilerek (Hemositometrik yöntem) dozlanır (2 x 106 sperm hücresi/ml) ve fertilizasyonda kullanılır

Percoll Gradient Yöntemi üBu yöntemdeki amaç canlı-ölü sperm hücrelerinin ayrılmasıdır. Ölü sperm hücrelerinin ağırlıklarının canlı olanlardan daha az olmasından dolayı, yoğunlukları farklı iki değişik ortamın oluşturduğu tabaka ile ölü ve canlı sperma hücrelerini ayrılması mümkün olmaktadır. üBu amaçla, konik bir santrifüj tüpüne katman oluşturacak biçimde tabana %90’lık Percoll ve bunun üzerine %45’lik Percoll eşit miktarlarda konulur üEn üst kısmada yine katman oluşturacak biçimde sperma ilave edilir ve 700– 800 g’de 10– 15 dakika santrifüj edilir. üBu işlem sonunda ölü sperm hücreleri iki Percoll katmanı arasında ve canlı sperm hücreleri ise tabanda pellet şeklinde toplanmaktadır. üSantrifüj işleminden sonra sadece tüpün tabanında şekillenen pellet bırakılır ve diğer kısımlar uzaklaştırılır. üElde edilen bu pellet uygun bir biçimde yoğunluk tespiti yapılır ve dozlandıktan sonra fertilizasyonda kullanılır. üSperm hücrelerinin oositlere Penetrasyonunu kolaylaştırmak amacıyla fertilizasyon medyumu içerisine PHE (penisilamin, hypotaurine ve epinefrin

Swim-up Yöntemi üBu yöntemde yaklaşık 1. 5 ml sperm-TALP bulunan bir test tüpünün taban kısmına çözülmüş sperma tabakalandırılır ü 38. 5 °C’de, %5 CO içeren ve %95 oranında neme doyurulmuş inkübatörde 0. 5 -1 2 saat bekletilir. üBu süre boyunca motil spermalar yüzeye doğru yüzmeye başlar üSürenin sonunda test tüpünün üstünde spermatozoonları bulunduran süpernatandan 800 -1000 µl alınarak 250 g’de, 10 dk santrifüj yapılır. üBu yöntemle hem spermetozoanın kapasitasyonu ve hem de canlı sperm hücrelerinin ölü sperm hücrelerinden ayrılması sağlanmış olur. üSantrifüj sonrası supernatan uzaklaştırılır ve elde edilen pellet uygun bir biçimde yoğunluk tespiti yapılır ve dozlandıktan sonra fertilizasyonda kullanılır üSperm hücrelerinin oositlere Penetrasyonunu kolaylaştırmak amacıyla fertilizasyon medyumu içerisine PHE (penisilamin, hypotaurine ve epinefrin karışımı) ve Heparin eklenir.

İn-vitro Fertilizasyon üMature olmuş COCs’lar 2 kez TCM 199 (Hepes tamponlu)’da ve 2 kez de fertilizasyon medyumunda (modifiye Tyrode’s Lactate medyumu) yıkanır. üFertilizasyon medyumundan hazırlanan ve üzeri mineral yağla kaplanmış 44 μl’lik damlacıklar içerisine alınır. üFertilizasyondamlasınıniçersinekonsantrasyonubelirlenmiş olan 2 µl boğa sperması (2 x 106 sperm hücresi/ml), 2 µl Heparin ve 2 µl PHE (Penicillamine-Hypotaurine-Epinephrine) ilavesi yapılır ü 38. 5 ºC sıcaklık, %5 CO 2 ve %5 O 2 içeren inkübatöre 22

İn-vitro Fertilizasyon Medyumu Fertilizasyon TL Medyumu (100 ml Stok)* Fertilizasyonda kullanılacak medyumun hazırlanması (TALP) 100 ml embryo tested su 5 ml TL stok 666 mg Na. Cl 30 mg BSA-FAF ( Fatty Acid Free) 23. 5 mg KCl 210. 4 mg Na. HCO 3 50 l Pyruvate stok (2. 2 mg Na. Piruvat + 1 ml TL stok ve filtre et) 5. 52 mg Na. H 2 PO 4. H 2 O 2. 5 l penisilin-streptomisin 186 µl Na-lactate (% 60 şurup) 1 ml penisilin-streptomisin 1 mg Phenol Red (P/R) 30 mg *Ca. Cl 2. 2 H 2 O 10 mg *Mg. Cl 2. 6 H 2 O * p. H’yı 7. 4’e ayarla (p. H’yı düşürmek için 1 normal hidroklorik asit-HCl artırmak için 1 normal sodyum hidroksit-Na. OH kullan). Osmolorite 280 -300 m. OSM olmalı.
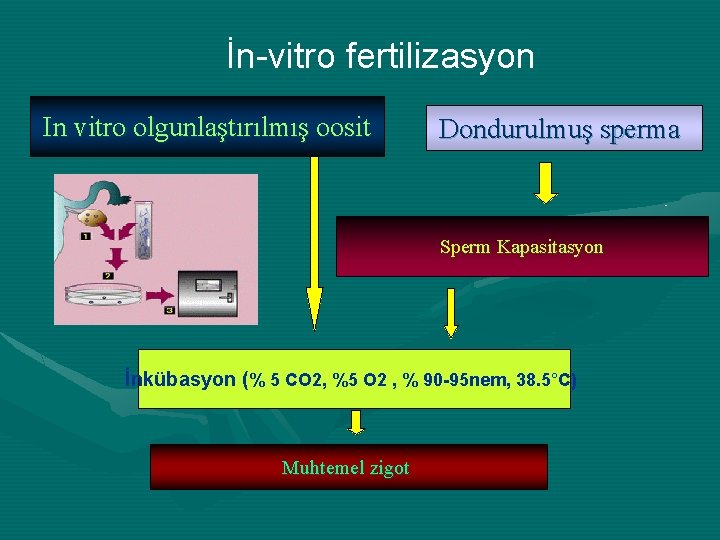
İn-vitro fertilizasyon In vitro olgunlaştırılmış oosit Dondurulmuş sperma Sperm Kapasitasyon İnkübasyon (% 5 CO 2, %5 O 2 , % 90 -95 nem, 38. 5°C) Muhtemel zigot

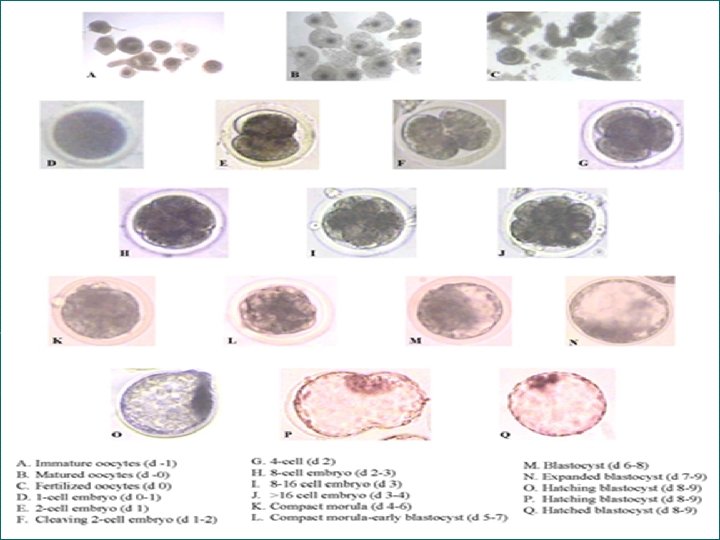
İn-vitro Kültür (IVC) üFertilizasyondan sonra gebeliğin şekillenebilmesi için embriyoların transferinde, transfer edilecek yere uygun olabilmesi açısından, 2 hücreli dönemden 8 hücreli ve blastosist devresine gelişmelerini sağlamak amacıyla kültür edilmeleri gerekmektedir. üEmbriyoların gelişimi için kültür koşullarının implantasyon öncesi oviduct ve uterus sıvılarının temel bileşenlerini ihtiva etmesi gerekir. üYapılan ilk çalışmalarda embriyolar kesimle, laparotomiyle veya verici genital kanalının yıkanmasıyla elde edilmiştir. üEmbriyoların kültürü için çeşitli kültür medyumları kullanılmaktadır (SOFaa, KSOM, CR 1 aa, IVD 101 vb. ). üElde edilen 1, 2 -4 veya 8 hücreli embriyolar belli sürelerde uygun kültür medyumlarında kültür edildiklerinde 12, 16, 20 (erken morula), 32 (morula), 64 (geç morula), erken blastosist ve blastosist dönemlerine geliştirilir.

Sığır embriyosunun gelişim süreleri ve dönemle Östrustan sonraki günler 0– 2 1– 3 2– 3 Embriyoların gelişme dönemi 1 Hücreli 2 Hücreli 4 Hücreli 3– 5 4– 5 5– 6 8 Hücreli 16 Hücreli Morula 5– 7 7– 8 7– 9 8– 10 Geç Morula Erken Blastosist Genişlemiş (expanded) Blastosist

İn-vitro Kültür (IVC) üFertilizasyondan sonra muhtemel zigotlar TCM 199 (Hepes tamponlu)’da iki-üç kez yıkanır. Eğer IVF’de kumulus hücreleri pipetleme yöntemiyle uzaklaştırılmamışsa, muhtemel fertilize oositler vorteksleme yöntemi ile veya Hyaluronidaz enzimi kullanılarak kumulus hücrelerinden uzaklaştırılır. Elde edilen zigotlar sentetik oviduk sıvısında (SOF) iki-üç kez yıkandıktan sonra zigotlar 50 l’lik SOF damlacıklarına aktarılır ve 38. 5 ºC sıcaklık, %5 CO 2, %5 O 2 içeren ve %95 oranında neme doyurulmuş inkübatörde kültür edilir. üGelişmenin 3. gününde iki hücre ve daha ileriki hücre aşamalarına bölünmüş zigot oranı stereo veya invert mikroskop altında belirlenir. Embriyoların gelişme safhaları 6, 7, 8. günlerde morula/blastosis

İn-vitro Kültür Medyum (SOFaa) Kimyasal 10 ml Na. Cl 62. 94 mg KCl 5. 34 mg KH 2 PO 4 1. 62 mg Na. HCO 3 21. 06 mg Na. Lactate 2. 8 µl Na. Pyruvate 0. 4 mg Penisilin-streptomisin 100 µl Ca. Cl 2 2 H 2 O 2. 51 mg Mg. Cl 2 6 H 2 O 1 mg BSA (FAF) 80 mg FİLTRASYON BME non-aa sol. 100 µl MEM non-aa sol. 200 µl
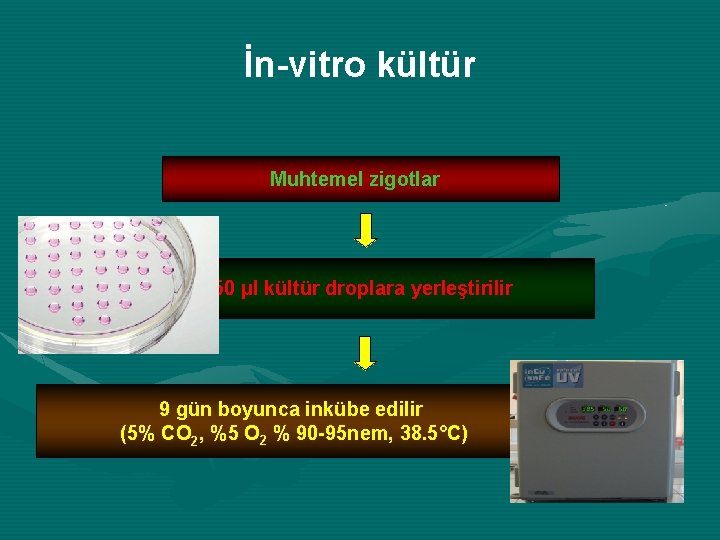
İn-vitro kültür Muhtemel zigotlar 50 μl kültür droplara yerleştirilir 9 gün boyunca inkübe edilir (5% CO 2, %5 O 2 % 90 -95 nem, 38. 5°C)

üYönteme bağlı olmakla birlikte ovaryumdaki foliküllerden elde edilen oosit sayısı 3 -40 arasındadır. üOlgunlaştırmaya bırakılan oositlerin %60 -90’ı olgunlaşmada başarılı olmakta üBunlardan %20 -50’si Morula-Blastosist aşamasına ulaşabilmektedir Sonuç olarak; v. Ovulasyon, fertilizasyon ve embriyonik gelişme fizyolojisi arasındaki bağların in vitro taklit edilmesi ile mezbahanede kesilen hayvanlardan , bazı infertil hayvanlardan ve genetik yönden üstün verimli hayvanlardan daha fazla oranda yararlanılması ve daha ekonomik olması dolayısıyla bu teknik üzerindeki çalışmaların ilerletilerek yapılmasına ihtiyaç duyulmaktadır.
- Slides: 30