Hatkarg ATP sintze H ATP veic atgriezenisku protondzinjspka





- Slides: 24

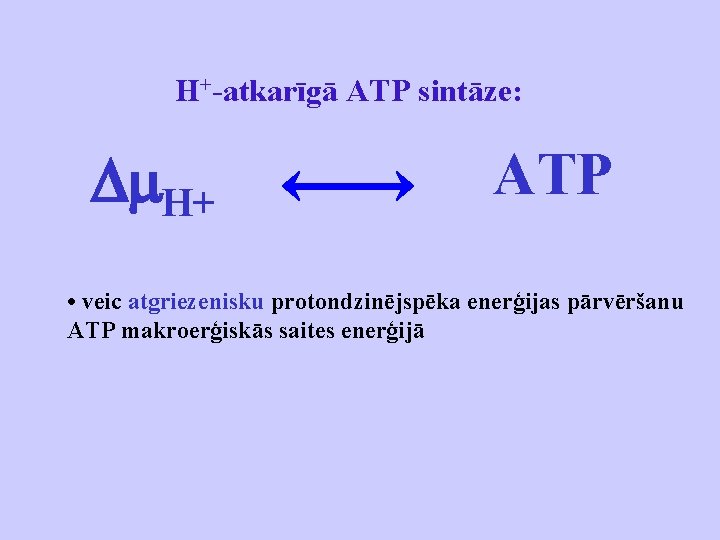
H+-atkarīgā ATP sintāze: H+ ATP • veic atgriezenisku protondzinējspēka enerģijas pārvēršanu ATP makroerģiskās saites enerģijā

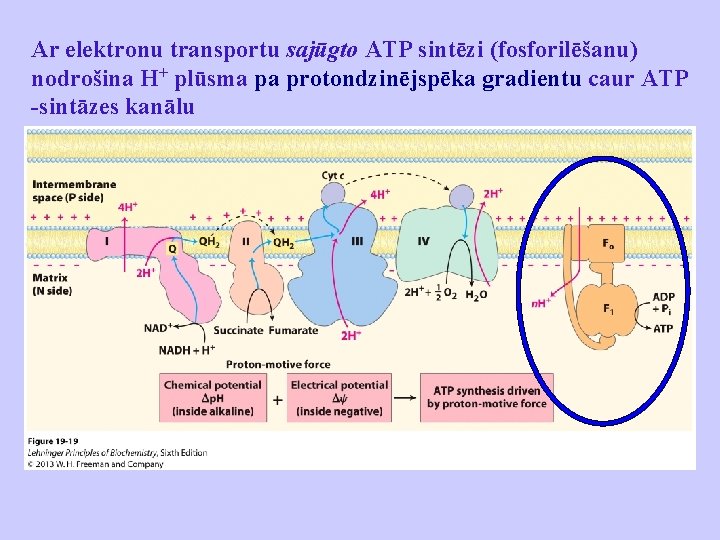
Ar elektronu transportu sajūgto ATP sintēzi (fosforilēšanu) nodrošina H+ plūsma pa protondzinējspēka gradientu caur ATP -sintāzes kanālu


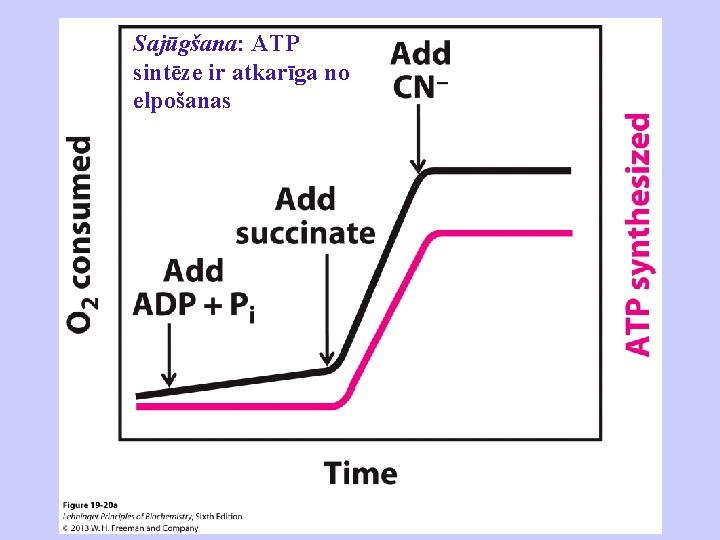
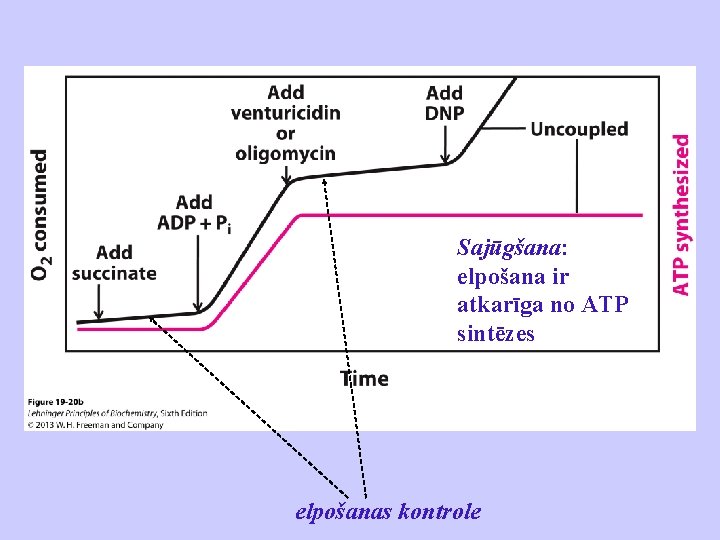
Sajūgšana: ATP sintēze ir atkarīga no elpošanas

Sajūgšana: elpošana ir atkarīga no ATP sintēzes elpošanas kontrole

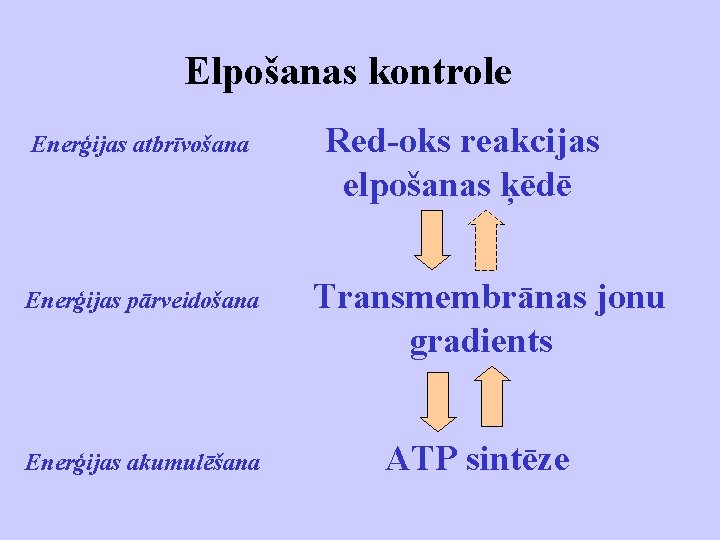
Elpošanas kontrole Enerģijas atbrīvošana Enerģijas pārveidošana Enerģijas akumulēšana Red-oks reakcijas elpošanas ķēdē Transmembrānas jonu gradients ATP sintēze

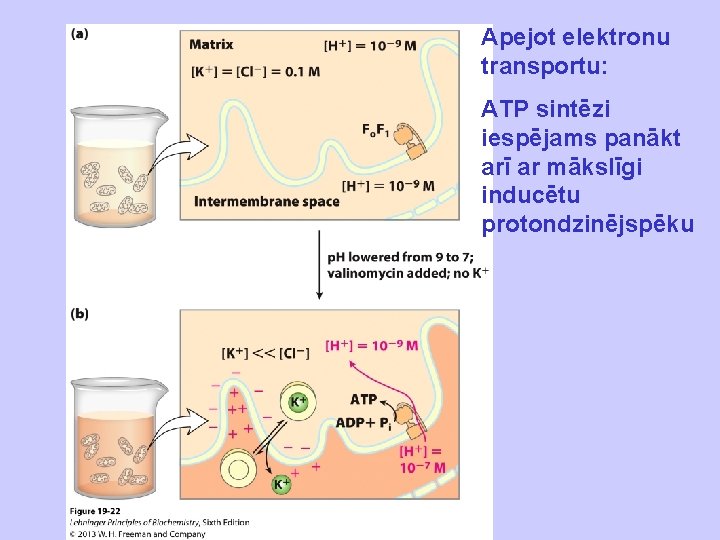
Apejot elektronu transportu: ATP sintēzi iespējams panākt arī ar mākslīgi inducētu protondzinējspēku

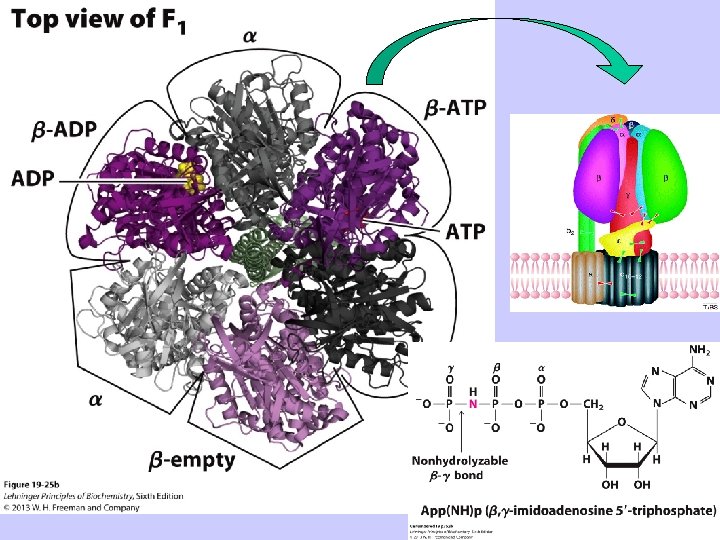
• elektronu mikroskopā F 1 uz mitohondriju iekšējās membrānas ir redzamas kā “sēņveida struktūras” • no membrānas atrautas F 1 daļiņas spēj veikt ATP hidrolīzi, bet ne bruto ATP sintēzi

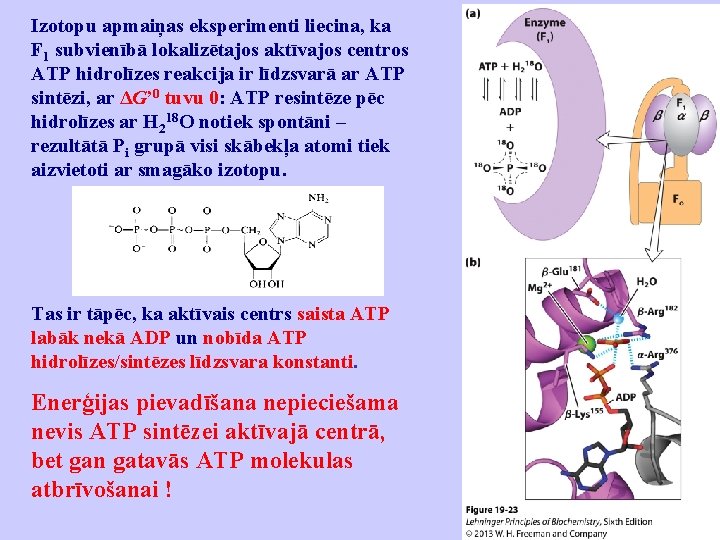
Izotopu apmaiņas eksperimenti liecina, ka F 1 subvienībā lokalizētajos aktīvajos centros ATP hidrolīzes reakcija ir līdzsvarā ar ATP sintēzi, ar ΔG’ 0 tuvu 0: ATP resintēze pēc hidrolīzes ar H 218 O notiek spontāni – rezultātā Pi grupā visi skābekļa atomi tiek aizvietoti ar smagāko izotopu. Tas ir tāpēc, ka aktīvais centrs saista ATP labāk nekā ADP un nobīda ATP hidrolīzes/sintēzes līdzsvara konstanti. Enerģijas pievadīšana nepieciešama nevis ATP sintēzei aktīvajā centrā, bet gan gatavās ATP molekulas atbrīvošanai !

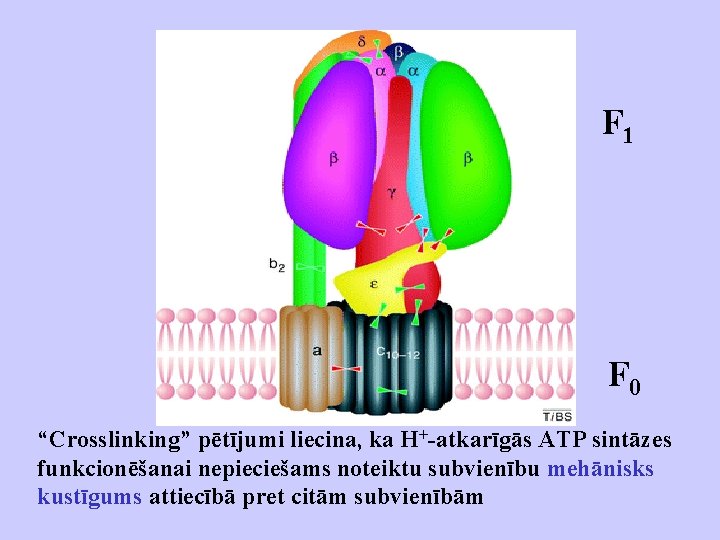
F 1 F 0 “Crosslinking” pētījumi liecina, ka H+-atkarīgās ATP sintāzes funkcionēšanai nepieciešams noteiktu subvienību mehānisks kustīgums attiecībā pret citām subvienībām

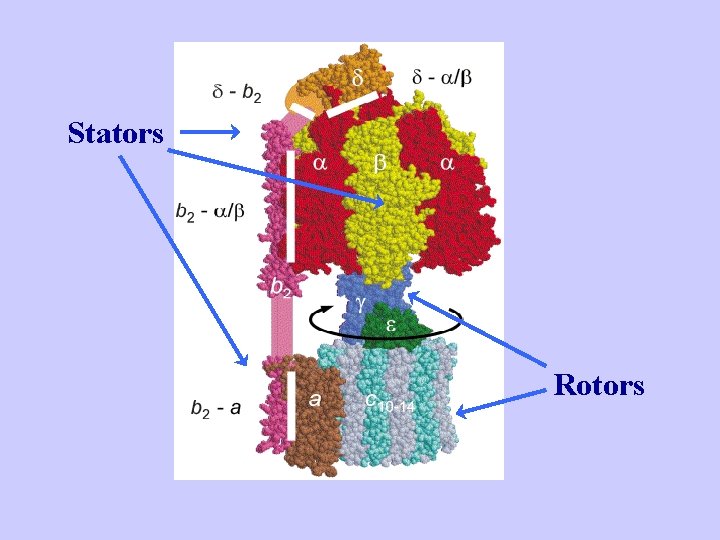
Stators Rotors

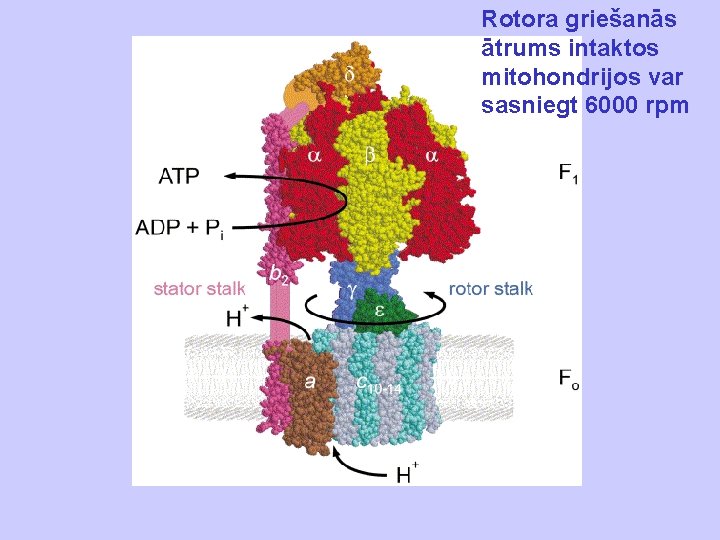
Rotora griešanās ātrums intaktos mitohondrijos var sasniegt 6000 rpm


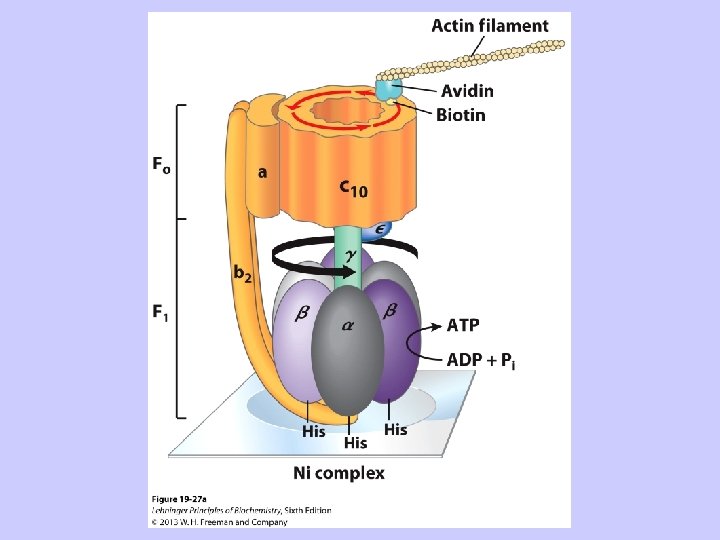
Intervāls starp attēliem – 133 msec Redzams, ka secīgi atkārtojas trīs ar fluorescento krāsvielu iezīmētā aktīna filamenta stāvokļi

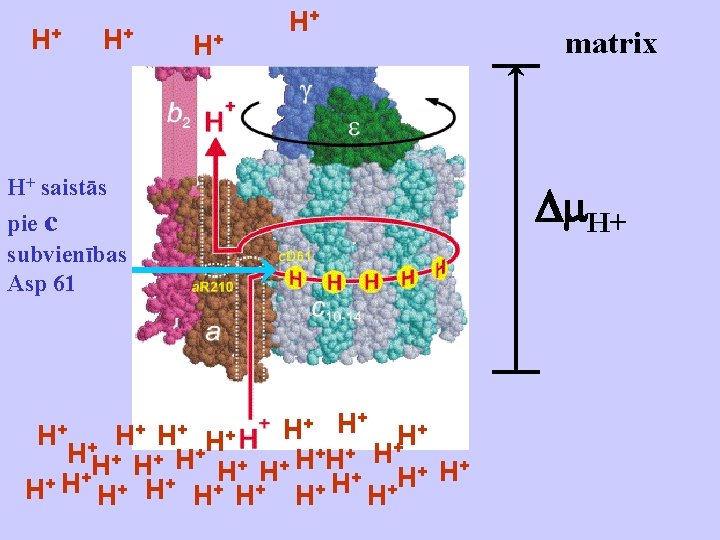
H+ H+ H+ saistās H+ pie c subvienības Asp 61 + H+ + H H H+H+ H+ H+ + + H+H+ H+ H H + + H H+ H+ H+ matrix H+

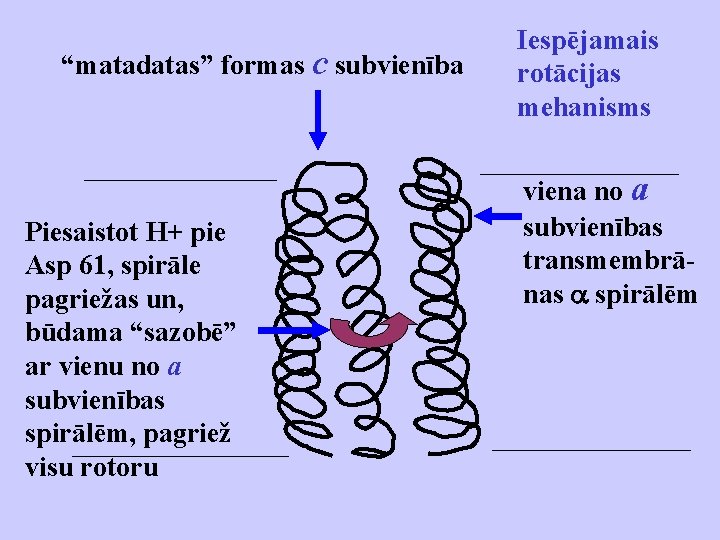
“matadatas” formas c subvienība Piesaistot H+ pie Asp 61, spirāle pagriežas un, būdama “sazobē” ar vienu no a subvienības spirālēm, pagriež visu rotoru Iespējamais rotācijas mehanisms viena no a subvienības transmembrānas spirālēm

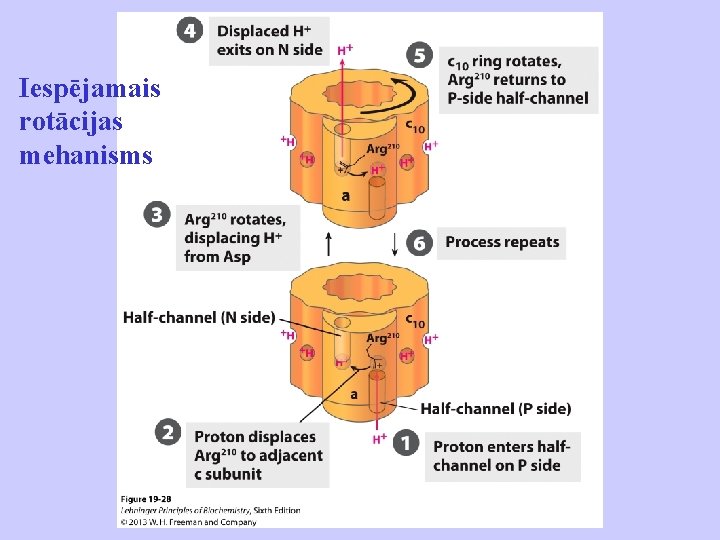
Iespējamais rotācijas mehanisms


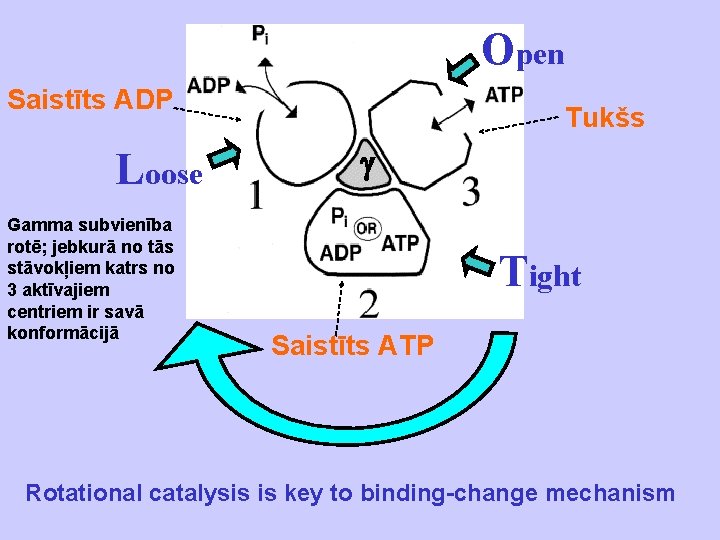
Open Saistīts ADP Loose Gamma subvienība rotē; jebkurā no tās stāvokļiem katrs no 3 aktīvajiem centriem ir savā konformācijā Tukšs Tight Saistīts ATP Rotational catalysis is key to binding-change mechanism

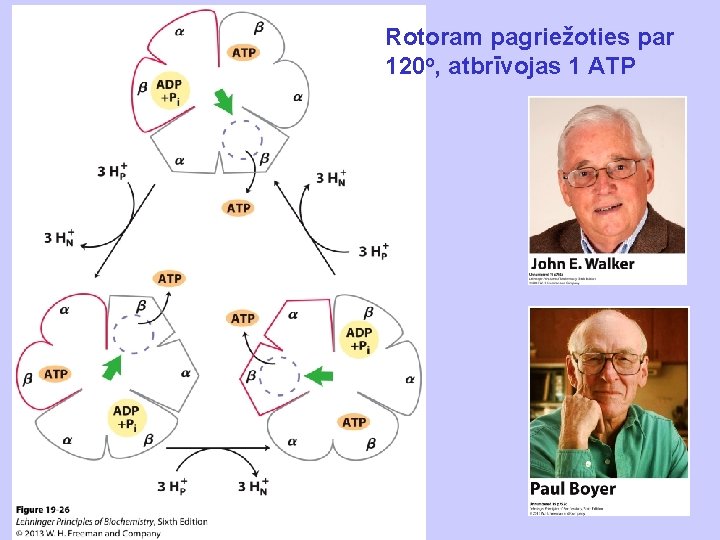
Rotoram pagriežoties par 120 o, atbrīvojas 1 ATP

ATP sintēzes stehiometrija mitohondrijos Eksperimentālie mērījumi: Ja pārnesot 2 e- no NADH uz O, H+ veidošanā piedalās 10 H+, un vienlaikus tiek sintezētas 2. 5 – 3 molekulas 3 līdz 4 ATP, tad H+/ATP = No termodinamikas viedokļa: Ja H+= 200 m. V jeb 19, 2 k. J uz molu H+, un Gp= 57 k. J uz molu ATP, 3 līdz 4 tad H+/ATP = No mehanistiskā viedokļa: Ja pagriežoties rotoram par 120 o sintezējas 1 ATP, un rotorā ir 8 – 12 protonu pārnesošu c subvienību, 3 līdz 4 tad H+/ATP =

ATP sintēzes stehiometrija hloroplastos Eksperimentālie mērījumi: Ja pārnesot 4 e- no H 2 O uz NADP+ (un atbrīvojot vienu O 2 molekulu), H+ veidošanā piedalās 12 H+ (4 no Mn kompleksa un 8 no b 6 f), un vienlaikus tiek sintezētas aptuveni 3 molekulas ATP, tad H+/ATP = ≈4 No mehanistiskā viedokļa: Ja pagriežoties rotoram par 120 o sintezējas 1 ATP, un rotorā ir 14 protonu pārnesošu c subvienību (piem. spināta H+-ATP sintāzei), tad H+/ATP = ≈4

Energosajūgšana ATP sintāzē: H+ piesaistīšanās / disociācija pie c subvienības c gredzena un subvienības rotācija secīgas L – T – O konformāciju izmaiņas aktīvajos centros subvienībās

Protonatkarīgā ATP sintāze darbojas abos virzienos: • ja protondzinējspēks ir pietiekami liels, tā sintezē ATP, izmantojot protondzinējspēka enerģiju • ja H+ ir mazs – tā hidrolizē ATP, lai uzturētu protondzinējspēku – darbojas kā protonus pumpējoša ATPāze • ja elektronu transports neuztur H+ (piem. daudzās anaerobajās baktērijās) tad H+ATPāze ir galvenais protondzinējspēka uzturētājs