Halogeny Obr 2 Obr 1 fluor chlor brom
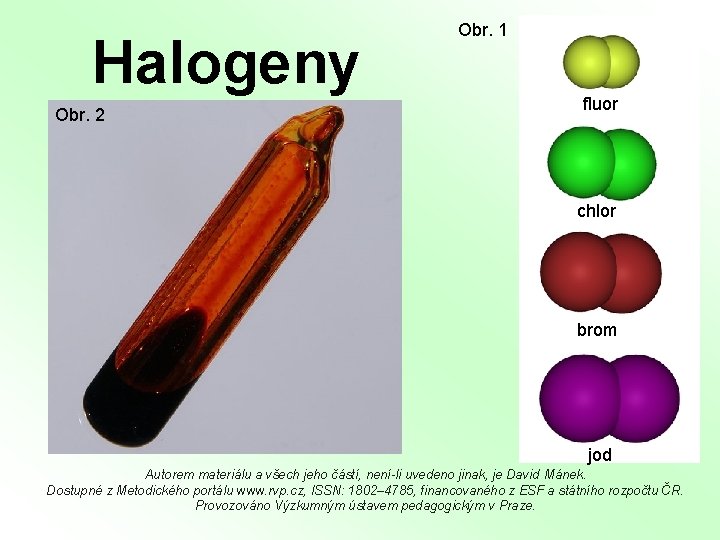
Halogeny Obr. 2 Obr. 1 fluor chlor brom jod Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je David Mánek. Dostupné z Metodického portálu www. rvp. cz, ISSN: 1802– 4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze.
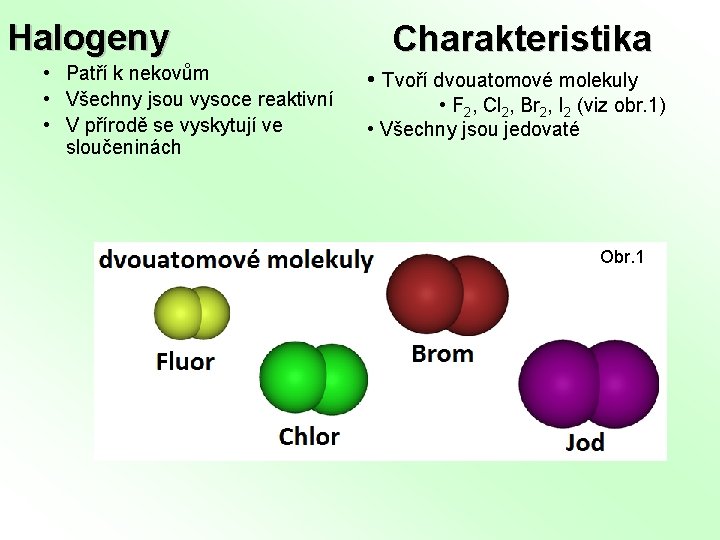
Halogeny • Patří k nekovům • Všechny jsou vysoce reaktivní • V přírodě se vyskytují ve sloučeninách Charakteristika • Tvoří dvouatomové molekuly • F 2, Cl 2, Br 2, I 2 (viz obr. 1) • Všechny jsou jedovaté Obr. 1
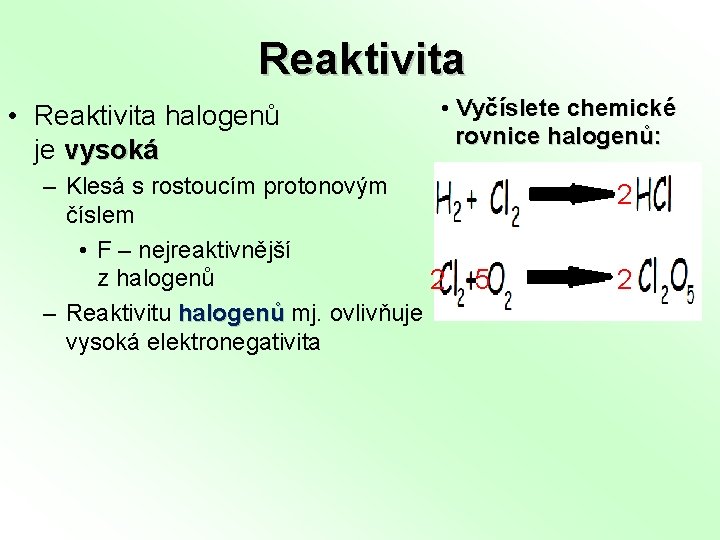
Reaktivita • Reaktivita halogenů je vysoká • Vyčíslete chemické rovnice halogenů: – Klesá s rostoucím protonovým číslem • F – nejreaktivnější z halogenů 2 – Reaktivitu halogenů mj. ovlivňuje vysoká elektronegativita 2 5 2
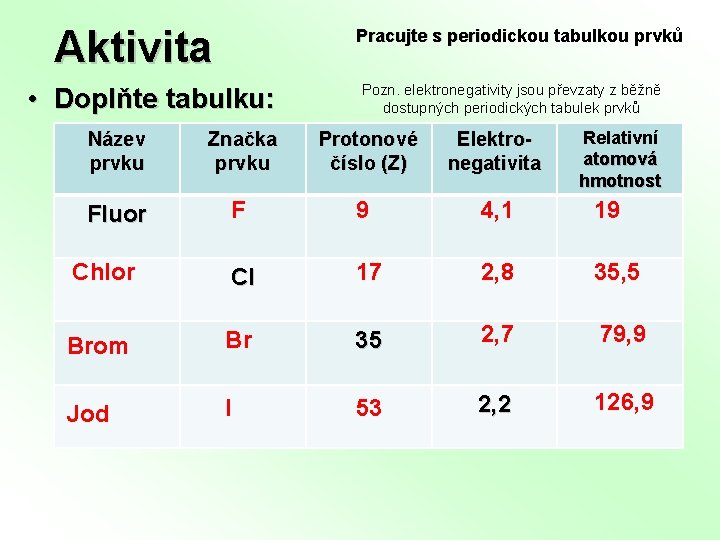
Aktivita Pracujte s periodickou tabulkou prvků • Doplňte tabulku: Pozn. elektronegativity jsou převzaty z běžně dostupných periodických tabulek prvků Protonové číslo (Z) Elektronegativita Relativní atomová hmotnost Název prvku Značka prvku Fluor F 9 4, 1 19 Chlor Cl 17 2, 8 35, 5 Brom Br 35 2, 7 79, 9 Jod I 53 2, 2 126, 9

Fluor • • Značka ‒ F Vlastnosti: – Vysoce reaktivní, toxický a nažloutlý plyn • Využití: – Je velmi účinným oxidačním činidlem – Větší význam sloučeniny (např. teflon nebo fluorovodík) Obr. 4 – Při práci s fluorem

Chlor • • Obr. 5 – Zkapalněný chlor Značka ‒ Cl Vlastnosti: – Jedovatý, vysoce reaktivní plyn, těžší než vzduch • Využití: – K výrobě chlorovodíku, chloridů a plastů – K dezinfekci vody nejen v bazénech • Zajímavosti: – Yperit – bojový plyn využitý v 1. světové válce

Aktivita • Vyluštěte osmisměrku: osmisměrku D V F L U O R E CH Y B E T S S A S H L P CH CH Z E H L O O O E L J E I F O L R R R O E M M N L I M I I R D E E I F O O D T A B R O M E E N Y : -) J Í V Z D U CH K Y : -) O P L Y N Y G N C : -) D H A L O G E N Y E Tajenka: ___________ Bavíme se s halogeny

Brom • Značka ‒ Br • Vlastnosti: – Červenohnědá, jedovatá kapalina, vysoce reaktivní • Jak připravíme brom: – Do směsi bromidu draselného a oxidu manganičitého přidáme kyselinu sírovou – Baňku uzavřeme vatou namočenou v roztoku sody a pozorujeme. • Zajímavost: – Brom snižuje mužskou potenci Obr. 6

Jod Obr. 7 • Značka ‒ I • Vlastnosti: – Tmavě fialová, pevná, sublimující látka • Využití: – Jodová tinktura (lékařství) • Důležitost: – Je součástí pro organismus důležitých hormonů štítné žlázy Obr. 8
![Použité zdroje informací Obr. 1 – [cit. 2011 -03 -19]. Dostupný pod licencí Public Použité zdroje informací Obr. 1 – [cit. 2011 -03 -19]. Dostupný pod licencí Public](http://slidetodoc.com/presentation_image_h2/5be13e3c92abed4827ccba2957fbe2b0/image-10.jpg)
Použité zdroje informací Obr. 1 – [cit. 2011 -03 -19]. Dostupný pod licencí Public domain na WWW: <http: //commons. wikimedia. org/wiki/File: Halogens-3 D-vd. W. png>. Obr. 2 – Jurii, [cit. 2011 -03 -19]. Dostupný pod licencí Creative Commons na WWW: <http: //commons. wikimedia. org/wiki/File: Bromine-ampoule. jpg? uselang=cs>. Obr. 4 – [cit. 2011 -03 -19]. Dostupný pod licencí Public domain na WWW: <http: //commons. wikimedia. org/wiki/File: Fluor_Fernald_Workers. jpg? uselang=cs>. Obr. 5 – [cit. 2011 -03 -19]. Dostupný pod licencí Public domain na WWW: <http: //commons. wikimedia. org/wiki/File: Chlor_1 a. jpg? uselang=cs>. Obr. 6 – Matthew Sergei Perrin, [cit. 2011 -03 -19]. Dostupný pod licencí Creative Commons na WWW: <http: //commons. wikimedia. org/wiki/File: Bromine_water. jpg? uselang=cs>. Obr. 7 – [cit. 2011 -03 -19]. Dostupný pod licencí Public domain na WWW: <http: //commons. wikimedia. org/wiki/File: Jod_pevny. jpg? uselang=cs>. Obr. 8 – Matias Molnar, [cit. 2011 -03 -19]. Dostupný pod licencí Creative Commons na WWW: <http: //commons. wikimedia. org/wiki/File: Iodo. Atomico. JPG? uselang=cs>.
- Slides: 10