Halogenki kwasowe pochodne kwasw karboksylowych budowa halogenkw kwasowych

Halogenki kwasowe – pochodne kwasów karboksylowych Ø Ø Ø budowa halogenków kwasowych, fosgen – halogenek kwasu węglowego, otrzymywanie halogenków kwasowych, właściwości fizyczne halogenków kwasowych, właściwości chemiczne halogenków kwasowych
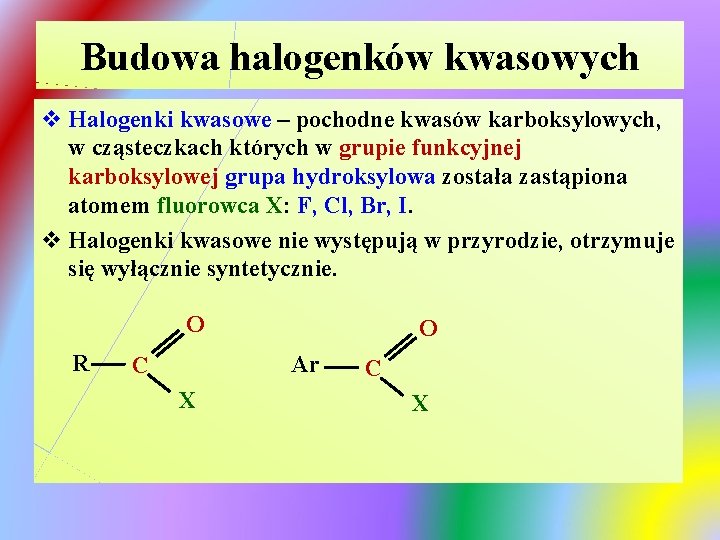
Budowa halogenków kwasowych v Halogenki kwasowe – pochodne kwasów karboksylowych, w cząsteczkach których w grupie funkcyjnej karboksylowej grupa hydroksylowa została zastąpiona atomem fluorowca X: F, Cl, Br, I. v Halogenki kwasowe nie występują w przyrodzie, otrzymuje się wyłącznie syntetycznie. O R O Ar C X
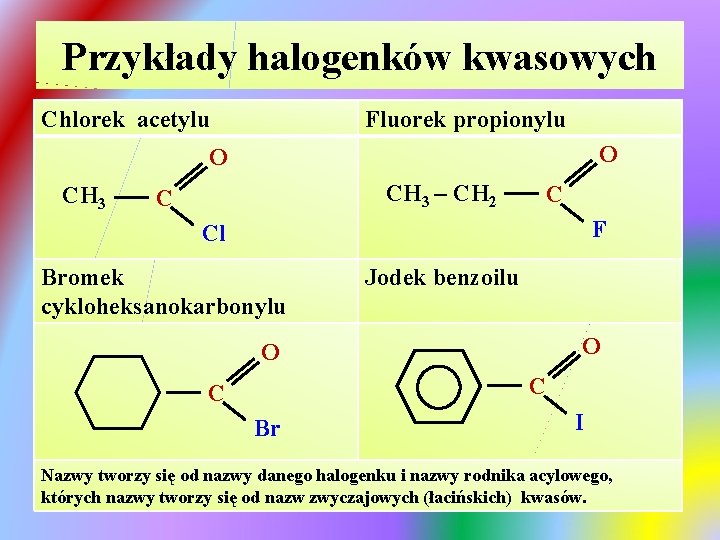
Przykłady halogenków kwasowych Chlorek acetylu Fluorek propionylu O O CH 3 – CH 2 C C F Cl Bromek cykloheksanokarbonylu Jodek benzoilu O O C C Br I Nazwy tworzy się od nazwy danego halogenku i nazwy rodnika acylowego, których nazwy tworzy się od nazw zwyczajowych (łacińskich) kwasów.
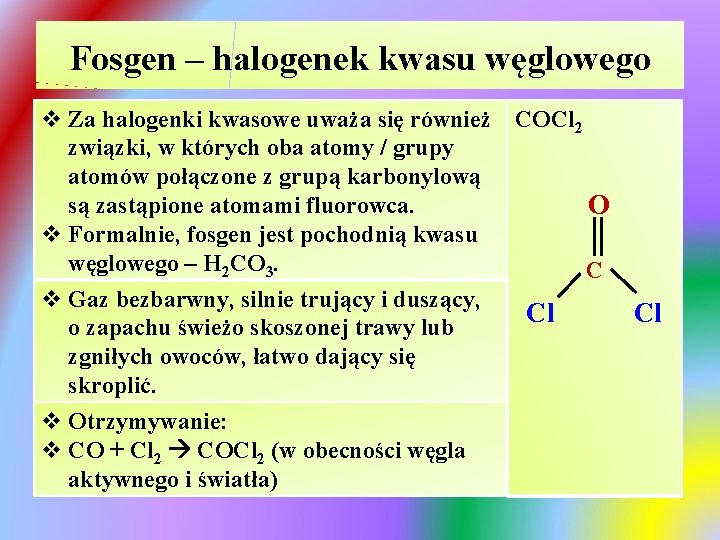
Fosgen – halogenek kwasu węglowego v Za halogenki kwasowe uważa się również COCl 2 związki, w których oba atomy / grupy atomów połączone z grupą karbonylową są zastąpione atomami fluorowca. O v Formalnie, fosgen jest pochodnią kwasu węglowego – H 2 CO 3. C v Gaz bezbarwny, silnie trujący i duszący, Cl o zapachu świeżo skoszonej trawy lub zgniłych owoców, łatwo dający się skroplić. v Otrzymywanie: v CO + Cl 2 COCl 2 (w obecności węgla aktywnego i światła) Cl

Fosgen - właściwości i zastosowanie v Właściwości chemiczne: Ø reakcje z alkoholami, produktem są estry – chloromrówczany: O ü COCl 2 + HO-CH 3 Cl – C – O – CH 3 + HCl Ø reakcja z amoniakiem, produktem jest mocznik/ amid NH 2 kwasu węglowego: ü COCl 2 + 2 NH 3 O = C + 2 HCl NH 2 Ø hydroliza w roztworze wodnym: ü COCl 2 + H 2 O 2 HCl + CO 2 v Zastosowanie: Ø przemył farmaceutyczny, produkcji barwników, tworzyw sztucznych, np. : poliwęglanów, pianki poliuretanowej.
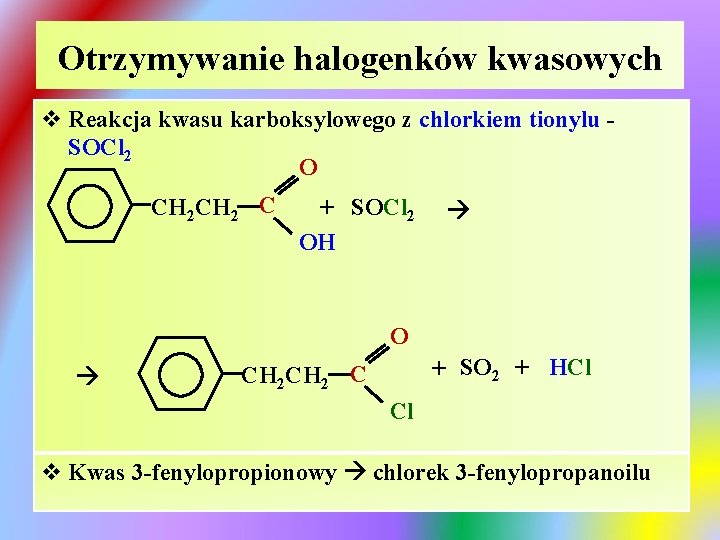
Otrzymywanie halogenków kwasowych v Reakcja kwasu karboksylowego z chlorkiem tionylu SOCl 2 O CH 2 C + SOCl 2 OH O + SO 2 + HCl CH 2 C Cl v Kwas 3 -fenylopropionowy chlorek 3 -fenylopropanoilu
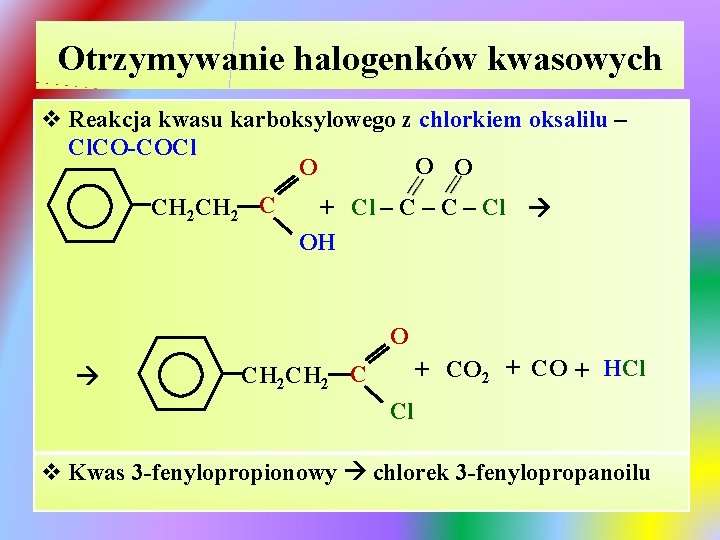
Otrzymywanie halogenków kwasowych v Reakcja kwasu karboksylowego z chlorkiem oksalilu – Cl. CO-COCl O O O CH 2 C + Cl – C – Cl OH O + CO 2 + CO + HCl CH 2 C Cl v Kwas 3 -fenylopropionowy chlorek 3 -fenylopropanoilu
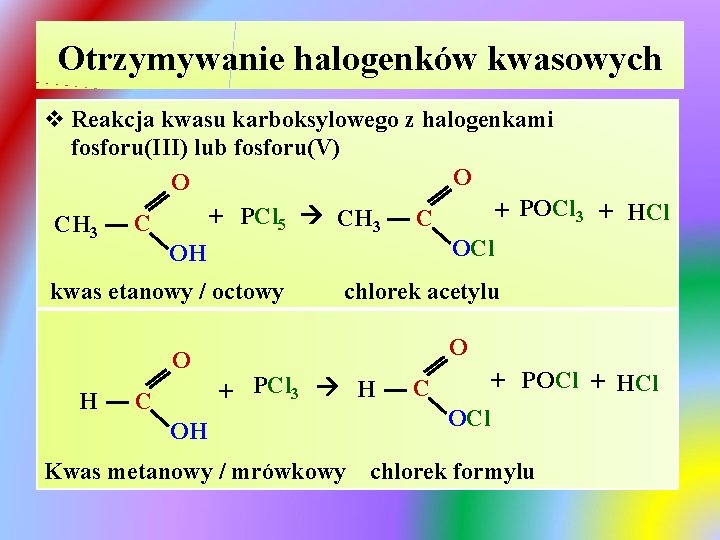
Otrzymywanie halogenków kwasowych v Reakcja kwasu karboksylowego z halogenkami fosforu(III) lub fosforu(V) O O + POCl 3 + HCl + PCl 5 CH 3 C OCl OH kwas etanowy / octowy O H C chlorek acetylu O + PCl 3 H OH Kwas metanowy / mrówkowy + POCl + HCl C OCl chlorek formylu

Właściwości fizyczne v. Właściwości fizyczne: Ø halogenki kwasowe kwasów karboksylowych o niewielkiej masie cząsteczkowej: ü są cieczami o ostrym, drażniącym zapachu, ü nierozpuszczalnymi w wodzie, rozpuszczają się w rozpuszczalnikach organicznych, ü mają niższe temp. wrzenia niż wyjściowe kwasy karboksylowe, ponieważ brak grupy hydroksylowej w halogenkach uniemożliwia ich asocjację.

Właściwości chemiczne v Właściwości chemiczne: Ø aromatyczne halogenki kwasowe są mniej reaktywne niż alifatyczne, Ø reaktywność halogenków kwasowych wzrasta wraz z mocą wyjściowych kwasów karboksylowych, Ø przy tych samych podstawnikach węglowodorowych reaktywność halogenków wzrasta w szeregu: ü jodki - bromki - chlorki - fluorki ü wraz ze wzrostem elektroujemności podstawnika powstaje silniejszy ujemny efekt indukcyjny niż wywołuje podstawnik wodorowy, co prowadzi do zmiany polaryzacji wiązań w cząsteczce.
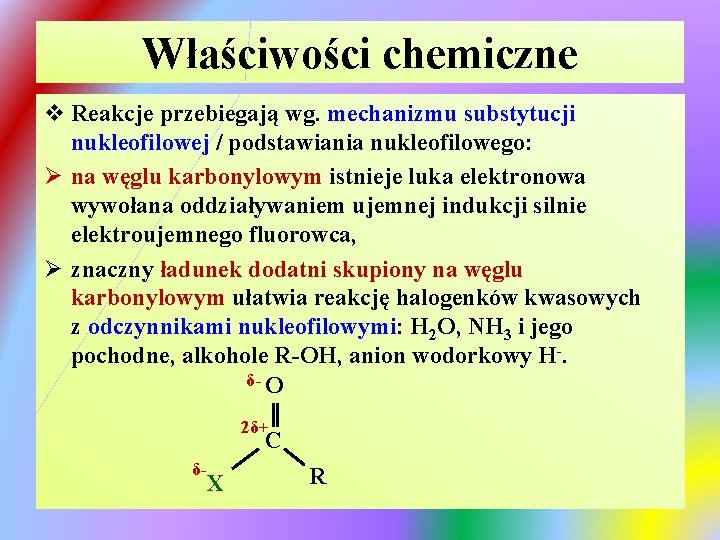
Właściwości chemiczne v Reakcje przebiegają wg. mechanizmu substytucji nukleofilowej / podstawiania nukleofilowego: Ø na węglu karbonylowym istnieje luka elektronowa wywołana oddziaływaniem ujemnej indukcji silnie elektroujemnego fluorowca, Ø znaczny ładunek dodatni skupiony na węglu karbonylowym ułatwia reakcję halogenków kwasowych z odczynnikami nukleofilowymi: H 2 O, NH 3 i jego pochodne, alkohole R-OH, anion wodorkowy H-. δ- O 2δ+ C δ- X R

Właściwości chemiczne Ø reakcje z wodą - produktami są odpowiednie kwasy karboksylowe: ü CH 3 -COCl + H-OH CH 3 -COOH + HCl Ø reakcje z alkoholami - produktami są odpowiednie estry: ü CH 3 -COCl + HO-CH 3 CH 3 -CO-OCH 3 + HCl Ø reakcje z amoniakiem – produktami są odpowiednie amidy ü CH 3 -COCl + NH 3 CH 3 -CO-NH 2 + HCl Ø reakcja redukcji H- / (Li. Al. H 4) – produktami są odpowiednie aldehydy: Ø CH 3 -COCl + Li. Al. H 4 CH 3 -CHO + Li. Cl + Al. H 3
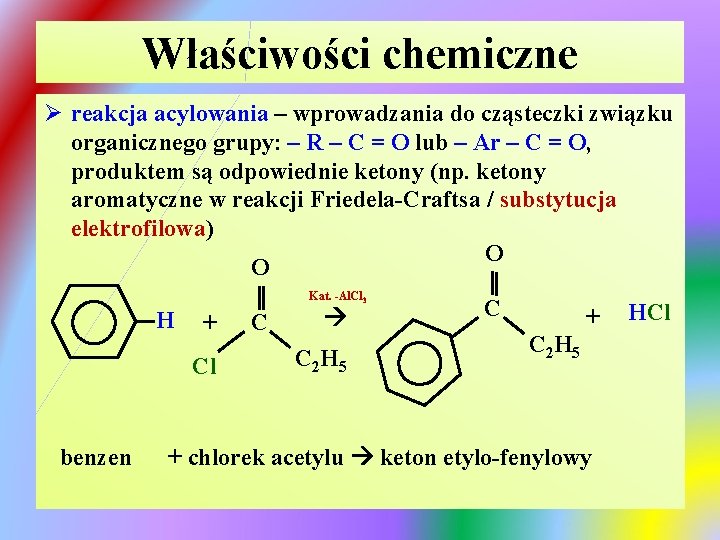
Właściwości chemiczne Ø reakcja acylowania – wprowadzania do cząsteczki związku organicznego grupy: – R – C = O lub – Ar – C = O, produktem są odpowiednie ketony (np. ketony aromatyczne w reakcji Friedela-Craftsa / substytucja elektrofilowa) O O Kat. -Al. Cl 3 H + Cl benzen C C 2 H 5 C + C 2 H 5 + chlorek acetylu keton etylo-fenylowy HCl
- Slides: 13