HALOGENDERIVTY RNDr Marta Najbertov Gymnzium a Jazykov kola

HALOGENDERIVÁTY RNDr. Marta Najbertová
Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Název školy Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Adresa školy IČO Operační program Registrační číslo Označení vzdělávacího materiálu Vzdělávací oblast Vzdělávací obor Tematický okruh Sokolovská 1638 620 330 26 Operační program Vzdělávání pro konkurenceschopnost CZ. 1. 07/1. 1. 28/01. 0050 K_INOVACE_1. CH. 19 Člověk a příroda Chemie Deriváty uhlovodíků - halogenderiváty Zhotoveno Ročník Vyšší stupeň osmiletého gymnázia a čtyřleté gymnázium (RVP – G) Anotace Materiál je určen jako studijní materiál v předmětu chemie. Je zaměřen na obecnou charakteristiku, rozdělení, vlastnosti a popis zástupců halogenderivátů. Předpokládá zvládnutí teorie atomového obalu, chemické vazby a obecné chemie. Materiál je určen pro seminář chemie, lze jej využít i v hodinách chemie.

Obecná charakteristika Halogenderiváty jsou organické sloučeniny, ve kterých je v původní molekule uhlovodíku jeden nebo více atomů vodíku nahrazen halogenem. Obecný vzorec je R-X, kde X může být F, Cl, Br, I. Je – li R alkylový zbytek, jedná se o alkylhalogenidy, je – li R aryl, jedná se o arylhalogenidy. Až na malé výjimky se v přírodě nevyskytují, jsou připravovány synteticky. Důkaz v organickém materiálu – Beilsteinova zkouška plamenem – pro možnost vzniku jedovatých dioxinů nahrazována reakcí s taveninou sodíku – vznik halogenidů sodíku.
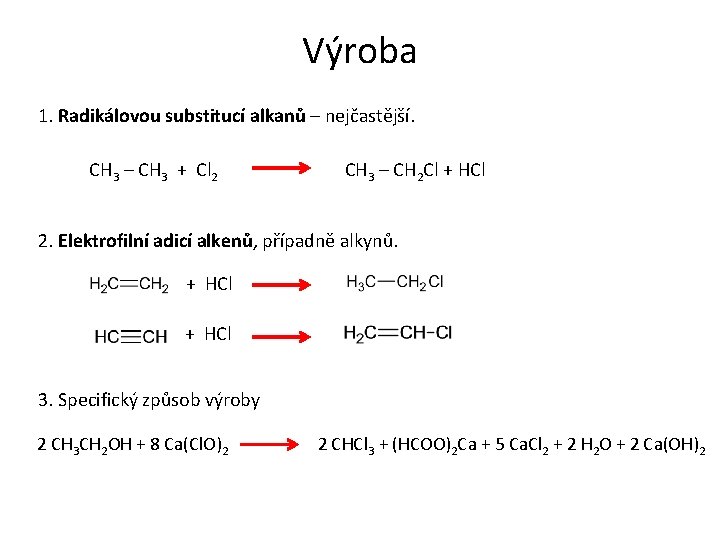
Výroba 1. Radikálovou substitucí alkanů – nejčastější. CH 3 – CH 3 + Cl 2 CH 3 – CH 2 Cl + HCl 2. Elektrofilní adicí alkenů, případně alkynů. + HCl 3. Specifický způsob výroby 2 CH 3 CH 2 OH + 8 Ca(Cl. O)2 2 CHCl 3 + (HCOO)2 Ca + 5 Ca. Cl 2 + 2 H 2 O + 2 Ca(OH)2

Názvosloví 1. Nesystematické – bude uvedeno u jednotlivých zástupců. 2. Dvousložkové – používáno u jednodušších alkylhalogenidů, podle zásad „anorganického“ názvosloví. ethylchlorid 3. Systematické - pro označení polohy substituentu nebo jejich počtu platí zásady názvosloví uhlovodíků. 2 -chlorpropan 1, 2 -dichlor-1, 2 -difluorethan

Fyzikální vlastnosti V důsledku polarity vazby (vyšší hodnota elektronegativity halogenu) mají alkylhalogenidy vyšší bod varu než původní uhlovodíky (slabé vazebné interakce). Nižší jsou obvykle kapaliny s bodem varu do 100 °C (chloroform, tetrachlormethan). Polarita vazby ale neumožňuje rozpustnost v polárních rozpouštědlech => rozpustné v nepolárních rozpouštědlech, sami jsou nepolárními rozpouštědly. Barva, chuť a zápach závisí na typu, počtu a rozložení atomů halogenu v molekule.
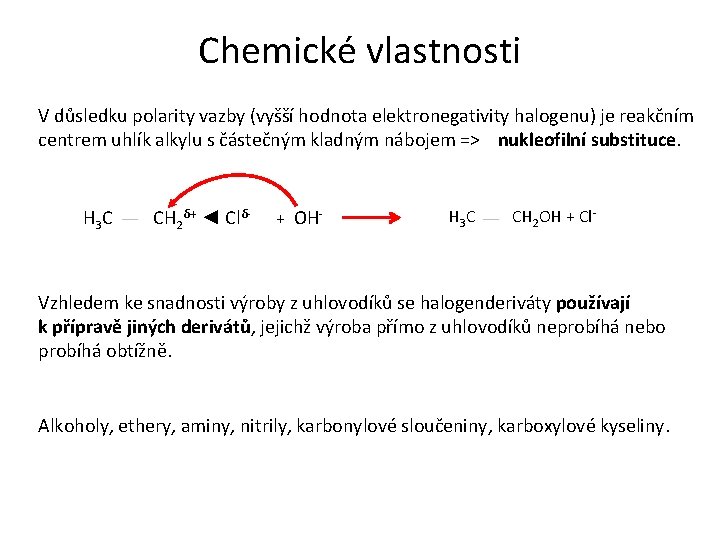
Chemické vlastnosti V důsledku polarity vazby (vyšší hodnota elektronegativity halogenu) je reakčním centrem uhlík alkylu s částečným kladným nábojem => nukleofilní substituce. H 3 C CH 2δ+ ◄ Clδ- + OH- H 3 C CH 2 OH + Cl- Vzhledem ke snadnosti výroby z uhlovodíků se halogenderiváty používají k přípravě jiných derivátů, jejichž výroba přímo z uhlovodíků neprobíhá nebo probíhá obtížně. Alkoholy, ethery, aminy, nitrily, karbonylové sloučeniny, karboxylové kyseliny.
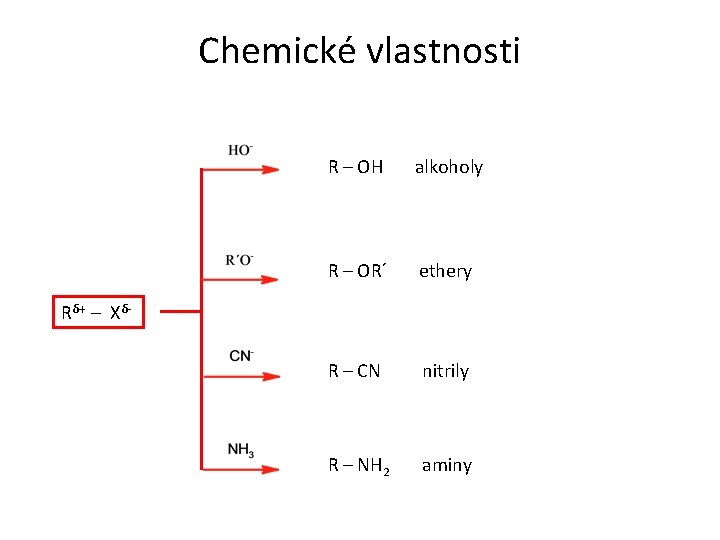
Chemické vlastnosti R – OH alkoholy R – OR´ ethery R – CN nitrily R – NH 2 aminy Rδ+ – Xδ-
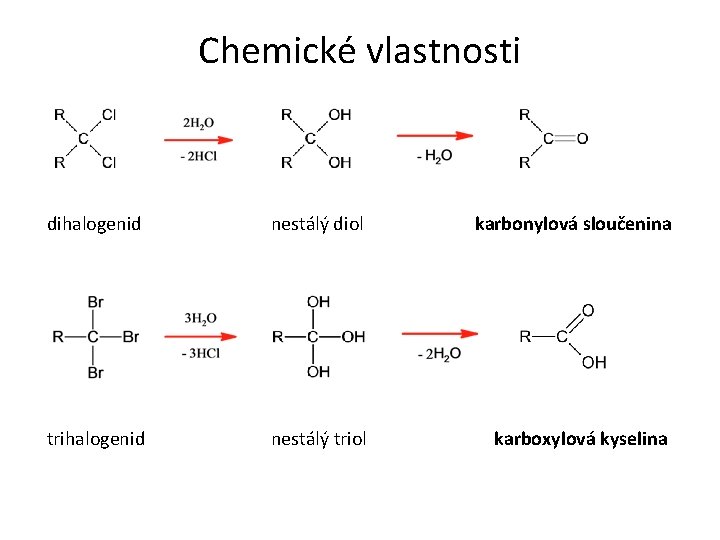
Chemické vlastnosti dihalogenid nestálý diol karbonylová sloučenina trihalogenid nestálý triol karboxylová kyselina
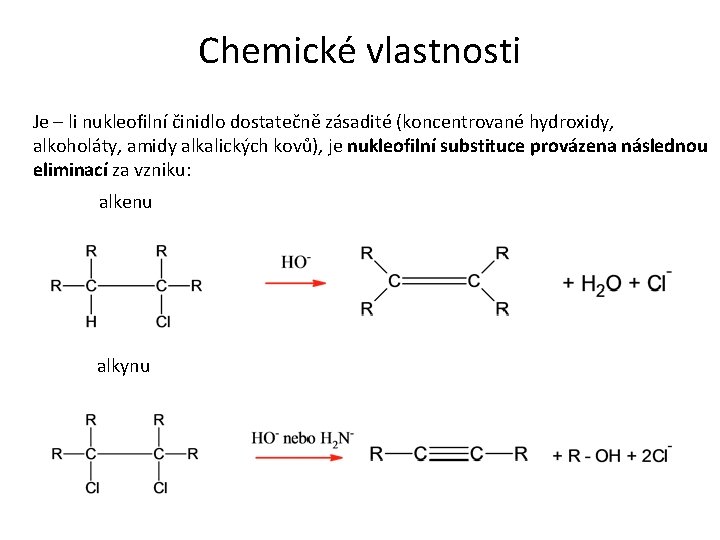
Chemické vlastnosti Je – li nukleofilní činidlo dostatečně zásadité (koncentrované hydroxidy, alkoholáty, amidy alkalických kovů), je nukleofilní substituce provázena následnou eliminací za vzniku: alkenu alkynu

Reakce alkylhalogenidů s kovy S hořčíkem vznikají Grignardovy sloučeniny, důležité v organické syntéze. CH 3 -CH 2 -Br + Mg CH 3 -CH 2 Mg. Br S Na, Zn, Ag vznikají uhlovodíky s dvojnásobným počtem atomů uhlíku. Využíváno při zušlechťování benzínových frakcí.

Přehled zástupců Chlormethan CH 3 Cl, jodmethan CH 3 I – metylační činidla v organických syntézách Trichlormethan, chloroform CHCl 3 – rozpouštědlo, anestetické účinky. Nebezpečí vzniku fosgenu reakcí se vzdušným kyslíkem působením světla. 2 Trijodmethan, jodoform CHI 3 – desinfekční činidlo, k analytickému důkazu primárních alkoholů a ketonů (jodoformová reakce).
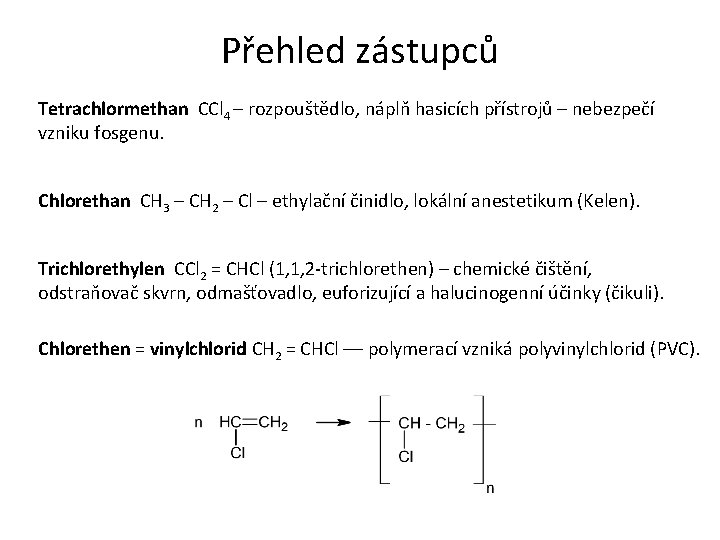
Přehled zástupců Tetrachlormethan CCl 4 – rozpouštědlo, náplň hasicích přístrojů – nebezpečí vzniku fosgenu. Chlorethan CH 3 – CH 2 – Cl – ethylační činidlo, lokální anestetikum (Kelen). Trichlorethylen CCl 2 = CHCl (1, 1, 2 -trichlorethen) – chemické čištění, odstraňovač skvrn, odmašťovadlo, euforizující a halucinogenní účinky (čikuli). Chlorethen = vinylchlorid CH 2 = CHCl –– polymerací vzniká polyvinylchlorid (PVC).
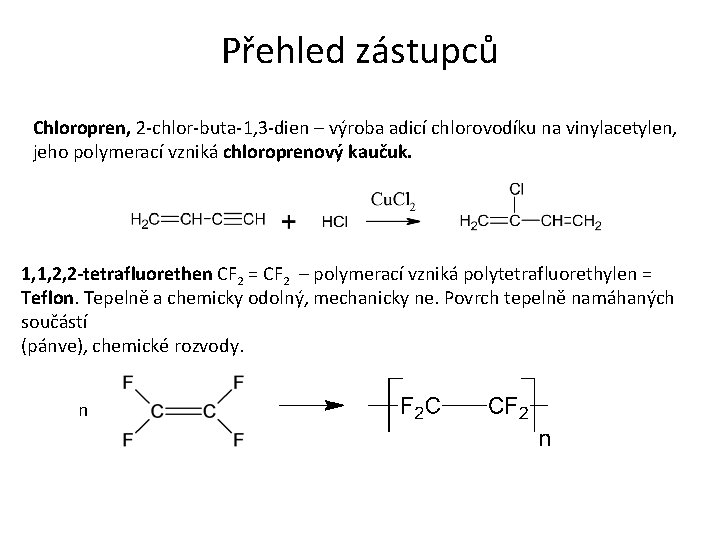
Přehled zástupců Chloropren, 2 -chlor-buta-1, 3 -dien – výroba adicí chlorovodíku na vinylacetylen, jeho polymerací vzniká chloroprenový kaučuk. 1, 1, 2, 2 -tetrafluorethen CF 2 = CF 2 – polymerací vzniká polytetrafluorethylen = Teflon. Tepelně a chemicky odolný, mechanicky ne. Povrch tepelně namáhaných součástí (pánve), chemické rozvody. n

Přehled zástupců Gamexan – C 6 H 6 Cl 6 (1, 2, 3, 4, 5, 6 -hexachlorcyklohexan) – insekticid – od roku 2009 podle Stockholmské úmluvy u nás nepoužíván, v zemích, které nepodepsaly, používán. Zařazen mezi POP – perzistentní organické polutanty. Freony – polyhalogenderiváty, musí obsahovat alespoň dva halogeny, jedním z nich musí být fluor. Nejedovaté, nehořlavé, chemicky odolné, nízké body varu => chladící media, hnací plyny, izolanty. Omezování jejich použití – při úniku do atmosféry narušení ozonové vrstvy. Polychlorované bifenyly (PCB) – 210 derivátů. Snižují povrchové napětí => zvýšená přilnavost, nižší tření – barviva, hydraulická zařízení, teplonosná média, elektrotechnika. Karcinogenní, kumulativní jedy.
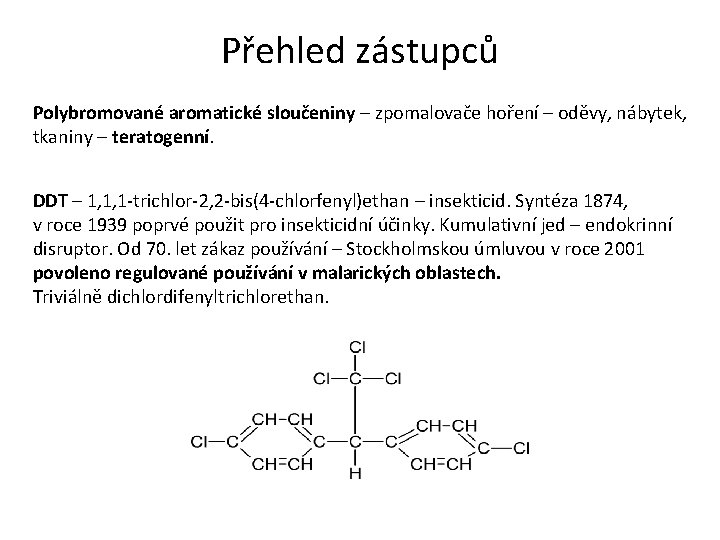
Přehled zástupců Polybromované aromatické sloučeniny – zpomalovače hoření – oděvy, nábytek, tkaniny – teratogenní. DDT – 1, 1, 1 -trichlor-2, 2 -bis(4 -chlorfenyl)ethan – insekticid. Syntéza 1874, v roce 1939 poprvé použit pro insekticidní účinky. Kumulativní jed – endokrinní disruptor. Od 70. let zákaz používání – Stockholmskou úmluvou v roce 2001 povoleno regulované používání v malarických oblastech. Triviálně dichlordifenyltrichlorethan.

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura 1. ČERVINKA, Otakar a kol. Mechanismy organických reakcí: učebnice pro vys. školy chemickotechnologické. 1. vyd. Praha: SNTL, 1976. 483, [1] s. Řada chemické literatury. 2. HALBYCH, Josef a KLÍMOVÁ, Helena. Didaktika organické chemie: příklady vyučovacích postupů. 1. vyd. Praha: Univerzita Karlova, 1988. 158 s. 3. MCMURRY, John. Organická chemie. Vyd. 1. V Brně: VUTIUM, 2007. xxv, 1176, 61, 31 s. Překlady vysokoškolských učebnic; sv. 2. ISBN 978 -80 -214 -3291 -8. 4. PACÁK, Josef. Stručné základy organické chemie. 1. vydání. Praha: SNTL Nakladatelství technické literatury, 1975. Řada chem. literatury. 5. Fotografie a vzorce z vlastní databáze autora. Vytvořeny programy ACD FREE 12, Snagit Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 17