HALOGENDERIVTY reakce bimolekulrn substituce SN 2 reakce charakteristick

HALOGENDERIVÁTY reakce bimolekulární - substituce SN 2 reakce charakteristická pro nerozvětvené halogenderiváty S N 2
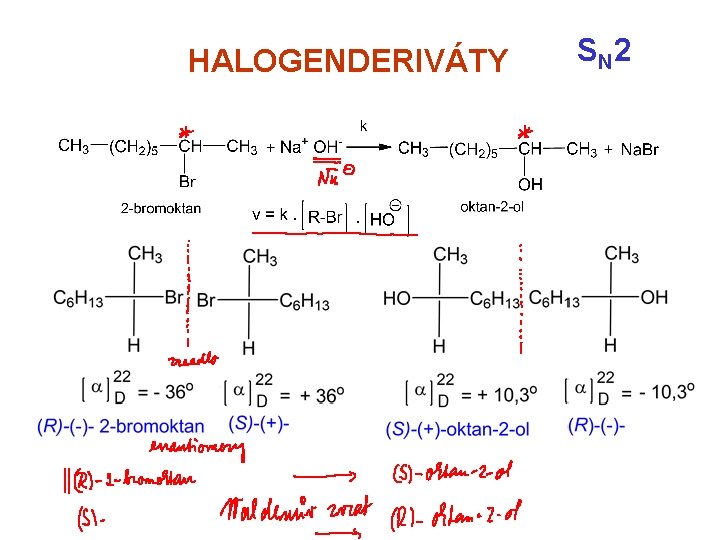
HALOGENDERIVÁTY S N 2
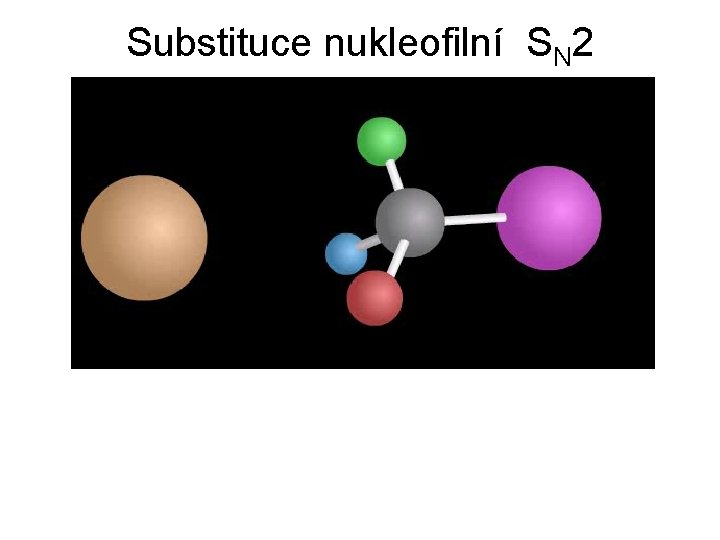
Substituce nukleofilní SN 2
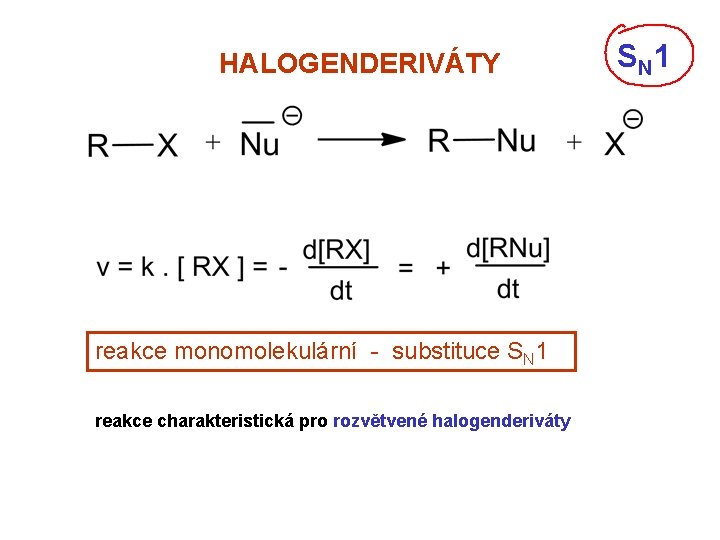
HALOGENDERIVÁTY reakce monomolekulární - substituce SN 1 reakce charakteristická pro rozvětvené halogenderiváty S N 1
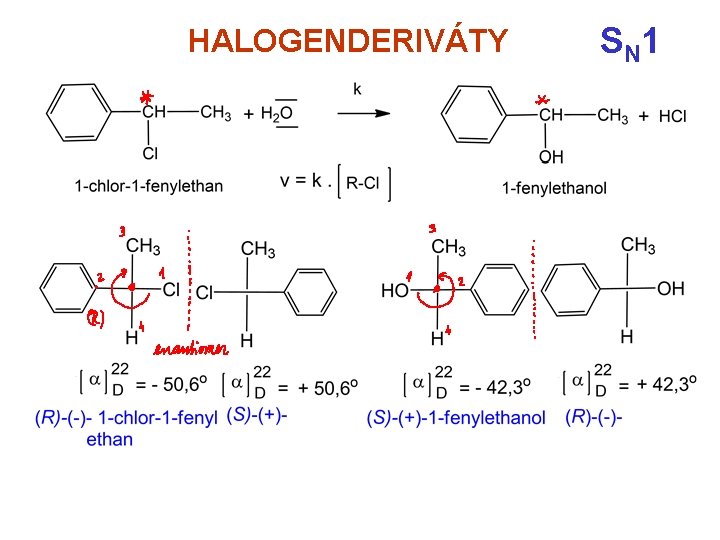
HALOGENDERIVÁTY S N 1
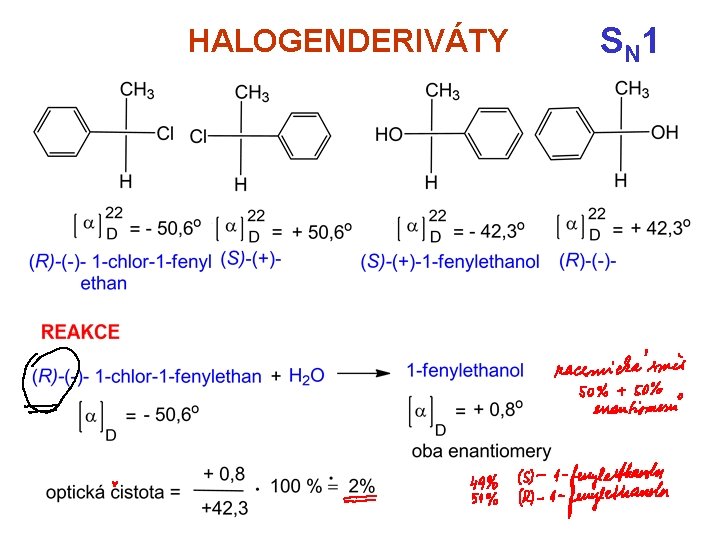
HALOGENDERIVÁTY S N 1
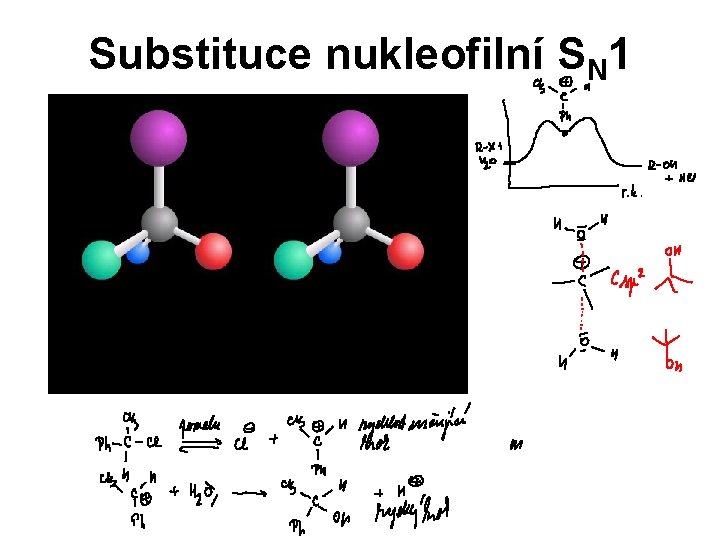
Substituce nukleofilní SN 1
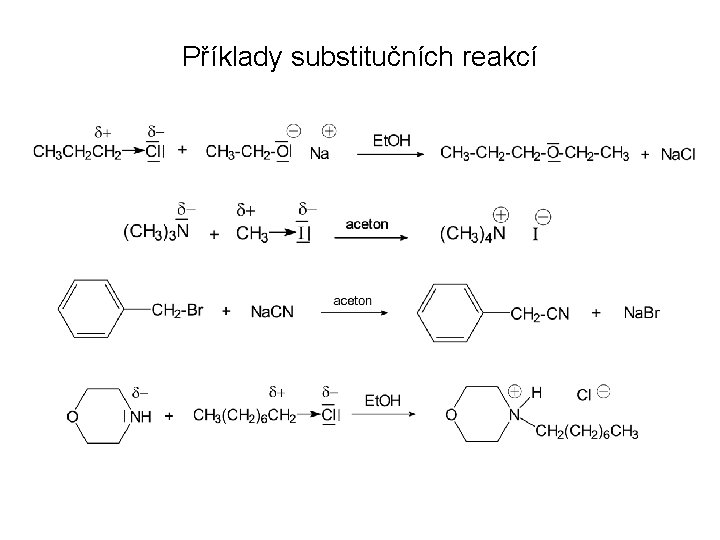
Příklady substitučních reakcí
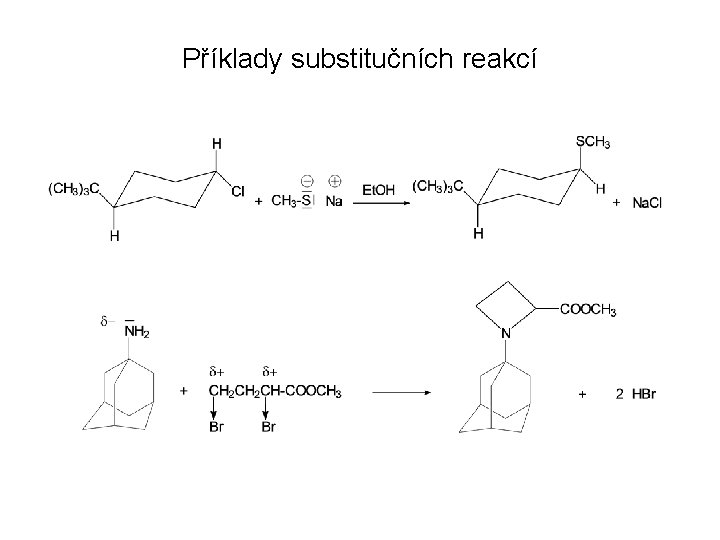
Příklady substitučních reakcí

• Průběh reakce ovlivňuje: struktura: nerozvětvené ---- SN 2 rozvětvené --- SN 1 při SN 2 se liší jednotlivé deriváty rychlostí reakce: methyl>prim. halogenid>sek. hal. >terc. hal 30 1 0, 02 důvodem je sterická zábrana rel. rychlost při SN 1 hraje roli elektronový vliv jsou omezeny na terciární halogenderiváty nebo allyl či benzylderiváty

Průběh reakce ovlivňuje: • vliv koncentrace a síly nukleofilu ovlivnění jen u reakcí SN 2 (u SN 1 se v rychlostní rovnici nevyskytuje koncentrace nukleofilu) -nukleofilita roste u atomů v periodickém systému zleva doprava a shora dolů -nabitý ion je vždy nukleofilnější než jeho konjugovaná kyselina(neutrální molekula) -nukleofilita u stejných atomů je paralelní s bazicitou

Průběh reakce ovlivňuje: • rozpouštědlo typy rozpouštědel: nepolární protická aprotická

Průběh reakce ovlivňuje: • nukleofilita se mění s polaritou rozpouštědla -v polárním rozpouštědle je větší atom nukleofilnější (polarizovatelnost je větší – měkkčí, malý atom je solvatován vodíkovými můstky a tak vyřazen z reaktivity) R-SH > ROH J- > Br- > Cl- > F- - v aprotickém prostředí je pořadí opačné - F- > Cl- > Br- > I-

Průběh reakce ovlivňuje: • vliv odstupující skupiny - čím stabilnější skupina odstupuje, tím snazší je substituce I- > Br- > Cl- > F- v kyselém prostředí můžeme ulehčit substituci např. u alkoholů či etherů - významnou odstupují skupinou jsou sirné zbytky (tosyláty, mesyláty, nosyláty, brosyláty atp. )

- Slides: 15