Hallo liebe 8 A Endspurt Schaut euch bitte

Hallo liebe 8 A! Endspurt! • Schaut euch bitte diese Power Point Präsentation als Bildschirmpräsentation vorne nach hinten an. • Versucht dabei bitte die gestellten Aufgaben zu erfüllen. • Das Tafelbild am Ende der Präsentation übertragt ihr bitte in euer Chemieheft und schickt mir ein Foto des Hefteintrags bis spätestens Sonntag (23: 59) an: c. keonig. lehrer@gmail. com
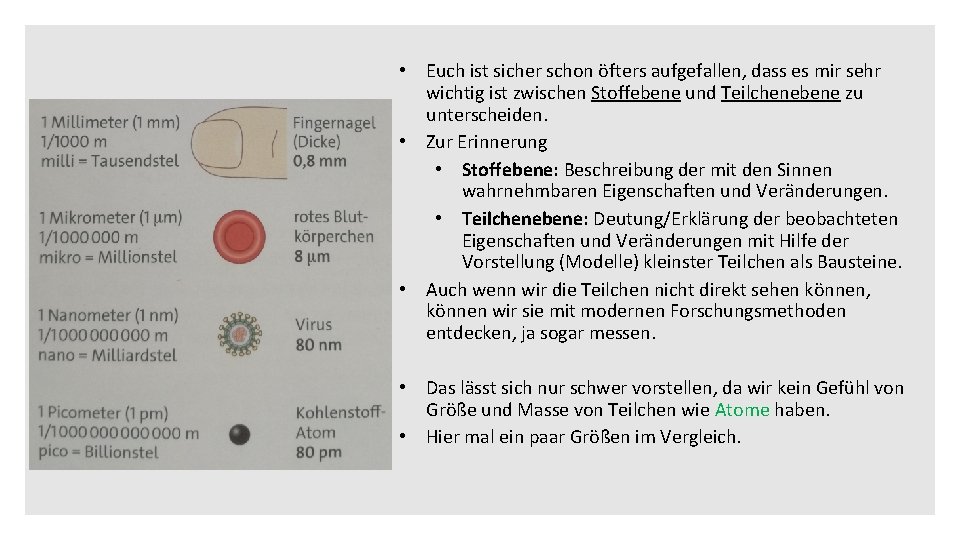
Stoffe und Teilchen • Euch ist sicher schon öfters aufgefallen, dass es mir sehr wichtig ist zwischen Stoffebene und Teilchenebene zu unterscheiden. • Zur Erinnerung • Stoffebene: Beschreibung der mit den Sinnen wahrnehmbaren Eigenschaften und Veränderungen. • Teilchenebene: Deutung/Erklärung der beobachteten Eigenschaften und Veränderungen mit Hilfe der Vorstellung (Modelle) kleinster Teilchen als Bausteine. • Auch wenn wir die Teilchen nicht direkt sehen können, können wir sie mit modernen Forschungsmethoden entdecken, ja sogar messen. • Das lässt sich nur schwer vorstellen, da wir kein Gefühl von Größe und Masse von Teilchen wie Atome haben. • Hier mal ein paar Größen im Vergleich.

• Natürlich können wir ein Atom nicht einfach auf die Waage legen, um zu bestimmen welche Masse es hat. • Die Massen von einzelnen Atomen (absolute Atommasse) können über eine physikalische Methode ermittelt werden, die Massenspektrometrie heißt. Atommassen Nur bei Interesse: • Dazu werden die Atome verdampft und erhalten eine Ladung. • Die so gewonnenen Ionen werden durch ein elektrisches Feld geführt und anschließend nach der Masse sortiert. • Leichte Ionen legen einen relativ langen Weg im elektrischen Feld zurück, schwere Ionen werden kaum abgelenkt.

Absolute Atommassen

Relative Atommassen • Die Verwendung der tatsächlichen absoluten Atommassen ist weder praktisch noch sinnvoll. • Um das chemische Rechnen mit den sehr kleinen Zahlenwerten der absoluten Atommassen zu vermeiden, nutzt man einen interessanten Zusammenhang: • Die Massen unterschiedlicher Atomsorten (Elemente) sind häufig ein ganzzahliges Vielfaches der Masse eines Wasserstoff-Atoms. • Darum wählte man das Wasserstoff-Atom als Bezugspunkt. • Ihm ordnete man die relative Atommasse 1 zu. • Da es sich um Verhältniszahlen handelt, haben die relativen Atommassen keine Einheit. • In vielen Periodensystemen ist die relative Atommasse der Elemente oben links angegeben.

Relative Molekülmassen Absolute Atommasse von Sauerstoff

• Schau dir zur Zusammenfassung nochmal dieses Video an: https: //www. youtube. com/watch? v=x. Qaafi 2 z. Lik Die Masse von Atomen

• Auf der nächsten Seite findest du das Tafelbild und Übungsaufgaben • Übertrage das bitte in dein Chemieheft und schicke mir ein Foto des Hefteintrags und deiner Lösungen bis spätestens Sonntag (23: 59) an: c. keonig. lehrer@gmail. com


Relative Atommassen kann man im Periodensystem bei den einzelnen Elementen links oben ablesen. Zum Beispiel Kohlenstoff (C) mit 12. Für beide Arten von Massen gilt: Die Masse der Moleküle ist die Summe der Masse der einzelnen Atome, aus denen sie zusammengesetzt sind. Bsp: relative Masse von. . . H 2 O 1 + 16 = 18 CO 2 12 + 16 = 44

Übung 1: Welches Element ist ungefähr halb so schwer wie Kohlenstoff, welches ist doppelt und welches dreimal so schwer? Für Hilfe hier klicken Übung 2: Berechne die relative Molekülmasse von H 2 O 2 und NH 3! Übung 3: Berechne die relative Molekülmasse von C 6 H 12 O 6! Für Hilfe hier klicken
- Slides: 11