HALGENOS Fluor Cloro Bromo Iodo y At GENERALIDADES

HALÓGENOS Fluor, Cloro , Bromo, Iodo y At GENERALIDADES : Forman moléculas en fase gaseosa, líquida o sólida. Electronegatividad, poder oxidante, longitud de enlace. ENERGÍA DE ENLACE Pequeño tamaño de los átomos, repulsión de electrones sin compartir, interaccion de orbitales d-d. Métodos de obtención de los Halógenos. a) b) Métodos electrolíticos ( todos) Empleo de agentes oxidantes ( todos , menos el fluor )
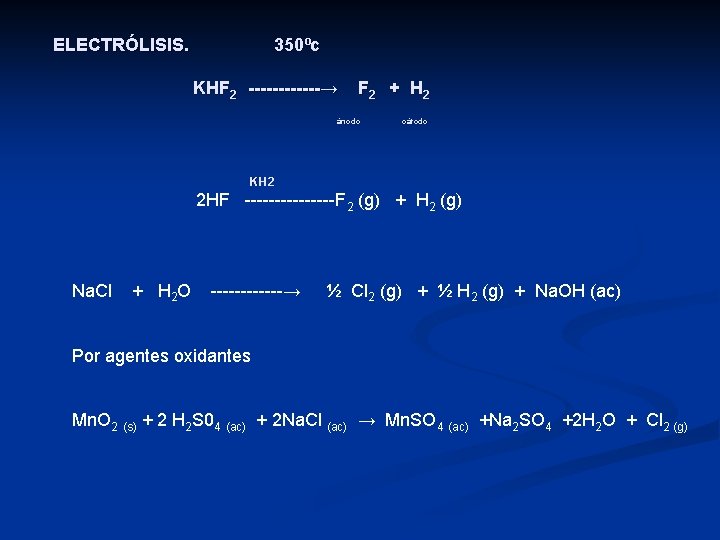
ELECTRÓLISIS. 350ºc KHF 2 ------→ F 2 + H 2 ánodo cátodo KH 2 2 HF --------F 2 (g) + H 2 (g) Na. Cl + H 2 O ------→ ½ Cl 2 (g) + ½ H 2 (g) + Na. OH (ac) Por agentes oxidantes Mn. O 2 (s) + 2 H 2 S 04 (ac) + 2 Na. Cl (ac) → Mn. SO 4 (ac) +Na 2 SO 4 +2 H 2 O + Cl 2 (g)

Métodos industriales de obtención de Bromo y Yodo. BROMO. A partir de las aguas de mar : Cl 2 + 2 Br- ----→ Br 2 + 2 Cl. Cuidado, el bromo a BAJAS CONCENTRACIONES HIDROLIZA DANDO : Br 2 + H 20 -------> Br- + Br. O- + 2 H + Los vapores de bromo ( p. e = 58ºC ) son arrastrados mediante una corriente de aire hacia una solución de Na 2 CO 3 3 Br 2 + 3 Na 2 C 03 →Na. Br 03 (ac) + 5 Na. Br (ac) + 3 CO 2 (g) Br. O 3 - + 5 Br- + 6 H+ → 3 Br 2 (l) + 3 H 2 O ( destilación fraccionada)

OBTENCIÓN INDUSTRIAL DEL YODO. A partir del caliche 2 IO 3 – (ac) + 5 HSO 3 - → ·HSO 4 - + 2 SO 4 - + H 2 O + I 2 (s) El yodo asi obtenido se filtra y se purifica por sublimación. PROPIEDADES QUÍMICAS 1. GRAN PODER OXIDANTE : F 2 > Cl 2 > Br 2 > I 2 2 Reaccionan entre si para dar compuestos interhalogenados Ej : ICl y con iones haluros para dar polihaluros : I 2 + I- → I 3 3. Los halógenos presentan alguna solubilidad en agua , mediante alguno de los siguientes mecanismos

2 X 2 + H 2 O → 4 H+ + 4 X - + O 2 F 2 Eº n Cl 2 2, 0 0, 54 X 2 + H 2 0 → n Br 2 0, 25 H+ + X - F 2 Cl 2 ------ , 7 x 10 -4 Eº I 2 -0, 28 + HXO Br 2 I 2 n n K= 5, 8 x 10 -9 3 x 10 -13

Acción decolorante y desinfectante del cloro = Cl. O- n 3. Acción de los halógenos frente a los álcalis : Fluor : a) con soluciones diluídas y en frío n 2 F 2 + 2 KOH → 2 KF + F 2 O + H 2 O n n n B) Con soluciones concentradas y en caliente : 2 F 2 + 4 OH- → 4 F- + O 2 + 2 H 2 O El resto de los halògenos (Cl 2 , Br 2; I 2 ) reaccionan en forma diferente

A ) Con álcalis diluídos y en frío: 2 OH - + X 2 → X- + XO- + H 2 O B) Con álcalis concentradas y en caliente: C) 6 OH- + 3 X 2 → 5 X - + XO 3 - + 3 H 2 O Caso especial del yodo con álcalis diluído y en frío

2 OH - + I 2 <-----> I - + IO - + H 2 O 3 IO- → IO 3 - + 2 I - HIDRÁCIDOS Ver propiedades físicas Obtención de laboratorio de ( HCl y HF) Ca. F 2 + H 2 SO 4 → Na. Cl + H 2 SO 4 Ca. SO 4 (s) 2 HF (g) → Na. HSO 4 + HCl (g)

El resto de los hidrácidos no se forman así, debido a que el ácido sulfúrico oxida a los hidrácidos formados al halógeno correspondiente, de la forma siguiente. 2 HX + H 2 SO 4 → n Se emplea H 3 PO 4 que no es oxidante: n Na. Br + H 3 PO 4 → n Na. I n n X 2 + SO 2 +2 H 2 O + H 3 PO 4 → HBr + Na. H 2 PO 4 HI + Na. H 2 PO 4 -------------------Por qué el HF es el único líquido a tº ambiente

Hacer esquema : El HF concentrado disuelve a la mayoría de los metales, excepto Au y Pt también ataca a la sílice y silicatos ( ataca al vidrio, se debe almacenar en frascos de polietileno ) a) Si. O 2 (s) + 4 HF → b) Si. O 3 -2 + 6 HF → Si. F 4 (g) + 2 H 2 O Si. F 6 -2 + 3 H 2 O Los hidrácidos al estado gaseoso son esencialmente covalentes, pero en solución acuosa ionizan completamente , actuando como ácidos fuertes a excepción del HF. Como sabemos a mayor dilución mayor % de disociación, lo contrario sucede con el HF, la disociación aumenta en soluciones concentradas debido a la formación del HF 2 - , ya que el HF dimeriza H 2 F 2 → HF 2 - + H +

Cuál de los hidrácidos es el mas fuerte. Determínelo a partir de las tablas. Factores que desfavorecen al HF : a) puente de hidrógeno desfavorece el Δ H de disociación b) pequeño tamaño del F- alto grado de hidratación hace disminuir el ΔS. n n LOS OXACIDOS Son buenos agentes oxidantes Cl 2 Br 2 H+ + HXO + e- → ½ X 2 (g, l, s) + H 2 O 1, 63 1, 59 6 H+ + XO 3 - + 5 e- → ½ X 2 (g, l, s) + H 2 O 1, 47 n 1, 52 I 2 1, 45 1, 20

ACIDOS HIPOHALOSOS. Obtención X 2 + H 20 2 X 2 <---→> H+ + X - + HXO + H 2 O + Hg. O → 2 HXO + Hg. X 2 (s) n ACIDOS HALOSOS. El ùnico existente es el HCl. O 2 , mucho mas fuerte que el ácido hipocloroso, pero sigue siendo un ácido débil: n Preparación : n Ba(OH)2 n Ba (Cl. O 2)2 + H 2 SO 4 n Por su carácter oxidante se usa como blanqueador industrial. + H 2 O 2 + Cl. O 2 → → Ba( Cl. O 2)2 + 2 H 2 O + O 2 (g) Ba. SO 4 (s) + 2 HCl. O 2

Ácidos hálicos y halatos Δ 3 X 2 (g, l) + 6 OH – (ac) → XO 3 – (ac) + 5 X- (ac) + 3 H 2 O El HIO 3 se puede preparar también : I 2 (ac) + 10 HNO 3 (ac) → 2 HIO 3 + 10 NO 2 (g) + 4 H 2 O El yodato se encuentra en grandes cantidades en algunos minerales chilenos y de aquí se obtiene eol yodo : 2 IO 3 – (ac) + 5 HSO 3 – (ac) → I 2 (s) + 5 SO 4 -2 + 3 H+ + H 2 O También el yodo se puede obtener : IO 3 - + 5 I- + 6 H+ → 3 I 2 (ac) + 3 H 2 O

Los halatos (sales) se obtienen al hacer reaccionar el halógeno respectivo con una solución concentrada y caliente de álcali : X 2 + 6 OH - → XO 3 - + 5 X- + 3 H 2 O n n n ACIDOS PERHÁLICOS. El HCl. O 4 , es el ácido mas fuerte en la química inorgánica , es muy inestable, EXPLOTA en contacto de sustancias orgánicas. En soluciones concentradas , actúa como agente oxidante : Cl. O 4 - + 2 H+ + 2 e- → Cl. O 3 - + H 2 O Obtención de laboratorio: KCl. O 4 + H 2 SO 4 → KHSO 4 + HCl. O 4 Eº = 1, 19 V

El ácido peryódico se presenta en varias formas en soluciones fuertemente ácidas, es el ácido paraperyódico , el cuál en solución acuosa esta en equilibrio con el ácido metaperyódico 80ºC 100ºC 2 H 5 IO 6 → H 4 I 2 O 9 → 2 HIO 4 ac. Paramesoperac. Metaperperyódico yodico. n n n Dado el siguiente diagrama de Latimer en medio básico, señale si el Cl 2(g ) es estable, fundamente su respuesta, empleando las semireacciones respectivas con sus potenciales y la reacción final con su Δ Eº -1, 38 Cl - ----- - O, 4 Cl 2 ----- Cl. O -

2 OH - + ½ Cl 2 → Cl. O- + H 2 O + e- Eº = - 0, 4 V e- + ½ Cl 2 → Cl Eº = 1, 38 V -----------------------------------------------Cl 2 + 2 OH - → Cl. O - + Cl - + H 2 O Δ Eº = 0. 98 V El cloro no es estable en una solución acuosa alcalina , porque desproporciona COMPUESTOS INTERHALOGENADOS. AX , AX 3 , AX 5 , AX 7. A = Halógeno menos electronegativo. Compuestos formados por enlace covalente, mínima diferencia de electronegatividad ( Ver guia)

Los compuestos AX estructuralmente son análogos a las moléculas de halógenos pero con cierta polaridad. En los otros tipos de compuestos, existe un elemento central de mayor tamaño, rodeados de otros átomos de halógenos de menor tamaño. Estas relaciones de tamaño explica porque existe el I F 7 y no el Br. F 7 , si el Br. F 5 y no el Cl. F 5 Estructura de los compuestos: AX 3 AX 5 D. E. = bipirámide trigonal Geometria Forma de T D. E. = bipirámide AX 7 D. E. = bipirámide de base cuadrada Pirámide de base cuadrada DIBUJAR LAS ESTRUCTURAS RESPECTIVAS pentagonal idem.

Grupo VI Anfigenos O , Se , Te , ( Po ) Un isótopo importante del oxígeno es el ozono. Introducción : mas o menos a 100 Km de la corteza terrestre se ubica una capa de la atmosfera llamada Ionosfera en donde se encuentran iones como O + , NO+ , O 2 + , N 2+ y e La ruptura de enlaces y remoción de e- son inducidos por la luz ( fotodisociación , fotoionización ) O 2 Si hν -----> O + O ( fotodisociación ) = 1, 21 Aº ----- = 1, 49 Aº Cuál será la estructura del ozono ? ? ?

Mecanismo de reacción de la fotodisociación del O 2 N 2 → N 2 + + e – N 2+ + e - → N + N N + O 2 → NO + O N + NO → N 2 + O Aunque la mayoría de la radiación de alta energía, se absorbe en la ionosfera, una pequeña cantidad llega a la estratosfera , rompe el enlace O 2 en O , estos a su vez colisionan con otras moléculas de oxigeno , para formar ozono O 2 (g) -----> 2 O (g) M* + O (g) + O 2 (g) -----> O 3 (g) + M.

El ozono estratosférico es esencial para la vida, pues absorbe las radiaciones U. V. las que asu vez descomponen al ozono. O 3 (g) UV ------→ O 2 (g) + O (g) Si estas radiaciones llegasen a la tierra : cáncer, mutaciones génicas, incluso romper enlaces en el ADN. VARIACIONES ESTACIONALES DE LA CAPA DE OZONO. Pero a lo largo del año hay una constante en su formación y destrucción a traves de los siguientes procesos O 2 (g) + O (g) -----→ O 3 (g) formación O 3 (g) + O (g) ------→ 2 O 2 (g) Ruptura. Por que entonces se dice que esta desapareciendo la capa de ozono. Por que hay elementos contaminantes, aportados por el hombre que han destruído a este elemento tan importante.
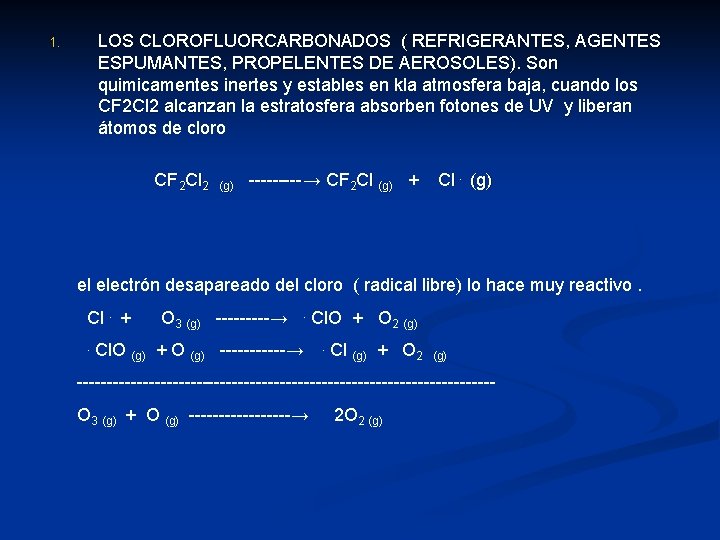
LOS CLOROFLUORCARBONADOS ( REFRIGERANTES, AGENTES ESPUMANTES, PROPELENTES DE AEROSOLES). Son quimicamentes inertes y estables en kla atmosfera baja, cuando los CF 2 Cl 2 alcanzan la estratosfera absorben fotones de UV y liberan átomos de cloro 1. CF 2 Cl 2 (g) -----→ CF 2 Cl (g) + Cl. (g) el electrón desapareado del cloro ( radical libre) lo hace muy reactivo. Cl. +. O 3 (g) -----→ . Cl. O (g) + O (g) ------→ Cl. O + O 2 (g). Cl (g) + O 2 (g) -----------------------------------O 3 (g) + O (g) ---------→ 2 O 2 (g)

Oxidos de nitrógeno y Smog N 2 + O 2 ---> NO (g) 2 NO (g) + O 2 (g) Δ H = 180 kj ----> 2 NO 2 (g) Δ H = - 113 Kj hv NO 2 (g) -------> NO (g) + O (g) 393 nm O (g) + O 2 (g) + M * -----→ O 3 (g) + M AZUFRE. Presenta diversas formas alotrópicas y las propiedades estructurales de algunas de ellas son muy complejas, la estructura primitiva es S 8 para las estructuras mas estables a tº ambiente ( ROMBICA Y MONOCLÍNICA )

S ( romb) 95, 5 ºC ------> S (monocl. ) ΔH = 760 cal. Las velocidades a que tienen lugar estas transformaciones reversibles son tan pequeñas que con frecuencia pueden conservarse en cualquier de las dos formas durante dias alejadas del punto de transición. Ambas formas son solubles en solventes orgánicos especialmente en CS 2 Cuando se tiene S líquido aprox. Por sobre los 200ºC las moléculas se abren y forman largas cadenas que si se vierten en agua fría adquieren un aspecto gomoso conocido como azufre plástico que son cadenas helicoidales de átomos. Este azufre plástico es inestable y se transforma lentamente a la forma cristalina rómbica. Vapor de S : S 8 , S 4, S 2, dependiendo de la temperatura. De esta forma, tanto en su fase sólida, líquida y gaseosa el azufre presenta una variedad de estructuras moleculares

El Selenio también en su estructura molecular presenta Se 8 en forma rómbica y monoclínica, existe una tercera forma alotrópica que se denomina gris , que tiene forma de espiras. Conduce la electricidad en presencia de luz y muy poco en la oscuridad, se emplean en celdas fotoeléctricas. El telurio presenta una forma alotrópica color blanco plata, semi metálica e isomorfa de la forma gris del Selenio SO 2 : Obtención Industrial Δ 2 Zn. S + 3 O 2 (g) -----> 2 SO 2 (g) + 2 Zn. O Obtención de Laboratorio : Δ Cu + 2 H 2 SO 4 PROPIEDADES. ------> Cu. SO 4 + SO 2 (g) + H 2 O.
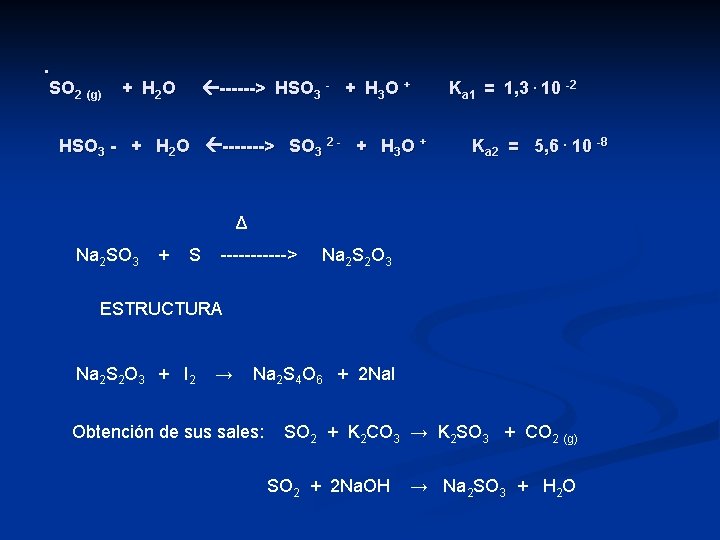
. SO 2 (g) + H 2 O ------> HSO 3 - + H 3 O + HSO 3 - + H 2 O -------> SO 3 2 - + H 3 O + Ka 1 = 1, 3. 10 -2 Ka 2 = 5, 6. 10 -8 Δ Na 2 SO 3 + S ------> Na 2 S 2 O 3 ESTRUCTURA Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I Obtención de sus sales: SO 2 + K 2 CO 3 → K 2 SO 3 + CO 2 (g) SO 2 + 2 Na. OH → Na 2 SO 3 + H 2 O

Es un enérgico reductor: Br 2 + SO 2 + 2 H 2 O → 2 Br- + HSO 4 - + 3 H+ 2 IO 3 - + 5 SO 2 + 2 H 2 O → I 2 + 5 SO 4 -2 + 4 H+ APLICACIONES : Pt SO 2 (g) + ½ O 2 -----> SO 3 450ºC Blanquedor de lanas , pulpas de papel. En fumigaciones para destruir bacterias y hongos H 2 SO 4. Obtención industrial : Método de contacto: 450 ºC a) SO 2 (g) + ½ O 2 (g) -------> Pt SO 3

b) SO 3 + H 2 SO 4 c) H 2 S 2 O 7 + H 2 O → H 2 S 2 O 7 ac. Pirosulfúrico. ( 0 leum = H 2 SO 4 + SO 3) → 2 H 2 SO 4 MÉTODO DE LAS CAMARAS DE PLOMO A) 2 NO (g) + O 2 (g) → 2 NO 2 (g) B) 3 NO 2 (g) + SO 2 (g) + H 2 O → 2 NOHSO 4 + NO C ) 2 NOHSO 4 + H 2 O → 2 H 2 SO 4 + NO 2 Reacciones caracteristicas : Ba. SO 4 + HCl → N. H. R. Ba. SO 3 + HCl → Ba. Cl 2 + SO 2 (g) + H 2 O PROBLEMA. Una muestra de 6, 55 g de una mezcla de. Na 2 SO 3 y Na 2 SO 4 se disolvió en agua y se calentó con azufre sólido. El Na 2 SO 4 no reacciona , pero el Na 2 SO 3 si : Na 2 SO 3 + S → Na 2 S 2 O 3 y 1, 23 g de azufre se disolvieron y formaron Na 2 S 2 O 3. ¿ Que % de la muestra original era Na 2 SO 3 ?

n 126 g de Na 2 SO 3 / 32 g de S n X = 4, 84 g de Na 2 SO 3 = x g de Na 2 SO 3 / 1, 23 g de S 4, 84 / 6, 55 x 100 = 79, 94 % El ácido sulfúrico puro es un líquido viscoso, conductor de la electricidad, porque sufre una pequeña disociación. El ácido sulfúrico puro, tiene poder deshidratante H –COOH + H 2 SO 4 → CO (g) + SO 2 (g) + 2 H 20 En soluciones concentradas actua como un buen agente oxidante disolviendo metales como el cobre : Cu + H 2 SO 4 (conc ) → Cu +2 (ac) + SO 2 (ac) + 2 H 2 O en cambio el H 2 SO 4 en soluciones diluídas, no posee capacidad oxidante, solo actúa como ácido H 2 SO 4 + Ba. Cl 2 → Ba. SO 4 (s) + 2 HCl

HIDRUROS DEL GRUPO VI Ver tabla. Ka 1 H 2 O 1 O 4, 5º H 2 S 92 º H 2 Se 91 º H 2 Te 90º 10 -7 10 -4 2 x 10 -3 Mayor tamaño, aumenta la acidez a pesar de que son menos iónicos. ¿ Por que ? Por que disminuye el ángulo: Interacción de electrones no compartidos en el átomo central, el oxigeno por ser muy electronegativo, atrae los electrones enlazantes con tal fuerza que interactúa con los electrones no enlazantes. En el S aumenta el tamaño del átomo , la electronegatividad disminuye, lo que determina que disminuya la interacción entre electrones enlazantes y no enlazantes

H 2 S : es un ácido débil diprótico cuyas constantes de acidez son : H 2 S -----> H+ + HS - ------>H+ + S -2 Ka 1 = 10 -7 Ka 2 = 10 -14 [ H + ] 2 [ S -2 ] ------------ = Ka 1. Ka 2 [ H 2 S ] Su principal aplicación en el laboratorio, es el empleo como agente pp, debido a que puede liberar una cantidad determinada de S -2 de acuerdo al p. H del medio, lo que permite separar diversos iones que estan presentes en una misma solución

n PROBLEMA Se hace burbujear H 2 S sobre una solución que contiene los siguientes cationes en una concentración 0, 01 M : Pb +2 Fe +2 y Mn +2 suponga que la solución se satura con 0, 01 M de H 2 S. a) Que cationes pp a p. H = 1 b) A que p. H pp solamente el Fe +2 ? c ) A que p. H pp. el Mn +2 ? Datos : Kps : Pb. S = 3, 4 x 10 -28 Fe. S = 3, 7 x 10 -19 De la formula señalada anteriormente se deduce: Ka 1 x Ka 2 x [ H 2 S] [ S -2 ] = --------------[H+]2 Mn. S = 1, 4 x 10 -15
![a) Que cationes pp a p. H = 1 [ S -2] = 10 a) Que cationes pp a p. H = 1 [ S -2] = 10](http://slidetodoc.com/presentation_image_h/dec414256ad00a125b42bd8d52dbd777/image-32.jpg)
a) Que cationes pp a p. H = 1 [ S -2] = 10 -21. [ 10 -2] ---------- = 10 -21 [ 10 -2] [ x +2] [ S -2] = 10 -2 x 10 -21 Kps) b) A que p. H pp solamente el Fe +2 = 10 -23 Sólo pp Pb. S ( > ? Ka 1 x Ka 2 x [ H 2 S ] [ H +] 2 = --------------------------- [ S Kps Fe. S / [ Fe -2 ] +2]
![10 -21 x 10 -4 [ H+ ] 2 10 x 10 -26 = 10 -21 x 10 -4 [ H+ ] 2 10 x 10 -26 =](http://slidetodoc.com/presentation_image_h/dec414256ad00a125b42bd8d52dbd777/image-33.jpg)
10 -21 x 10 -4 [ H+ ] 2 10 x 10 -26 = -----------3, 7 x 10 = -------- = 2, 7 x 10 = 7. 14 x 10 -7 3, 7 x 10 -19 [ H+ ] = 5, 2 x 10 -4 p. H = 3, 28 ~ 3, 3 C ) A que p. H pp. el Mn +2? 10 -21 x 10 -4 [ H+] = -------1, 4 x 10 [ H+] = 8, 45 x 10 -6 -15 10 -26 = ------1, 4 x 10 -15 p. H = 5, 07 ~ 5, 1 -11
![Si el p. H es ácido [ S -2 ] disminuye, pp aquellos cationes Si el p. H es ácido [ S -2 ] disminuye, pp aquellos cationes](http://slidetodoc.com/presentation_image_h/dec414256ad00a125b42bd8d52dbd777/image-34.jpg)
Si el p. H es ácido [ S -2 ] disminuye, pp aquellos cationes que tienen un Kps muy pequeño. Si el p. H es básico la [ S= ] aumenta. Por lo tanto en medio alcalino pp los sulfuros que tienen un Kps alto. PODER REDUCTOR DEL H 2 S. 1. 5 H 2 S + 2 Mn 04 - + 6 H+ → 2 Mn +2 + 5 S º + 8 H 2 O 2. 3 H 2 S + Cr 2 O 7 -2 + 8 H + → 2 Cr +3 + 3 Sº + 7 H 20 3. 3 H 2 S + H 2 SO 4 4. → 4 Sº + 4 H 2 S + 2 HNO 3 → Sº + 2 H 2 O + 2 NO 2 (g)

GRUPO V. N , P , AS , Sb y Bi Prop. fisicas : VER TABLA 14 -1 Estados de oxidación del nitrógeno ( N 2 O 5 , NO 2 , HNO 3 , NO , N 2 , NH 2 OH , N 2 H 4 , NH 3 ) Est. de Oxidación : -3 ( NH 3 , PH 3 As. H 3 , Sb H 3 , Bi. H 3 ) Propiedades reductoras : PH 3 (g) <→ P + 3 H+ + 3 e- Eº = -0, 06 V As. H 3 ----> As + 3 H+ + 3 e- Eº = 0. 66 V ·OH - + As. H 3 ↔ As + 3 H 20 + 3 e- Eº = 1, 43 V

Estado de oxidación +3 Öxidos : N 2 O 3 , P 2 O 3 (ácidos) As 2 O 3 , Sb 2 O 3 (anfóteros) Bi 2 O 3 (básico) Estado de oxidación : +5 : N 2 O 5 , As 2 O 5 , Sb 2 O 5 , no existe el Bi 2 O 5 Acidos : HNO 3 , HPO 3 , H 3 As. O 4 , Sb(OH)6 – ( pentóxido de antimonio , contenido variable de agua, , debilmente soluble en ella dando una solución de carácter ácido. Compuestos iónicos : El N -3 sólo al estado sólido , en solución hidroliza : Li 3 N + 3 H 2 O → NH 3 + 3 Li+ + 3 OH El Bismuto podría presentar carácter iónico en Bi. F 3 , pero el Bi en solución acuosa hidroliza : Bi +3 + H 2 O ↔ Bi. O + + 2 H+ Por qué el N 2 presenta propiedades diferentes al resto de los elementos del grupo ?

1. Tamaño pequeño. 2. No puede expandir su capa de valencia 3. Es el único elemento que presenta enlaces múltiples. en su molécula el resto de los elementos están incapacitados por su tamaño a un recubrimiento pπ -- pπ ? : N? N: 0: [ : 0 -- N ] ? : 0 : _ 4. El P forma cadenas, en menos grado el As y el Sb NITROGENO. Estado Natural: Aislado 78% del aire , combinado ( NO 3 - ) en el salitre. Forma parte de las proteínas. Alcaloides , vitaminas , fertilizantes, TNT , hidracinas sustituídas , nylon.

OBTENCION INDUSTRIAL : Destilar aire líquido a -195 ºC OBTENCIÖN EN EL LABORATORIO. 1. descomposición térmica de sales de amonio en que el anión es oxidante: Δ NH 4 NO 2 ------> N 2 + 2 H 2 O Δ ( NH 4)2 Cr 2 O 7 -----> N 2 + Cr 2 O 3 + 4 H 2 O Δ EXCEPCIÓN : NH 4 NO 3 -----> N 2 O + H 2 O 2. Oxidación del amoniaco: Δ 2 NH 3 (g) + 3 Cu. O ------> 3 Cu + N 2 (g) + 3 H 2 O ·

Δ 2 N H 3 (g) + · 3 Na. Br. O ------> N 2 + 3 Na. Br + 3 H 2 O Δ 8 NH 3 (g) + 3 Cl 2 (g) -----> N 2 (g) + 6 NH 4 Cl · 3. Descomposición térmica de la azida de sodio : Δ 2 Na. N 3 ------> 2 Na + 3 N 2 (g) PROPIEDADES QUÍMICAS. : Keq = 10 -120. N 2 (g) ↔ 2 N (g) ΔHº = 226 Kcal / mol Por sobre 2000 ºC no disocia. Por eso se dice que es un gas inerte. Bacteria raices. leguminosas

NITROGENO. Forma 3 tipos de compuestos: a) Iónicos. Gana 3 electrones : Li 3 N b) Covalentes : comparte 3 electrones : NH 3 c) covalente coordenado : : NH 3 + H+ → NH 4 + El ion amonio es isoelectrónico con el metano ? Demuéstrelo. . El ion amida NH 2 – con quien podría ser isoelectrónico. Dibuje la estructura. NH 3. gas soluble en agua → NH 4 + , a tº ambiente basta con ejercer 7, 5 atm. para licuarlo El ángulo H—N—H es de 106º, 45 Obtención Industrial del NH 3. : a) Hidrólisis de un nitruro : 2 Al. N + 3 H 2 O → Al 2 O 3 + 2 NH 3

b) Acción de una base fuerte, sobre una sal de amonio: 2 NH 4 Cl + Ca (OH)2 → Ca. Cl 2 + 2 H 2 O + 2 NH 3 (g) c) Descomposición térmica de una sal de amonio con ANION NO OXIDANTE. Δ NH 4 Cl -----> NH 3 (g) + HCl Δ NH 4 HCO 3 -------→ NH 3 ( g) + H 2 O + CO 2 (g) PROPIEDADES QUÍMICAS DEL AMONIACO: Ag + (ac) + 2 NH 3 (ac) → [ Ag ( NH 3)2 ] + ion diamino Ag ( I) Cr +3 (ac) + 6 NH 3 (ac) → [ Cr (NH 3)6 ] + 3 ion hexaamino de Cr (III) El ion amonio, radio( 1, 34 Aº ) semejante al ion K + y ion Rb + forman sales isomorfas, solubles en agua, excepto percloratos y tartratos , en general con aniones voluminosos como [ Pt F 6 ] -2

OXIDACION DEL AMONIACO. Δ 4 NH 3 (g) + 5 O 2 (g) ----→ 2 N 2 (g) + 6 H 2 O (g) K 298ºC = 10 228 Ostwald realizó el siguiente procedimiento : 750 ºC 4 NH 3 (g) + 5 O 2 (g) ------> 4 NO (g) + 6 H 2 O K 298ºc = 10 168 Pt 2 NO (g) + O 2 (g) → 2 NO 2 (g) 3 NO 2 (g) + H 2 O ↔ 2 HNO 3 + NO (g) AMONIACO LÍQUIDO. ¿ Por que es el mejor solvente inorgánico después del agua ?

a) Disuelve metales alcalinos y alcalino terreos sin reaccionar con ellos b) Exalta la acidez de los ácidos débiles en solución acuosa. c) Muchas sales se disuelven en amoniaco líquido dando soluciones altamente conductoras. d) Debido a que contiene una constante dieléctrica menoe que el agua (16, 9 contra 82) no es tan buen disolvente inorg, pero es mejor solvente que el agua para con sust. orgánicas. Posee una constante de autoionización muy pequeña : 2 NH 3 ↔ NH 4 + + NH 2 - ACIDO HIDRAZOICO HN 3 Obtención de laboratorio: N 2 H 5 + HNO 2 → HN 3 + H+ + 2 H 2 O: Sus sales se llaman azidas. Obtención de laboratorio : K – 33ºc = 10 -30

175 ºC 3 Na. NH 2 + Na. NO 3 -----→ Na. N 3 + 3 Na. OH + NH 3 (g) Ion azida : Molécula lineal, híbrido de resonancia (DIBUJARLA) HNO 3 hν 2 HNO 3 -----→ 2 NO 2 (g) + H 2 O + ½ O 2 C → CO 2 + ……. S → H 2 SO 4 + …… HNO 3 (conc) + + NO 2 (g) P → H 3 PO 4 + ……. I → HIO 3 + …… Cuando el HNO 3· actúa de mediana concentración, su producto reducido es NO (g)
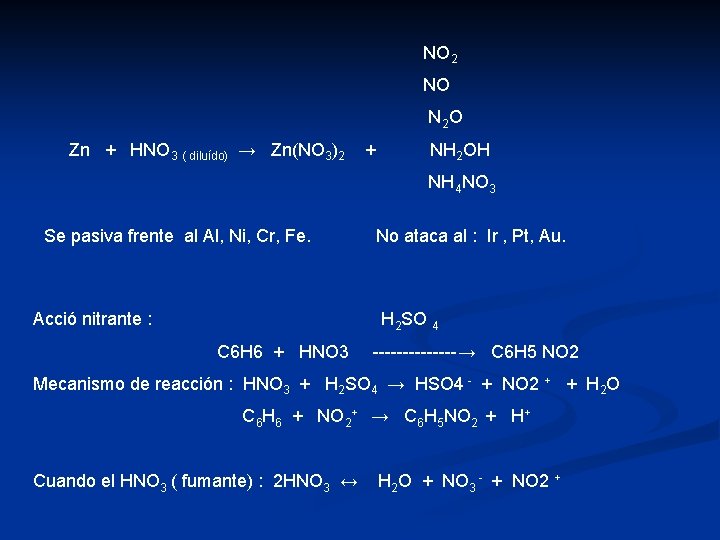
NO 2 NO N 2 O Zn + HNO 3 ( diluído) → Zn(NO 3)2 + NH 2 OH NH 4 NO 3 Se pasiva frente al Al, Ni, Cr, Fe. Acció nitrante : No ataca al : Ir , Pt, Au. H 2 SO 4 C 6 H 6 + HNO 3 -------→ C 6 H 5 NO 2 Mecanismo de reacción : HNO 3 + H 2 SO 4 → HSO 4 - + NO 2 + + H 2 O C 6 H 6 + NO 2+ → C 6 H 5 NO 2 + H+ Cuando el HNO 3 ( fumante) : 2 HNO 3 ↔ H 2 O + NO 3 - + NO 2 +
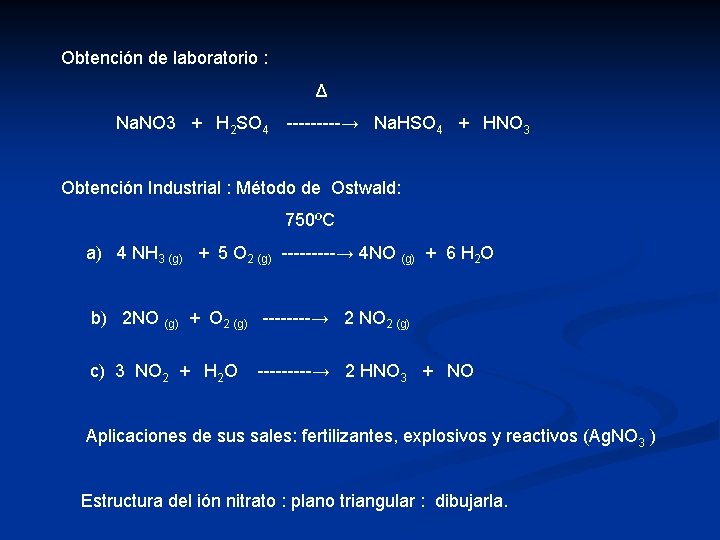
Obtención de laboratorio : Δ Na. NO 3 + H 2 SO 4 -----→ Na. HSO 4 + HNO 3 Obtención Industrial : Método de Ostwald: 750ºC a) 4 NH 3 (g) + 5 O 2 (g) -----→ 4 NO (g) + 6 H 2 O b) 2 NO (g) + O 2 (g) ----→ 2 NO 2 (g) c) 3 NO 2 + H 2 O -----→ 2 HNO 3 + NO Aplicaciones de sus sales: fertilizantes, explosivos y reactivos (Ag. NO 3 ) Estructura del ión nitrato : plano triangular : dibujarla.

P blanco ( P 4) P rojo P negro As amarillo As negro As metálico Sb amarillo Sb negro Sb metálico El bismuto sólo existe en la variedad metálica El P blanco soluble en CS 2 , punto de fusión 44, 2 ºC , el P rojo insoluble en CS 2, punto de fusión 592ºC Obtención Industrial del P , a partir de la fosforita: Δ 2 Ca 3(PO 4)2 + 6 Si. O 2 ------→ 6 Ca. Si. O 3 + P 4 O 10 Δ P 4 O 10 + 10 C ------→ 10 CO + P 4 ( vapor)

Hidrólisis de las sales del P PCl 3 + 3 H 2 O -----→ H 3 PO 3 + 3 HCl PBr 5 + 4 H 2 O ------→ H 3 PO 4 + 5 HBr Oxidos del fosforo : P 4 O 6 Obtención : carácter ácido ( anhidrido fosforoso) P 4 + 3 O 2 -----→ P 4 O 6 + 6 H 2 O ----→ 4 H 3 PO 3 As 4 O 6, Sb 4 O 6 ( dímeros ) anfotéricos As 4 O 6 + 4 Na. OH As 4 O 6 + 12 HCl ----→ 4 Na. As. O 2 + 2 H 2 O → 4 As. Cl 3 + 6 H 2 O Bi 2 O 3 : básico. Bi +3 + H 2 O ----→ Bi. O+ + 2 H+

P 4 O 10 ( Dimero) Ver guia para su estructura Obtención: P 4 + 502 ----→ P 4 O 10 Propiedades: a ) Poder deshidratante : P 4 O 10 + 2 H 2 SO 4 -------→ 4 HPO 3 + 2 SO 3 P 4 O 10 + 4 HNO 3 ------→ 4 HPO 3 + 2 N 2 O 5 H 3 PO 2 : ácido hipofosforoso. un solo hidrógeno reemplazable, sus sales se obtienen por la desproporcionación del P 4 en medio básico : P 4 + 3 OH - + 3 H 2 O ----→ log K = 16, 9 x n x ΔEº PH 3 + 3 H 2 PO 2 - Δ Eº = 1, 15 V Estructura : Dibujar. H 3 PO 4 : solubilidad de sus sales H 2 PO 4 – son solubles en agua, HPO 4 -2 y PO 4 -3 son solubles solo las de metales alcalinos.

El H 3 PO 4 tiene una estructura tetraédrica : Cuál es Polimeriza dando origen al ácido pirofosfórico : Dibujar. Hay dos tipos de polimerizaciones , los polifosfatos que forman cadenas lineales y los polimetafosfatos ( HPO 3)n forman estructuras cíclicas o anillos. APLICACIONES. SE emplean en detergentes para ablandar aguas, formando complejos con iones metálicos presentes en el agua. Este uso se ha criticado porque da origen al fenómeno de hiperfertilización en plantas, efecto eutrófico, sobretodo en lagos. BIBLIOGRAFIA. “ QUIMICA “ : R. CHANG “ QUIMICA INORGÁNICA AVANZADA “. Cotton and Wilkinson.
- Slides: 50