HABITAT Entretien et rnovation dans lhabitat Programme Term

HABITAT Entretien et rénovation dans l’habitat Programme Term STI 2 D/Term STL 23 Mai 2012 S. CALLEA Lycée Gay-Lussac

Programme de Terminale STI 2 D et Terminale STL Entretien et rénovation dans l’habitat Notions et contenus Capacités exigibles Réactions acide-base et transfert de protons. Solutions acides, basiques. p. H ü Citer des produits d’entretien couramment utilisés dans l’habitat (détartrants, déboucheurs, savons, détergents, désinfectants, dégraissants, etc. . ) ; reconnaître leur nature chimique et leur précaution d’utilisation (étiquette, pictogramme). ü Définir les termes suivants : acide, base, couple acide-base. ü Ecrire une réaction acide-base, les couples acide-base étant donnés. ü Citer le sens de variation du p. H en fonction de l’évolution de la concentration en H+(aq). Solubilisation. Solvants de nettoyage. üChoisir un solvant pour éliminer une espèce chimique à partir de données sur sa solubilité ou à partir d’une démarche expérimentale

Produits d’entretien utilisés dans l’habitat Dégraissant Déboucheur Détartrant Produit qui élimine la formation de tartre Produit qui permet de déboucher une canalisation par réaction avec le bouchon Produit qui enlève les traces de graisse sur une surface.

Produits d’entretien utilisés dans l’habitat Désinfectant Savon - Détergent Produit qui détruit les bactéries, les virus ou tout au moins les rend inactifs Produit qui élimine les graisses, les salissures à la surface de matériaux, cheveux, corps humain
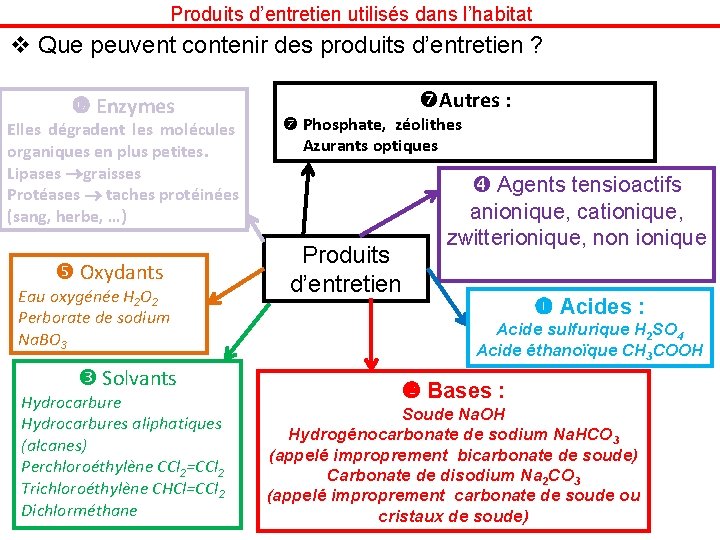
Produits d’entretien utilisés dans l’habitat v Que peuvent contenir des produits d’entretien ? Enzymes Elles dégradent les molécules organiques en plus petites. Lipases graisses Protéases taches protéinées (sang, herbe, …) Oxydants Eau oxygénée H 2 O 2 Perborate de sodium Na. BO 3 Solvants Hydrocarbures aliphatiques (alcanes) Perchloroéthylène CCl 2=CCl 2 Trichloroéthylène CHCl=CCl 2 Dichlorméthane Autres : Phosphate, zéolithes Azurants optiques Produits d’entretien Agents tensioactifs anionique, cationique, zwitterionique, non ionique Acides : Acide sulfurique H 2 SO 4 Acide éthanoïque CH 3 COOH Bases : Soude Na. OH Hydrogénocarbonate de sodium Na. HCO 3 (appelé improprement bicarbonate de soude) Carbonate de disodium Na 2 CO 3 (appelé improprement carbonate de soude ou cristaux de soude)
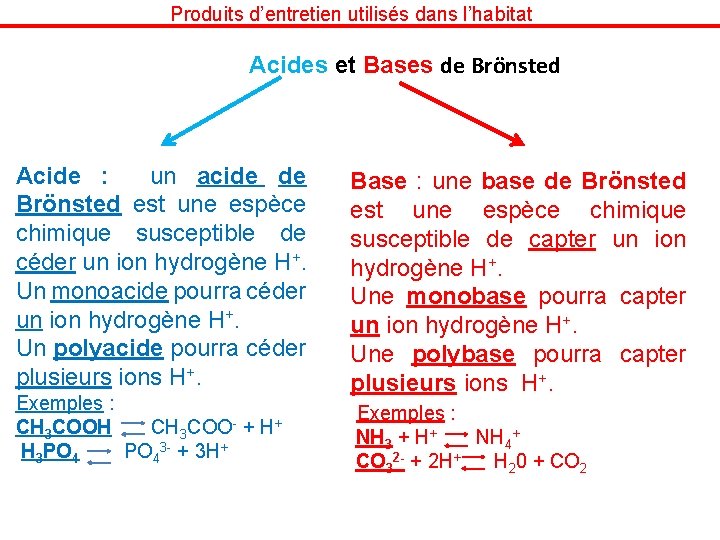
Produits d’entretien utilisés dans l’habitat Acides et Bases de Brönsted Acide : un acide de Brönsted est une espèce chimique susceptible de céder un ion hydrogène H+. Un monoacide pourra céder un ion hydrogène H+. Un polyacide pourra céder plusieurs ions H+. Exemples : CH 3 COOH CH 3 COO- + H+ H 3 PO 4 PO 43 - + 3 H+ Base : une base de Brönsted est une espèce chimique susceptible de capter un ion hydrogène H+. Une monobase pourra capter un ion hydrogène H+. Une polybase pourra capter plusieurs ions H+. Exemples : NH 3 + H+ NH 4+ CO 32 - + 2 H+ H 20 + CO 2
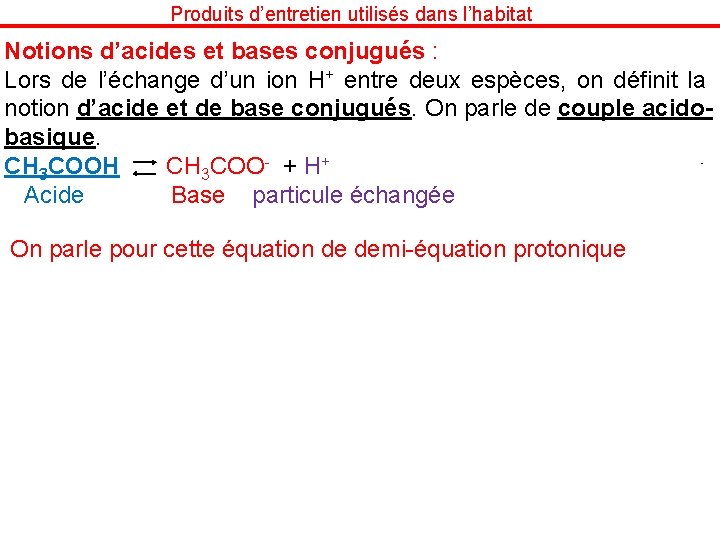
Produits d’entretien utilisés dans l’habitat Notions d’acides et bases conjugués : Lors de l’échange d’un ion H+ entre deux espèces, on définit la notion d’acide et de base conjugués. On parle de couple acidobasique. CH 3 COOH CH 3 COO- + H+ couple : CH 3 COOH/CH 3 COO Acide Base particule échangée On parle pour cette équation de demi-équation protonique

Produits d’entretien utilisés dans l’habitat v Couples acide-base de l’eau, autoprotolyse : L’eau participe à deux couples dans lesquels elle joue soit le rôle d’acide soit le rôle de base. Les couples sont : H 20/HO- et H 3 O+/H 2 O HO- + H+(aq) et H 2 O + H+(aq) H 3 O+ v Ampholyte ou Espèce amphotère : un ampholyte est une espèce amphotère. Il s’agit d’une espèce qui est un acide dans un couple et une base dans un autre couple. Exemples : üeau ü H 20, CO 2 /HCO 3 - et HCO 3 -/ CO 32 -

Produits d’entretien utilisés dans l’habitat v Réaction acide-base en solution aqueuse : Une réaction acido-basique fait intervenir deux couples acide/base. L’acide d’un couple libère un ion H+ pour le concéder à la base de l’autre couple. Exemple : réaction entre CH 3 COOH et HO- qui appartiennent aux couples CH 3 COOH/CH 3 COO- et H 2 O/HO CH 3 COOH CH 3 COO- + H+(aq) HO- + H+(aq) H 2 O CH 3 COOH + HO- CH 3 COO- + H 2 O Méthode pour écrire une réaction acido-basique : Identifier les deux couples Repérer l’acide et la base qui réagissent. Attention, réaction entre un acide d’un couple et une base d’un autre couple. Ecrire les 2 demi-équations protoniques Sommer ces réactions, il s’agit d’éliminer les ions H+

Produits d’entretien utilisés dans l’habitat v Autoprotolyse de l’eau : Dans l’eau, il existe un équilibre appelé autoprotolyse de l’eau. 2 H 20 H 3 O+ + HO- K = Ke = 10 -14 Cet équilibre se caractérise à 25 °C par une constante Ke appelée produit ionique de l’eau valant Ke = [H 3 O+]. [HO-] = 10 -14 Le bilan macroscopique de autoprotolyse de l’eau implique : Si on forme x mol d’ions H 3 O+, on forme x mol d’ions HO- Dans l’eau pure, il y a autant d’ions H 3 O+ que d’ions HO- [H 3 O+] = [HO-] Ke = [H 3 O+]. [HO-] = 10 -14 = [H 3 O+]2 [H 3 O+] = [HO-] = 10 -7 mol. L-1 Objectif : trouver une grandeur qui permet d’évaluer et de comparer les concentrations d’ions H 3 O+ et HO- dans les solutions.

Produits d’entretien utilisés dans l’habitat v Définition du p. H : Le p. H est une grandeur qui va donner une information sur la comparaison entre les concentrations des ions H 3 O+ et HO-. H 3 O+ est l’acide conjugué de l’eau HO- est la base conjuguée de l’eau ü Si [H 3 O+] > [HO-] l’acide conjugué de l’eau est en proportion plus importante que la base conjuguée de l’eau Solution dite acide üSi [H 3 O+] < [HO-] la base conjuguée de l’eau est en proportion plus importante que l’acide conjugué de l’eau Solution dite basique üSi [H 3 O+] = [HO-] la base conjuguée de l’eau est en proportion égale à l’acide conjugué de l’eau D’après l’autoprotolyse de l’eau : [H 3 O+] = [HO-] = 10 -7 mol. L-1 Solution dite neutre
![Produits d’entretien utilisés dans l’habitat p. H = - log[H 3 O+] v Définition Produits d’entretien utilisés dans l’habitat p. H = - log[H 3 O+] v Définition](http://slidetodoc.com/presentation_image/3986133483cad53595eb02524ea0faad/image-12.jpg)
Produits d’entretien utilisés dans l’habitat p. H = - log[H 3 O+] v Définition du p. H (solutions diluées) : ü Pour les solutions neutres, [H 3 O+] = [HO-] = 10 -7 mol. L-1 p. H = 7, 0 ü Pour les solutions dite acides [H 3 O+] > 10 -7 mol. L-1 > [HO-] p. H < 7, 0 üPour les solutions dite basiques [HO-] > 10 -7 mol. L-1 > [H 3 O+] p. H > 7, 0 0 p. H 14

p. H acide – p. H basique Jus de citron p. H = 2, 4 – 2, 6 Cola p. H = 2, 5 Vinaigre p. H = 2, 5 – 2, 9 Jus de pomme p. H = 3, 5 Bière p. H = 4, 5 Café p. H = 5, 0 Thé p. H = 5, 5 Lait p. H = 6, 5 Sang p. H = 7, 3 – 7, 4 Eau de mer p. H = 8, 0 Savon p. H = 9 - 10 Chaux p. H = 12, 5

Produits d’entretien utilisés dans l’habitat v Influence de la dilution sur le p. H d’une solution acide ou basique : p. H = - log[H 3 O+] ü Si on dilue une solution acide, la concentration de H 3 O+ diminue donc p. H augmente. üSi on dilue une solution basique, la concentration en HO- diminue, le produit ionique implique la concentration en ions H 3 O+ augmente donc p. H diminue. ü Si on dilue fortement la solution acide ou basique, le p. H tend vers 7, 0, solution neutre.

La mesure du p. H Utilisation d’indicateurs colorés naturels Indicateur naturel qui change de couleur suivant l’acidité du milieu 1767 : W. LEWIS emploie un extrait de tournesol pour quantifier l’acidité. William Lewis (1714 – 1781) : chimiste et médecin anglais. Papier de tournesol (rouge en milieu acide)
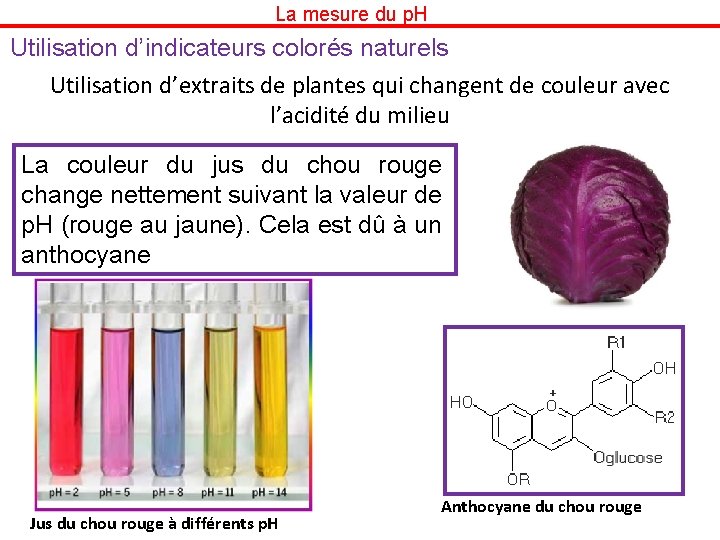
La mesure du p. H Utilisation d’indicateurs colorés naturels Utilisation d’extraits de plantes qui changent de couleur avec l’acidité du milieu La couleur du jus du chou rouge change nettement suivant la valeur de p. H (rouge au jaune). Cela est dû à un anthocyane Jus du chou rouge à différents p. H Anthocyane du chou rouge
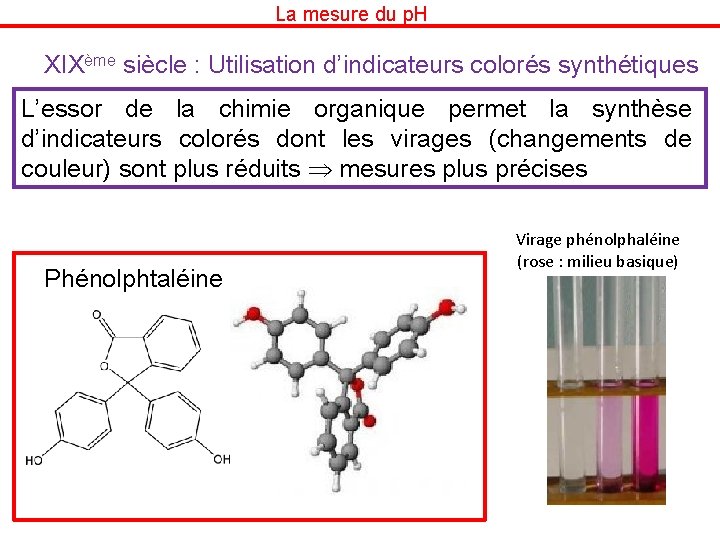
La mesure du p. H XIXème siècle : Utilisation d’indicateurs colorés synthétiques L’essor de la chimie organique permet la synthèse d’indicateurs colorés dont les virages (changements de couleur) sont plus réduits mesures plus précises Phénolphtaléine Virage phénolphaléine (rose : milieu basique)
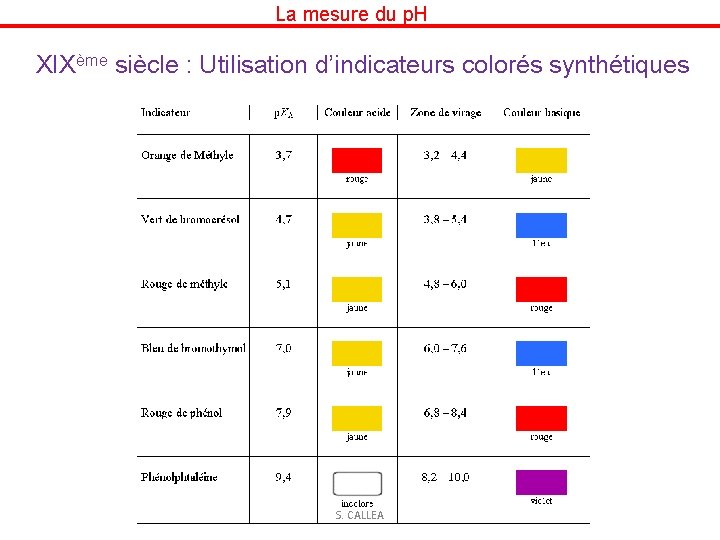
La mesure du p. H XIXème siècle : Utilisation d’indicateurs colorés synthétiques S. CALLEA

La mesure du p. H Mesure du p. H au XXème siècle Utilisation de papier p. H contenant des indicateurs colorés. Le papier p. H mis en contact de la solution prend une coloration qui dépend du p. H.

La mesure du p. H Mesure du p. H au XXème siècle Nature des électrodes permettant la mesure du p. H : Il faut deux électrodes, une de mesure (électrode de verre) dont le potentiel dépend du p. H et une de référence de potentiel constant (électrode au calomel par exemple) Une électrode de verre auquel il faut associer une électrode de référence Electrode combinée 1948 : Ingold propose une électrode combinée (comprenant électrode de verre + électrode de référence)

Produits d’entretien utilisés dans l’habitat v Utilisation d’acide dans les produits d’entretien : ü Exemple des détartrants : détruire le tartre Le tartre est du carbonate de calcium ou du carbonate de magnésium Ca 2+(aq) + CO 32 -(aq) = Ca. CO 3(s) Mg 2+(aq) + CO 32 -(aq) = Mg. CO 3(s) Tartre et tuyauterie bouchée
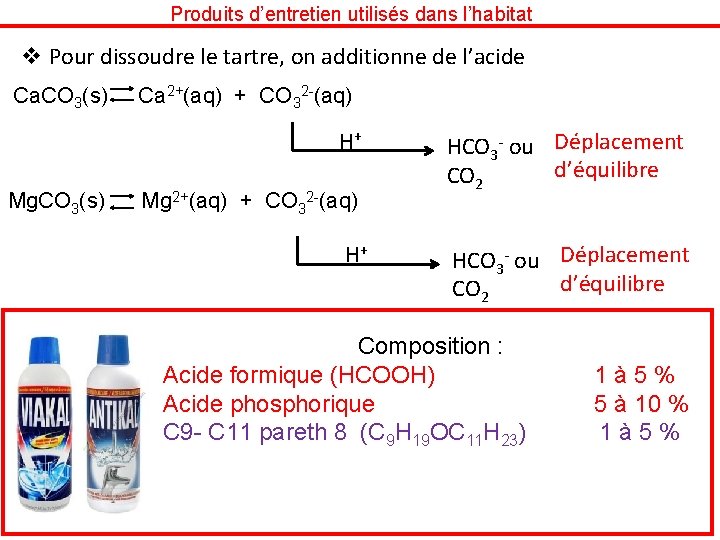
Produits d’entretien utilisés dans l’habitat v Pour dissoudre le tartre, on additionne de l’acide Ca. CO 3(s) Ca 2+(aq) + CO 32 -(aq) H+ Mg. CO 3(s) Mg 2+(aq) + CO 32 -(aq) H+ HCO 3 - ou Déplacement d’équilibre CO 2 Composition : Acide formique (HCOOH) 1 à 5 % Acide phosphorique 5 à 10 % C 9 - C 11 pareth 8 (C 9 H 19 OC 11 H 23) 1 à 5 %
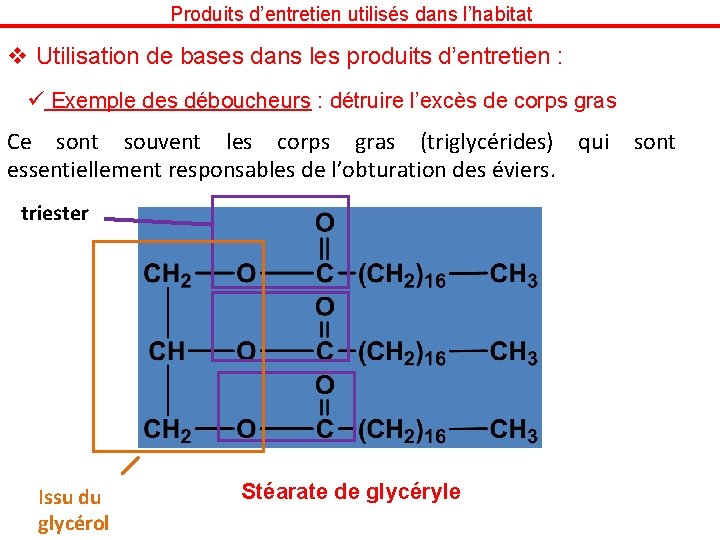
Produits d’entretien utilisés dans l’habitat v Utilisation de bases dans les produits d’entretien : ü Exemple des déboucheurs : détruire l’excès de corps gras Ce sont souvent les corps gras (triglycérides) qui sont essentiellement responsables de l’obturation des éviers. triester Issu du glycérol Stéarate de glycéryle
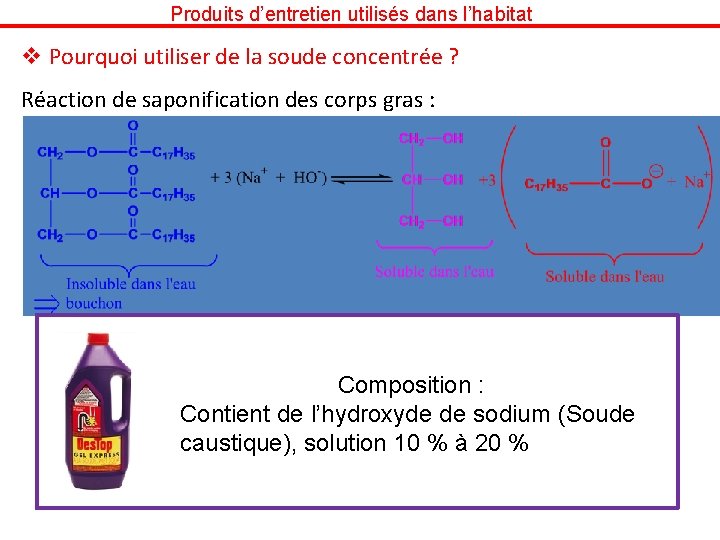
Produits d’entretien utilisés dans l’habitat v Pourquoi utiliser de la soude concentrée ? Réaction de saponification des corps gras : Composition : Contient de l’hydroxyde de sodium (Soude caustique), solution 10 % à 20 %

Produits d’entretien utilisés dans l’habitat v Utilisation de solvants dans les produits d’entretien : Pour comprendre l’utilisation et le choix d’un solvant, il convient de connaître : les propriétés physiques et chimiques des solvants Fonction d’un solvant : dissoudre, diluer une espèce chimique sans modifier chimiquement l’espèce.
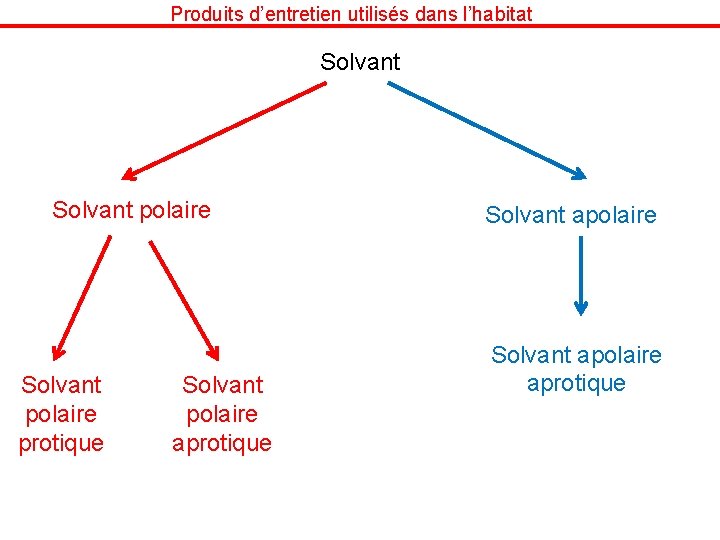
Produits d’entretien utilisés dans l’habitat Solvant polaire protique Solvant polaire aprotique Solvant apolaire aprotique
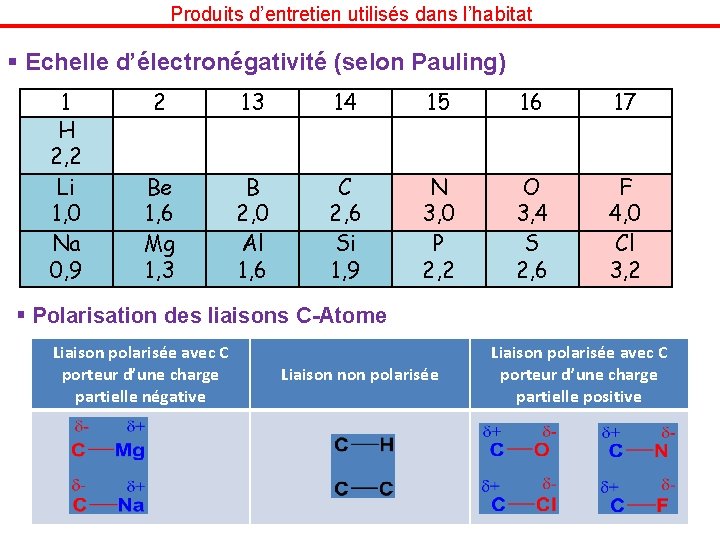
Produits d’entretien utilisés dans l’habitat § Echelle d’électronégativité (selon Pauling) 1 H 2, 2 Li 1, 0 Na 0, 9 2 13 14 15 16 17 Be 1, 6 Mg 1, 3 B 2, 0 Al 1, 6 C 2, 6 Si 1, 9 N 3, 0 P 2, 2 O 3, 4 S 2, 6 F 4, 0 Cl 3, 2 § Polarisation des liaisons C-Atome Liaison polarisée avec C porteur d’une charge partielle négative Liaison non polarisée Liaison polarisée avec C porteur d’une charge partielle positive
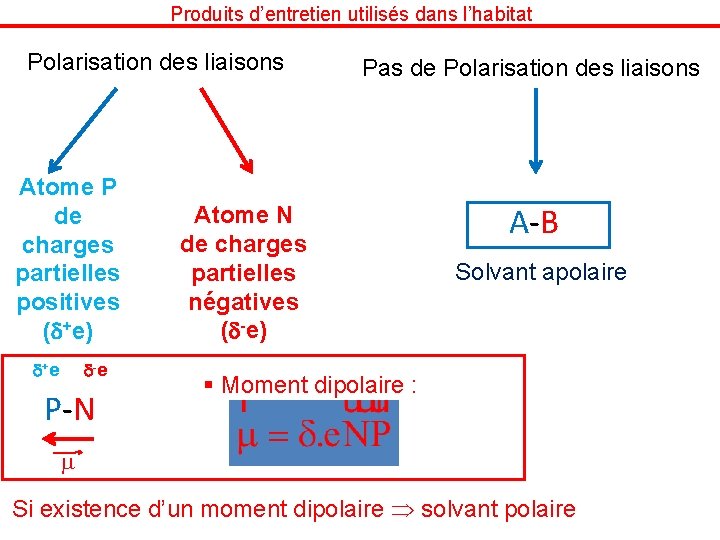
Produits d’entretien utilisés dans l’habitat Polarisation des liaisons Atome P de charges partielles positives (d+e) d+ e d- e P-N Pas de Polarisation des liaisons Atome N de charges partielles négatives (d-e) A-B Solvant apolaire § Moment dipolaire : m Si existence d’un moment dipolaire solvant polaire
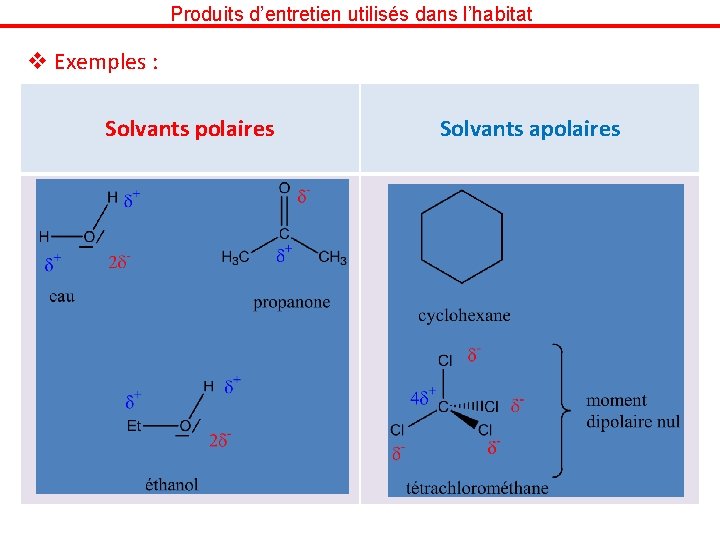
Produits d’entretien utilisés dans l’habitat v Exemples : Solvants polaires Solvants apolaires
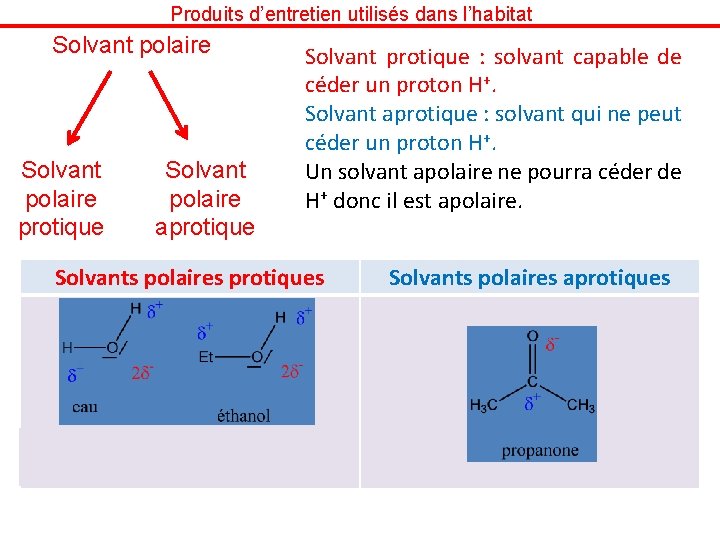
Produits d’entretien utilisés dans l’habitat Solvant polaire protique Solvant polaire aprotique Solvant protique : solvant capable de céder un proton H+. Solvant aprotique : solvant qui ne peut céder un proton H+. Un solvant apolaire ne pourra céder de H+ donc il est apolaire. Solvants polaires protiques H 2 O HO- + H+ Et. OH Et. O- + H+ Solvants polaires aprotiques

Produits d’entretien utilisés dans l’habitat v Solubilité des espèces et nature des solvants : « Qui se ressemble, s’assemble » ü Composés polaires : Les composés polaires auront une solubilité plus importante dans les solvants polaires Interaction de Van der Waals polaire/polaire (Keesom)
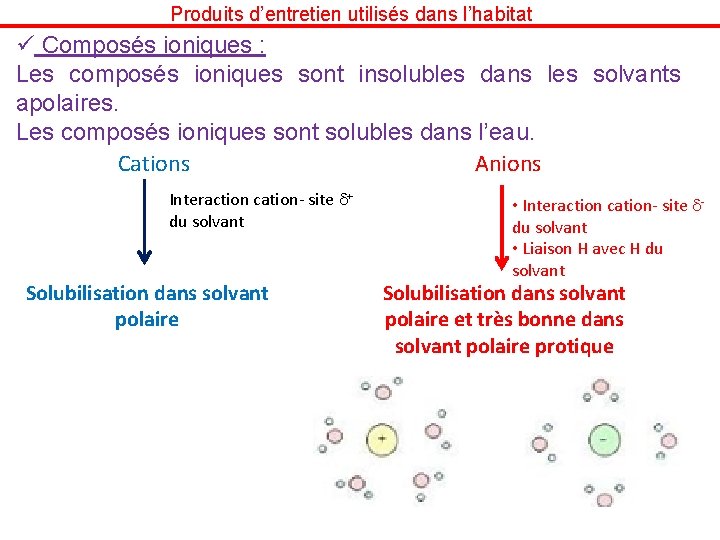
Produits d’entretien utilisés dans l’habitat ü Composés ioniques : Les composés ioniques sont insolubles dans les solvants apolaires. Les composés ioniques sont solubles dans l’eau. Cations Anions Interaction cation- site d+ du solvant Solubilisation dans solvant polaire • Interaction cation- site d- du solvant • Liaison H avec H du solvant Solubilisation dans solvant polaire et très bonne dans solvant polaire protique

Produits d’entretien utilisés dans l’habitat ü Composés apolaires : Les composés apolaires sont solubles dans les solvants apolaires et insolubles dans les solvants polaires. Soluble dans le cyclohexane Insoluble dans l’eau, l’éthanol

Produits d’entretien utilisés dans l’habitat ü Composés comportant des groupements apolaires, et des groupements polaires : Plus la chaîne carbonée augmente, plus la solubilité dans solvant polaire diminue et plus la solubilité dans solvant apolaire augmente.

Produits d’entretien utilisés dans l’habitat v Utilisation de solvants dans les produits d’entretien : ü Exemple de dégraissants : l’eau écarlate Composition : Mélange de solvants aliphatiques (hydrocarbures apolaires à nbre de C (C 5 à C 20) Fonction « Le détacheur liquide instantané d’Eau Ecarlate Professionnel élimine en douceur taches et salissures puis s’évapore en laissant un léger parfum. Nettoie, ravive, rafraîchit et élimine en toute sécurité les taches fraîches, incrustées, grasses, collantes et enlève les traces de goudron, cambouis, résine… »
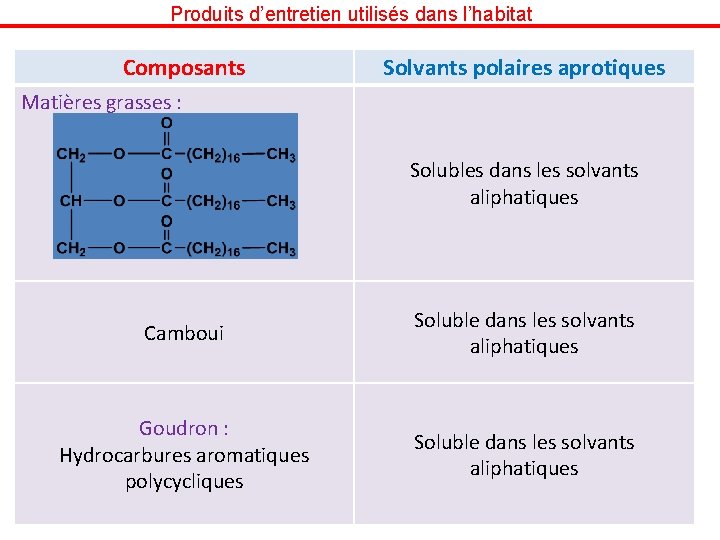
Produits d’entretien utilisés dans l’habitat Composants Solvants polaires aprotiques Matières grasses : Solubles dans les solvants aliphatiques Camboui Soluble dans les solvants aliphatiques Goudron : Hydrocarbures aromatiques polycycliques Soluble dans les solvants aliphatiques

Produits d’entretien utilisés dans l’habitat ü Exemple nettoyants four : 5 à 15 % d’hydrocarbures aliphatiques (éliminer les graisses du four)
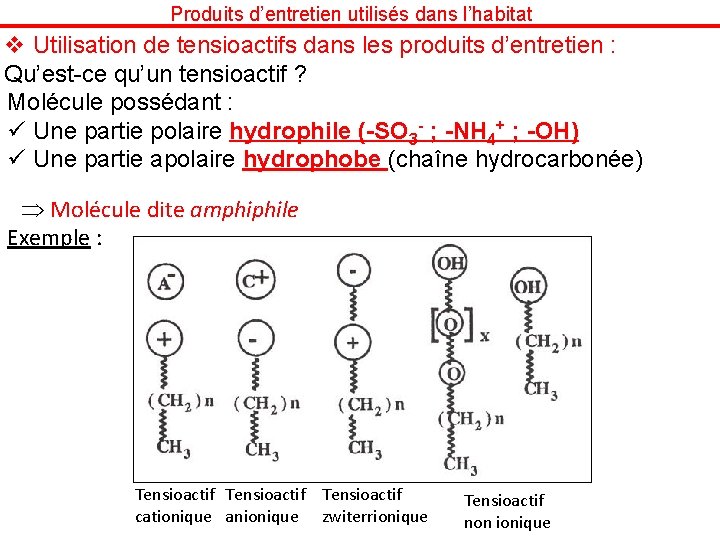
Produits d’entretien utilisés dans l’habitat v Utilisation de tensioactifs dans les produits d’entretien : Qu’est-ce qu’un tensioactif ? Molécule possédant : ü Une partie polaire hydrophile (-SO 3 - ; -NH 4+ ; -OH) ü Une partie apolaire hydrophobe (chaîne hydrocarbonée) Molécule dite amphiphile Exemple : Tensioactif cationique anionique zwiterrionique Tensioactif non ionique
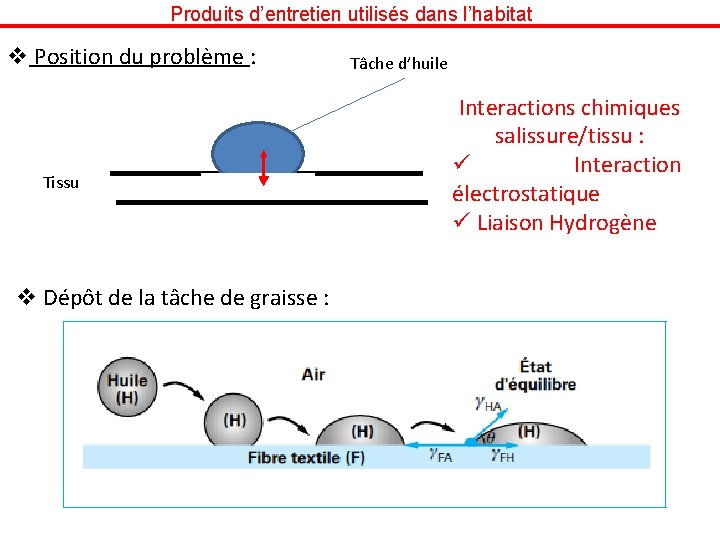
Produits d’entretien utilisés dans l’habitat v Position du problème : Tissu v Dépôt de la tâche de graisse : Tâche d’huile Interactions chimiques salissure/tissu : ü Interaction électrostatique ü Liaison Hydrogène

Produits d’entretien utilisés dans l’habitat Le système tend à minimiser les surfaces entre milieu Forces interfaciales appelées tensions superficielle g. FA : tension superficielle fibre – air g. HA : tension superficielle huile – air g. FH : tension superficielle fibre – huile Equilibre mécanique : g. FA = g. HAcos + g. FH
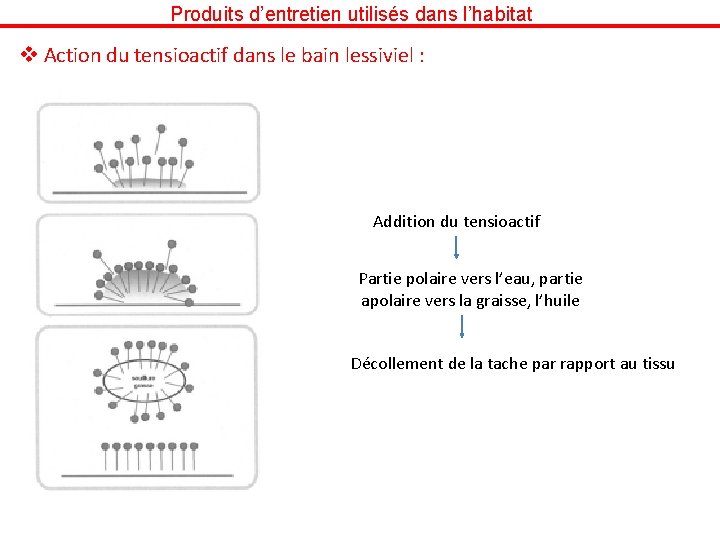
Produits d’entretien utilisés dans l’habitat v Action du tensioactif dans le bain lessiviel : Addition du tensioactif Partie polaire vers l’eau, partie apolaire vers la graisse, l’huile Décollement de la tache par rapport au tissu
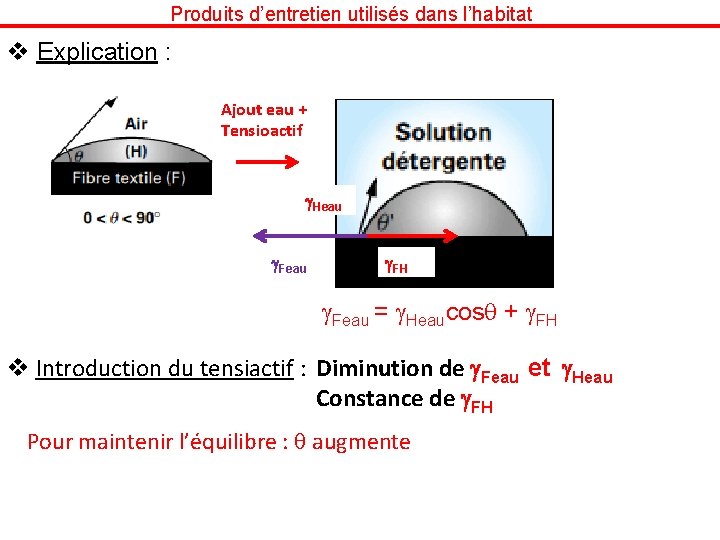
Produits d’entretien utilisés dans l’habitat v Explication : Ajout eau + Tensioactif g. Heau g. FH g. Feau = g. Heaucos + g. FH v Introduction du tensiactif : Diminution de g. Feau et g. Heau Constance de g. FH Pour maintenir l’équilibre : augmente
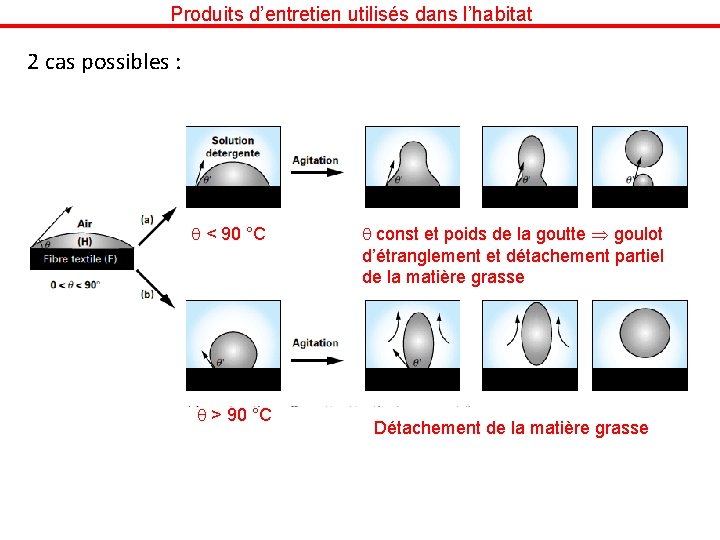
Produits d’entretien utilisés dans l’habitat 2 cas possibles : < 90 °C > 90 °C const et poids de la goutte goulot d’étranglement et détachement partiel de la matière grasse Détachement de la matière grasse

Produits d’entretien utilisés dans l’habitat v Utilisation des agents de blanchiment dans les produits d’entretien : Certaines taches colorées ou salissures maigres ne peuvent être enlevées du tissu par des mécanismes physiques. Utilisation des agents de blanchiment capables de décolorer irréversiblement les systèmes colorés par une réaction chimique, le plus souvent une oxydation Agents de blanchiment : composés capables de libérer in situ des formes activées de H 2 O 2. Exemple : Composition : Agent de surface moins de 15 % Agent de blanchiment moins de 5 % Azurants optiques < 5 %
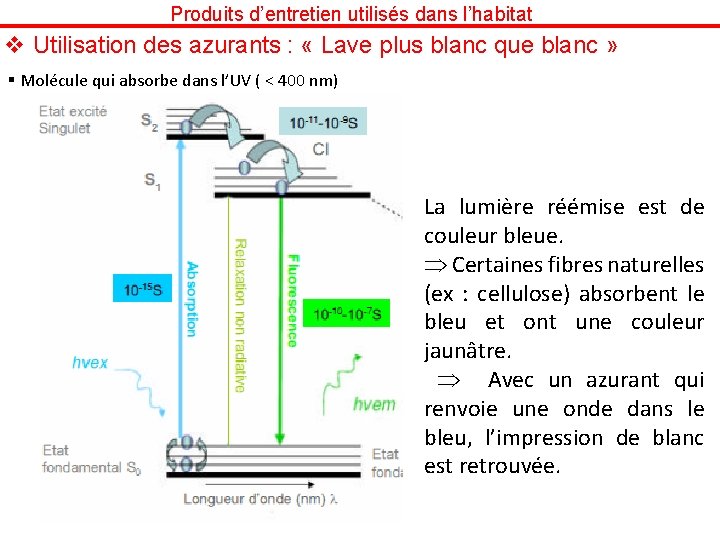
Produits d’entretien utilisés dans l’habitat v Utilisation des azurants : « Lave plus blanc que blanc » § Molécule qui absorbe dans l’UV ( < 400 nm) La lumière réémise est de couleur bleue. Certaines fibres naturelles (ex : cellulose) absorbent le bleu et ont une couleur jaunâtre. Avec un azurant qui renvoie une onde dans le bleu, l’impression de blanc est retrouvée.

Protection dans l’utilisation des produits d’entretien v Les produits d’entretien doivent être utilisés avec précaution. Etiquettes Conseils d’utilisation : Eviter le contact avec les yeux, … Pictogrammes Conduites à tenir en cas d’accident : Rincer abondamment avec l’eau

Protection dans l’utilisation des produits d’entretien Inflammable (combustible) Corrosif Toxique, irritant Dangereux pour l’environnement
- Slides: 47