H H N H H KMYASAL BALAR H

H H N H H KİMYASAL BAĞLAR
H H N H H Kimyasal bağ: çekirdekteki atomları bir arada tutan kuvvettir. İki ya da daha fazla atom arasında elektron alışverişi veya ortak kullanımı ile kimyasal bağlar oluşmaktadır. Atomlar tek başına bulundukları zamankinden daha düşük enerjili duruma ( daha kararlı ) erişmek için bir araya gelirler ve kimyasal bağlar sayesinde atomlar birarada, düzenli olarak belli bir geometri oluştururlar.

H H N H H Atomlar Neden Soygazlara Benzemek İsterler? Soygazlar kararlı bir yapıya sahiptir ve elektron alıp verme eğilimleri yoktur. Yani denge halindedirler ve en dış elektron kabukları tamamen elektron larla doludur.
H H N H H Periyodik cetvelin en kararlı grubu olmalarından dolayı diğer bütün elementler Soygazlara benzeyebilmek için elektron alışverişi veya ortak kullanımına girerler. Elementin, son yörüngesinde 2 elektron bulunan He (helyum) soygazına benzemek istemesi dublete(2′ye) varmasıdır.

H H N H H Diğer son yörüngelerinde 8 elektron bulunan soygazlara benzemek istemesi ise oktede (8′e) varmasıdır. Soygazların kararlı olması ve boş orbitallerinin bulunmaması normal şartlarda onlara bağ yapma özelliği vermez.
H H N H H Kimyasal İyonik Bağ Kovalent Bağ

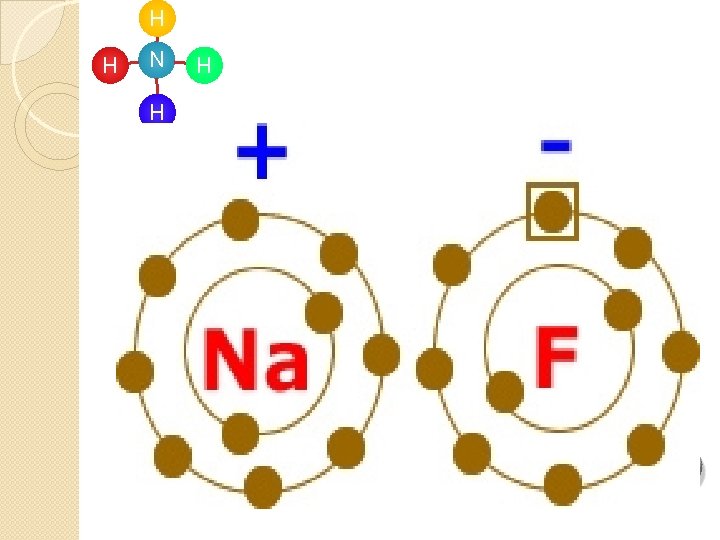
H H N H İyonik Bağ H Farklıyüklü İyonların ( + ve – yüklü taneciklerin) elektriksel çekim kuvvetlerinden ortaya çıkan bağ türüdür. Metaller ile ametaller arasında gerçekleşir ve metallerin elektron vermesi, ametallerin ise elektron almasıyla oluşur.

H H N H H İyonik bağı yapan atomlardan elektron veren (+) yüklü, elektron alan (–) yüklü iyon olur ve zıt çekim kuvveti iyonları bir kristal içinde tutar. Bu kuvvetli çekim iyonik bağlı bileşikleri ayrıştırmayı zorlaştırır. Atomlardan biri , elektron kaybedip pozitif yüklü iyona dönüşürken, diğer atom elektron kazanıp negatif yüklü iyonu oluşturur. Son durumda kaybedilen ve kazanılan elektronu eşit olmaktadır. Atomlardan elektron kaybı sonucu oluşan pozitif (+) iyonlara katyon; elektron kazanarak oluşan negatif (-) iyonlara ise anyon denilmektedir.

H H N H İyonik Bağlı Bileşiklerin H Özellikleri Nelerdir? İyonik bileşikler kristal yapıdadırlar ve oda sıcaklığında katı halde bulunurlar. Katı halleri elektriği iletmezken, sulu çözeltileri ve sıvı halleri elektirik akımını iletir. İyonlaşma enerjisi düşük elementler ile elektron ilgisi yüksek elementler arasında en kararlı bileşikler oluşur.
H H N H H

H H N H H Zıt kutuplar birbirini çeker
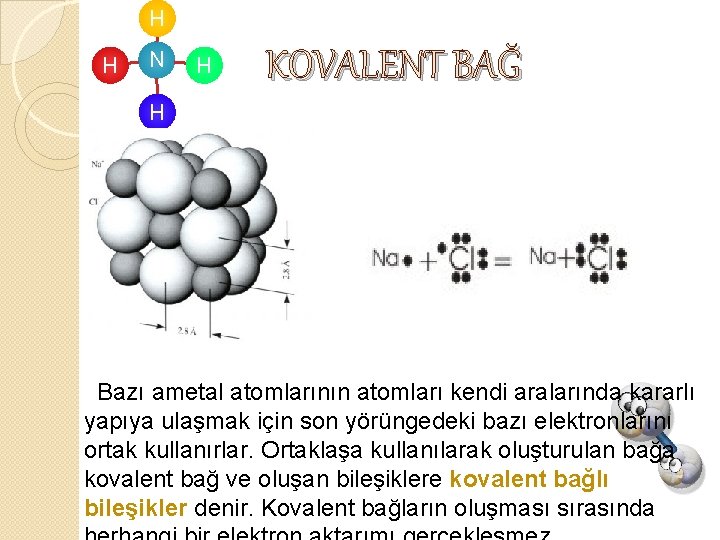
H H N H KOVALENT BAĞ H Bazı ametal atomlarının atomları kendi aralarında kararlı yapıya ulaşmak için son yörüngedeki bazı elektronlarını ortak kullanırlar. Ortaklaşa kullanılarak oluşturulan bağa kovalent bağ ve oluşan bileşiklere kovalent bağlı bileşikler denir. Kovalent bağların oluşması sırasında
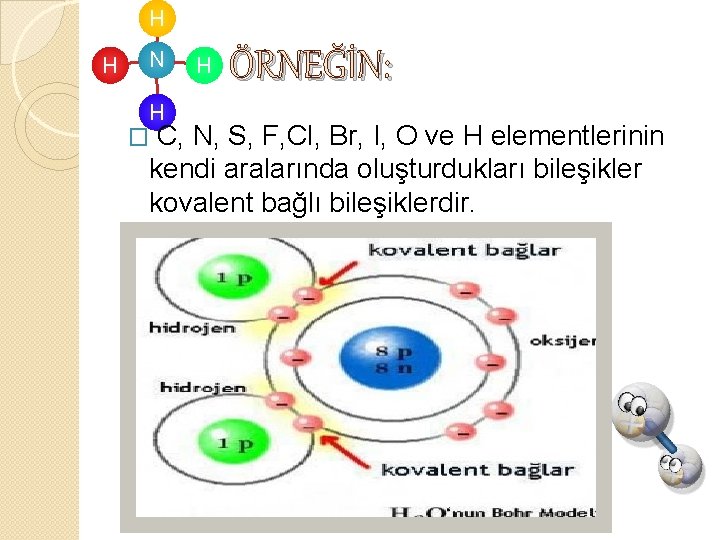
H H N H � C, H ÖRNEĞİN: N, S, F, Cl, Br, I, O ve H elementlerinin kendi aralarında oluşturdukları bileşikler kovalent bağlı bileşiklerdir.

H H N H H Kovalent bağlı bileşikleri apolar kovalent ve polar kovalent bağ olmak üzere ikiye ayırırız. Apolar Kovalent Bağ: Aynı cins ametal atomları arasında kovalent bağlı bileşikler oluşur. Örneğin; Cl 2, H 2, O 2 gibi moleküller apolar kovalent bağlıdır.

H H N H H Ortaklaşa kullanılan elektronlar eşit paylaşıldığından molekülün pozitif veya negatif kutbu yoktur; yani kutupsuz bir bağdır.
H H N H H Polar Kovalent Bağ Farklı cins ametal atomların yapmış oldukları kutuplu bağlardır. Elektronlar iki atom arasında eşit olarak paylaşılmadığından kutuplaşma oluşur. Ametallerden biri ortaklaşa kullanıldığından dolayı molekülün bir ucu pozitif (+), diğer ucu negatif (-) yüklenir.
H H N H H HCl, HF, CO 2, NO, CO, OF 2, CO 2, H 2 O gibi moleküller polar kovalent bağa örnek verilebilir.
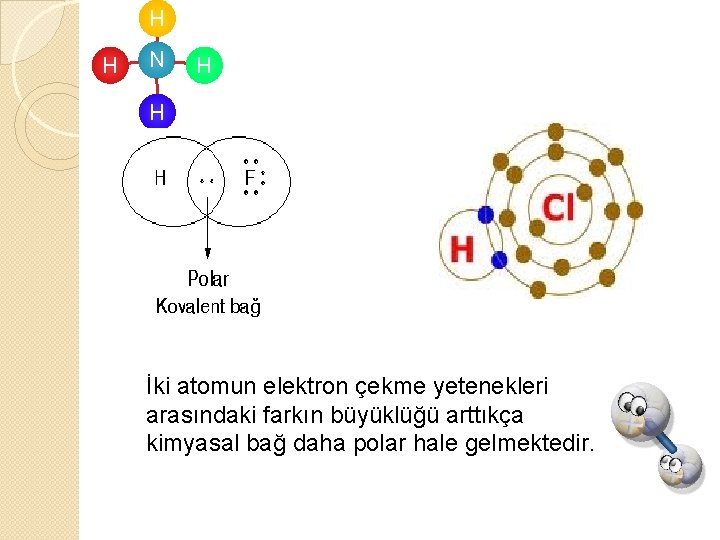
H H N H H İki atomun elektron çekme yetenekleri arasındaki farkın büyüklüğü arttıkça kimyasal bağ daha polar hale gelmektedir.

H H N H Metalik Bağ H Metal atomlarını katı ve sıvı halde bir arada tutan kuvvetlerdir ve metal atomları arasında metal bağı etkişimini oluştururlar. Metallerde değerlik elektronlar, atom çekirdekleri tarafından kuvvetli tutulmazlar. Bunun sebebi metallerin iyonlaşma enerjilerinin ve elektronegatifliklerinin oldukça düşük olmasıdır.
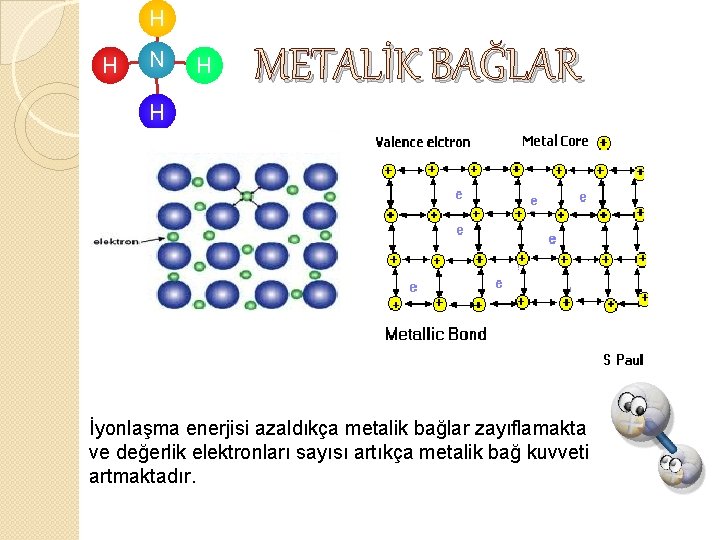
H H N H METALİK BAĞLAR H İyonlaşma enerjisi azaldıkça metalik bağlar zayıflamakta ve değerlik elektronları sayısı artıkça metalik bağ kuvveti artmaktadır.
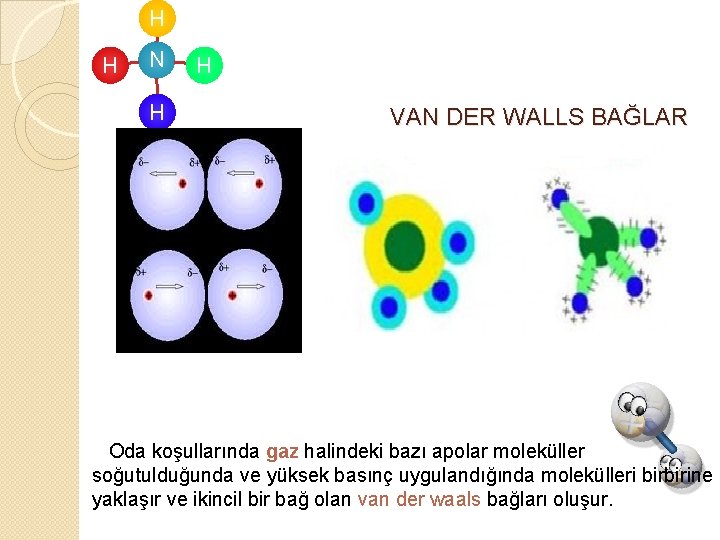
H H N H H VAN DER WALLS BAĞLAR Oda koşullarında gaz halindeki bazı apolar moleküller soğutulduğunda ve yüksek basınç uygulandığında molekülleri birbirine yaklaşır ve ikincil bir bağ olan van der waals bağları oluşur.
H H N H Van Der Waals Bağı H Pozitif olarak yüklenmiş molekülün bir kısmı ve negatif olarak yüklenmiş ikinci molekülün bir kısmı arasındaki kısa süreli zayıf çekim kuvvetidir. Molekülde elektronların yoğun olduğu taraf kısmen negatif, diğer taraf da kısmen pozitif yüklenir. Pozitif ve negatif yüklü kısımları arasındaki kuvvetlerin etkisi ile moleküller arasında oluşan bağlara van der waals bağları denilmektedir.

H H N H H Hidrojen Bağı Hidrojenin elektron ilgisi büyük atomlarla oluşturduğu bileşiklerde, molekülleri bir arada tutan kuvvete hidrojen bağı denir. H atomunun kovalent olarak bağlandığı yüksek elektronegatiflikteki atom, bağ elektronlarını kendine doğru çeker ve bir hidrojen bağı oluşturur. Biokimyasal sistemlerin yapıları kısmen hidrojen bağı etkileşmelerinin sonucu olarak belirlenir.
H H N H H HİDROJEN BAĞI
- Slides: 24