H 16 Berekeningen aan zuren en basen Algemene

H 16. Berekeningen aan zuren en basen

Algemene info • Zuur Deeltje dat H+ afstaat – HCl + H 2 O H 3 O+ + Cl- • Base Deeltje dat H+ opneemt – NH 3 + H 2 O NH 4+ + OH- • Notatie; – Sterk zuur/base: H 3 O+ + Z- (100% ionisatie) • Zuren tot H 3 O+, basen tot OH- – Zwak zuur/base: HZ(aq) (1 -10% ionisatie) • Zuren tot H 2 O, basen tot H 2 O – rest te zwak
![Algemene info • • p. H = -log [H 3 O+] = 10 -p. Algemene info • • p. H = -log [H 3 O+] = 10 -p.](http://slidetodoc.com/presentation_image_h/cabe3aabbf85746abf80b6b874b8248a/image-3.jpg)
Algemene info • • p. H = -log [H 3 O+] = 10 -p. H p. OH = -log [OH-] = 10 -p. OH p. H + p. OH = pkw (T afhankelijk, Binas 50 A) Significantie; aantal signi in conc geeft aantal decimalen. [H 3 O+] =1, 0 E-2 p. H=2, 00 • LET OP: instabiele zuren, bijv. H 2 CO 3 • Amfolyt; afhankelijk van kz en kb; HCO 3 - = base omdat kb>kz

p. H berekening Sterk • Sterk zuur: HNO 3 + H 2 O H 3 O+ + NO 3 • 0, 10 M HNO 3 p. H = -log [H 3 O+] = 1, 00 – 100% geïoniseerd, HNO 3 geeft 1 H+ af dus zoals hier boven. • Sterke base: 0, 20 gram calciumoxide in 0, 500 liter water bij kamertemperatuur, bereken p. H. • Ca. O(s) + H 2 O(l) Ca 2+(aq) + 2 OH-(aq) 0, 00357 mol x 2 0, 00713 mol : 56, 08 g/mol 0, 20 gram : 0, 500 liter [OH-] = 0, 014 M p. OH=-log [OH-]=1, 85 p. H=12, 15

Verloopt de reactie? • Sterk zuur met sterke base – Loopt 100% af • Sterk zuur met zwakke base en Zwak zuur met sterke base – Evenwicht ligt zeer sterk rechts (bijna 100%) • Zwak zuur met zwakke base – Controleer in Binas 49. Staat zuur boven base dan reactie. (Evenwichtsreactie) – Staat zuur onder base. Evenwicht sterk links (geen reactie)

Regels voor reactievergelijkingen 1. 2. 3. 4. 5. 6. 7. Noteer alle deeltjes Sorteer zure en basische deeltjes Sterkste zuur en base Verloopt een reactie en hoe vaak? Stel de vergelijking op Klopt je vergelijking wbt deeltjes en lading Check of er deeltjes dubbel staan of binding aangaan • Ammonia met azijnzuur • NH 3(aq), H 2 O, CH 3 COOH(aq) zuur base H 2 O CH 3 COOH NH 3 • Zwak zuur met zwakke base dus evenwicht! CH 3 COOH (aq) + NH 3 (aq) CH 3 COO- (aq) + NH 4+ (aq)

Vergelijkingen oefenen • Geef de vergelijking tussen – Overmaat HCl opl en Na 3 PO 4 (s) – NH 3 opl en HF opl – HIO opl en Na. OH (s) • Geef de vergelijking tussen – 3 H 3 O+ + Na 3 PO 4(s) H 3 PO 4 + 3 Na+(aq) + 3 H 2 O – NH 3(aq) + HF (aq) F-(aq) + NH 4+(aq) – HIO(aq) + Na. OH (s) Na+(aq) + IO-(aq) + H 2 O

Koolzuur evenwicht • Koolstofdioxide lost slecht op in water – CO 2(g) + H 2 O(l) H 2 CO 3 (aq) (1) • Koolzuur is zwak zuur – H 2 CO 3(aq) + H 2 O(l) H 3 O+(aq) + HCO 3 - (aq) – HCO 3 - (aq) + H 2 O(l) H 3 O+(aq) + CO 32 - (aq) (2) (3) • Stel; – We voegen OH- opl toe • • In (3) neemt H 3 O+(aq) af. Dus evenwicht naar recht. Minder HCO 3 - (aq) in (2) betekent ook ev in (2) naar rechts. Dus minder H 2 CO 3 in (1) dus ev naar rechts. Conclusie: door p. H omhoog minder [CO 2(g)] – We voegen H 3 O+ opl toe; • Conclusie: door p. H omlaag [CO 2(aq)] stijgt
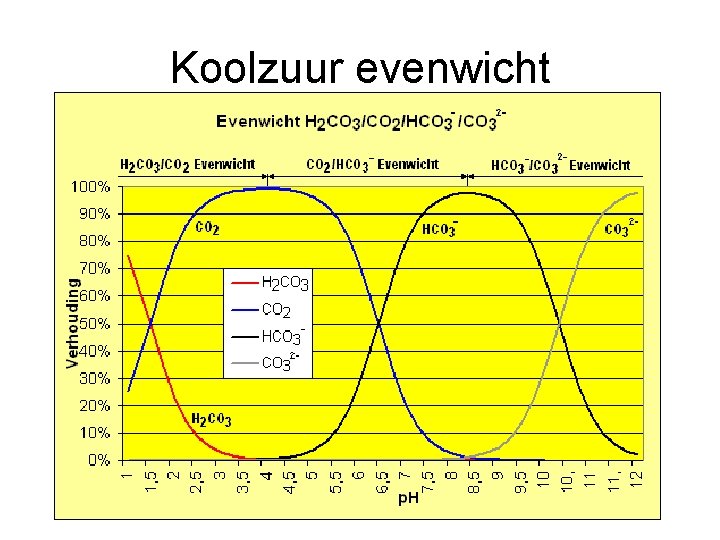
Koolzuur evenwicht

Koolzuur evenwicht • Exp 16. 2 • Bestuderen 16. 3 • Maken opgave tot en met 11
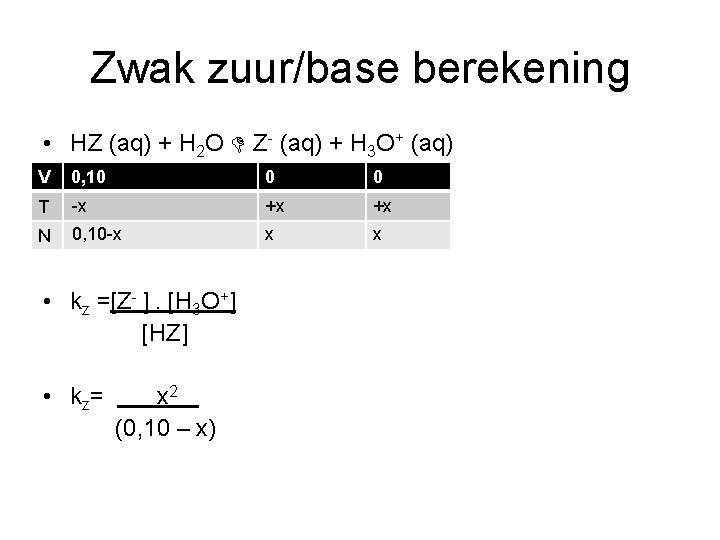
Zwak zuur/base berekening • HZ (aq) + H 2 O Z- (aq) + H 3 O+ (aq) V 0, 10 0 0 T -x +x +x N 0, 10 -x x x • kz =[Z- ]. [H 3 O+] [HZ] • kz= x 2 (0, 10 – x)
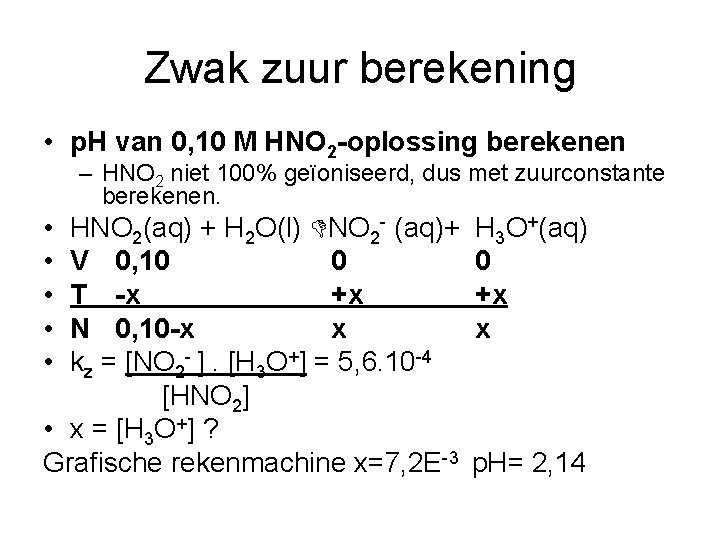
Zwak zuur berekening • p. H van 0, 10 M HNO 2 -oplossing berekenen – HNO 2 niet 100% geïoniseerd, dus met zuurconstante berekenen. • • • HNO 2(aq) + H 2 O(l) NO 2 - (aq)+ V 0, 10 0 T -x +x N 0, 10 -x x kz = [NO 2 - ]. [H 3 O+] = 5, 6. 10 -4 [HNO 2] • x = [H 3 O+] ? Grafische rekenmachine x=7, 2 E-3 H 3 O+(aq) 0 +x x p. H= 2, 14

Extra p. H • 1. 2. 3. 4. 5. 6. 7. Extra opgave 5; Bereken de p. H van een oplossing van 1, 0 · 10 -1 M azijnzuur 1, 0 · 10 -2 M HCN 0, 10 M zoutzuur 0, 10 M Na. CN-oplossing 0, 020 M waterstoffluoride-oplossing 1, 0 M HNO 2 0, 010 M KF-oplossing

Antwoorden extra p. H 1 • • • 2 3 4 5 6 7 CH 3 COOH(aq) + H 2 O ↔ CH 3 COO-(aq) + H 3 O+(aq) Kz = 1, 8 * 10 -5 0, 10 mol 0 0 -X +X +X 0, 10 -X X X Kz= [CH 3 COO-(aq)] * [H 3 O+(aq)]/ [CH 3 COOH(aq)] = X 2/(0. 1 -X) Gr X = 0. 0013 p. H = 2, 88 X= 2. 470 * 10 -6 p. H = 5. 61 Sterk zuur p. H= 1 X= 1. 25 * 10 -3 p. OH = 2. 90 p. H = 11. 10 X= 3. 25 * 10 -3 p. H = 2. 49 X= 2. 34 * 10 -2 p. H = 1. 63 X= 3. 99 * 10 -7 p. OH = 6. 4 p. H = 7. 6

instinker • • Wat is de p. H van een verzadigde oplossing van Ca(OH)2? Rv – • Ks – • • Ca(OH)2 �Ca 2+ + 2 OHKs =[Ca 2+]∙[OH-]2 = 4, 7 ∙ 10 -6 4 x 3 = 4, 7 ∙ 10 -6 x=1, 06 ∙ 10 -2 [OH-] = 2* 1, 06 ∙ 10 -2 p. OH=1, 67 p. H = 12, 32

Buffer • Oplossing waarvan de p. H maar klein beetje verandert, bij toevoegen van sterk zuur/base of bij verdunning • Bestaat uit mengsel van zwak zuur en geconjugeerde base in verhouding 1: 10 tot 10: 1 CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ • kz =[CH 3 COO- ]. [H 3 O+] [CH 3 COOH] • Buffercapaciteit; hoeveel zuur/base de buffer kan hebben. • Als 1: 1 dan is p. H=Kz • Buffer berekening – 0, 20 mol acetaat en 0, 80 mol azijnzuur in bepaald volume • p. H= 4, 14 – Nu 50 m. L 1 M zoutzuur toevoegen. (Vol verandering verwaarlozen) • p. H = 4, 0 geworden

Buffer in lichaam • • CO 2 (aq) + H 2 O (l) H 2 CO 3 (aq) +Hb(aq) HCO 3 - (aq) + HHb+(aq) HHb+ + O 2 HHb. O 2+ Spier Bloed Longen (1) (2) • Koolzuurbuffer in lichaam. Kz = 8, 0 E-7, p. H Bloed=7. 4 • 8, 0 E-7 = 4 E-8 · [HCO 3 -]/[H 2 CO 3] • [HCO 3 -]/[H 2 CO 3]= 20/1, kan vooral zuren bufferen
- Slides: 17