Gymnzium Hranice Zborovsk 293 Projekt Svt prce v

©Gymnázium Hranice, Zborovská 293 Projekt: Svět práce v každodenním životě Číslo projektu: CZ. 1. 07/1. 1. 26/02. 0007 Stavba atomu Aktivita č. 6: Poznáváme chemii Prezentace č. 9 Autor: Lenka Poláková 1

©Gymnázium Hranice, Zborovská 293 Historie – názory na stavbu hmoty • již od starověku se učenci snažili najít „pralátku“ – základ všech látek • Démokritos (5. století př. n. l. ) - autor filosofické teorie: látky jsou tvořeny z malých, dále nedělitelných částic, „atomů“ (z řeckého átomos = nedělitelný) – atomů existuje mnoho druhů – hmota je tvořena z různě uspořádaných atomů různého druhu – atomy není možno vytvářet ani ničit Démokritos 1 2

©Gymnázium Hranice, Zborovská 293 Historie – názory na stavbu hmoty • Robert Boyle (17. století) – základní stavební kameny látek jsou chemické prvky – ty jsou podle něj už nedělitelné 2 • John Dalton (19. století) – návrat k atomové teorii: látky jsou tvořeny z velmi malých, dále nedělitelných částic „atomů“ – prvek je soubor atomů stejného druhu – atomy jednoho prvku mají stejnou hmotnost na rozdíl od atomů jiných prvků Robert Boyle 3 John Dalton 3

©Gymnázium Hranice, Zborovská 293 Historie – názory na stavbu hmoty • J. J. Thomson – 1897 objev elektronu – popřel Daltonovu teorii o nedělitelnosti atomu – vytvořil Thomsonův (pudinkový) model atomu – atom je kladně nabitá hmota, ve které se volně pohybují záporně nabité elektrony (jako rozinky v pudinku) 4 Thomsonův model atomu 5 J. J. Thomson 4
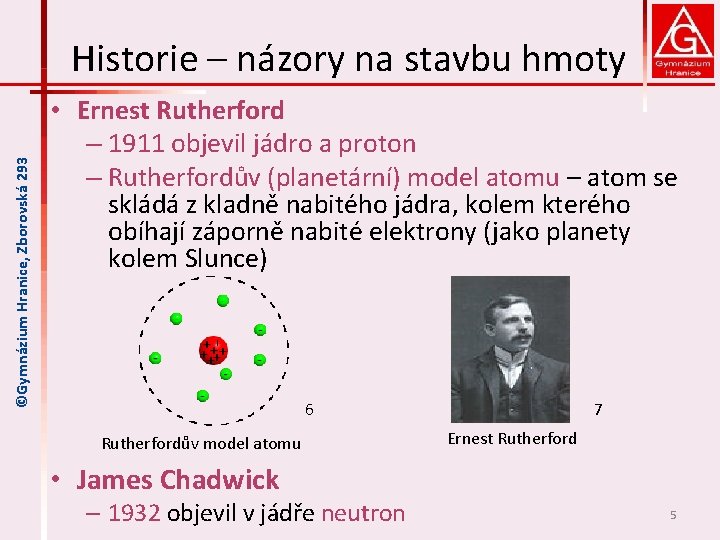
©Gymnázium Hranice, Zborovská 293 Historie – názory na stavbu hmoty • Ernest Rutherford – 1911 objevil jádro a proton – Rutherfordův (planetární) model atomu – atom se skládá z kladně nabitého jádra, kolem kterého obíhají záporně nabité elektrony (jako planety kolem Slunce) 6 Rutherfordův model atomu 7 Ernest Rutherford • James Chadwick – 1932 objevil v jádře neutron 5

©Gymnázium Hranice, Zborovská 293 Atom Ø z řeckého átomos = nedělitelný Ø je nejmenší částice hmoty Ø tvoří: • jádro – vnitřní část atomu • atomový (elektronový) obal Ø je tvořen menšími částicemi: protony, neutrony, elektrony 6
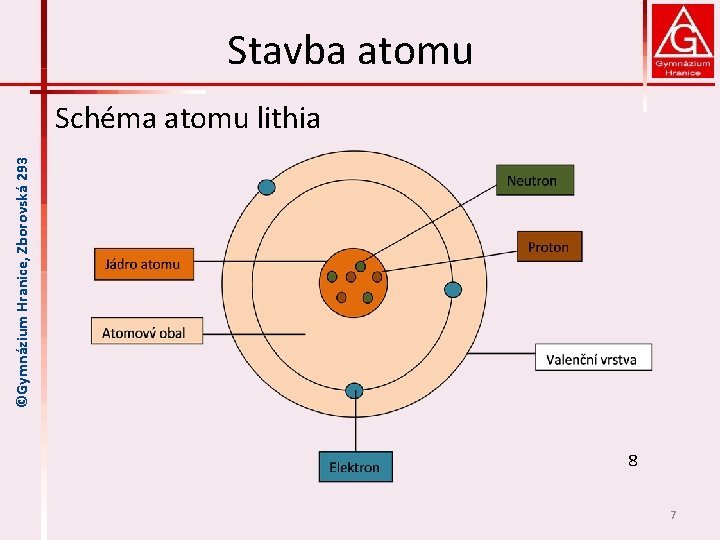
Stavba atomu ©Gymnázium Hranice, Zborovská 293 Schéma atomu lithia 8 7

©Gymnázium Hranice, Zborovská 293 Jádro atomu velmi malé v porovnání s velikostí celého atomu tvoří 99, 9 % hmotnosti atomu kladně nabitá část atomu obsažené částice: – protony – kladně nabité částice p+ – neutrony – elektricky neutrální částice n 0 • tyto částice v jádrech atomů jsou poutány silami, tj. jadernými silami • hmotnost částic v jádře atomu (protonů, neutronů) je mnohem větší než hmotnost elektronů v elektronovém obalu • • 8

©Gymnázium Hranice, Zborovská 293 Atomový (elektronový) obal • má záporný náboj • obsažené částice: elektrony e- – záporně nabité částice • mezi kladně nabitým jádrem a záporně nabitým elektronovým obalem působí přitažlivé elektrické síly, které drží celý atom pohromadě • atom je elektricky neutrální, tj. má stejný počet protonů v jádře a elektronů v elektronovém obalu 9

©Gymnázium Hranice, Zborovská 293 Elektronové vrstvy • elektrony se pohybují okolo jádra na vrstvách, tj. elektronové vrstvy • elektronové vrstvy: – liší se vzdáleností od jádra – elektrony se na jednotlivých vrstvách liší svou energií – s rostoucí vzdáleností vrstvy od jádra roste energie elektronů na této vrstvě – na jednotlivých vrstvách se liší počet elektronů 10

©Gymnázium Hranice, Zborovská 293 Valenční vrstva je poslední elektronová vrstva obsazená elektrony – nejvzdálenější vrstva od jádra – její elektrony mají největší energii – její elektrony jsou označovány valenční elektrony Valenční elektrony – ovlivňují vlastnosti atomů prvků (reaktivitu) 11

Zdroje ©Gymnázium Hranice, Zborovská 293 Obrázky: Použité obrázky jsou dostupné pod licencí Creative Commons nebo Public Domain. 1. 2. 3. 4. 5. 6. 7. Tomisti. File: Democritus 2. jpg. http: //commons. wikimedia. org. [Online] 17. 3 2006. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: Democritus 2. jpg. Manske, Magnus. File: Robert Boyle. jpg. http: //commons. wikimedia. org. [Online] 22. 5 2006. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: Robert_Boyle. jpg. Materialscientist. File: Dalton John desk. jpg. http: //commons. wikimedia. org. [Online] 9. 3 2012. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: Dalton_John_desk. jpg. Fastfission. File: Plum pudding atom. svg. http: //commons. wikimedia. org. [Online] 30. 12 2005. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: Plum_pudding_atom. svg. Adrian. benko. File: JJ Thomson. jpg. http: //commons. wikimedia. org. [Online] 15. 2 2005. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: JJ_Thomson. jpg. MILAN, Jean-Jacques. File: Rutherfordsches Atommodell. png. http: //commons. wikimedia. org. [Online] 27. 8 2005. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: Rutherfordsches_Atommodell. png. Blurpeace. File: Ernest Rutherford. jpg. http: //commons. wikimedia. org. [Online] 2. 10 2009. [Citace: 11. 1 2014. ] http: //commons. wikimedia. org/wiki/File: Ernest_Rutherford. jpg. obrázek č. 8 vlastní tvorba Knihy: Beneš Pavel, Pumpr Václav, Banýr Jiří. Základy chemie 1 - učebnice. Praha : Fortuna, 2005. ISBN 80 -7168 -720 -0. 12
- Slides: 12