Gymnzium Hranice Zborovsk 293 Projekt Svt prce v

©Gymnázium Hranice, Zborovská 293 Projekt: Svět práce v každodenním životě Číslo projektu: CZ. 1. 07/1. 1. 26/02. 0007 Látkové množství, molární hmotnost Aktivita č. 6: Poznáváme chemii Prezentace č. 17 Autor: Lenka Poláková 1

©Gymnázium Hranice, Zborovská 293 Látkové množství n • při práci v chem. laboratoři pracujeme s obrovským počtem částic (např. v malém krystalu kuchyňské soli, v kapce vody je asi 10²¹ molekul) • fyzikální veličina - látkové množství n - byla zavedena pro jednodušší vyjádření počtu částic chem. látky (atomů, molekul, iontů) • jednotka látkového množství 1 mol = 6, 023 ∙ 10²³ částic Avogadrova konstanta NA • 1 mol chemické látky obsahuje stejný počet částic jako je atomů ve 12 g uhlíku • 1 mol chem. látky představuje vždy stejný počet částic (atomů, molekul, iontů) 2

©Gymnázium Hranice, Zborovská 293 Látkové množství plynu • důležitou charakteristikou plynů je jejich objem – jaký je vztah mezi látkovým množstvím a objemem plynů? • za normálních podmínek (t = 0°C, p = 101 k. Pa) všechny plynné látky o látkovém množství 1 mol zaujímají stejný objem Vm = 22, 4 dm³ (22, 4 l) • 5 Si, 4 H₂, 10 P₄, 3 KCl s těmito zápisy jste se již setkali a umíte rozeznat v zápise atomy a molekuly, čísla v těchto zápisech vyjadřují také látková množství jednotlivých látek 5 Si 5 mol křemíku (5 ∙ 6, 023 ∙ 10²³ atomů křemíku) 4 H₂ 4 mol H₂ (4 ∙ 6, 023 ∙ 10²³ molekul H₂) 3 Přečtěte a vysvětlete zbývající 2 zápisy.

Molární hmotnost ©Gymnázium Hranice, Zborovská 293 Molární hmotnost M • je fyzikální veličina, která vyjadřuje hmotnost 1 molu látky • tento poměr je pro každou určitou látku konstantní • jednotka: g/mol • důležitá charakteristika chem. prvků a sloučenin, její hodnoty najdeme v tabulkách • molární hmotnost sloučeniny vypočítáme součtem molárních hmotností všech atomů ve vzorci sloučeniny 4

©Gymnázium Hranice, Zborovská 293 Výpočet molární hmotnosti Vypočítejte molární hmotnost amoniaku NH₃. • v tabulkách najdeme potřebné molární hmotnosti M (N) = 14, 01 g/mol M (H) = 1, 008 g/mol • vypočet: M (NH₃) = 1 ∙ M (N) + 3 ∙ M (H) M (NH₃) = 1 ∙ 14, 01 + 3 ∙ 1, 008 M (NH₃) = 17, 034 g/mol Vypočítejte molární hmotnost oxidu chromitého. • vzorec + molární hmotnosti z tabulek Cr₂O₃ M (Cr) = 52, 0 g/mol M (O) = 16, 0 g/mol • výpočet: M (Cr₂O₃) = 2 ∙ M (Cr) + 3 ∙ M (O) M (Cr₂O₃) = 2 ∙ 52, 0 + 3 ∙ 16, 0 M (Cr₂O₃) = 152 g/mol 5

©Gymnázium Hranice, Zborovská 293 Výpočet molární hmotnosti Vypočítejte molární hmotnosti následujících sloučenin: a) chlorid zinečnatý b) oxid vanadičný c) sulfid draselný d) Na. NO₃ Řešení: a) M (Zn. Cl₂) = 136, 28 g/mol b) M (V₂O₅) = 181, 88 g/mol c) M (K₂S) = 110, 26 g/mol d) M (Na. NO₃) = 85 g/mol 6

Látkové množství - shrnutí ©Gymnázium Hranice, Zborovská 293 Co všechno zjistíme z údaje o látkovém množství? hmotnost látky m = n ∙ M objem plynné látky V = n ∙ Vm n počet částic látky N = n ∙ NA Příklad: 6 Cl₂ • 6 mol dvouatomových molekul chloru • 36, 1 ∙ 10²³ molekul Cl₂ • hmotnost: M (Cl₂) = 70, 9 g/mol, m = 425, 4 g • objem: V = 6 ∙ 22, 4 = 134, 4 l chloru 7
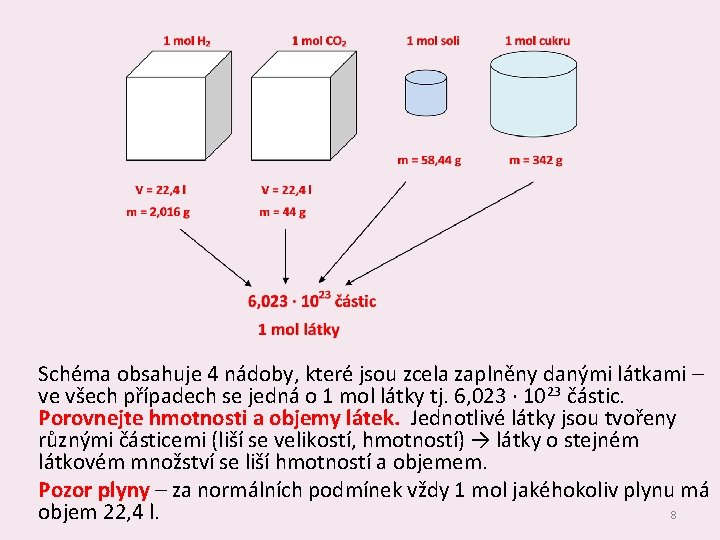
Schéma obsahuje 4 nádoby, které jsou zcela zaplněny danými látkami – ve všech případech se jedná o 1 mol látky tj. 6, 023 ∙ 1023 částic. Porovnejte hmotnosti a objemy látek. Jednotlivé látky jsou tvořeny různými částicemi (liší se velikostí, hmotností) → látky o stejném látkovém množství se liší hmotností a objemem. Pozor plyny – za normálních podmínek vždy 1 mol jakéhokoliv plynu má 8 objem 22, 4 l.
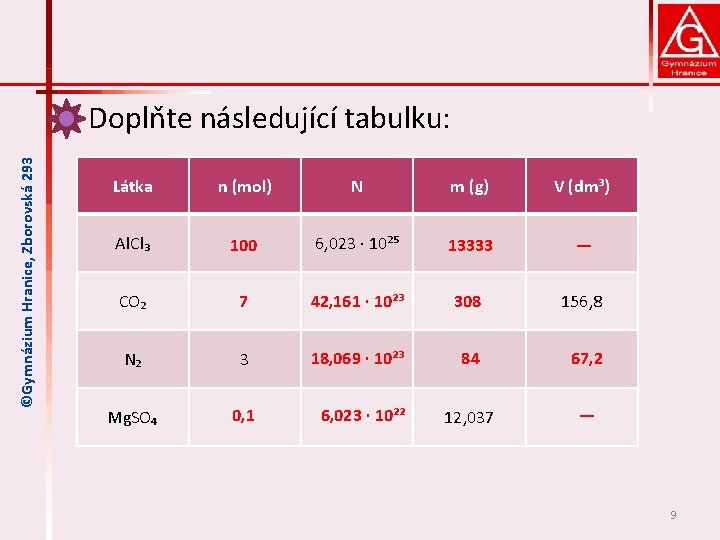
©Gymnázium Hranice, Zborovská 293 Doplňte následující tabulku: Látka n (mol) N m (g) V (dm³) Al. Cl₃ 100 6, 023 ∙ 10²⁵ 13333 ― CO₂ 7 42, 161 ∙ 10²³ 308 156, 8 N₂ 3 18, 069 ∙ 10²³ 84 67, 2 Mg. SO₄ 0, 1 12, 037 ― 6, 023 ∙ 10²² 9

Látková koncentrace ©Gymnázium Hranice, Zborovská 293 Látková koncentrace c látkové množství rozpuštěné látky objem roztoku • jednotka: mol/dm³ tj. mol/l • slouží k vyjádření složení roztoků • čím větší je koncentrace roztoku, tím větší množství rozpuštěné látky roztok obsahuje • 2 M roztok Na. Cl – označení pro roztok Na. Cl c = 2 mol/l 10

Výpočty – látková koncentrace ©Gymnázium Hranice, Zborovská 293 Příklad: Jakou látkovou koncentraci bude mít roztok, jestliže ve 3 litrech tohoto roztoku je rozpuštěno 120 g hydroxidu sodného Na. OH? M (Na. OH) = 40 g/mol Koncentrace roztoku Na. OH je 1 mol/l. Příklad: Vypočítejte látkovou koncentraci roztoku, jestliže ve 2 litrech tohoto roztoku je rozpuštěno 56 g hydroxidu draselného KOH. Výsledek: c = 0, 5 mol/l 11

Výpočty – látková koncentrace ©Gymnázium Hranice, Zborovská 293 Příklad: Vypočítejte objem roztoku o koncentraci 1, 4 mol/l, který vznikl rozpuštěním 28 g Na. OH. M (Na. OH) = 40 g/mol Objem 1, 4 M roztoku Na. OH je 0, 5 l. 12

©Gymnázium Hranice, Zborovská 293 Zdroje Obrázky: Schéma strana 4 vlastní tvorba Knihy: Beneš Pavel, Pumpr Václav, Banýr Jiří. Základy chemie 1 - učebnice. Praha : Fortuna, 2005. ISBN 807168 -720 -0. 13
- Slides: 13