Gymnzium Hranice Zborovsk 293 Projekt Svt prce v

©Gymnázium Hranice, Zborovská 293 Projekt: Svět práce v každodenním životě Číslo projektu: CZ. 1. 07/1. 1. 26/02. 0007 Molekula, prvek, sloučenina Aktivita č. 6: Poznáváme chemii Prezentace č. 10 Autor: Lenka Poláková 1

Chemický prvek • Protonové číslo je číslo, které vyjadřuje počet protonů v jádře atomu • Chemický prvek ‐ je základní stavební částice hmoty ‐ je látka složena z atomů stejného druhu, tj. se stejným protonovým číslem ‐ dnes je známo více než 120 různých druhů atomů = prvků ‐ má mezinárodní (latinský) název ‐ má český název ‐ má značku prvku ‐ prvky s protonovým číslem 1 – 92 existují v přírodě, další byly připraveny uměle a jsou nestabilní 2

Latinský název prvku může vyjadřovat: • významnou vlastnost prvku ‐ CHLOR – plyn světle zelené barvy, řecky „světle zelený“ je „chloros“ ‐ FOSFOR – prvek, který uvolňoval tajemné zelenkavé světlo, latinsky „phosphorus“, tj. „světlonoš“ ‐ STŘÍBRO – kov, který má bílý lesklý povrch, „argentum“ ve všech jazycích je „běloskvoucí“ • zdroj výskytu prvku ‐ KYSLÍK – název vycházel ze špatné myšlenky, že kyslík je součástí všech kyselin, „oxys“ – kyselý, „gennao“ – tvořím, pojmenován jako , , Ten, který tvoří kyselinu" ‐ SODÍK – název odvozen od jeho známé sloučeniny „sody“ ‐ VODÍK – řecky „hydro“ ‐ voda, „gennao“ ‐ tvořím, „Ten, 3 který tvoří vodu“

• jméno vědce, objevitele – einsteinium, mendelevium • na počest země – germanium (Germania je latinsky Německo) – gallium (Gallia je latinsky Francie) Český název prvku ‐ většinou odvozen z latinských názvů ‐ historické názvy některých prvků: kazík (F), solík (Cl), barvík (Cr), voník (Os), ďasík (Co), jermík (Mn), surmík (Sb), těžík (W), sitaník (As), sladík (Be) ‐ Jan Svatopluk Presl vytvořil názvy některých prvků pomocí koncovy –ík , př. stroncium ‐ strontík, yterbium ‐ ytřík, platina – platík, tyto názvy se většinou neuchytily Napište příklady českých názvů prvků, u kterých byly tyto názvy (s koncovkami –ík) zachovány dodnes: 4 vodík, kyslík, dusík, uhlík, hliník, hořčík, křemík, draslík, sodík, vápník

Značka prvku Symbol = značka prvku ‐ alchymisté a další chemici se snažili pro látky najít určité symboly (používaly se i grafické znaky – inspirací byla mytologie a astrologie) ‐ např. kruh s tečkou – symbol Slunce – zlato ‐ kopí a štít – znaky boha války Marse – železo ‐ zrcadlo – znak bohyně Venuše – vznikla z mořské pěny na Kypru (zásoby mědi) → měď Příklady některých používaných symbolů prvků 1 5

Značka prvku ‐ J. J. Berzelius – počátkem 19. století vytvořil systém jednoduchých chem. symbolů – používán dodnes ‐ symboly odvozeny také od latinských názvů prvků ‐ je tvořen 1 až 3 písmeny, první písmeno vždy velké ‐ př. vodík H (hydrogenium), kyslík O (oxygenium), dusík N (nitrogenium), síra S (sulphur), měď Cu (cuprum), cín Sn (stannum), křemík Si (silicium) Přečtěte následující zápisy: 6 Cu, 5 Ar, 4 S, 7 Fe, 4 Na, 2 O, 5 C, 8 Mg Zjistěte, zda vaše jméno a příjmení obsahuje ukryté značky prvků – napište je. 6

Charakteristiky prvku • Protonové číslo Z ‐ udává počet protonů v jádře atomu ‐ vyjadřuje počet elektronů v elektronovém obalu ‐ určuje umístění prvku v periodické soustavě prvků • Nukleonové (hmotnostní) číslo A ‐ udává počet protonů a neutronů (tj. nukleonů) v jádře atomu – odvozeno z latinského nukleus = jádro ‐ A – Z = počet neutronů 7
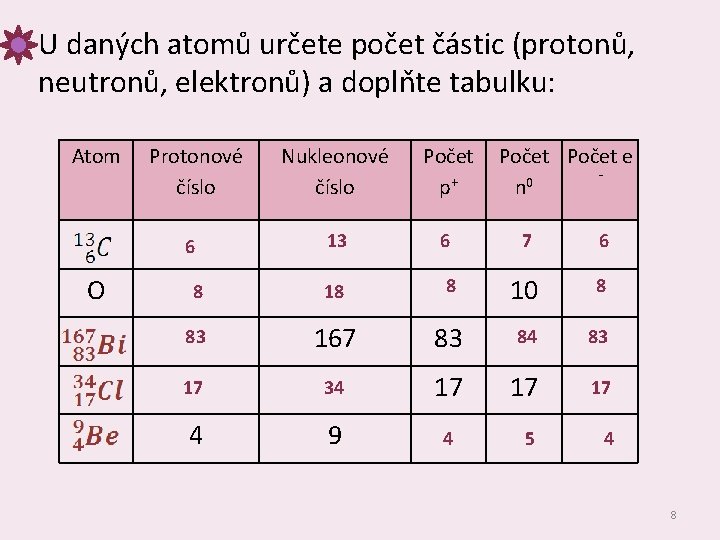
U daných atomů určete počet částic (protonů, neutronů, elektronů) a doplňte tabulku: Atom Protonové číslo Počet e ‐ + 0 p n 13 6 7 6 8 18 8 10 8 83 167 83 84 83 17 34 17 17 17 4 9 4 5 4 6 O Nukleonové číslo 8

Nuklid, izotop Prvek může existovat jako nuklid nebo izotop: • Nuklid je chemická látka složená z atomů se stejným protonovým a stejným nukleonovým číslem, např. nuklid uhlíku obsahuje pouze atomy s 6 protony a s 6 neutrony v jádře • Izotopy jsou atomy téhož prvku, které se liší počtem neutronů v jádře atomu ‐ jednotlivé izotopy se liší svými fyzikálními vlastnostmi (zejména hmotností a stálostí) ‐ např. vodík existuje v přírodě ve formě 3 izotopů Určete počet neutronů v jednotlivých izotopech vodíku. žádný neutron, 1 neutron, 2 neutrony 9
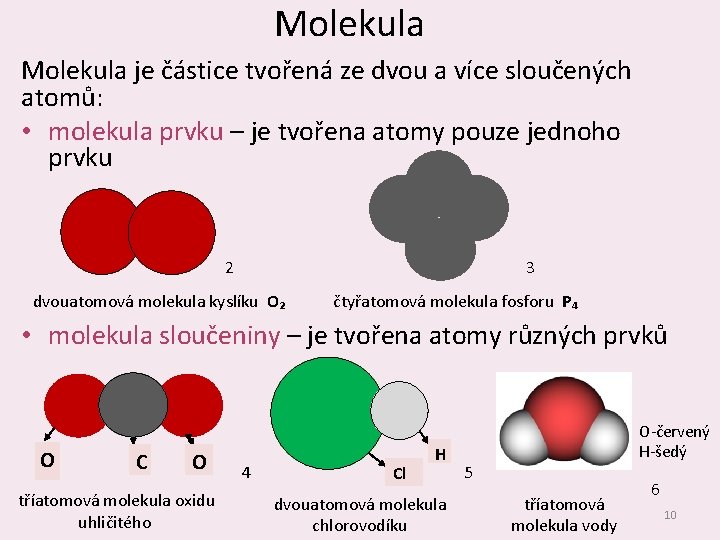
Molekula je částice tvořená ze dvou a více sloučených atomů: • molekula prvku – je tvořena atomy pouze jednoho prvku 2 3 dvouatomová molekula kyslíku O₂ čtyřatomová molekula fosforu P₄ • molekula sloučeniny – je tvořena atomy různých prvků O C O tříatomová molekula oxidu uhličitého 4 Cl H dvouatomová molekula chlorovodíku O‐červený H‐šedý 5 tříatomová molekula vody 6 10

Chemická sloučenina (sloučenina) je chemicky čistá látka tvořena jedním druhem molekul, které jsou složeny z atomů dvou a více různých prvků Chemický vzorec • slouží ke zjednodušenému zápisu složení sloučeniny • udává druh a počet atomů vázaných v molekule sloučeniny • obsahuje značky prvků, číslice – vyjadřují poměr jednotlivých prvků ve sloučenině molekula oxidu uhličitého: 1 C : 2 O → CO₂ O C O 4 11
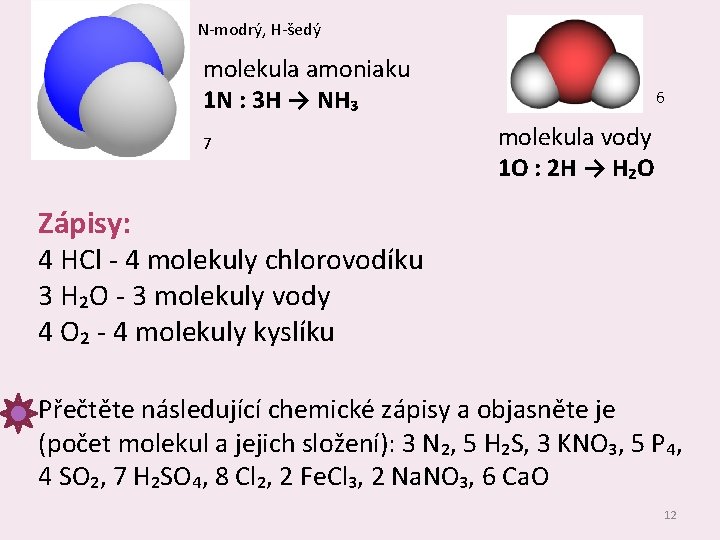
N‐modrý, H‐šedý molekula amoniaku 1 N : 3 H → NH₃ 7 6 molekula vody 1 O : 2 H → H₂O Zápisy: 4 HCl ‐ 4 molekuly chlorovodíku 3 H₂O ‐ 3 molekuly vody 4 O₂ ‐ 4 molekuly kyslíku Přečtěte následující chemické zápisy a objasněte je (počet molekul a jejich složení): 3 N₂, 5 H₂S, 3 KNO₃, 5 P₄, 4 SO₂, 7 H₂SO₄, 8 Cl₂, 2 Fe. Cl₃, 2 Na. NO₃, 6 Ca. O 12

Zdroje Obrázky: Použité obrázky jsou dostupné pod licencí Creative Commons nebo Public Domain. 1. Matanya. File: Alchemy symbols. jpg. http: //commons. wikimedia. org. [Online] 12. 4 2010. [Citace: 8. 2 2014. ] http: //commons. wikimedia. org/wiki/File: Alchemy_symbols. jpg? uselang=cs. 6. Lopossumi. File: H 2 O (water molecule) white. png. http: //commons. wikimedia. org. [Online] 25. 10 2006. [Citace: 19. 2 2014. ] http: //commons. wikimedia. org/wiki/File: H 2 O_%28 water_molecule%29_white. png. 7. Marbach, Frederic. File: 3 D ammoniac. PNG. http: //commons. wikimedia. org. [Online] 9. 4 2006. [Citace: 19. 2 2014. ] http: //commons. wikimedia. org/wiki/File: 3 D_ammoniac. PNG. Obrázky č. 2 – 5 vlastní tvorba. Knihy: Beneš Pavel, Pumpr Václav, Banýr Jiří. Základy chemie 1 - učebnice. Praha : Fortuna, 2005. ISBN 80‐ 7168‐ 720‐ 0. 13
- Slides: 13