Gymnzium Hranice Zborovsk 293 Projekt Svt prce v

©Gymnázium Hranice, Zborovská 293 Projekt: Svět práce v každodenním životě Číslo projektu: CZ. 1. 07/1. 1. 26/02. 0007 Fosfor Aktivita č. 6: Poznáváme chemii Prezentace č. 8 Autor: Hana Lovětínská 1

Fosfor Badatel Henning Brand si v Hamburku pořídil alchymistickou laboratoř a dal se do hledání kamene mudrců. Vycházel z předpokladu, že musí obsahovat prvotní hmotu, kterou však jistě obsahují i jiné látky, třeba lidská moč. Nashromáždil tedy asi tunu moči z místních kasáren. Odpařil ji na červený olej, ten předestiloval a zbytek potom žíhal. Po delší době zpozoroval, že se na stěnách usazuje bílý prášek, který ve tmě světélkoval. Svou látku nazval studený oheň. Teprve později vytvořil nový název spojením řeckých slov „phos“ (světlo) a „phero“ (nesu), který se dá přeložit jako „světlonoš“. Rok tohoto objevu není přesně znám, uvádí se 1669 nebo 1674. 2

Vlastnosti fosforu • nikdy se nevyskytuje volný, vždy ve sloučeninách • je biogenní prvek • spolu s dusíkem se vyskytuje: v nukleových kyselinách ATP - adenosintrifosfát • tvoří základní strukturu kostí a zubů • soli kyseliny fosforečné se nazývají fosfáty 3
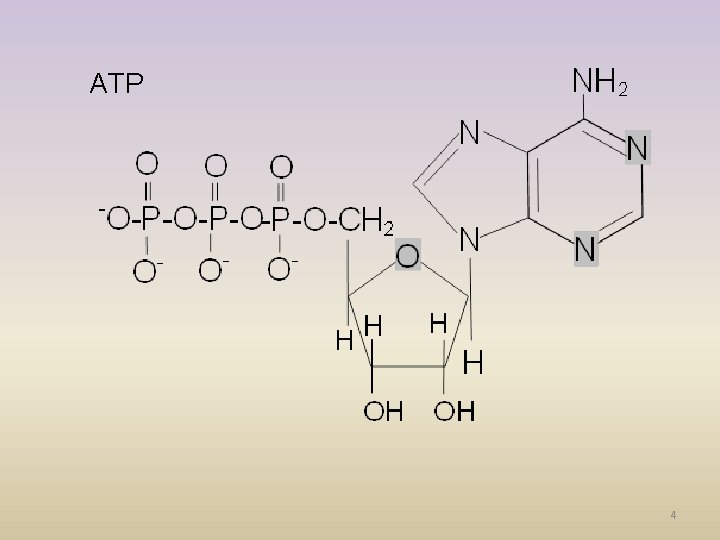
ATP 4

- v přírodě se vyskytuje ve formě málo rozpustných fosforečnanu = apatitů - z nich se taky získává Ca 5(PO 4)3 F Ca 5(PO 4)3 Cl Ca 5(PO 4)3 OH fluoroapatit chloroapatit hydroxoapatit - fosfor se vyrábí v elektrické peci, při 1400°C, redukcí uhlíkem za přítomnosti Si. O 2 5

Ca 5(PO 4)2 + Si. O 2 + C Ca. Si. O 3 + P 4 + CO - C je ve formě koksu, má redukující vlastnosti - Si. O 2 na sebe váže Ca, jinak by vznikal Ca 3 P 2 Rovnici vyčíslete! 6

Modifikace fosforu 1) bílý fosfor - žlutobílá voskovitá hmota - nerozpustný ve vodě - velmi jedovatý - tvořen molekulami P 4 (tetraedr) (1) 7

- na vzduchu se vzněcuje a hoří na P 4 O 10 - jeho oxidace je doprovázena světélkováním - uchovává se pod vodou 2) Červený fosfor – vzniká z bílého fosforu zahříváním za nepřítomnosti vzduchu po dobu několika dní. - tvoří řetězce, je to červenohnědý prášek - je poměrně stálý, nejedovatý, nerozpustný ve vodě - používá se na výrobu zápalek 8

3) Černý fosfor – nejstálejší modifikace - má makromolekulární strukturu - je elektricky vodivý - vyrábí se z bílého fosforu 9

Sloučeniny fosforu 1) PH 3 - mimořádně jedovatý plyn - s mdlým česnekovým zápachem - vysoce reaktivní, silné redukční činidlo 2) Oxidy a) P 2 O 3 - tvoří dimery b) P 2 O 5 - bílá pevná látka - velmi hygroskopická - s vodou tvoří kyselinu fosforečnou 10
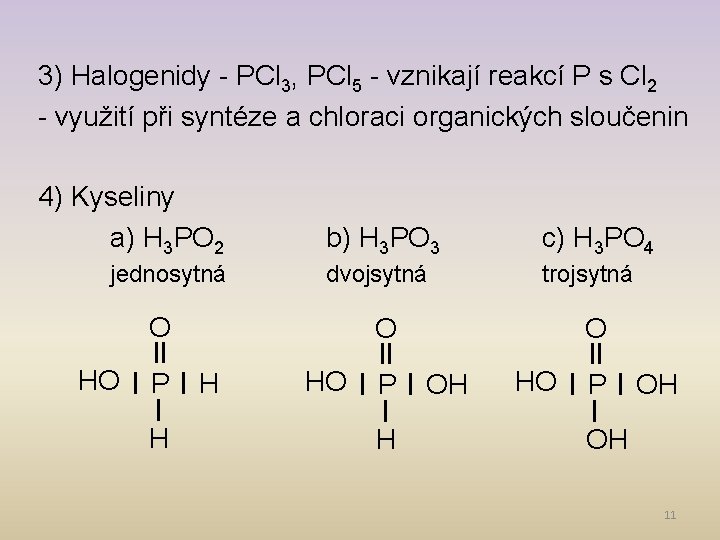
3) Halogenidy - PCl 3, PCl 5 - vznikají reakcí P s Cl 2 - využití při syntéze a chloraci organických sloučenin 4) Kyseliny a) H 3 PO 2 jednosytná b) H 3 PO 3 c) H 3 PO 4 dvojsytná trojsytná O HO P H O H HO P H O OH HO P OH OH 11

Kyselina trihydrogenfosforečná - středně silná, trojsytná, dobře rozpustná ve vodě - bezbarvá hmota, nejedovatá - v laboratoři se používá 85% - technická se vyrábí z apatitů - pro potravinářské účely se vyrábí oxidací fosforu a zaváděním vzniklého oxidu do vody - využití: součást kypřících prášků, zubních past, pracích prášků (snižuje tvrdost vody) - tvoří 3 řady solí – např. Na 2 HPO 4 a Na. H 2 PO 4 se využívají jako pufry 12

(2) 13
![Zdroje (1) Steinberg, Peter. 2005. commons. wikimedia. org. wikimedia commons. [Online] 5 2005. [Citace: Zdroje (1) Steinberg, Peter. 2005. commons. wikimedia. org. wikimedia commons. [Online] 5 2005. [Citace:](http://slidetodoc.com/presentation_image/26a3b6c5c875d933ba658f35c233465a/image-14.jpg)
Zdroje (1) Steinberg, Peter. 2005. commons. wikimedia. org. wikimedia commons. [Online] 5 2005. [Citace: 10. 10 2013. ] https: //es. m. wikipedia. org/wiki/Archivo: 120 px. Tetrahedron-slowturn. gif. (2) Hough, Cody. 2008. commons. wikimedia. org. wikimedia commons. [Online] 19. 6 2008. [Citace: 10. 10 2013. ] http: //commons. wikimedia. org/wiki/File: Russian_Coca-cola_. JPG. Vyhledavač neziskové organizace Creative Commons, která na internetu vyhledává a označí ty obrázky, fotografie a další zdroje, u kterých dal autor souhlas s jejich bezplatným využitím nebo u kterých již platnost autorských práv vypršela. Iniciativa Creative Commons v globálním měřítku garantuje, že je dané dílo volně k dispozici. 14
- Slides: 14