Gygyszerinterakcik a reumatolgiban Szekeres Lszl dr Hvzgygyfrd s

Gyógyszerinterakciók a reumatológiában Szekeres László dr. Hévízgyógyfürdő és Szent András Reumakórház Kht. Hévíz www. spaheviz. hu

A gyógyszer-interakciók farmakokinetikai – az egyik gyógyszer a vele egyidőben alkalmazott másik gyógyszer felszívódását, szervezeten belüli megoszlását, kiválasztódását megváltoztatja farmakodinamias – a gyógyszerek egyidejűleg alkalmazott hatása (vagy akár mellékhatása) lehet egyirányú (egymást erősítő), vagy gyengítheti egymást (kinetika befolyásolása nélkül)


„Speciálisan reumatológia gyógyszeres terápia” (gyakorlati szemszögből) Analgetikumok NSAID – coxib Izomrelaxánsok (centrális, perifériás) SYSADOA (symptomatic slow acting drugs in osteo-arthritis) DMARD (disease modifying antirheumatic drugs; goldstandard: MTX) Biológiai terápia (anti TNFalfa, anti IL 6 --- RA, SPA, Ps. A) Osteoporosis ellenes gyógyszeres terápia (first-line: bisphonat) Biológiai terápia… (osteoporosis, anyagcsere betegségek…) Adjuváns terápia (anxiolitikumok, antidepresszánsok, stb. ) …

NSAID jellemzői PG gátlás – COX-enzim inhibíció Bioaviability 20 -40% Májban zajló metabolizmus útja (főleg) CYP 2 C 9 Eliminációs fél-életidő 5 -11 h Magas protein-kötődés >90% GI/CV mellékhatások aránya „kedvezőtlen”

NSAID’s felszívódás: – gyomor p. H változása szervezeten belüli megoszlás - metabolizmus: – szérum fehérjéhez kötődés (albumin) ill. metabolikus enzim citokróm P 450 indukció, illetve kompetitív antagonizmus kettőssége kiválasztás (vese): – időskorban, vesebetegségben glomerularis filtráció (GFR <60!!) – probenecid aktív tubularis szekréciót – vizelet p. H eltolódása esetén passzív tubularis reabszorpció

NSAID’s Antihypertensiv szerek: -blokkoló, diuretikum, ACE-gátló PGE 2 szintézisének hiányában az antihypertensiv th. ellenregulációja hiányzik tenzió emelkedés, só-, víz retenció alakul ki. Érdemi különbség nélkül a coxibokhoz képest!! Oralis anitcoagulánsok (kumarin származékok) TXA 2 -, citokróm P 450 - és fehérje-kötődés útján

NSAID’s Sulphanylurea antidiabetikumok májban zajló metabolizmus ; fehérje-kötésről leszorít hypoglycaemia – adjunk: diclofenac, ibiprofen MTX csak nagy dózis (nem reumatológiában alkalmazott mennyiségben!!) esetén vesén keresztül kiválasztása Diphedan fehérjéről leszorít; máj metabolizmusát csökkenti Lithium, Digoxin, Aminoglycosid antibiotikumok vesén keresztül zajló kiválasztását Antiepileptikum metabolizmusa és albuminhoz kötődése (csak ASS)

NSAID’s Antacida aluminiumsó , bikarbonat tartalmú a felszívódást H 2 -antagonsita savi p. H Barbiturat citokróm P 450 enzim indukció gyorsabb NSAID metabolizmus (indomethacin) NSAID’s Csak adverz hatások: többszörösére emelkednek!

NSAID ismert veszélyei Felső GI mellékhatás gyakoriságának emelkedése (RR=2. 8 -4. 1)* További mellékhatások Kir. (fejfájás, szédülés, tinnitus, kábultság) Allergiás bőrkiütés Bronchospasmus Nephrotoxikus Hepatotoxikus Víz-, sóretenció (ödéma) Vérképzőszervi (agranulocytosis, leukopénia) – vérzékenység! Porckárosodás *Cochrane Collab. D. Henry et al. 2005

Mellékhatások-rizikók (felső-GI) Nagy számban alkalmazott gyógyszer – (abszolút értelemben is) több mellékhatás Összes ulcus-betegség hátterében 15 -35%-ban NSAID (USA-ban 41 ezer hospitalizáció/év)1 Peptikus fekély eseteiben 35, 3%-ban trad. NSAID adása előzte meg 2 Felső GI mellékhatás NSAID terápia mellett RR=3, 66 Co-morbiditás, co-medicatio, mindez időskorban HP infectio (!!) >65 év felett a mellékhatások gyakorisága és súlyossága szorosan korrelál 3 +anticoagulans 12 x 4 +kortikoszteroid (>10 mg prednisolon) 7 x 5 +ASA RR=8. 26 1 G Singh et al. Am J Med, 1998; 2 QRESEARCH database – J Hippisley-Cox et al. BMJ, 2005; 3 DJ Collier et al. Gut, 1985 4 JM Pipper et al. Ann Intern Med, 1991; 5 RI Shorr et al. Arch Intern Med, 1993; 6 LAG Rodríguez et al. Arthritis Res, 2001


Kétféle (? ) cyclooxigenáz izoenzim létezik (1991) COX- 1 izoenzim COX-2 izoenzim Konstitutív minden szövetben bizonyos állandó szinten van jelen élettani funkciók: gyomor, vese, thrombocyták ingere: hormon- és mediátorhatások Indukálható élettani funkció: remisszió, restitúció Ingere: bakteriális toxin, cytokinek, hisztamin, kininek a gyulladás helyén gyorsan felszabadul szintje 100 -szorosára nőhet Mennyisége gyorsan 2 -4 -szeresére nő
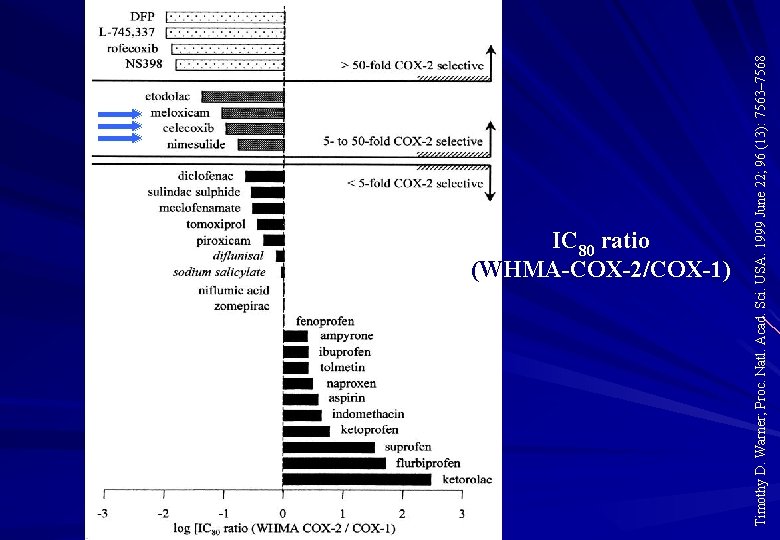
Timothy D. Warner; Proc. Natl. Acad. Sci. USA. 1999 June 22; 96 (13): 7563– 7568 IC 80 ratio (WHMA-COX-2/COX-1)

Coxib (etoricoxib) jellemzői P. Patrignani et al. 2008

Coxib (etoricoxib) jellemzői Grapefruit! CYP 3 A 4 gátlás toxikus mh!! P. Patrignani et al. 2008

Coxib (etoricoxib) jellemzői Bioaviability 100% (ellentétben minden mással; 2040%) Májban zajló metabolizmus útja (főleg) CYP 3 A 4 (ellentétben minden mással; CYP 2 C 9) Eliminációs fél-életidő 22 h (ellentétben minden mással; 5 -11 h) GI/CV mellékhatások aránya a legkedvezőbb (ellentétben minden mással) Magas protein-kötődés (megegyezően minden mással; >90%)

GI tolerálhatósági profil GI biopsziás vizsgálat etoricoxibbal: Átlagos gasztrikus PGE 2 -szintézis (pg/mg/perc) A gasztroprotektív PGE 2 szintézisére gyakorolt hatás 100 p<0. 001 p=NS 90 80 78, 01 72, 60 72. 60 71, 03 71. 03 Placebo Etoricoxib napi 1× 120 mg 70 60 50 40 30 17, 02 20 10 0 Placebo Naproxen 1000 mg* (n=10) GI = gasztrointesztinális; PGE 2 = prosztaglandin E 2; NS = nem szignifikáns *Napi 2× 500 mg Átvéve: Dallob A et al J Clin Pharmacol 2003; 43: 573– 585. (n=27) 5. nap

GI tolerálhatósági profil Etoricoxib vs. naproxen/ibuprofen endoszkópos vizsgálatok: gasztroduodenális eróziók 100 RA vagy OA 12 hetes kumulatív incidencia (%)a 90 80 71. 97 70 80 70 60 60 50 50 40 40 30 23. 22 b 30 22. 69 b 20 20 10 10 0 Placébó (n=229) Etoricoxib 120 mg (n=236) OA 90 Naproxen 1000 mgc (n=235) 0 58. 31 19. 69 b 17. 38 b Placébó (n=221) Etoricoxib 120 mg (n=216) Ibuprofen 2400 mgd (n=218) Az élettáblázatos elemzés szerinti kumulatív incidencia nem feltétlenül egyenlő az esményszám/n × 100 kalkuláció eredményével; bp<0, 001 placebo és etoricoxib vs. naproxen vagy ibuprofen; c. Napi 2× 500 mg; d. Napi 3× 800 mg

Egy farmakokinetikai példa a szisztolés nyomás ~3, 5 Hgmm emelkedés diclofenac csoporthoz viszonyítva (MEDAL) NSAID és COX-2 gátló hatása hypertónia miatt kezelt betegeknél WB. White et al. Hypertension, 2007

Coxib (etoricoxib) versus warfarin metabolizmusa warfarin CYP 2 C 9 P. Patrignani et al. 2008

Coxib (etoricoxib) COX 1 gátlása (TXA 2) P. Patrignani et al. 2008
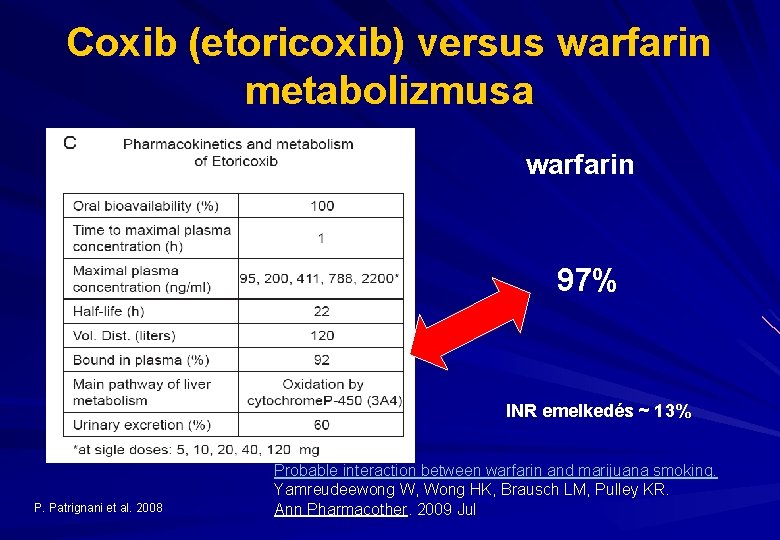
Coxib (etoricoxib) versus warfarin metabolizmusa warfarin 97% INR emelkedés ~ 13% P. Patrignani et al. 2008 Probable interaction between warfarin and marijuana smoking. Yamreudeewong W, Wong HK, Brausch LM, Pulley KR. Ann Pharmacother. 2009 Jul


MTX Az első választandó szerré válik az RA „bázis” terápiájában. A reumatológiában alkalmazott dózis (10 -15 mg/hét – 2 -4 hetente 5 mg-al emelhető, klinikai max. dózis: 30 mg/hét*) nem cytotoxikus tulajdonságú. Előnyei: – – egyszerű alkalmazás (heti 1 x – adherencia javulása) megbízható effektivitás (16 979 referencia)* kedvező mellékhatás profil kombinációs lehetőség (pl. sulfosalazinnal, „kötelezően” biológiai terápia – anti. TNFalfa – mellett) *K. Visser et al. ARD On Line 2008, Nov

MTX Leggyakoribb mellékhatásai (kb. 10%-os) a kezelés első 6 hónapjában jelentkeznek, ezek között 2. 5%-ban közepesen súlyos, illetve súlyos jellegű. Interakció: (részben) fólsav-antagonizmusból adódik bőr-, nyálkahártya (stomatitis erythaemaval, fájdalmas ulcus, erózió stb. - alopecia, erythaema, urticaria, cutan vasculitis) gastrointestinalis leg… hepatotoxicitás: fibrosis, cirrhosis! haemtológiai (-cytopenia) - mh. addikció: probenecid, sulfonamid kir. (fejfájás, depresszió, gyengeség, hangulati zavarok stb. ) fertilis korban veszély: oligospermia, abortív hatás (teratogén)

MTX Mindennapos kérdés: mellékhatás prevenció érdekében (esetünkben gyulladáscsökkentő dózis mellett) adjunk-e fólsavat? Ha igen: alteráló napokon, a MTX adásától 24 -48 órás különbséggel! (min. 5 mg fólsav/hét*) Ha nem: vállaljuk a lehetséges, de nem kötelező mellékhatásokat (cost/benefit) kötelesek vagyunk: szabályos időszakonként kontrollálni! *K. Visser et al. ARD On Line 2008, Nov


Bisphonatok a „valódi” kölcsönhatás és interakció „Bár szabályszerű interakciós vizsgálatokat nem végeztek, a klinikai vizsgálatokban számos különböző, gyakran rendelt gyógyszerrel együtt alkalmazták az alendronátot és nem észleltek klinikai szempontból kedvezőtlen kölcsönhatásokat. ” „Nem végeztek külön interakciós vizsgálatokat, de a klinikai vizsgálatok során nem észleltek klinikai szempontból jelentős gyógyszerkölcsönhatást. ” (RIS)

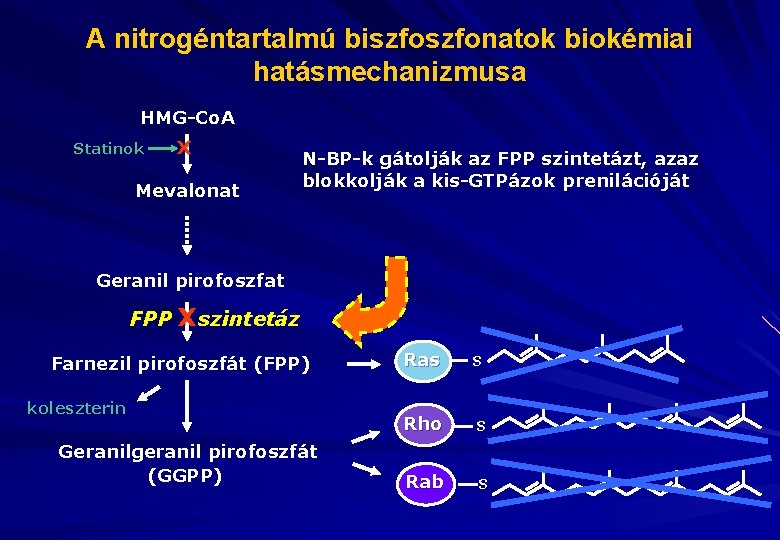
A nitrogéntartalmú biszfonatok biokémiai hatásmechanizmusa HMG-Co. A Statinok X Mevalonat N-BP-k gátolják az FPP szintetázt, azaz blokkolják a kis-GTPázok prenilációját Geranil pirofoszfat FPP X szintetáz Farnezil pirofoszfát (FPP) koleszterin Geranilgeranil pirofoszfát (GGPP) Ras S Rho S Rab S

Logikailag a bisphonatok és a statinok együttes alkalmazása egymást hatását csökkentik? Vagy épp fordítva (!) – a BSP antiresorptiv hatása statinok adása mellett fokozódik. risedronate + atorvastatin együtt lumbalis BMD emelkedést 6 hónap alatt szign. nagyobb mértékben eredményezett mint risedronate egyedül (1, 58% versus 0, 75%; p<0, 05) és LDL és teljes cholesterol szint-változásban is kedvező együtt-hatás volt mérhető* *HA. Tanriverdi et al. Eur J Obstet Gynecol Reprod Biol, 2005

Az alendronat-Na Orális adását követően abszorpció 0, 5 -1%-os (<1%) vs parenteralis BP’s Igen magas csont specificitása miatt kb. 50%-a csont felszín remodeling helyeihez kötődik - az új csontformáció során további 50%-a vizeleten keresztül eliminálódik. A csontszövetből mindössze kb. 1/3 -a igen lassan disszociálódik vissza a szérumba. A csont felszinén a fél-életideje (~ 5 hét) Az adagolás közötti idő minden esetben rövidebb, mint a resorptio (idő)tartama (minden BRU-ban). Az ALN a szervezetben nem metabolizálódik.

A risedronat-Na A maximális szérum koncentráció 5 mg-nál 0. 94 ng/ml; 30 mg-nál 5. 1 ng/ml (dózissal egyenesen arányos) A maximális szérum koncentráció – dózistól függetlenül < 1 óra Plazma felezési idő kb. 2 óra – igen rövid: nagyon nagy csont affinitás! Antireszorptív aktivitás (a csontban) hetek alatt alakul ki A gyógyszer-hatóanyag a lassú felezési idejű csontkompartement felé tolódik el – a risedronat T½ csontban (30 mg) > 220 óra… Clearence állandó (dózistól független)

ALN mellékhatás-profil FOSIT vizsgálat során felső GI mellékhatás: 20, 8% 10 éves kezelés során (8 -10. évben) 27. 9%, de ebből súlyos 0%, kezelés felfüggesztése 2. 3%-os volt 1 De!2 – – a gyógyszerbevételét megelőzően 2 órával étkezett: 10% 30 percnél rövidebb időn belül étkezett: 11, 6% nem „sima” vízzel történt a bevétel: 4% más gyógyszerrel együtt vette be: 18, 4% („nagy study”-k során nagyobb odafigyelés miatt a számok mások!) 1. H. G. Bone et al. N Engl J Med, 2004 2. Semih A. et al. Yonsei Med J, 2003
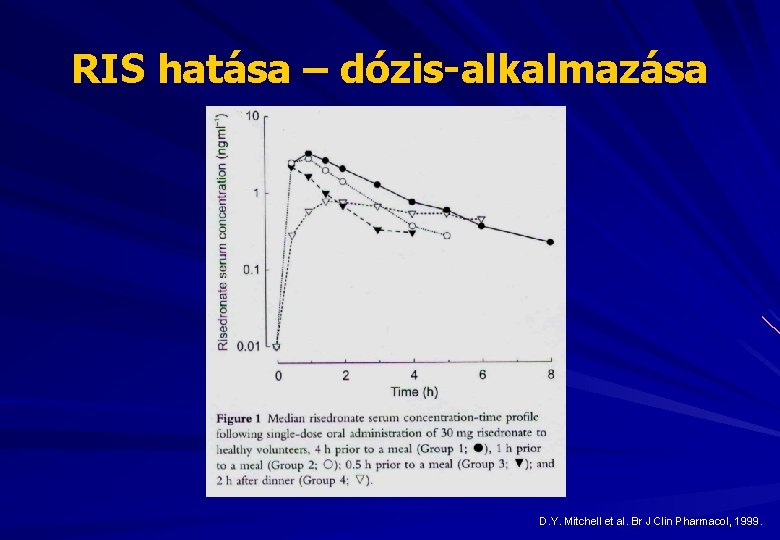
RIS hatása – dózis-alkalmazása D. Y. Mitchell et al. Br J Clin Pharmacol, 1999.

Co-medicatio és az alendronate mellékhatás-profil Simaizom relaxáns hatás ca-antagonsita, nitrát, nicotin, theophyllin, antimuscarin hatású szerek… Lokális toxicitás ALN, antibiotikum (tetracyclin, clindamycin), NSAID’s, kálium-, vaskészítmények Diagnosztika: egyedül gastroscopia értékelhető Prevencióra alkalmas: PPI, H 2 receptor blokkolók (double dose) – de hatását ez csökkenti (hyp-, anaciditas)!! Semih A. et al. Yonsei Med J Aug 2003 Petersen KU et al. Expert Opin Drug Saf Sept 2003

Az alendronat és naproxen GI mellékhatásának összegződése Endoszkópos gyomorfekély (%) 50 40 30 20 10 0 Alendronat Naproxen ALE+Naproxen Graham DY. Et al. Arch Intern Med 2001. 161: 107 -110.
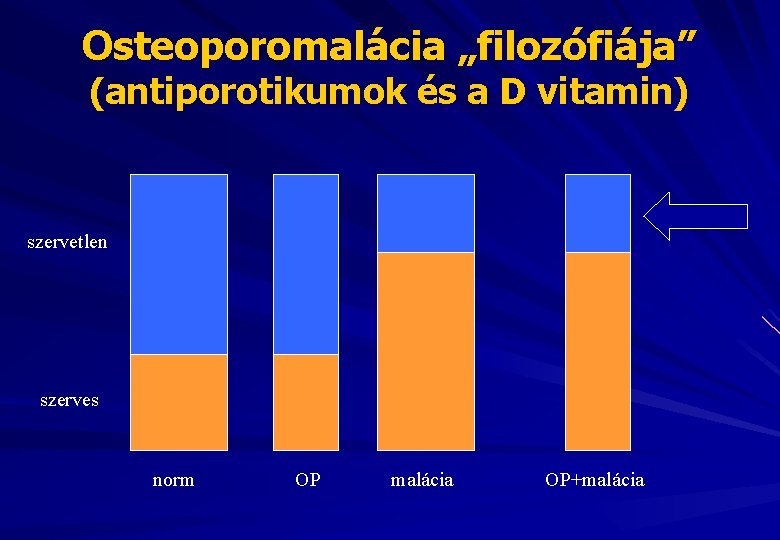
Osteoporomalácia „filozófiája” (antiporotikumok és a D vitamin) szervetlen szerves norm OP malácia OP+malácia

- Slides: 40