GUA Estrutura Abaixo est representado o envoltrio de

ÁGUA
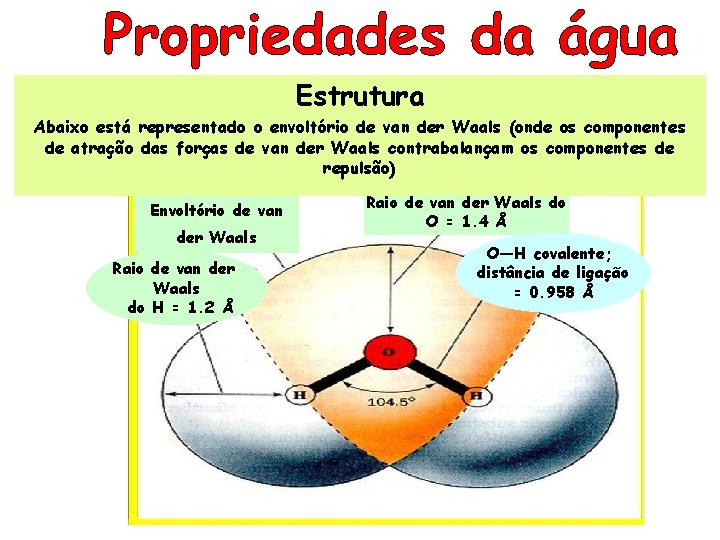
Estrutura Abaixo está representado o envoltório de van der Waals (onde os componentes de atração das forças de van der Waals contrabalançam os componentes de repulsão) Envoltório de van der Waals Raio de van der Waals do H = 1. 2 Å Raio de van der Waals do O = 1. 4 Å O—H covalente; distância de ligação = 0. 958 Å
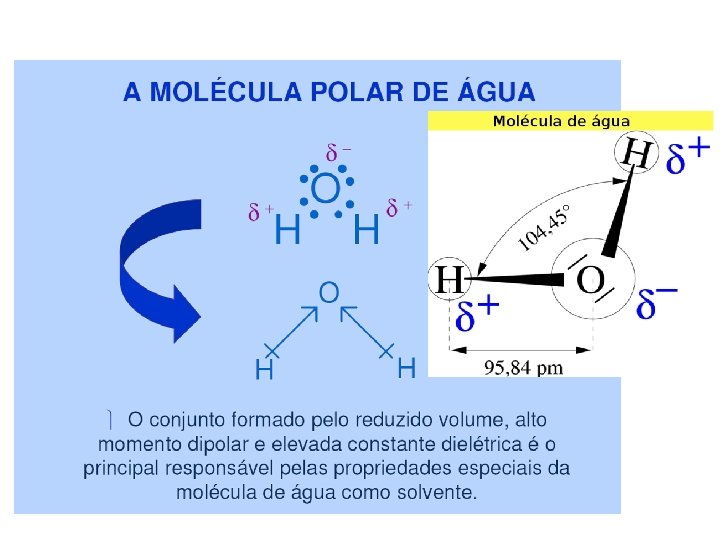
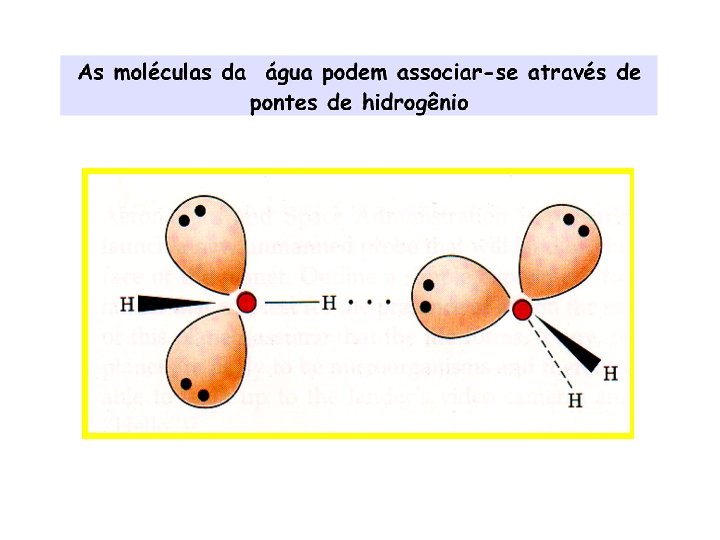
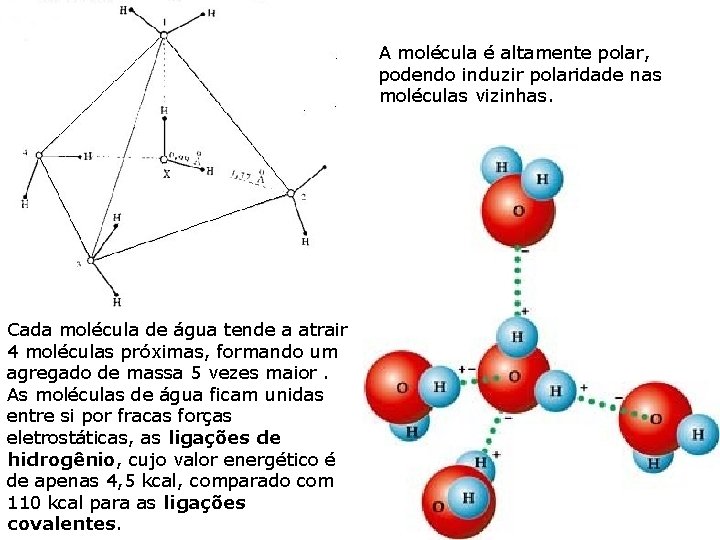
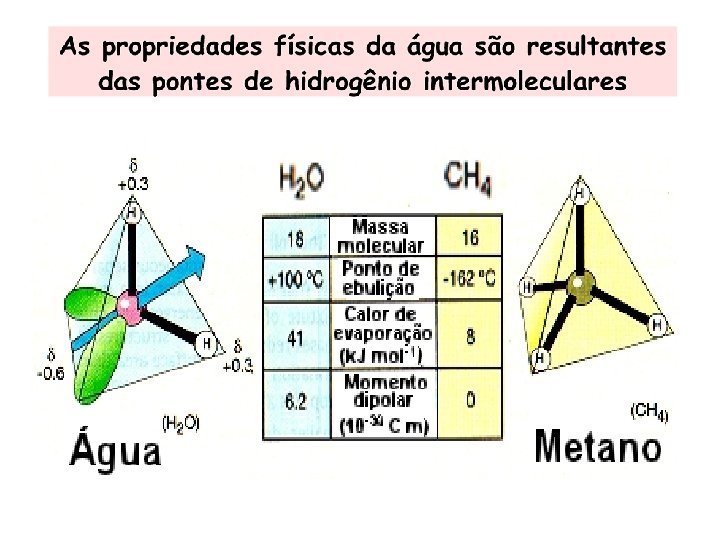
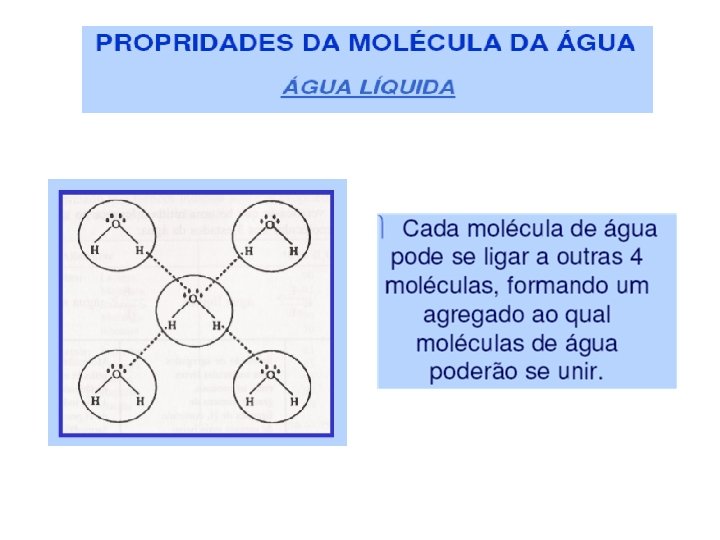
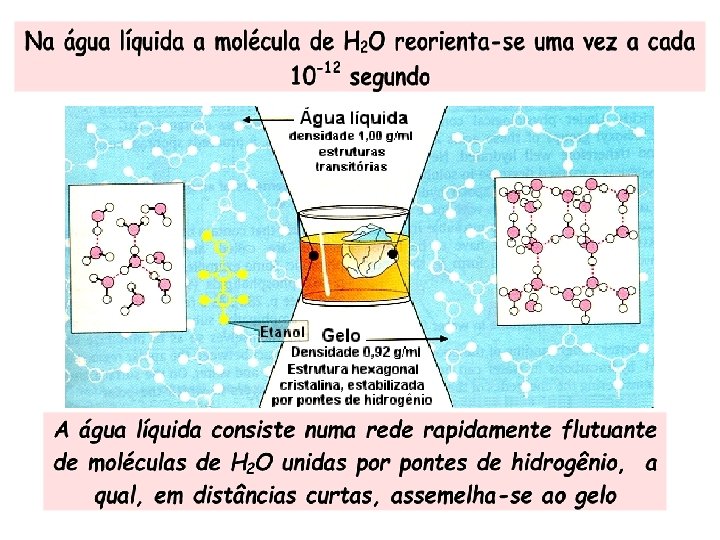
A molécula é altamente polar, podendo induzir polaridade nas moléculas vizinhas. Cada molécula de água tende a atrair 4 moléculas próximas, formando um agregado de massa 5 vezes maior. As moléculas de água ficam unidas entre si por fracas forças eletrostáticas, as ligações de hidrogênio, cujo valor energético é de apenas 4, 5 kcal, comparado com 110 kcal para as ligações covalentes.



Por quê a água dissolve sais? A estrutura cristalina dos sais é mantida por forças iônicas;
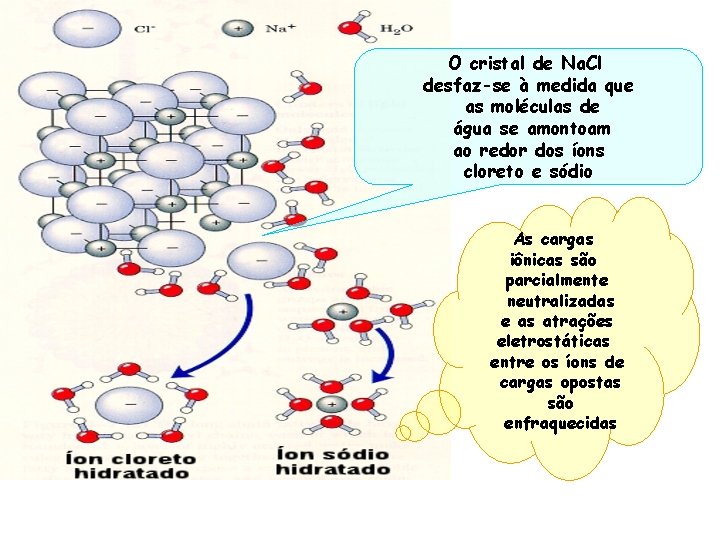
O cristal de Na. Cl desfaz-se à medida que as moléculas de água se amontoam ao redor dos íons cloreto e sódio As cargas iônicas são parcialmente neutralizadas e as atrações eletrostáticas entre os íons de cargas opostas são enfraquecidas
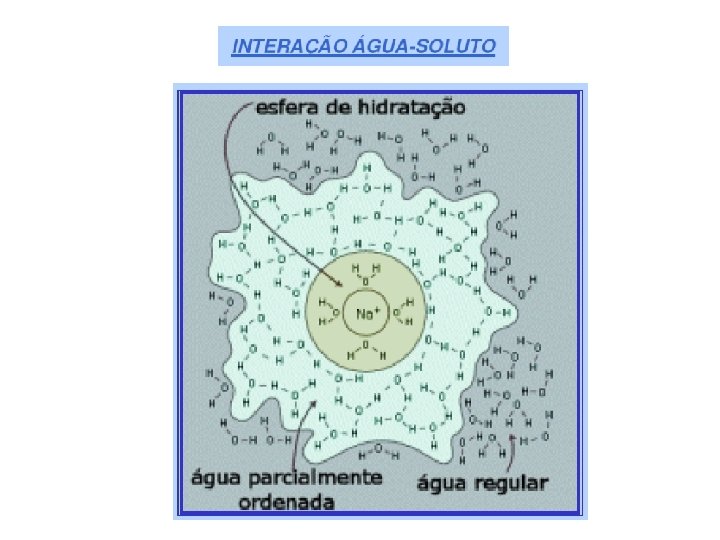
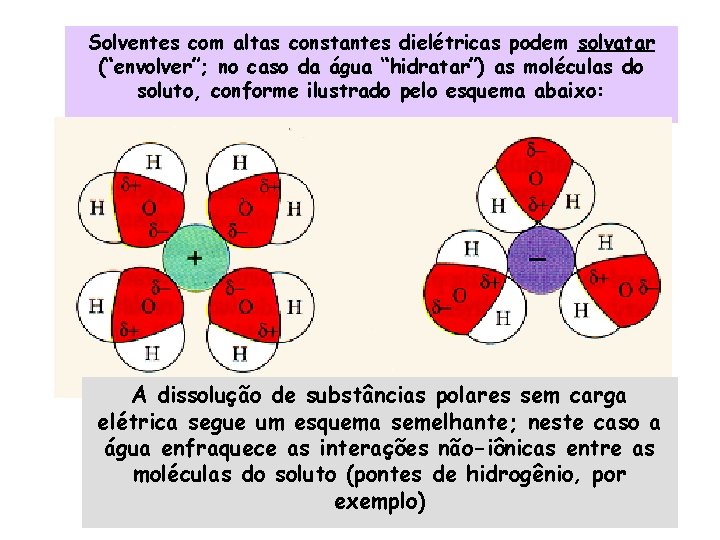
Solventes com altas constantes dielétricas podem solvatar (“envolver”; no caso da água “hidratar”) as moléculas do soluto, conforme ilustrado pelo esquema abaixo: A dissolução de substâncias polares sem carga elétrica segue um esquema semelhante; neste caso a água enfraquece as interações não-iônicas entre as moléculas do soluto (pontes de hidrogênio, por exemplo)

O sólido iônico, ao se dissolver em água, se quebra em pequenas unidades: cátions (íons de carga positiva) e ânios (íons de carga negativa). A equação química é a forma com que o processo é representado; no exemplo, a dissolução do cloreto de sódio (sal de cozinha) em água. NA HIDRATAÇÃO Na. Cl (s) Na + (aq) e Cl- (aq). O número de moléculas de água imediatamente próximas depende do tamanho e carga do cátion.

Etanol Þ 24, 3 Amônia Þ 16, 9 Acetona Þ 20, 7 Clorofórmio Þ 4, 8 Éter dietílico Þ 4, 3 Benzeno Þ 2, 3 Tetracloreto de carbonoÞ 2, 2 Hexano Þ 1, 9

A solubilidade dos gases em água é um bom exemplo do papel da polaridade
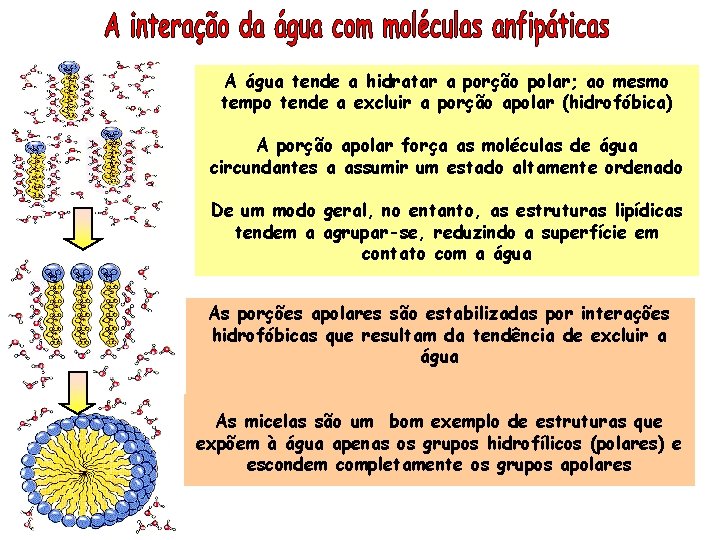
A água tende a hidratar a porção polar; ao mesmo tempo tende a excluir a porção apolar (hidrofóbica) A porção apolar força as moléculas de água circundantes a assumir um estado altamente ordenado De um modo geral, no entanto, as estruturas lipídicas tendem a agrupar-se, reduzindo a superfície em contato com a água As porções apolares são estabilizadas por interações hidrofóbicas que resultam da tendência de excluir a água As micelas são um bom exemplo de estruturas que expõem à água apenas os grupos hidrofílicos (polares) e escondem completamente os grupos apolares

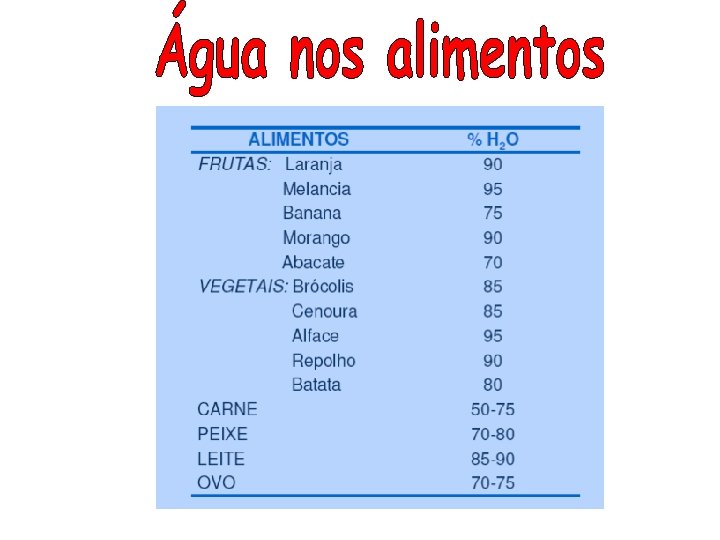
O conteúdo determinação alimento. de água é obtido pela da água total contida no Entretanto, esse valor não nos fornece indicações de como está distribuída a água nesse alimento, como também não permite saber se toda a água está ligada do mesmo modo ao alimento.

• Diferem significativamente em sua estabilidade ou vida útil. • O conteúdo de água por si mesmo não é um indicador real da estabilidade

A água fracamente ligada ao substrato, e que funciona como solvente, permitindo o crescimento dos microorganismos e reações químicas e que é eliminada com relativa facilidade. A água está fortemente ligada ao substrato, mais difícil de ser eliminada e que não é utilizada como solvente e não permite o desenvolvimento de microorganismos e retarda as reações químicas.
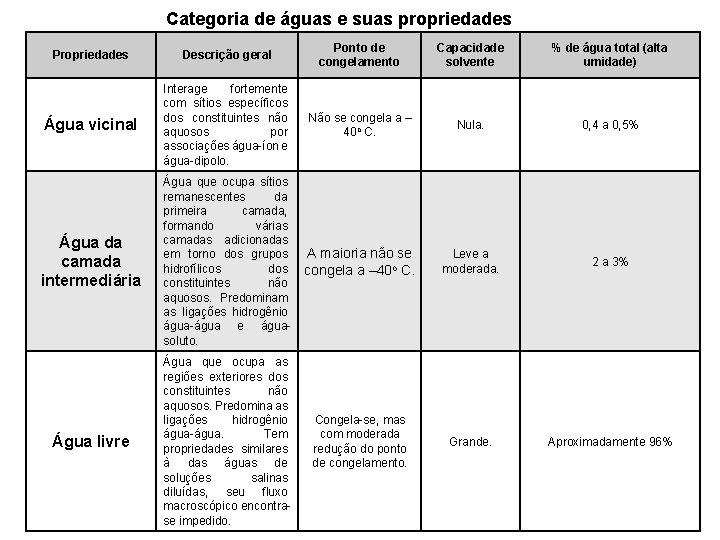
Categoria de águas e suas propriedades Propriedades Descrição geral Ponto de congelamento Capacidade solvente % de água total (alta umidade) Água vicinal Interage fortemente com sítios específicos dos constituintes não aquosos por associações água-íon e água-dipolo. Não se congela a – 40 o C. Nula. 0, 4 a 0, 5% Água da camada intermediária Água que ocupa sítios remanescentes da primeira camada, formando várias camadas adicionadas em torno dos grupos hidrofílicos dos constituintes não aquosos. Predominam as ligações hidrogênio água-água e águasoluto. A maioria não se congela a – 40 o C. Leve a moderada. 2 a 3% Água livre Água que ocupa as regiões exteriores dos constituintes não aquosos. Predomina as ligações hidrogênio água-água. Tem propriedades similares à das águas de soluções salinas diluídas, seu fluxo macroscópico encontrase impedido. Congela-se, mas com moderada redução do ponto de congelamento. Grande. Aproximadamente 96%

aw - Indica a intensidade das forças que unem a água com outros componentes não-aquosos e, conseqüentemente, a água disponível para o crescimento de microorganismos e para que se possam realizar diferentes reações químicas e bioquímicas.

• Diferenças na intensidade com que a água se associa com os constituintes não aquosos. • A água envolvida em associações mais fortes é menos suscetível ou propensa para as atividades de degradação (crescimento de microorganismos e reações químicas de hidrólise).

O termo atividade da água (aw) foi implantado para se ter o valor da intensidade com que a água se associa a diferentes componentes não aquosos. Quando se adiciona um soluto à água pura, as moléculas de água orientam-se na superfície do soluto e interrelacionam-se com ele. Como conseqüência, diminui o ponto de congelamento, aumenta o ponto de ebulição e reduz a pressão de vapor, segundo a lei de Raoult, que diz: “a diminuição relativa da pressão de vapor de um líquido ao dissolver-se em um soluto é igual “a fração molar do solvente”.

n n n Um líquido puro em contato com ar, perde (evapora) parte de suas moléculas = Fugacidade. Em ambiente fechado o que ocorre = condensação = pressão de vapor. Ao adicionar um soluto ao líquido a evaporação para a fase gasosa diminui = diminui a pressão de vapor.
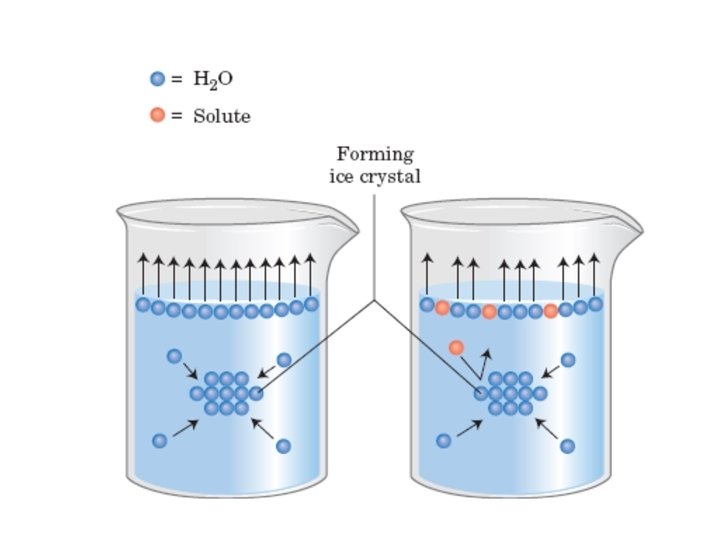

A atividade da água define-se como a relação existente entre a pressão de vapor de uma solução ou de um alimento (P) com relação à pressão de vapor da água pura (Po) à mesma temperatura.

Expressão matemática da Lei de Raoult:





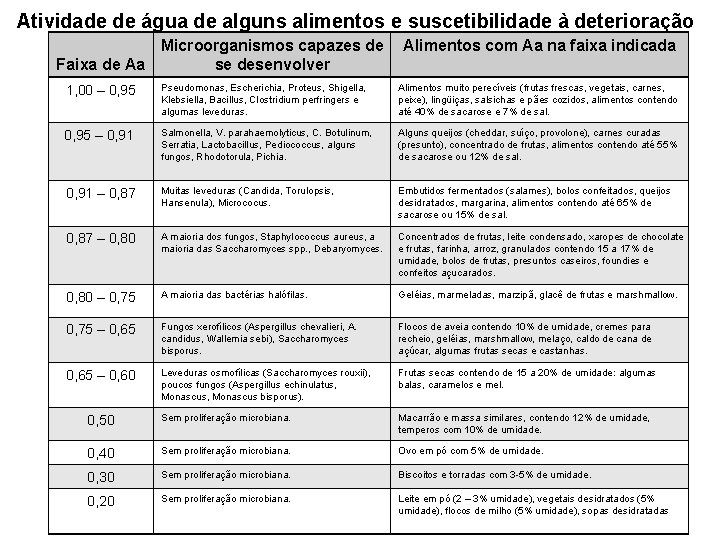
Atividade de água de alguns alimentos e suscetibilidade à deterioração Microorganismos capazes de Faixa de Aa se desenvolver Alimentos com Aa na faixa indicada 1, 00 – 0, 95 Pseudomonas, Escherichia, Proteus, Shigella, Klebsiella, Bacillus, Clostridium perfringers e algumas leveduras. Alimentos muito perecíveis (frutas frescas, vegetais, carnes, peixe), lingüiças, salsichas e pães cozidos, alimentos contendo até 40% de sacarose e 7% de sal. 0, 95 – 0, 91 Salmonella, V. parahaemolyticus, C. Botulinum, Serratia, Lactobacillus, Pediococcus, alguns fungos, Rhodotorula, Pichia. Alguns queijos (cheddar, suíço, provolone), carnes curadas (presunto), concentrado de frutas, alimentos contendo até 55% de sacarose ou 12% de sal. 0, 91 – 0, 87 Muitas leveduras (Candida, Torulopsis, Hansenula), Micrococus. Embutidos fermentados (salames), bolos confeitados, queijos desidratados, margarina, alimentos contendo até 65% de sacarose ou 15% de sal. 0, 87 – 0, 80 A maioria dos fungos, Staphylococcus aureus, a maioria das Saccharomyces spp. , Debaryomyces. Concentrados de frutas, leite condensado, xaropes de chocolate e frutas, farinha, arroz, granulados contendo 15 a 17% de umidade, bolos de frutas, presuntos caseiros, foundies e confeitos açucarados. 0, 80 – 0, 75 A maioria das bactérias halófilas. Geléias, marmeladas, marzipã, glacê de frutas e marshmallow. 0, 75 – 0, 65 Fungos xerofílicos (Aspergillus chevalieri, A. candidus, Wallemia sebi), Saccharomyces bisporus. Flocos de aveia contendo 10% de umidade, cremes para recheio, geléias, marshmallow, melaço, caldo de cana de açúcar, algumas frutas secas e castanhas. 0, 65 – 0, 60 Leveduras osmofílicas (Saccharomyces rouxii), poucos fungos (Aspergillus echinulatus, Monascus, Monascus bisporus). Frutas secas contendo de 15 a 20% de umidade: algumas balas, caramelos e mel. 0, 50 Sem proliferação microbiana. Macarrão e massa similares, contendo 12% de umidade, temperos com 10% de umidade. 0, 40 Sem proliferação microbiana. Ovo em pó com 5% de umidade. 0, 30 Sem proliferação microbiana. Biscoitos e torradas com 3 -5% de umidade. 0, 20 Sem proliferação microbiana. Leite em pó (2 – 3% umidade), vegetais desidratados (5% umidade), flocos de milho (5% umidade), sopas desidratadas



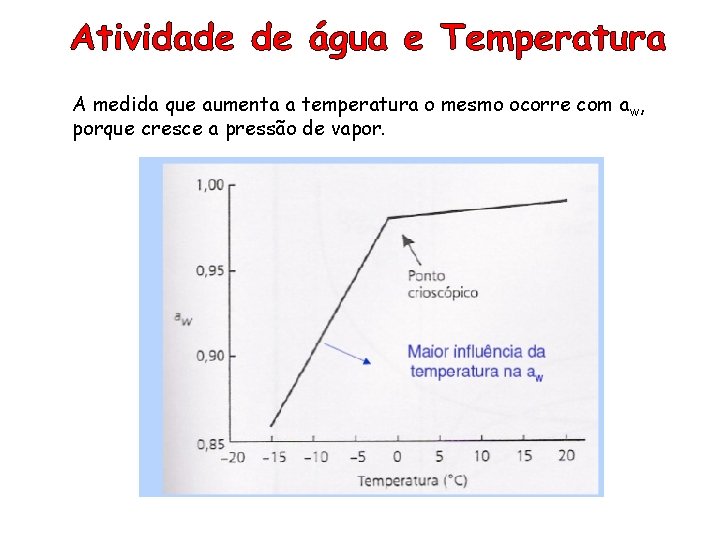
A medida que aumenta a temperatura o mesmo ocorre com a w, porque cresce a pressão de vapor.

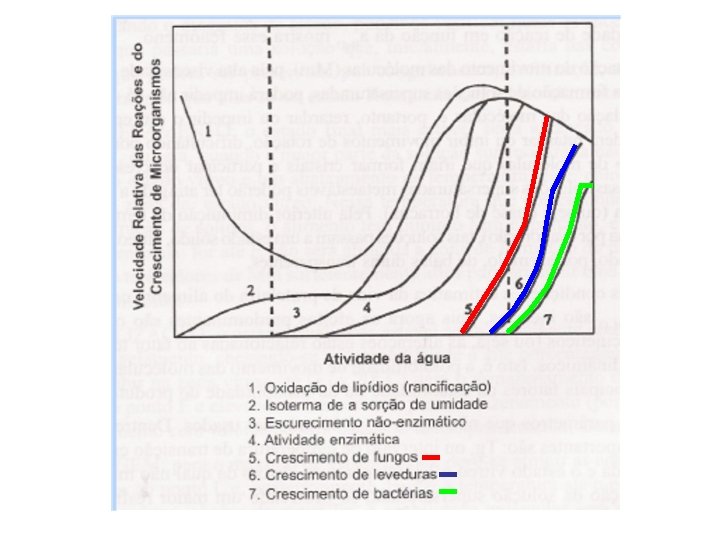
As isotermas de sorção de água são gráficos que relacionam a quantidade de água de um alimento com sua atividade de água, o que é o mesmo, em função da umidade relativa da atmosfera que circunda o alimento, uma vez alcançado o equilíbrio e a uma temperatura constante. A maioria das isotermas de sorção de água dos alimentos apresenta forma sigmóide, com pequenas variações conforme a estrutura física, a composição química, a temperatura e a capacidade de retenção de água do alimento. Há alimentos que apresentam uma zona mais plana na primeira parte da curva: essas curvas, em forma de J, são típicas de alimentos com grande quantidade de açúcar e solutos e que apresentam pouca adsorção por capilaridade, como as frutas e os doces de frutas.

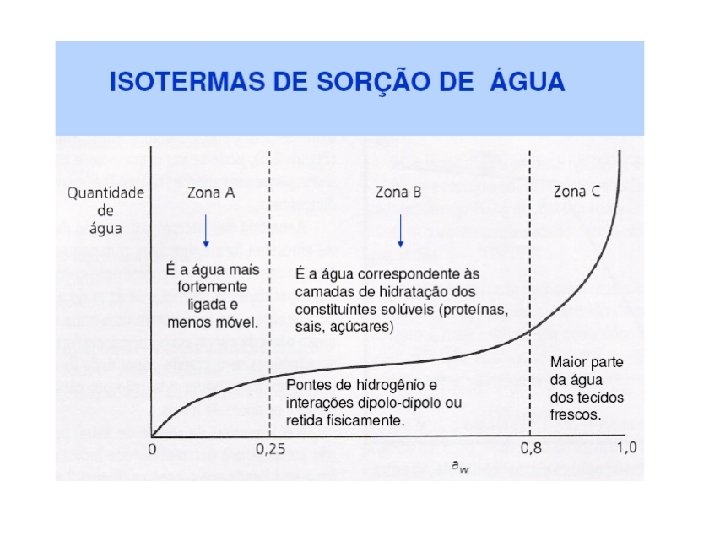


Quando se coloca o alimento em ambiente com umidade relativa (UR) superior à umidade relativa de seu equilíbrio (URE), ele fixa o vapor de água, tendendo a alcançar o equilíbrio, isto é, absorve água (adsorção). Ao contrário, se o alimento é colocado em um ambiente cuja UR é inferior URE correspondente ao conteúdo de água do produto, este cede água mediante o processo chamado dessorção.
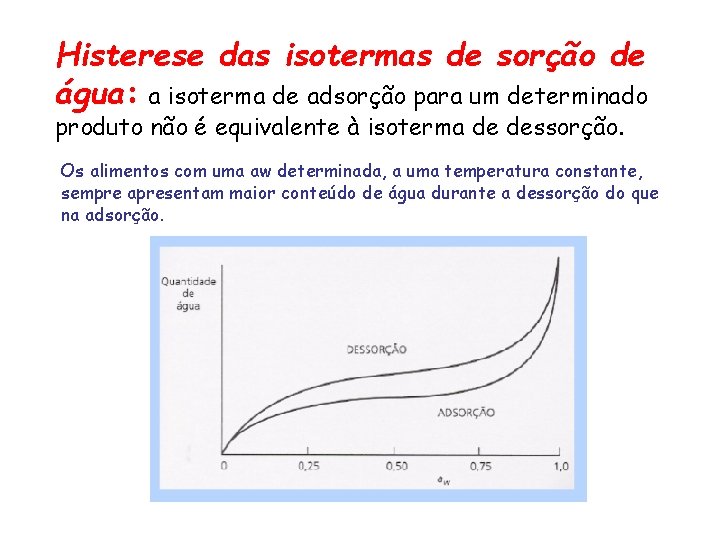
Histerese das isotermas de sorção de água: a isoterma de adsorção para um determinado produto não é equivalente à isoterma de dessorção. Os alimentos com uma aw determinada, a uma temperatura constante, sempre apresentam maior conteúdo de água durante a dessorção do que na adsorção.

Equipamento para medir AW

Equipamento para medir AW
- Slides: 51