Gruppi funzionali Residuo organico idrocarbonico Legami CC e

Gruppi funzionali Residuo organico (idrocarbonico) Legami C-C e C-H Gruppo funzionale §Eteroatomi e/o legami C=C e C=O. Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E’ la parte reattiva della molecola Fondamenti di chimica organica Janice Gorzynski Smith Copyright © 2009 – The Mc. Graw-Hill Companies srl
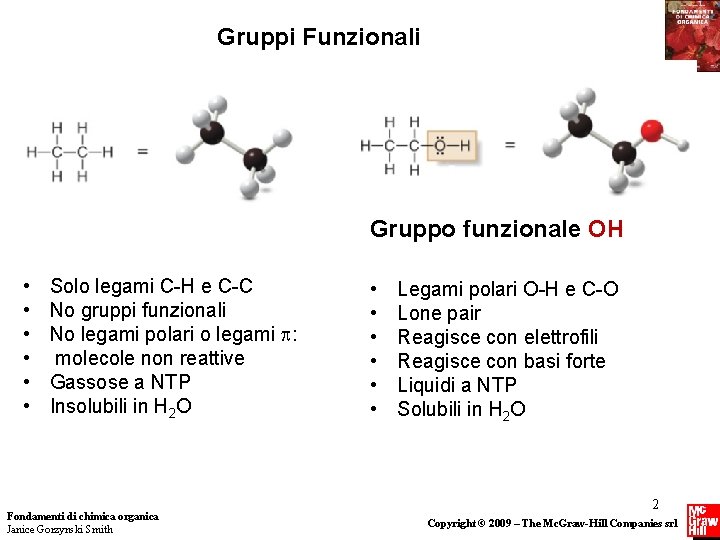
Gruppi Funzionali Gruppo funzionale OH • • • Solo legami C-H e C-C No gruppi funzionali No legami polari o legami p: molecole non reattive Gassose a NTP Insolubili in H 2 O Fondamenti di chimica organica Janice Gorzynski Smith • • • Legami polari O-H e C-O Lone pair Reagisce con elettrofili Reagisce con basi forte Liquidi a NTP Solubili in H 2 O 2 Copyright © 2009 – The Mc. Graw-Hill Companies srl
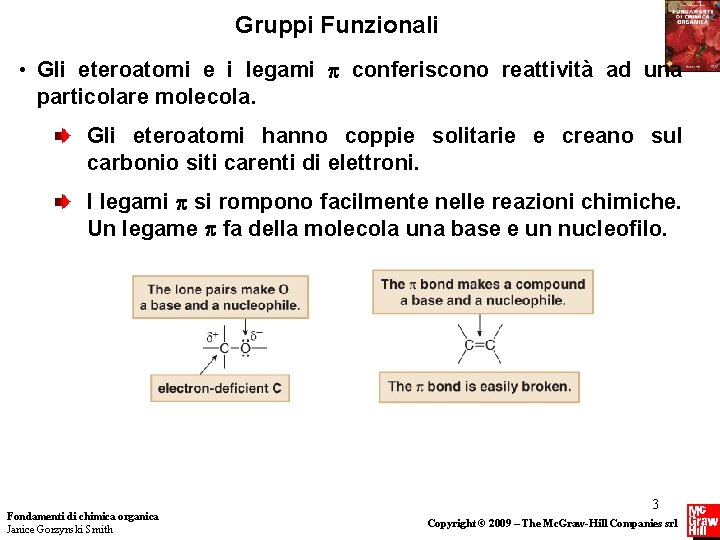
Gruppi Funzionali • Gli eteroatomi e i legami conferiscono reattività ad una particolare molecola. Gli eteroatomi hanno coppie solitarie e creano sul carbonio siti carenti di elettroni. I legami si rompono facilmente nelle reazioni chimiche. Un legame fa della molecola una base e un nucleofilo. Fondamenti di chimica organica Janice Gorzynski Smith 3 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Gruppi Funzionali 1. Definiscono una classe di composti -Composti che appartengono alla stessa classe Hanno simili proprietà e reattività. 2. Sono spesso i siti di reazione - Definiscono la reattività di una molecola 3. Determinano il nome - Es. tutti i chetoni hanno suffisso –one: acetone ciclopropanone cortisone Fondamenti di chimica organica Janice Gorzynski Smith 4 Copyright © 2009 – The Mc. Graw-Hill Companies srl
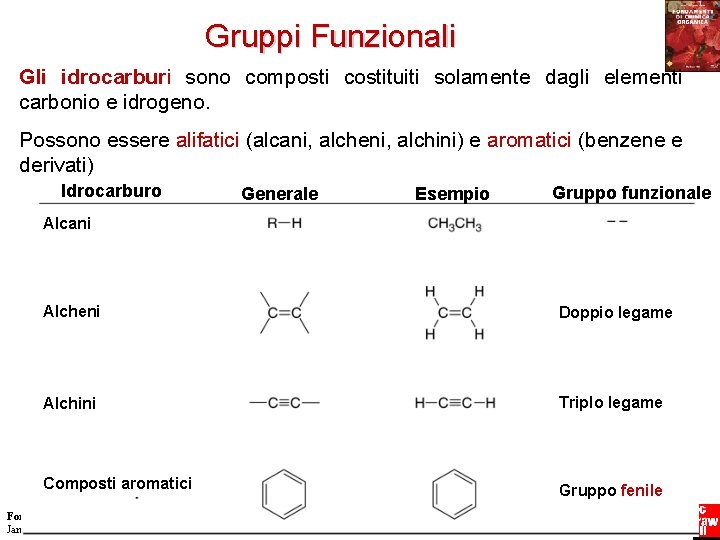
Gruppi Funzionali Gli idrocarburi sono composti costituiti solamente dagli elementi carbonio e idrogeno. Possono essere alifatici (alcani, alcheni, alchini) e aromatici (benzene e derivati) Idrocarburo Generale Esempio Gruppo funzionale Alcani Alcheni Doppio legame Alchini Triplo legame Composti aromatici Gruppo fenile Fondamenti di chimica organica Janice Gorzynski Smith 5 Copyright © 2009 – The Mc. Graw-Hill Companies srl
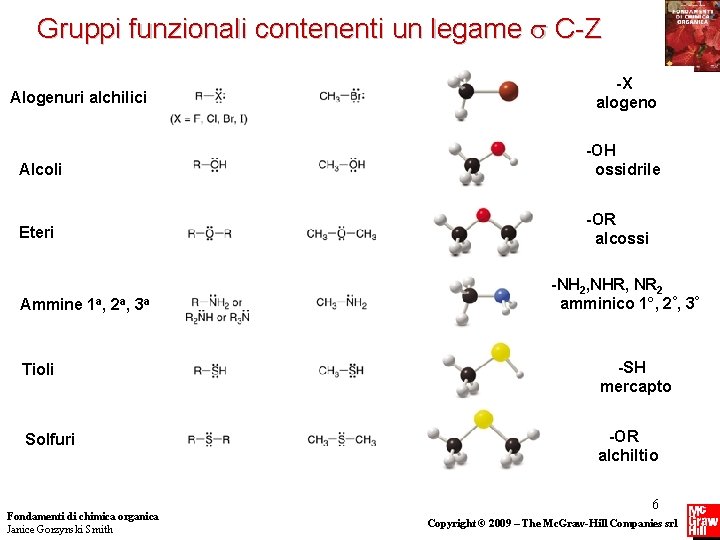
Gruppi funzionali contenenti un legame s C-Z Alogenuri alchilici -X alogeno Alcoli -OH ossidrile Eteri -OR alcossi Ammine 1 a, 2 a, 3 a -NH 2, NHR, NR 2 amminico 1°, 2°, 3° Tioli -SH mercapto Solfuri -OR alchiltio Fondamenti di chimica organica Janice Gorzynski Smith 6 Copyright © 2009 – The Mc. Graw-Hill Companies srl
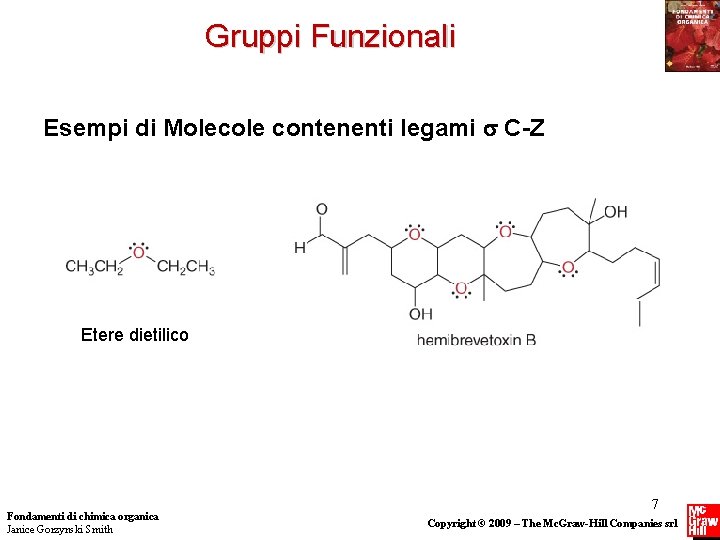
Gruppi Funzionali Esempi di Molecole contenenti legami C-Z Etere dietilico Fondamenti di chimica organica Janice Gorzynski Smith 7 Copyright © 2009 – The Mc. Graw-Hill Companies srl
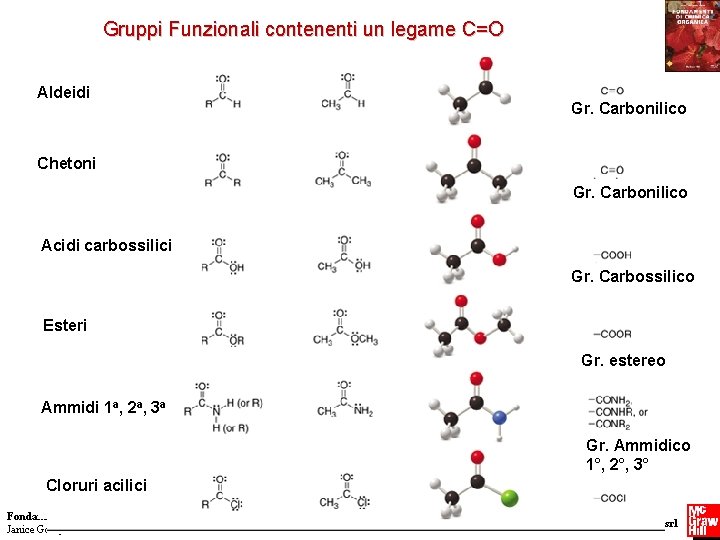
Gruppi Funzionali contenenti un legame C=O Aldeidi Gr. Carbonilico Chetoni Gr. Carbonilico Acidi carbossilici Gr. Carbossilico Esteri Gr. estereo Ammidi 1 a, 2 a, 3 a Gr. Ammidico 1°, 2°, 3° Cloruri acilici Fondamenti di chimica organica Janice Gorzynski Smith 8 Copyright © 2009 – The Mc. Graw-Hill Companies srl
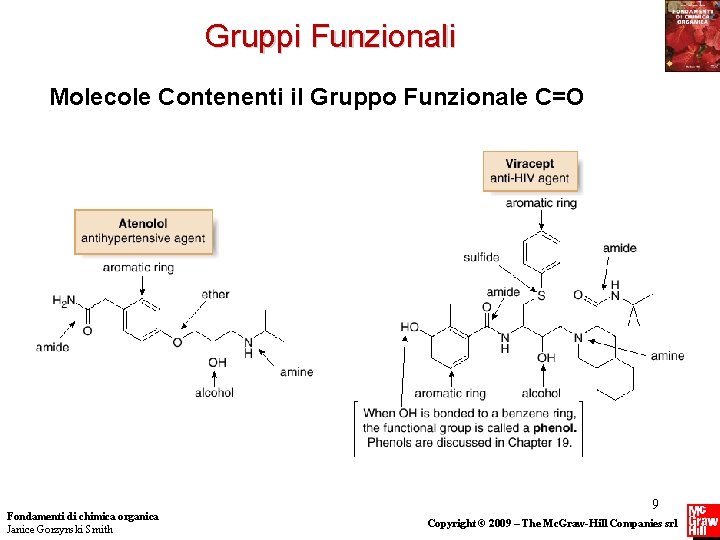
Gruppi Funzionali Molecole Contenenti il Gruppo Funzionale C=O Fondamenti di chimica organica Janice Gorzynski Smith 9 Copyright © 2009 – The Mc. Graw-Hill Companies srl
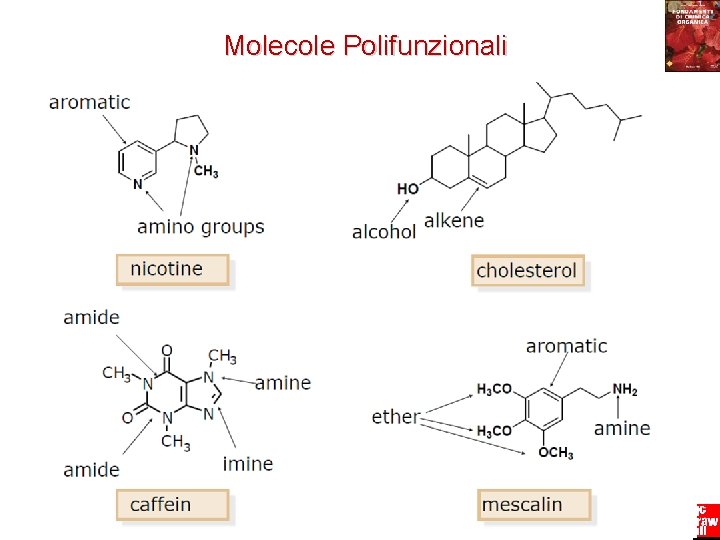
Molecole Polifunzionali Fondamenti di chimica organica Janice Gorzynski Smith 10 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Gruppi Funzionali Un gruppo funzionale determina tutte le seguenti proprietà di una molecola: § Legami e forma § Tipo e intensità delle forze intermolecolari § Proprietà fisiche § Nomenclatura § Reattività chimica Fondamenti di chimica organica Janice Gorzynski Smith 11 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Forze Intermolecolari • Le forze (interazioni) intermolecolari sono chiamate anche interazioni covalenti e interazioni di non legame • Le forze intermolecolari dipendono dal tipo e dal numero di gruppi funzionali • Nelle molecule neuter ci sono tre tipi principali di interazioni intermolecolari, in ordine di intensità crescente: I n t e n s it à • Interazioni di Van der Waals (Forze di dispersion di London) VDW • Interazioni di Vand der Waals DD • Legami idrogeno HB Fondamenti di chimica organica Janice Gorzynski Smith 12 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Forze di van der Waals (London) • Sono interazioni deboli causate da variazioni momentanee nella densità elettronica di una molecola. • Sono le sole forze attrattive presenti in composti non polari. Fondamenti di chimica organica Janice Gorzynski Smith 13 Copyright © 2009 – The Mc. Graw-Hill Companies srl
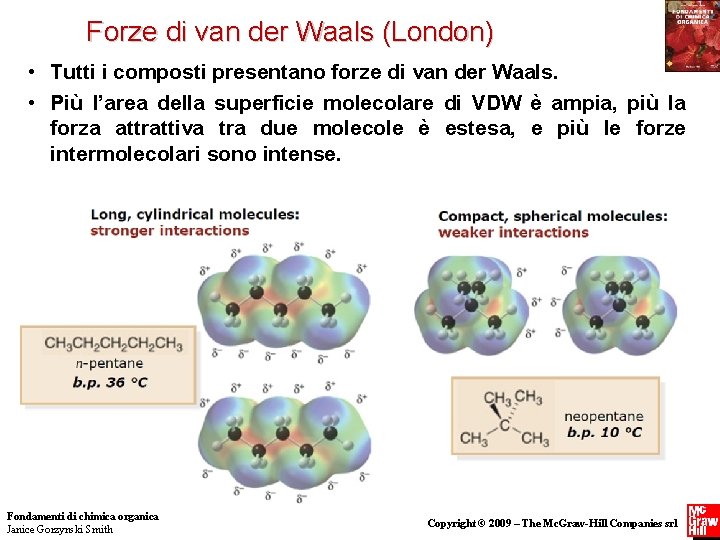
Forze di van der Waals (London) • Tutti i composti presentano forze di van der Waals. • Più l’area della superficie molecolare di VDW è ampia, più la forza attrattiva tra due molecole è estesa, e più le forze intermolecolari sono intense. Figura 3. 1 Area della superficie e forze di van der Waals Fondamenti di chimica organica Janice Gorzynski Smith 14 Copyright © 2009 – The Mc. Graw-Hill Companies srl
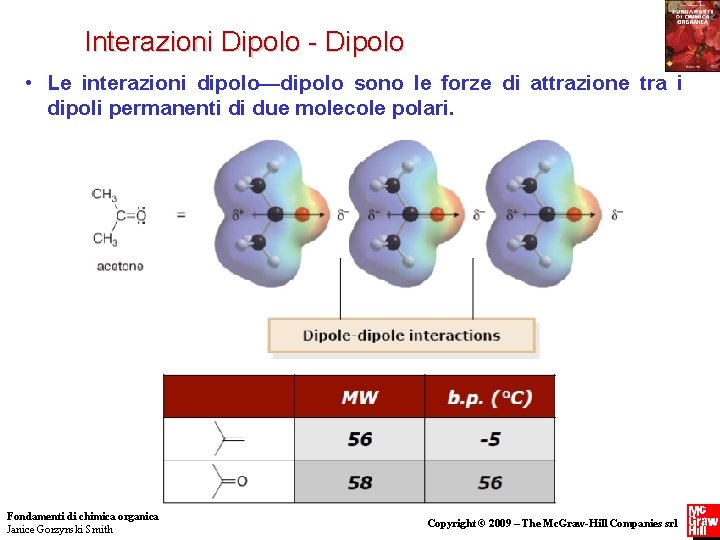
Interazioni Dipolo - Dipolo • Le interazioni dipolo—dipolo sono le forze di attrazione tra i dipoli permanenti di due molecole polari. Fondamenti di chimica organica Janice Gorzynski Smith 15 Copyright © 2009 – The Mc. Graw-Hill Companies srl
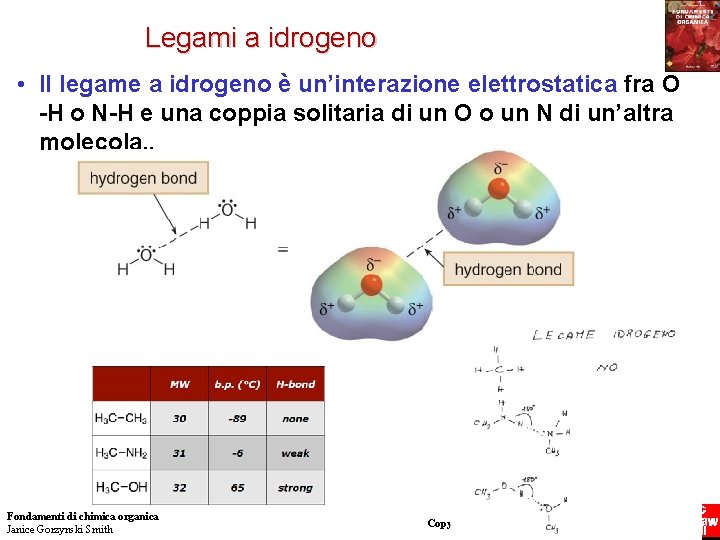
Legami a idrogeno • Il legame a idrogeno è un’interazione elettrostatica fra O -H o N-H e una coppia solitaria di un O o un N di un’altra molecola. . Fondamenti di chimica organica Janice Gorzynski Smith 16 Copyright © 2009 – The Mc. Graw-Hill Companies srl
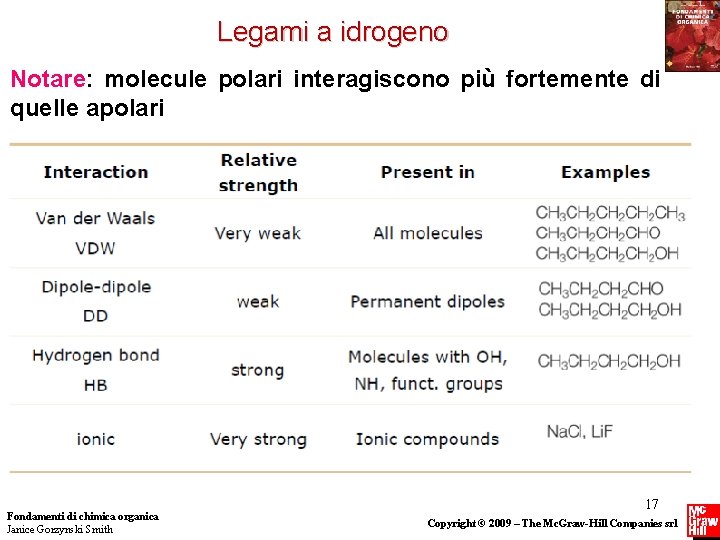
Legami a idrogeno Notare: molecule polari interagiscono più fortemente di quelle apolari Fondamenti di chimica organica Janice Gorzynski Smith 17 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Proprietà Fisiche—Punto di Ebollizione • Il punto di ebollizione di un composto è la temperatura alla quale la pressione di vapore di un liquid eguaglia la pressione esterna. • All’ebollizione serve energia intermoleoclari per rompere le interazioni • Più intense sono le forze intermolecolari, più il punto di ebollizione è alto. • Per composti che hanno approssimativamente lo stesso peso molecolare: Fondamenti di chimica organica Janice Gorzynski Smith 18 Copyright © 2009 – The Mc. Graw-Hill Companies srl
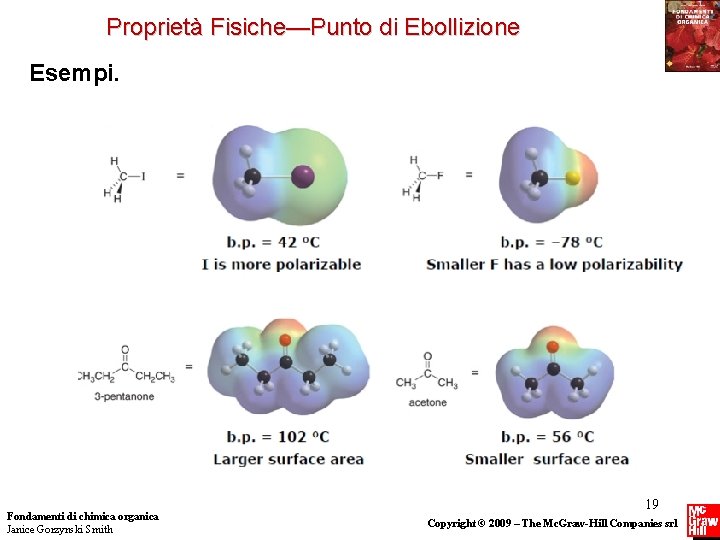
Proprietà Fisiche—Punto di Ebollizione Esempi. Fondamenti di chimica organica Janice Gorzynski Smith 19 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Proprietà Fisiche—Punto di Fusione • Il punto di fusione è la temperatura alla quale un solido si converte nella sua fase liquida. • M. p. e B. p seguono lo stesso trend. • Per uno stesso gruppo funzionale, più il composto è simmetrico, più il punto di fusione è alto. Fondamenti di chimica organica Janice Gorzynski Smith 20 Copyright © 2009 – The Mc. Graw-Hill Companies srl
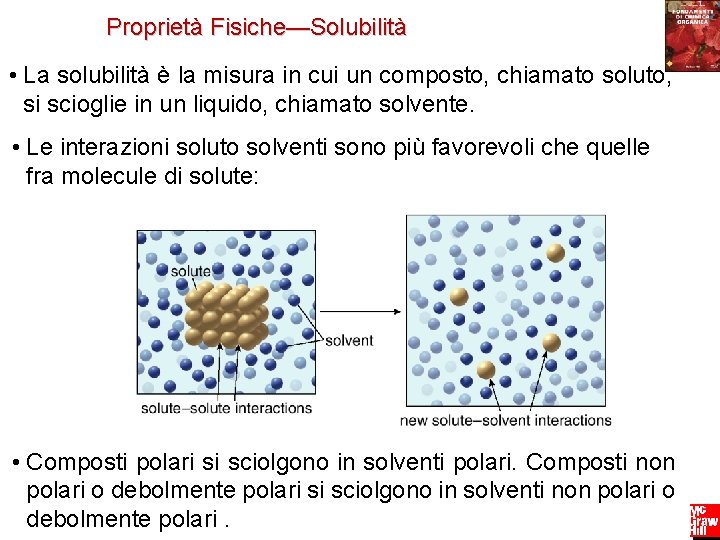
Proprietà Fisiche—Solubilità • La solubilità è la misura in cui un composto, chiamato soluto, si scioglie in un liquido, chiamato solvente. • Le interazioni soluto solventi sono più favorevoli che quelle fra molecule di solute: • Composti polari si sciolgono in solventi polari. Composti non polari o debolmente polari si sciolgono in solventi non polari 21 o Fondamenti di chimica organica Copyright © 2009 – The Mc. Graw-Hill Companies srl debolmente polari. Janice Gorzynski Smith

Introduzione alle Molecole Organiche e ai Gruppi Funzionali Influenza dei Gruppi Funzionali sulla Reattività Ricordare che: • I gruppi funzionali danno origine a siti reattivi nelle molecole. • Siti elettron-ricchi reagiscono con siti elettron-poveri. Tutti i gruppi funzionali contengono un eteroatomo, un legame bond o entrambi, e queste caratteristiche creano in una molecola siti elettron-poveri (o elettrofili) e siti elettron-ricchi (o nucleofili). Le molecole reagiscono in questi siti. Fondamenti di chimica organica Janice Gorzynski Smith 22 Copyright © 2009 – The Mc. Graw-Hill Companies srl
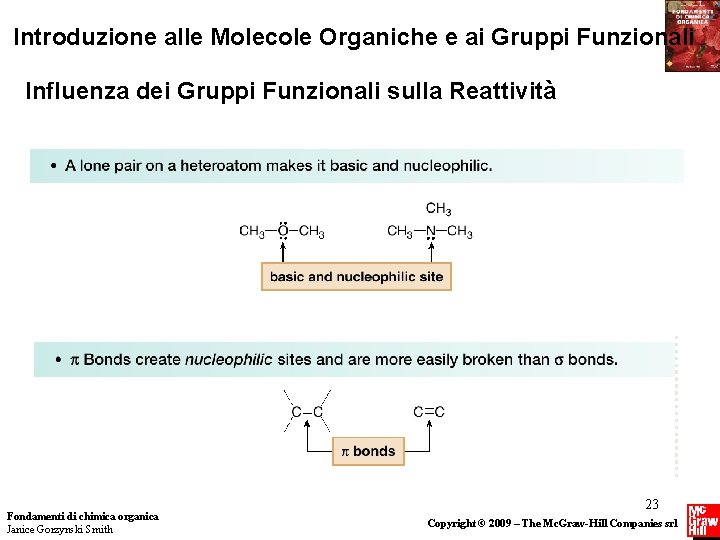
Introduzione alle Molecole Organiche e ai Gruppi Funzionali Influenza dei Gruppi Funzionali sulla Reattività Fondamenti di chimica organica Janice Gorzynski Smith 23 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Introduzione alle Molecole Organiche e ai Gruppi Funzionali Influenza dei Gruppi Funzionali sulla Reattività • Un atomo di carbonio elettron-povero reagisce con un nucleofilo, rappresentato nelle reazioni con il simbolo Nu¯. • Un atomo di carbonio elettron-ricco reagisce con un elettrofilo, rappresentato nelle reazioni con il simbolo E+. Per esempio, gli alcheni contengono un doppio legame C-C, ricco di elettroni, e perciò reagiscono con elettrofili E+. Fondamenti di chimica organica Janice Gorzynski Smith 24 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Introduzione alle Molecole Organiche e ai Gruppi Funzionali Influenza dei Gruppi Funzionali sulla Reattività D’altra parte, gli alogenuri alchilici possiedono un atomo di carbonio elettrofilo, quindi reagiscono con centri elettron-ricchi, nucleofili. Fondamenti di chimica organica Janice Gorzynski Smith 25 Copyright © 2009 – The Mc. Graw-Hill Companies srl
- Slides: 25