Grupo 1 Metais Alcalinos Elementos Smbolo Configurao Eletrnica
![Grupo 1: Metais Alcalinos Elementos Símbolo Configuração Eletrônica Lítio Li Sódio Na [He] 2 Grupo 1: Metais Alcalinos Elementos Símbolo Configuração Eletrônica Lítio Li Sódio Na [He] 2](https://slidetodoc.com/presentation_image/43fa37c37d228776a5fcc88e5df9e01e/image-1.jpg)
Grupo 1: Metais Alcalinos Elementos Símbolo Configuração Eletrônica Lítio Li Sódio Na [He] 2 s 1 Configuração Eletrônica [Ne] 3 s 1 Potássio K [Ar] 3 d 104 s 1 Rubídio Rb [Kr] 4 d 105 s 1 Césio Cs [Xe] 4 f 145 d 106 s 1 Frâncio Fr [Rn] 5 f 146 d 107 s 1 1

Propriedades Gerais q q q q Metais Excelentes condutores de eletricidade Moles Altamente reativos Fortes agentes redutores São eletropositivos Compostos monovalentes, iônicos e incolores Hidróxidos e óxidos são bases muito fortes Sódio metálico Explosão do sódio Lâmpada de sódio 2

Lítio Li Menor metal alcalino 35º em abundância Descoberto por J. A. Afrvedson (1817) Encontrado nos minérios Spodumena Li. Al(Si. O 3)2 e Petalita Li 2 Al 2(Si. O 3)3(FOH)2 Obtido por redução eletrolítica Usado em baterias recarregáveis e plataformas espaciais para remoção de CO 2 e ar Usado no tratamento de depressão maníaca 3

Sódio Na Metal branco prateado 7º em abundância Descoberto por Sir Humphrey Davy em 1807 Encontrado na sal gema Na. Cl e água do mar Obtido por eletrólise do Na. Cl Usado na síntese de organo-metálicos, em sistemas de refrigeração de usinas nucleares e na iluminação pública 4

Potássio K Metal branco prateado 8º em abundância Descoberto por Sir Humphrey Davy em 1807 Encontrado na silvita KCl e água do mar Obtido por eletrólise do KOH Usado na forma de sais como fertilizante K 2 SO 4 (aditivo do gesso), K 2 CO 3 (vidros e cerâmicas), KNO 3 (explosivo), KBr (sedativo), KMn. O 4 (bactericida) 5

Rubídio Metal sólido que funde a 40ºC 23º em abundância (16º metal) Descoberto por Robert Bunsen e Gustav Kirchhoff em 1861 Encontrado em diversos minerais. A lepidolita (principal fonte) contém 1, 5% de rubídio metal Obtido como sub-produto do processamento do Lítio Usado em motores iônicos para naves espaciais É utilizado na fabricação de cristais especiais para sistemas de telecomunicação de fibra óptica e equipamentos de visão noturna Aula 4: Química de Elementos 6

Césio Polucita Metal sólido que funde a 28, 5ºC 46º em abundância Descoberto por Robert Bunsen e Gustav Kirchhoff em 1860 Coloração amarelo prateada Usado nas indústrias de energia nuclear, Obtido por eletrólise do cianeto ou cloreto de césio 7

Frâncio Metal radioativo Obtido como resultado da desintegração do actínio. Encontrado em minerais de urânio Pode ser feito artificialmente bombardeando tório com prótons. É o mais instável dos primeiros 101 elementos. O seu isótopo 223 Fr têm uma meia-vida de 22 minutos. Este é o único isótopo que ocorre na natureza Existe no máximo 20 -30 g na crosta terrestre. 8
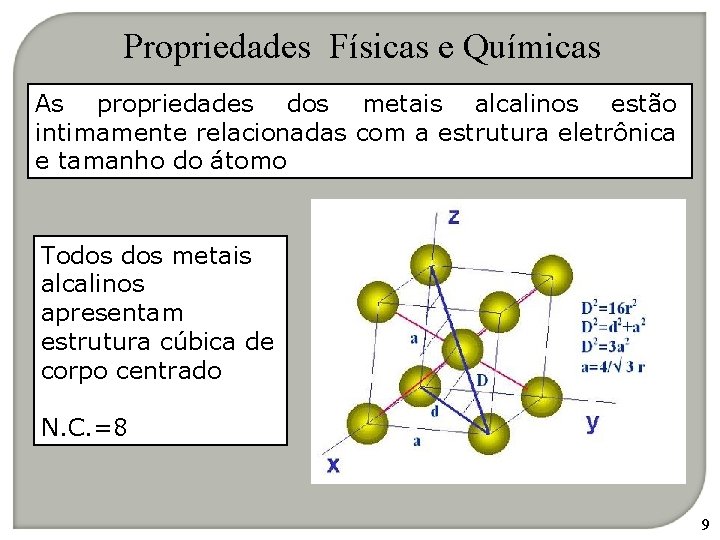
Propriedades Físicas e Químicas As propriedades dos metais alcalinos estão intimamente relacionadas com a estrutura eletrônica e tamanho do átomo Todos metais alcalinos apresentam estrutura cúbica de corpo centrado N. C. =8 9
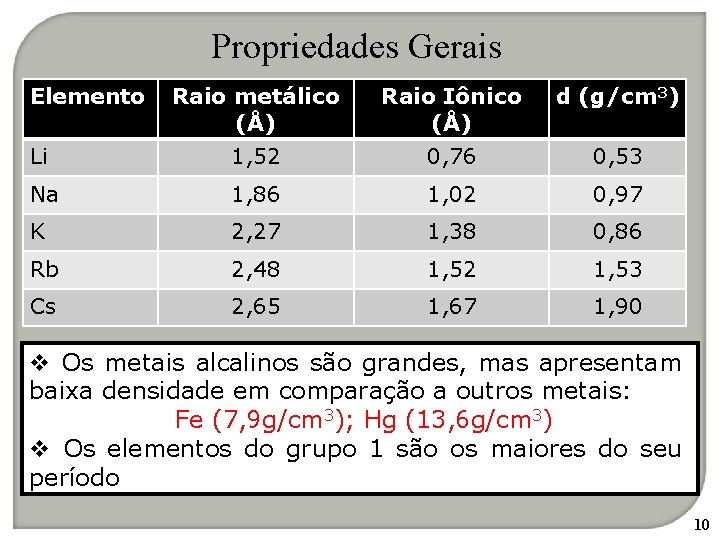
Propriedades Gerais Elemento Raio metálico (Å) Raio Iônico (Å) d (g/cm 3) Li 1, 52 0, 76 0, 53 Na 1, 86 1, 02 0, 97 K 2, 27 1, 38 0, 86 Rb 2, 48 1, 52 1, 53 Cs 2, 65 1, 67 1, 90 v Os metais alcalinos são grandes, mas apresentam baixa densidade em comparação a outros metais: Fe (7, 9 g/cm 3); Hg (13, 6 g/cm 3) v Os elementos do grupo 1 são os maiores do seu período 10
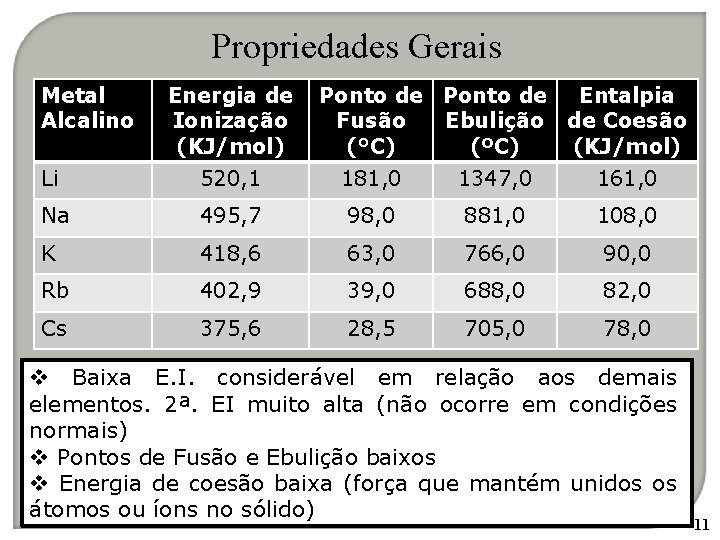
Propriedades Gerais Metal Alcalino Energia de Ionização (KJ/mol) Ponto de Entalpia Fusão Ebulição de Coesão (°C) (ºC) (KJ/mol) Li 520, 1 181, 0 1347, 0 161, 0 Na 495, 7 98, 0 881, 0 108, 0 K 418, 6 63, 0 766, 0 90, 0 Rb 402, 9 39, 0 688, 0 82, 0 Cs 375, 6 28, 5 705, 0 78, 0 v Baixa E. I. considerável em relação aos demais elementos. 2ª. EI muito alta (não ocorre em condições normais) v Pontos de Fusão e Ebulição baixos v Energia de coesão baixa (força que mantém unidos os átomos ou íons no sólido) 11

Eletronegatividade e tipo de ligação Eletronegatividade baixa (menor do que qualquer outro elemento) Formam ligações iônicas Eletronegatividade Na 0, 9 Cl 3, 0 Diferença = 2, 1 Diferença entre as eletronegatividades entre 1, 7 a 1, 8 ligação 50% iônica 12

Aplicação dos Metais Alcalinos e Compostos v Estereato de Lítio: usado na fabricação de graxas e lubrificantes v Carbonato de Lítio: usado no tratamento de doenças mentais, na produção eletrolítica do Al adicionado à bauxita e no endurecimento do vidro v Lítio metálico: usado em células eletroquímicas, pilhas e ligas. Li: Pb (metal branco), Li: Al (peças de avião), Li: Mg (chapas de blindagem) v. Hidróxido de Sódio: usado na fabricação de papel, obtenção de alumina, sabões 13

v Carbonato de Sódio: usado na fabricação de sabão e detergentes, vidros e produtos de limpeza v Hipoclorito de Sódio: usado como alvejante e desinfetante v Bicarbonato de Sódio: usado como fermento químico v Cloreto, Sulfato e Nitrato de Potássio: usados como fertilizante v Permanganato de Potássio: fabricação de sacarina v Carbonato e Óxido de Potássio: usado em cerâmicas 14

Importância Biológica Na e K são essenciais manter pressão osmótica e equilibrar cargas elétricas associadas com macromoléculas orgânicas 15
Propriedades Químicas Reatividade em água Na(s) + H 2 O → Na+ (aq) + OH- (aq) + ½H 2 (g) Velocidade da reação: Li<Na<K 16

Reatividade com oxigênio 2 Li(s) + ½O 2 → Li 2 O (s) (Formação de óxidos) Na(s) + O 2 → Na 2 O 2 (s) (Formação de peróxidos) K(s) + O 2 → KO 2 (s) (Formação de superóxidos) 17
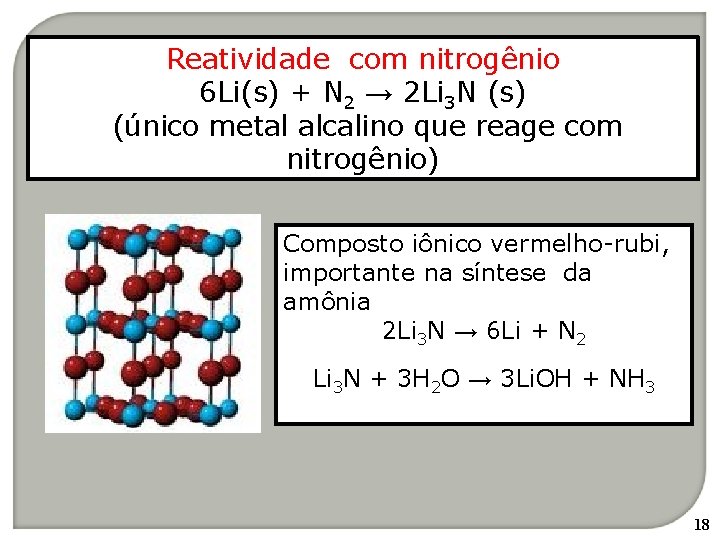
Reatividade com nitrogênio 6 Li(s) + N 2 → 2 Li 3 N (s) (único metal alcalino que reage com nitrogênio) Composto iônico vermelho-rubi, importante na síntese da amônia 2 Li 3 N → 6 Li + N 2 Li 3 N + 3 H 2 O → 3 Li. OH + NH 3 18
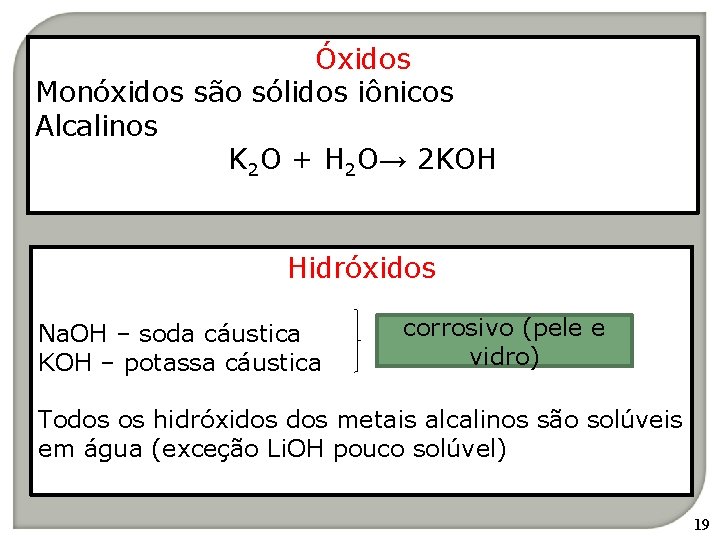
Óxidos Monóxidos são sólidos iônicos Alcalinos K 2 O + H 2 O→ 2 KOH Hidróxidos Na. OH – soda cáustica KOH – potassa cáustica corrosivo (pele e vidro) Todos os hidróxidos metais alcalinos são solúveis em água (exceção Li. OH pouco solúvel) 19

Reações dos hidróxidos de metais alcalinos Ácidos Na. OH + HCl Na. Cl + H 2 O Dióxido de Carbono 2 Na. OH + CO 2 Na 2 CO 3 + H 2 O Sais de amônio Na. OH + NH 4 Cl NH 3 + Na. Cl + H 2 O Álcoois Na. OH + Et. OH Na. OEt (alcóxidos) + H 2 O 20

Diferença entre o lítio e os demais elementos do Grupo 1 Assemelha-se mais aos elementos do Grupo 2 (particularmente o Mg) 1 – p. f. e p. e. maior que os demais elementos do Grupo 1 2 – Li possui maior dureza 3 – Menos reativo com o oxigênio 4 – Li. OH é menos básico 5 – Li forma nitreto (Li. N 3) – nenhum outro elemento do Grupo 1 forma nitreto, mas os elementos do Grupo 2 sim 6 – Li 2 CO 3, Li 3 PO 4 e Li. F são insolúveis em água (semelhante ao Mg) 7 – O Li+ e seus compostos são mais fortemente hidratados que os compostos demais elementos do grupo 1 21

Razões e Generalizações Generalização Primeiros elementos de cada um dos grupos representativos (Li, Be, C, N, O e F) diferem do restante dos elementos de seus respectivos grupos Razões 1 – Menor tamanho dos primeiros elementos em relação aos demais elementos do grupo 2 – Primeiro elemento forma no máximo 4 ligações (apenas 1 orbital s e 3 p). Os demais podem usar orbitais d em suas ligações 3 – As similaridades entre o Li(1º. Elemento grupo 1) e o Mg (2º. Elemento grupo 2) seguem a correlação diagonal na TP. 22
- Slides: 22