Grulica Wybrane Dane Epidemiologiczne Diagnosyka Laboratoryjna Katedra i

Gruźlica Wybrane Dane Epidemiologiczne Diagnosyka Laboratoryjna Katedra i Klinika Chorób Wewnętrznych, Pneumonologii i Alergologii Akademii Medycznej w Warszawie 2005/2006
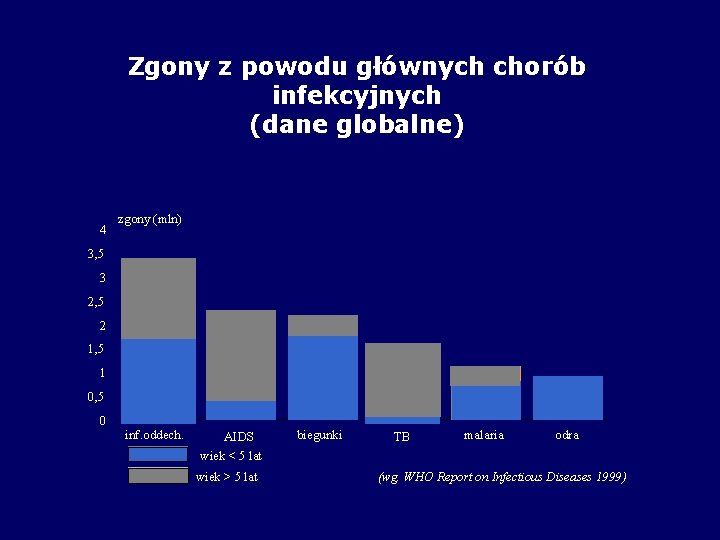
Zgony z powodu głównych chorób infekcyjnych (dane globalne) 4 zgony (mln) 3, 5 3 2, 5 2 1, 5 1 0, 5 0 inf. oddech. AIDS wiek < 5 lat wiek > 5 lat biegunki TB malaria odra (wg. WHO Report on Infectious Diseases 1999)

Gruźlica na świecie Na świecie prątkiem gruźlicy zakażonych jest 1, 9 mld osób (1/3 światowej populacji) · Rocznie na gruźlicę zapada 7 - 8 mln osób, w tym 1, 5 mln dzieci · Rocznie na gruźlicę umiera 2 mln osób, w tym 100 tys. Dzieci · 95% nowych zachorowań oraz 80% zgonów z powodu gruźlicy dotyczy krajów ubogich · W krajach rozwijających się 80% chorych na gruźlicę to osoby w wieku produkcyjnym · Szacuje się, że nieleczony chory zakaża 10 - 15 osób w ciągu roku · Problemem globalnym jest gruźlica wielolekooporna (Raporty WHO)
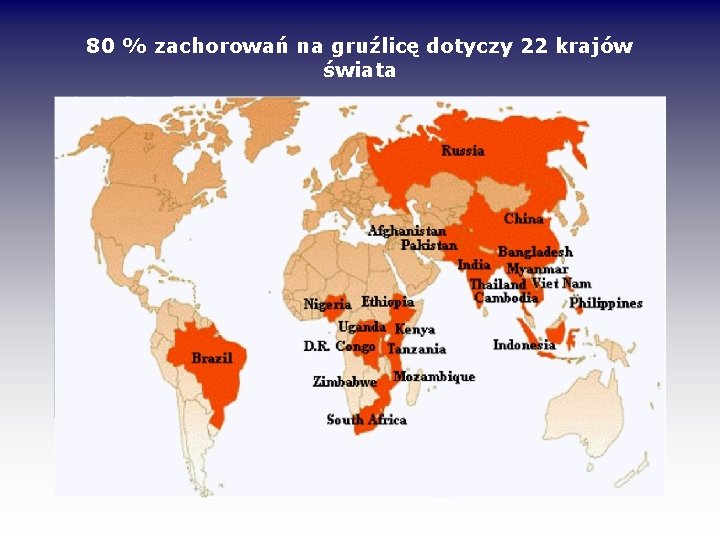
80 % zachorowań na gruźlicę dotyczy 22 krajów świata
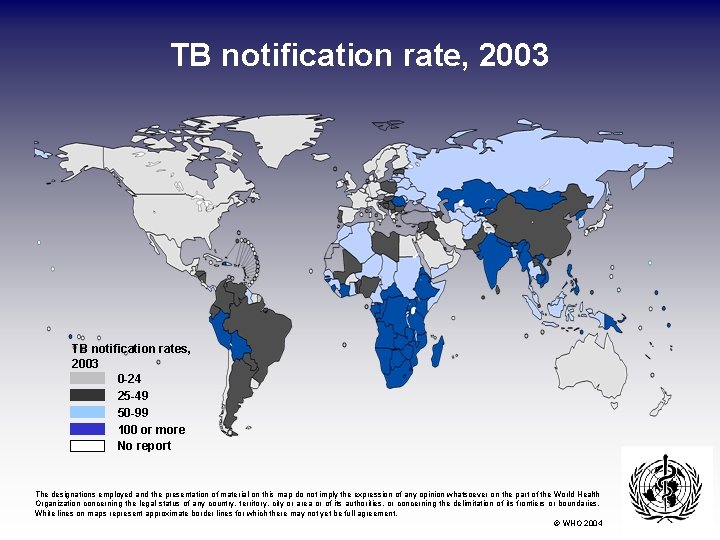
TB notification rate, 2003 TB notification rates, 2003 0 -24 25 -49 50 -99 100 or more No report The designations employed and the presentation of material on this map do not imply the expression of any opinion whatsoever on the part of the World Health Organization concerning the legal status of any country, territory, city or area or of its authorities, or concerning the delimitation of its frontiers or boundaries. White lines on maps represent approximate border lines for which there may not yet be full agreement. © WHO 2004
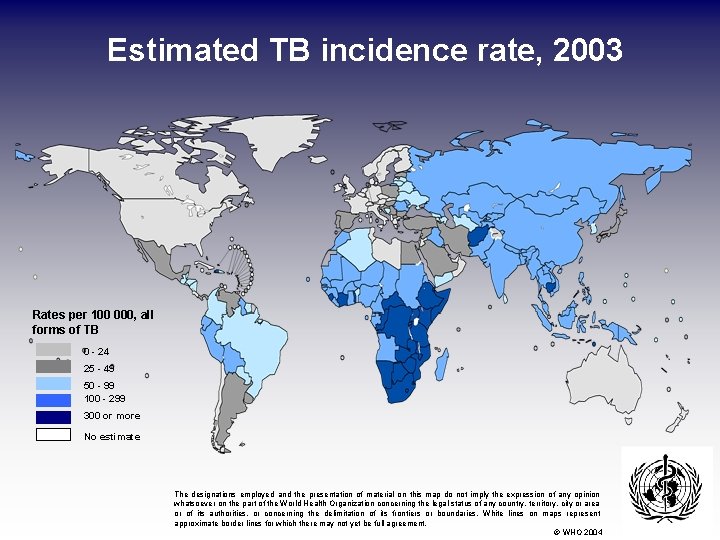
Estimated TB incidence rate, 2003 Rates per 100 000, all forms of TB 0 - 24 25 - 49 50 - 99 100 - 299 300 or more No estimate The designations employed and the presentation of material on this map do not imply the expression of any opinion whatsoever on the part of the World Health Organization concerning the legal status of any country, territory, city or area or of its authorities, or concerning the delimitation of its frontiers or boundaries. White lines on maps represent approximate border lines for which there may not yet be full agreement. © WHO 2004
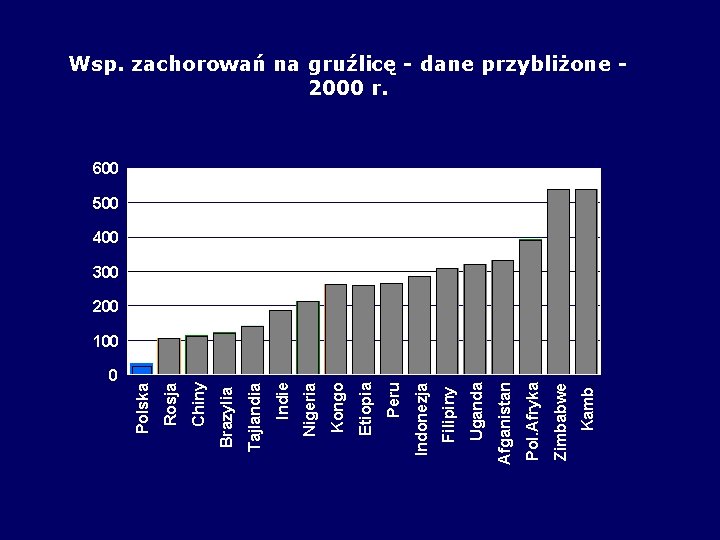
0 Kamb. Zimbabwe Pol. Afryka Afganistan Uganda Filipiny Indonezja Peru Etiopia Kongo Nigeria Indie Tajlandia Brazylia Chiny Rosja Polska Wsp. zachorowań na gruźlicę - dane przybliżone 2000 r. 600 500 400 300 200 100
Polska - zapadalność na gruźlicę - 2005 r. Nowo zarejestrowanych chorych 9 280 (wsp. 24, 9) (wszystkie postacie gruźlicy, w tym 260 więźniów, 17 cudzoziedmców) kobiety mężczyźni miasta 3 200 (wsp. 16, 2) 5 509 (wsp. 32, 9) 6 279 wieś 3 771 • Nowe zachorowania 8 203 (wsp. 21, 5) • Wznowy 1 077 (wsp. 2, 8)
Polska – umieralność z powodu gruźlicy 2004 r. Gruźlica jako przyczyna zgonu - 813 osób Gruźlica układu oddechowego 786 osób - Zgony z powodu gruźlicy stanowiły 0, 2 % ogółu zgonów Zgony z powodu gruźlicy stanowiły 37, 8% zgonów z powodu wszystkich chorób zakaźnych i pasożytniczych

Polska – 2005 r. 91, 2 % wszystkich zachorowań stanowiła gruźlica płuc 8 459 przypadków (w tym 3 258 AFB+) Lokalizacja pozapłucna 821 przypadków (8, 8 % nowo zarejestrowanych) 52 przypadki gruźlicy pozapłucnej z jednoczesną gruźlicą płuc inne lokalizacje to gruźlica: opłucnej 351 przypadków narządów moczowo-płciowych 111 przypadków obwodowych węzłów chłonnych 143 przypadków kości i stawów 87 przypadków gruźlicze zapalenie opon mózgowo-rdzeniowych 19 przypadków (w tym 2 dzieci z woj. mazowieckiego)
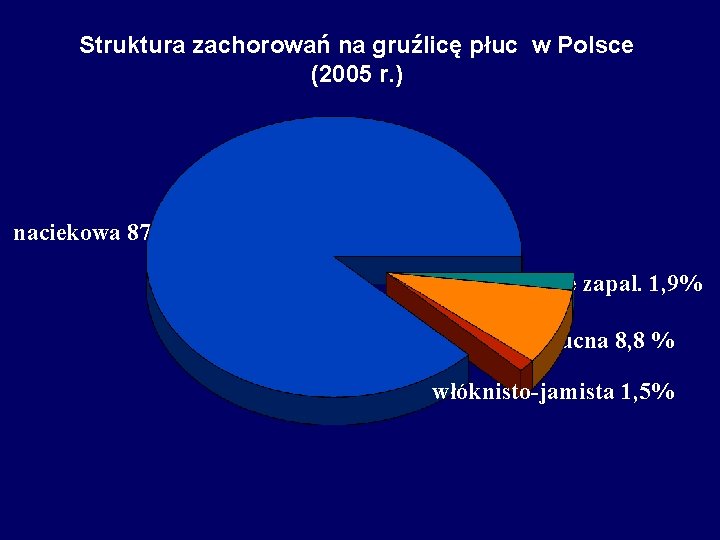
Struktura zachorowań na gruźlicę płuc w Polsce (2005 r. ) naciekowa 87, 2% serowate zapal. 1, 9% pozaplucna 8, 8 % włóknisto-jamista 1, 5%
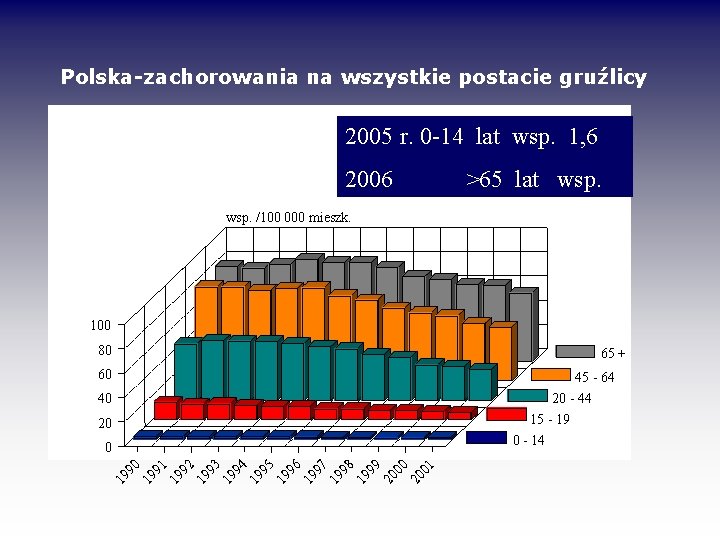
Polska-zachorowania na wszystkie postacie gruźlicy 2005 r. 0 -14 lat wsp. 1, 6 2006 50, 3 wsp. /100 000 mieszk. >65 lat wsp. 0 -14 15 -19 20 -44 45 -64 65+ 100 80 65 + 60 40 20 19 91 19 92 19 93 19 94 19 95 19 96 19 97 19 98 19 99 20 00 20 01 0 45 - 64 20 - 44 15 - 19 0 - 14
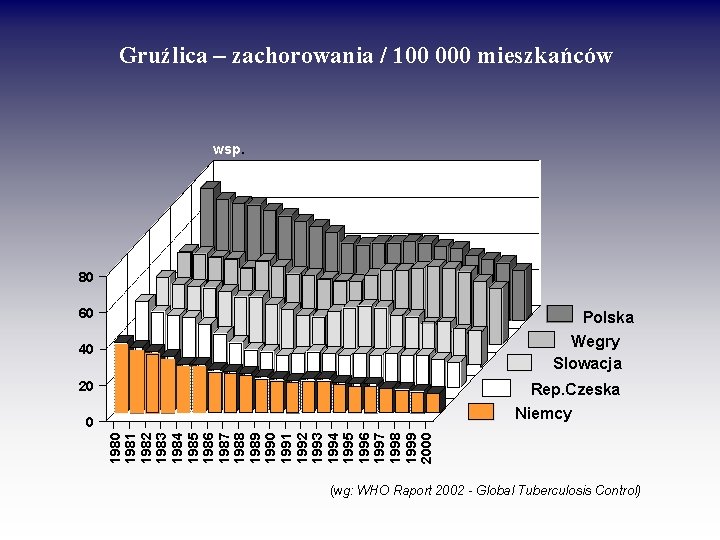
Gruźlica – zachorowania / 100 000 mieszkańców wsp. 80 60 Polska Wegry Slowacja 40 20 Rep. Czeska Niemcy 1980 1981 1982 1983 1984 1985 1986 1987 1988 1989 1990 1991 1992 1993 1994 1995 1996 1997 1998 1999 2000 0 (wg: WHO Raport 2002 - Global Tuberculosis Control)
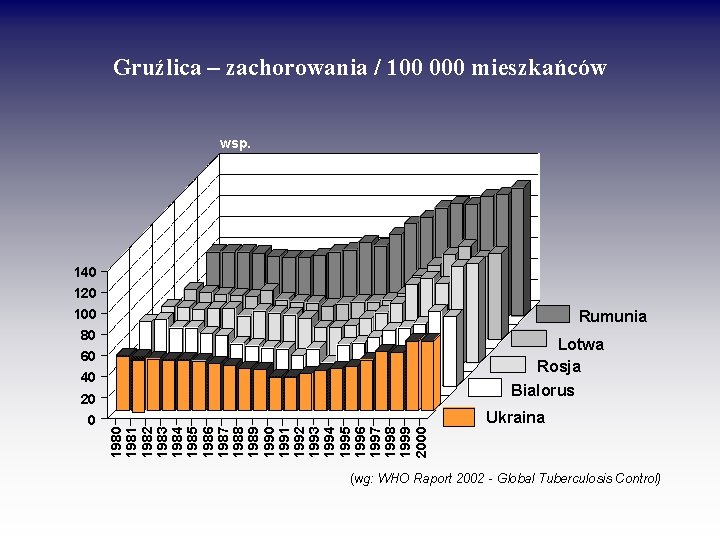
Gruźlica – zachorowania / 100 000 mieszkańców wsp. 140 120 100 Rumunia 80 60 40 1981 1982 1983 1984 1985 1986 1987 1988 1989 1990 1991 1992 1993 1994 1995 1996 1997 1998 1999 2000 20 0 Lotwa Rosja Bialorus Ukraina (wg: WHO Raport 2002 - Global Tuberculosis Control)
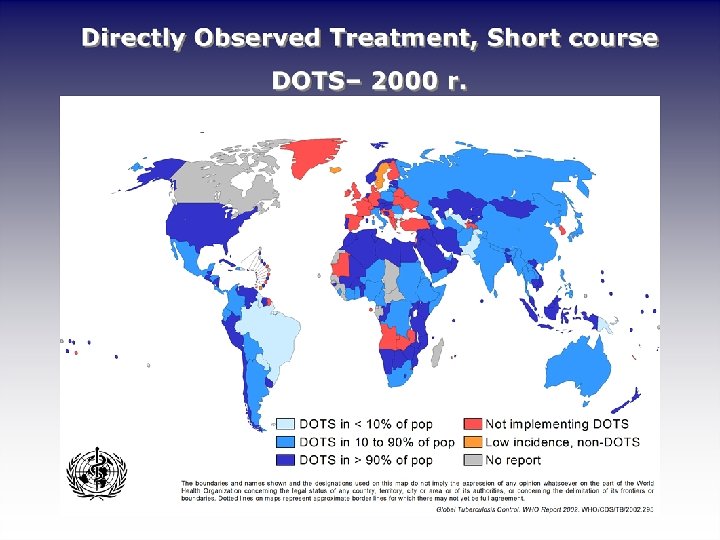

Strategia DOTS: 1. Instytucjonalny nadzór rządowy zwalczania gruźlicy 2. 2. Zgłaszanie przypadków bk(+) rej. służbom epidemiol. 3. 3. Nieprzerwane 6 -8 miesięczne leczenie 4. 4. Standardowy system rejestracji i sprawozdawczości
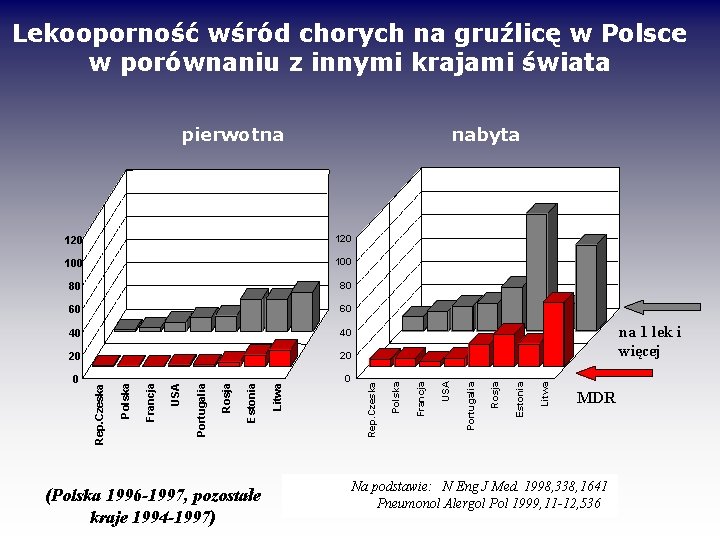
Lekooporność wśród chorych na gruźlicę w Polsce w porównaniu z innymi krajami świata pierwotna nabyta (Polska 1996 -1997, pozostałe kraje 1994 -1997) Litwa Estonia Rosja 0 Portugalia 0 USA 20 Francja 20 na 1 lek i więcej Polska 40 Rep. Czeska 40 Litwa 60 Estonia 60 Rosja 80 Portugalia 80 USA 100 Francja 100 Polska 120 Rep. Czeska 120 MDR Na podstawie: N Eng J Med. 1998, 338, 1641 Pneumonol Alergol Pol 1999, 11 -12, 536

Wzrost oporności na leki wśród szczepów Mycobacterium tuberculosis Polska Oporność ogółem (nowe zach. ) Oporność wielolekowa pierwotna Oporność na 4 leki (INH+RMP+SM+EMB) Oporność wielolekowa wtórna 1997 2000 3, 6 % 6, 12% p<0, 001 0, 6% 1, 15% p<0, 001 0, 0% 0, 5%*/ p<0, 001 7, 0 % 8, 55% */ 15 chorych (wg. Augustynowicz i wsp. Zakażenia 1, 2003) Badanie na ok. 1000 szczepów gruźlicy wtórnej i ok. 3000 pierwotnej n. s.

Laboratoryjna Diagnostyka Gruźlicy

Około 80% zachorowań na gruźlicę wykrywa się z objawów o Jedynym, niepodważalnym potwierdzeniem wstępnego rozpoznania choroby jest uzyskanie dodatnich wyników diagnostyki mikrobiologicznej o w 2005 r. wśród nowo zarejestrowanych chorych (9 280) jedynie u 5 409 potwierdzono gruźlicę bakteriologicznie (58, 3 %), wśród chorych na gruźlicę płuc 6

Specyfika laboratoryjnej diagnostyki gruźlicy wiąże się z: * niskim tempem namnażania się prątków na pożywkach * koniecznością stosowania wielu technik wykrywania zakażenia (mikroskopia, techniki hodowlane, techniki biologii molekularnej) Ujemne wyniki badań laboratoryjnych nie wykluczają rozwoju choroby bowiem żadna z metod laboratoryjnych nie charakteryzuje się 100% czułością

Nowoczesna laboratoryjna diagnostyka gruźlicy obejmuje (i) bakterioskopię oraz metody molekularne (ii) wyhodowanie prątków • pożywka L-J • pożywki płynne z różnymi systemami detekcji wzrostu prątków (iii) określenie gatunku wyhodowanych prątków • konwencjonalne metody biochemicznomikrobiologiczne • metody molekularne (PCR, sondy genetyczne) • analiza kwasów mikolowych techniką HPLC (iv) określenie lekowrażliwości

Miarą nowoczesności laboratorium diagnostyki gruźlicy jest spełnienie powyższych wymogów diagnostycznych w maksymalnie krótkim czasie Docelowo powinno dążyć się do skrócenia czasu diagnostyki do < 25 dni

Laboratoria prątka gruźlicy I Rzędu: mikroskopia II Rzędu: hodowla identyfikacja M. tuberculosis complex ocena lekowrażliwości na INH, RMP, SM, EMB III Rzędu: identyfikacja ważniejszych gatunków testy lekowrażliwości dla leków drugiej linii testy lekowrażliwości dla prątków atypowych

Bakterioskopia (+) (-) Wykrywa chorych silnie prątkujących Nie różnicuje prątków żywych i martwych Czas wykonania około 3 godzin Nie różnicuje gatunku prątków Niska cena badania Czułość w wykrywaniu gruźlicy w plwocinie około 30 %
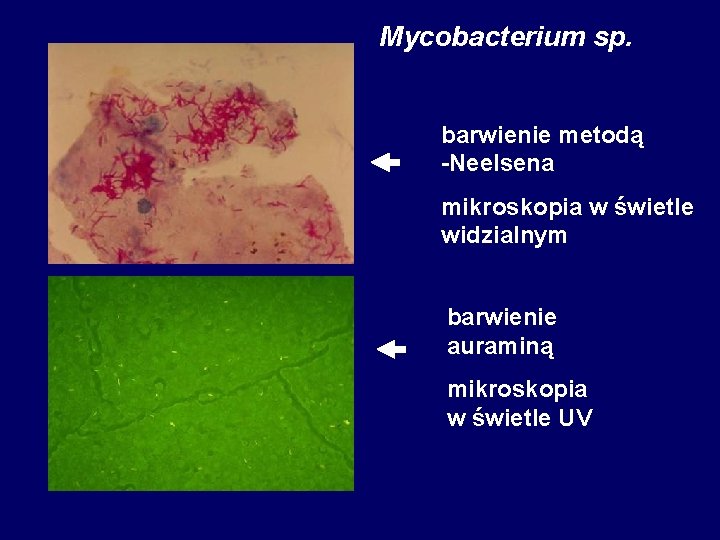
Mycobacterium sp. barwienie metodą -Neelsena mikroskopia w świetle widzialnym barwienie auraminą mikroskopia w świetle UV
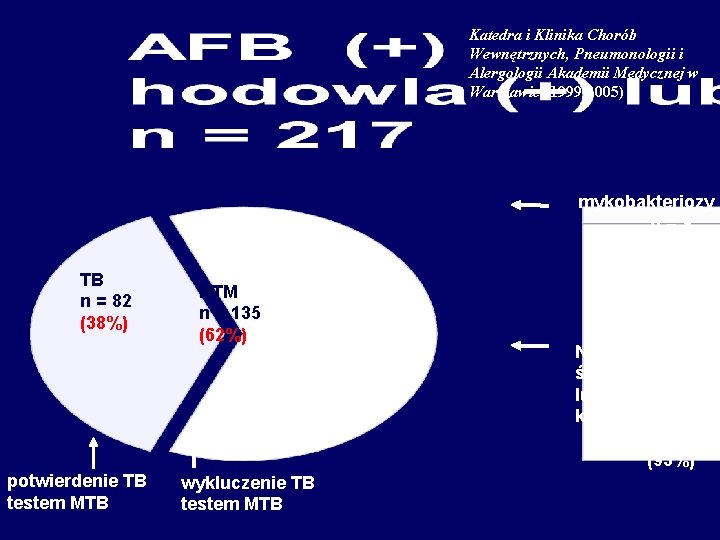
Katedra i Klinika Chorób Wewnętrznych, Pneumonologii i Alergologii Akademii Medycznej w Warszawie (1999 -2005) mykobakteriozy n=9 (7%) TB n = 82 (38%) potwierdenie TB testem MTB NTM n = 135 (62%) wykluczenie TB testem MTB NTM środowiskowe lub kolonizacja n = 126 (93%)

obecność prątków wynik O Prawdopodobnie negatywny (nie wystarczająca liczba prątków dla wykrycia w bekterioskopii) 1 -2 / 300 pól widzenia Nie uznawany za pozytywny, konieczność badania dalszych próbek 1 -9 / 100 pól widzenia + 1 -9 / 10 pól widzenia ++ 1 -9 / 1 pole widzenia +++ (średnio liczna) > 9 / 1 pole widzenia ++++ (liczne) */ przy powiększeniu 800 x - 1000 x (sporadyczne) (nieliczne)
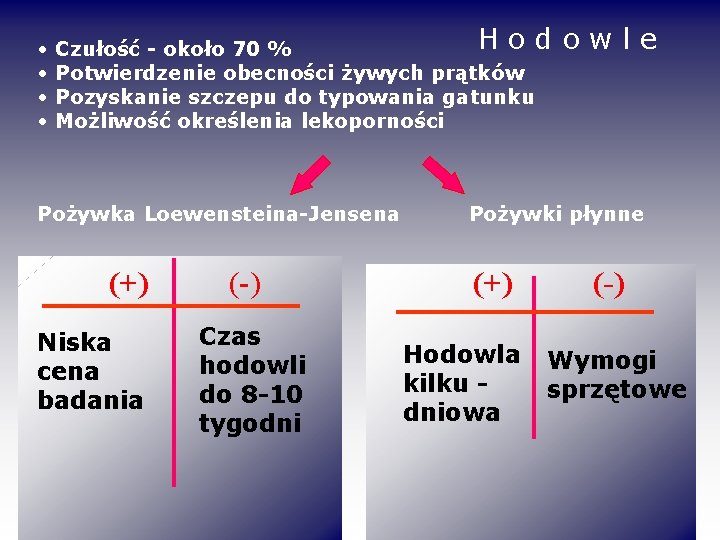
• • Hod Czułość - około 70 % Potwierdzenie obecności żywych prątków Pozyskanie szczepu do typowania gatunku Możliwość określenia lekoporności Pożywka Loewensteina-Jensena (+) Niska cena badania (-) Czas hodowli do 8 -10 tygodni owle Pożywki płynne (+) Hodowla kilku dniowa (-) Wymogi sprzętowe

Systemy detekcji wzrostu prątków na pożywkach płynnych *radiometryczny Bactec 460 Tb (Becton Dickinson) (możliwość różnicowania M. Tbc /MOTT) *kolorymetryczny system - MB Bac T (Organon Teknika Corporation), (możliwość badania lekooporności na podstawowe leki przeciwgruźlicze, osobne podłoża dla próbek krwawych) *system fluorymetryczny MGIT (Mycobacterial Growth Indicatory Tube) (Beckton Dickinson) (możliwość badania lekooporności na podstawowe leki przeciwgruźlicze)

Identyfikacja gatunku prątków W większości laboratoriów wykonuje się jedynie test niacynowy
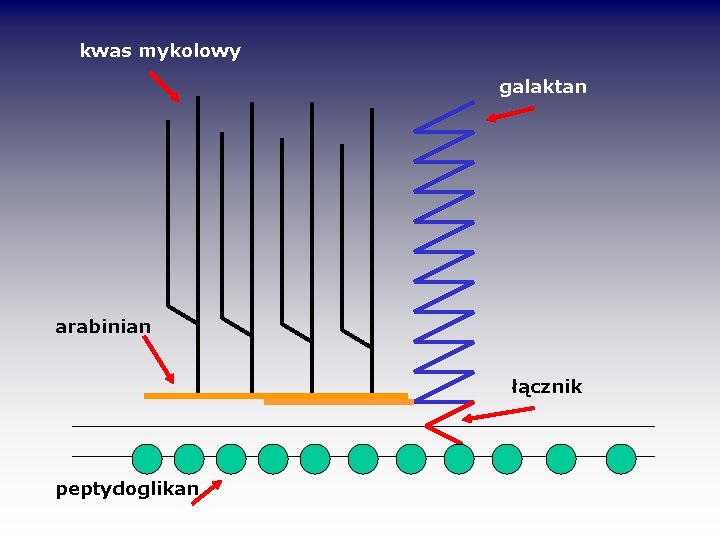
kwas mykolowy galaktan arabinian łącznik peptydoglikan
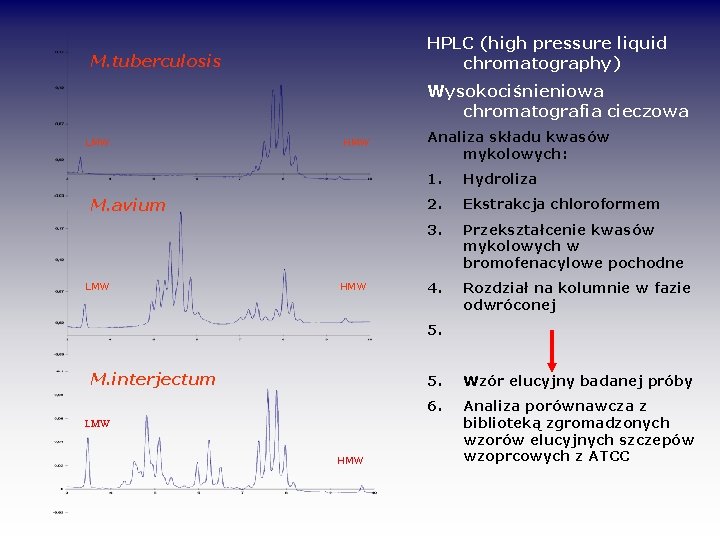
HPLC (high pressure liquid chromatography) M. tuberculosis Wysokociśnieniowa chromatografia cieczowa LMW HMW M. avium LMW HMW Analiza składu kwasów mykolowych: 1. Hydroliza 2. Ekstrakcja chloroformem 3. Przekształcenie kwasów mykolowych w bromofenacylowe pochodne 4. Rozdział na kolumnie w fazie odwróconej 5. M. interjectum LMW HMW 5. Wzór elucyjny badanej próby 6. Analiza porównawcza z biblioteką zgromadzonych wzorów elucyjnych szczepów wzoprcowych z ATCC

Metody biologii molekularnej (+) Czas wykonania badania – kilka / kilkanaście godzin Czułość wykrywania gruźlicy około 70 - 90 % Swoistość 97 -100 % Wykrywanie zakażeń w bardzo wczesnej fazie (-) Stosunkowo wysoka cena badania Szkolenie, aparatura Możliwość identyfikacji jedynie 5 gatunków prątków: • M. tbc complex, • M. avium, • M. intracellulare, • M. konsasii, • M. gordonae Jedynie metodą molekularną można w czasie kilku godzin wykryć obecność prątków gruźlicy bezpośrednio w materiale klinicznym
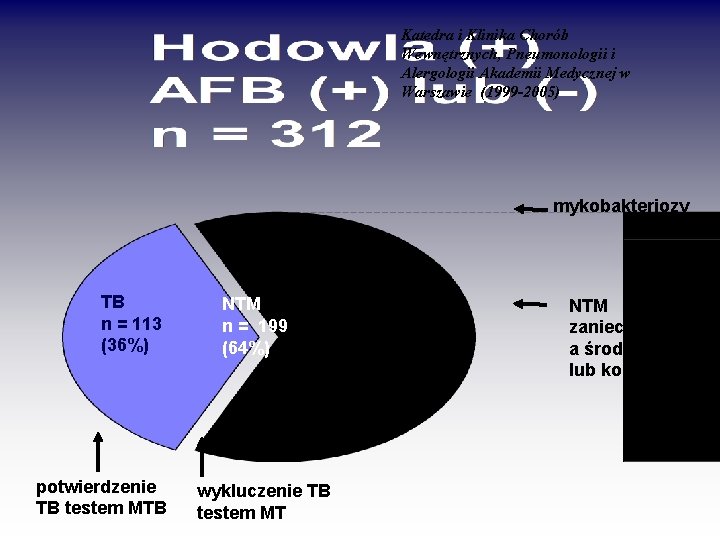
Katedra i Klinika Chorób Wewnętrznych, Pneumonologii i Alergologii Akademii Medycznej w Warszawie (1999 -2005) mykobakteriozy n = 22 (11%) TB n = 113 (36%) potwierdzenie TB testem MTB NTM n = 199 (64%) wykluczenie TB testem MT NTM zanieczyszczeni a środowiskowe lub kolonizacja n = 170 (89%)
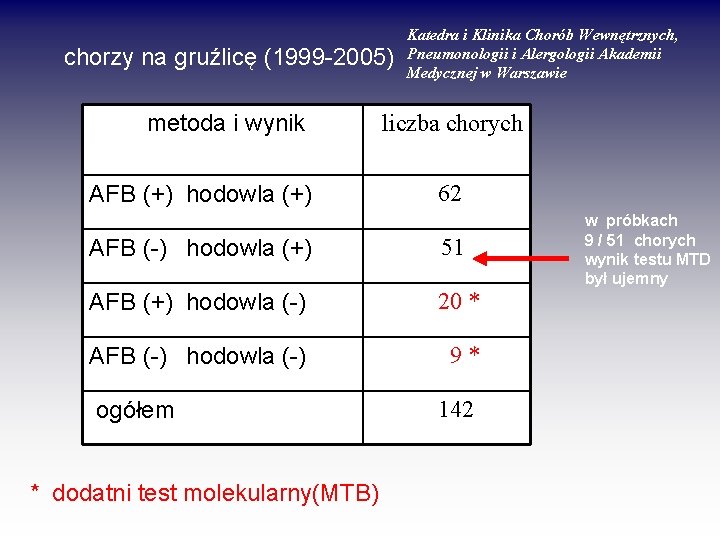
chorzy na gruźlicę (1999 -2005) metoda i wynik AFB (+) hodowla (+) Katedra i Klinika Chorób Wewnętrznych, Pneumonologii i Alergologii Akademii Medycznej w Warszawie liczba chorych 62 AFB (-) hodowla (+) 51 AFB (+) hodowla (-) 20 * AFB (-) hodowla (-) 9* ogółem * dodatni test molekularny(MTB) 142 w próbkach 9 / 51 chorych wynik testu MTD był ujemny

Systemy molekularne w diagnostyce gruźlicy * Amplicor MTB (Roche Molecular System, Somerville, New Jersey) - w systemie rozpoznaje się M. tuberculosis complex PCR * Mycobacterium tuberculosis Direct Test (MTD) test (Gen-Probe Inc. San Diego, Ca) – w systemie rozpoznaje się M. tuberculosis complex, M. avium, M. intracellulare, M. kansasii, M. gordonae, r. RNA * BDProbe Tec ET Mycobacterium tuberculosis Complex Direct Detection Assay (SDA - Strand Displacement Amplification); (Becton Dickinson Biosciences, Sparks, Md. ) - rozpoznaje M. tbc complex, M. avium complex oraz M. kansasii SDA
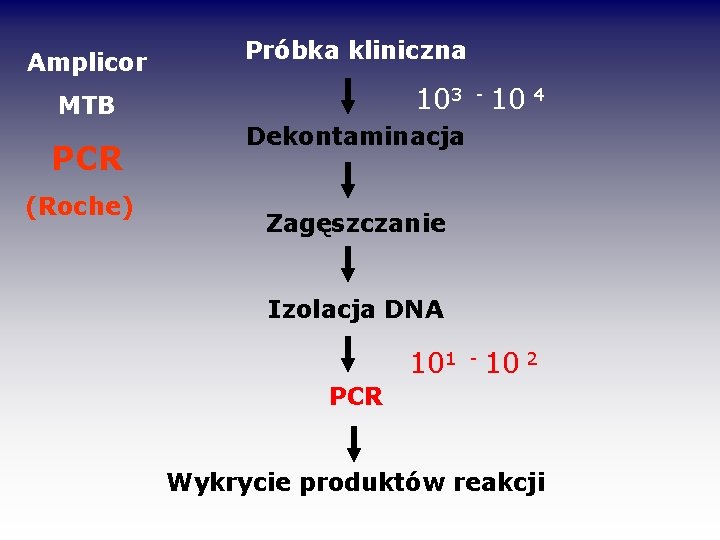
Amplicor Próbka kliniczna 103 - 10 4 MTB PCR (Roche) Dekontaminacja Zagęszczanie Izolacja DNA 101 - 10 2 PCR Wykrycie produktów reakcji

Mycobacterium tuberculosis complex : Mycobacterium tuberculosis Mycobacterium bovis BCG Mycobacterium africanum Mycobacterium microti Do niedawna nierozróżnialne metodami biologii molekularnej dopuszczonymi do diagnostyki rutynowej

Porównanie czułości i czasochłonności metod laboratoryjnych w wykrywaniu gruźlicy metody molekularne 70 – 90 % kilka godz. hodowle mikroskopia 70 % kilka dni - 8 tygodni 30 % 3 godz.
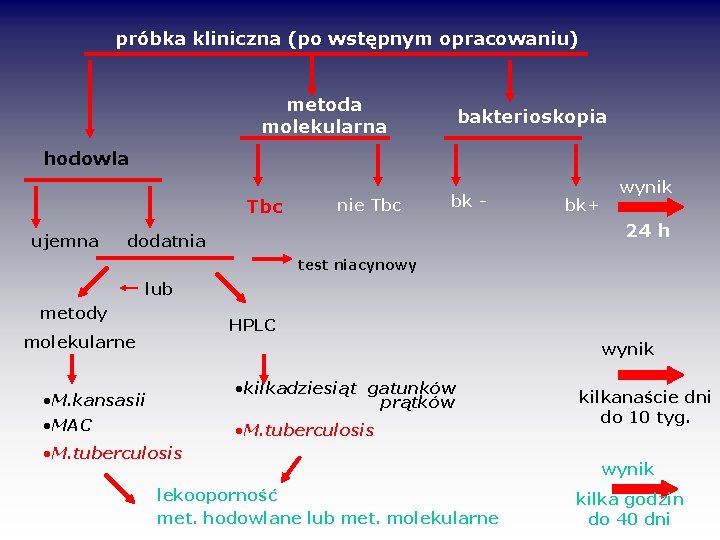
próbka kliniczna (po wstępnym opracowaniu) metoda molekularna bakterioskopia hodowla Tbc ujemna nie Tbc bk - bk+ wynik 24 h dodatnia test niacynowy lub metody HPLC molekularne wynik • M. kansasii • kilkadziesiąt gatunków prątków • MAC • M. tuberculosis lekooporność met. hodowlane lub met. molekularne kilkanaście dni do 10 tyg. wynik kilka godzin do 40 dni

Najczęstsze błędy laboratoryjne lub interpretacyjne w mikrobiologicznej diagnostyce gruźlicy I Jednoznaczna interpretacja mikroskopii bk (+) jako gruźlicy, może być to: * gruźlica * saprofit środowiskowy – (NTM / MOTT) * mykobakterioza * w przypadku materiałów bronchoskop. , zanieczyszczenie instrumentarium

II Brak typowania do gatunku wyrośniętych szczepów prątków - poprzestanie na wykonaniu testu niacynowego różnicujacego jedynie M. tbc oraz MOTT nie pozwala to na: * diagnozowanie mykobakterioz * wykrywanie systematycznych zanieczyszczeń prątkami środowiskowymi

III Zaniechanie wzywania na dodatkowe badania mikrobiologiczne chorych ze wskazaniami klinicznymi, u których wyhodowano prątki niegruźlicze Z tej grupy rekrutują się chorzy na mykobakeriozy

IV Brak systematycznej oceny mikrobiologicznej czystości sprzętu endoskopowego

Immunologiczna diagnostyka zakażenia M. tuberculosis w warunkach in vitro Diagnostyka uśpionych zakażeń M. tbc Latent Tuberculosis Infection - LTBI
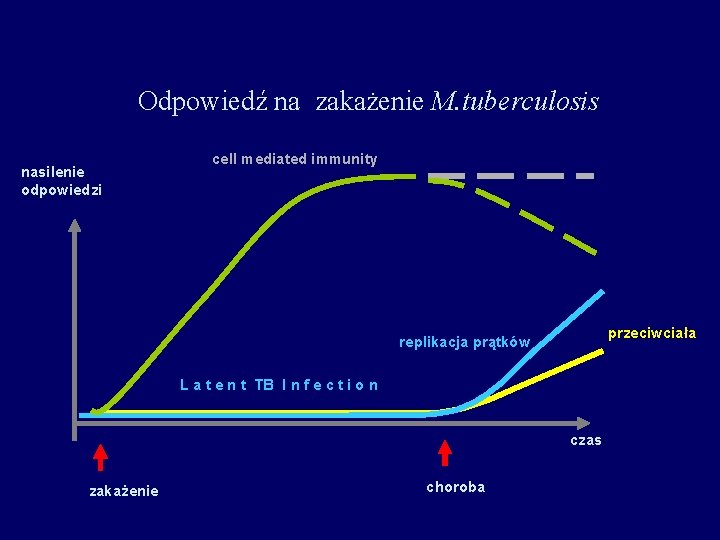
Odpowiedź na zakażenie M. tuberculosis nasilenie odpowiedzi cell mediated immunity przeciwciała replikacja prątków L a t e n t TB I n f e c t i o n czas zakażenie choroba

Zjawisko, które było podstawą współcześnie stosowanego testu tuberkulinowego opisał w 1890 roku Robert Koch, kontynuatorami jego pracy byli Charles Mantoux i Clemens von Pirquet skórny test tuberkulinowy (tuberculin skin test -TST) stosowany jest od 1907 roku.
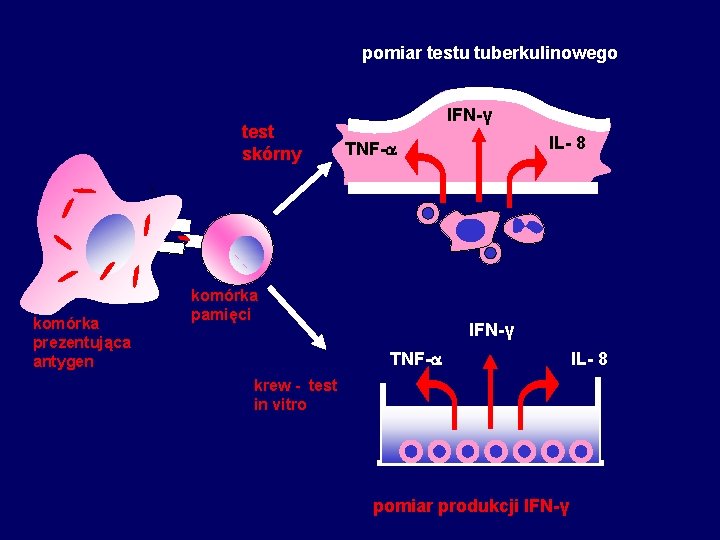
pomiar testu tuberkulinowego test skórny komórka prezentująca antygen IFN-γ IL- 8 TNF- komórka pamięci IFN-γ TNF- krew - test in vitro pomiar produkcji IFN-γ IL- 8

Czynniki negatywizujące TST: o Zależne od osoby badanej infekcje (wirusowe, bakteryjne, grzybicze) zaburzenia metaboliczne niedożywienie choroby narządów limfatycznych(np. . białaczka, sarkoidoza) leki (glikokortykoidy, leki immunosupresyjne) wiek o Zależne od preparatu tuberkulinowego nieodpowieednie rozcieńczenie chemiczna denaturacja adsorpcja na szkle kontaminacja o Zła technika szczepienia o Zła technika odczytu

ekspozycja na M. tbc zakażenie 95 % zakażanie uśpione 95 % nie dochodzi do rozwoju choroby 90% brak dowodów zakażenia 5% gruźlica 5% 5 -10 % wg E. Tortoli 2005

o Postępy immunologii i genomiki ostatnich lat stworzyły test alternatywny dla skórnego testu tuberkulinowego o Jest to test in vitro nowej generacji mierzący poziom odporności komórkowej o Podstawą testu jest oddziaływanie na komórki w warunkach in vitro wysoko swoistych dla M. tuberculosis antygenów ESAT-6 oraz CP-10 stymulujących wydzielanie IFN-gamma

ESAT-6 - early secretory antigenic target 6 CP-10 - culture filtrate protein Antygen ESAT-6 M tuberculosis BCG moreau pasteur tokyo danish glaxo montreal niskocząsteczkowe białka swoiste dla M. tuberculosis NTM CFP-10 + + - - Antygen M abscessus M avium M branderi M celatum M chelonae M fortuitum M gordonae M intracellulare M kansasii M malmoense M marinum M genavense M scrofulaceum M smegmatis M szulgai M terrae M vaccae M xenopi + + + - ESAT-6 + + + -

Quanti. FERON -TB Gold Maj 2005 – test uzyskał aprobatę FDA U. S. Badanie polega na wykrywaniu IFN-gamma w hodowlach limfocytów heparynizowanej, pełnej krwi stymulowanych syntetycznymi peptydami: ESAT-6 (early secretory antigenic target-6) CFP-10 (culture filtrate protein-10) swoistymi dla M. tuberculosis oraz patogennych szczepów M. bovis. Białek ESAT-6 oraz CFP-10 nie stwierdza się w BCG oraz w większości gatunków prątków środowiskowych z wyjątkami M. kansasii, M. szulgai, M. marinum Test jest rekomendowany przez CDC w każdej sytuacji, w której wykonuje się TST włączając gruźlicę oraz kontakty z TB (Latent Tuberculosis Infection -LTBI) CDC MMWR Recomendations and Reports Dec 16, 2005/54 (RR 15; 49 -55)
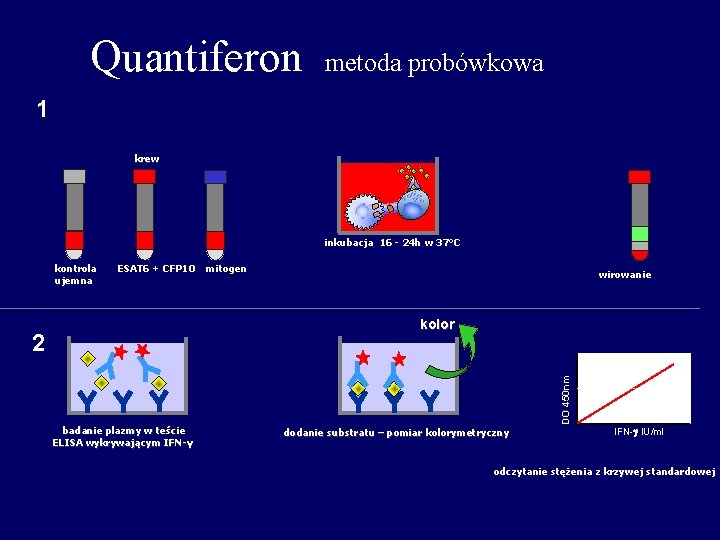
Quantiferon metoda probówkowa 1 krew inkubacja 16 - 24 h w 37°C kontrola ujemna ESAT 6 + CFP 10 mitogen wirowanie 2 badanie plazmy w teście ELISA wykrywającym IFN-γ DO 450 nm kolor dodanie substratu – pomiar kolorymetryczny IFN-g IU/ml odczytanie stężenia z krzywej standardowej

Quantiferon – metoda płytkowa K pobranie krwi ESAT-6 CFP-10 mitogen krew + antygeny inkubacja 24 h , wydzielenie IFN-γ DO 450 nm KOLOR IFN-g IU/ml ‘sandwich’ ELISA, (incubacja 120 min) dodanie substratu, reakcja barwna odczyt stężenia IFNγ z krzywej standardowej
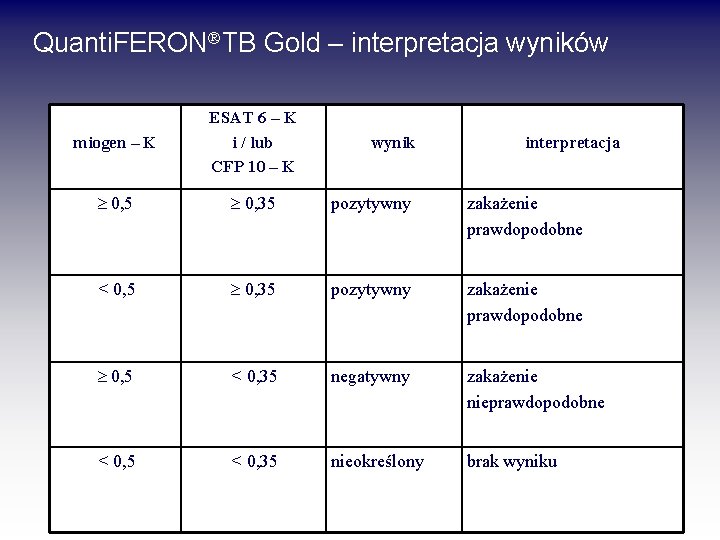
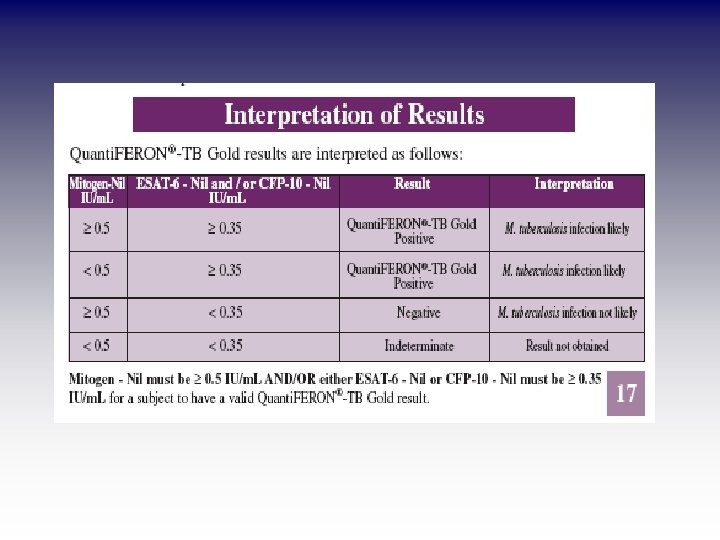
Quanti. FERON TB Gold – interpretacja wyników miogen – K ESAT 6 – K i / lub CFP 10 – K 0, 5 0, 35 pozytywny zakażenie prawdopodobne < 0, 5 0, 35 pozytywny zakażenie prawdopodobne 0, 5 < 0, 35 negatywny zakażenie nieprawdopodobne < 0, 5 IU IFN- γ /ml < 0, 35 nieokreślony brak wyniku wynik interpretacja
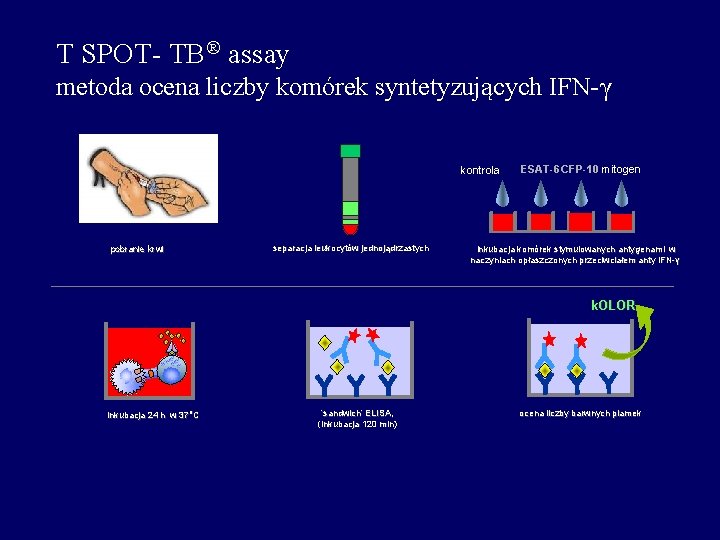
T SPOT- TB assay metoda ocena liczby komórek syntetyzujących IFN-γ kontrola pobranie krwi separacja leukocytów jednojądrzastych ESAT-6 CFP-10 mitogen inkubacja komórek stymulowanych antygenami w naczyniach opłaszczonych przeciwciałem anty IFN-γ k. OLOR inkubacja 24 h w 37 o. C ‘sandwich’ ELISA, (Ink Inkubacja 120 min) ocena liczby barwnych plamek
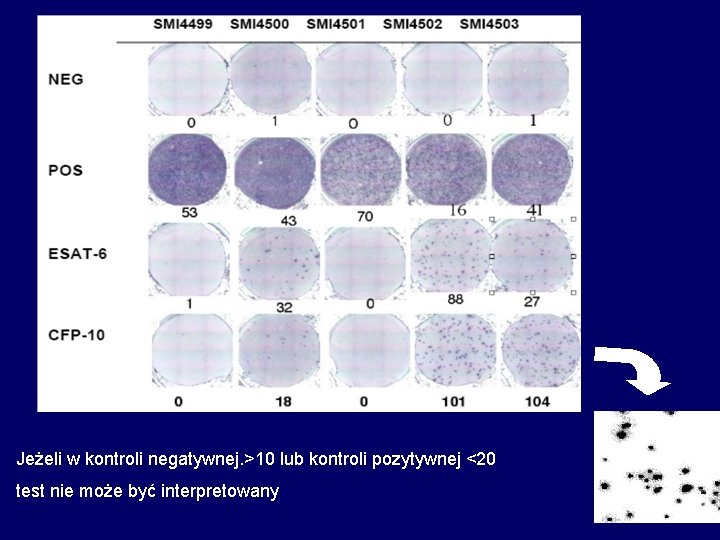
Jeżeli w kontroli negatywnej. >10 lub kontroli pozytywnej <20 test nie może być interpretowany
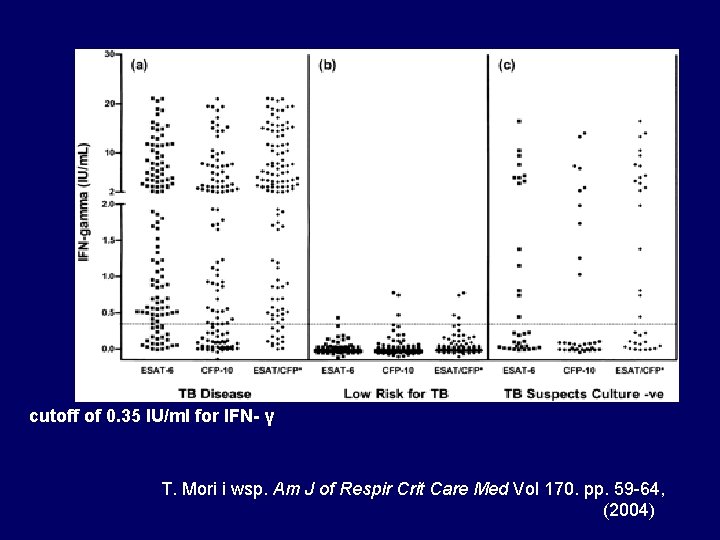
cutoff of 0. 35 IU/ml for IFN- γ T. Mori i wsp. Am J of Respir Crit Care Med Vol 170. pp. 59 -64, (2004)




ekspozycja na M. tbc zakażenie 95 % zakażanie uśpione 95 % nie dochodzi do rozwoju choroby 90% brak dowodów zakażenia 5% gruźlica 5% 5 - 10 % wg E. Tortoli 2005

Quanti. FERON -TB Gold Maj 2005 – test uzyskał aprobatę FDA U. S. Badanie polega na wykrywaniu IFN-gamma w hodowlach limfocytów heparynizowanej, pełnej krwi stymulowanych syntetycznymi peptydami: ESAT-6 (early secretory antigenic target-6) CFP-10 (culture filtrate protein-10) swoistymi dla M. tuberculosis oraz patogennych szczepów M. bovis. Białek ESAT-6 oraz CFP-10 nie stwierdza się w BCG oraz w większości gatunków prątków środowiskowych z wyjątkami M. kansasii, M. szulgai, M. marinum. Test jest rekomendowany przez CDC w każdej sytuacji, w której wykonuje się TST włączając gruźlicę oraz kontakty z TB (LTBI). CDC MMWR Recomendations and Reports Dec 16, 2005/54 (RR 15; 49 -55)
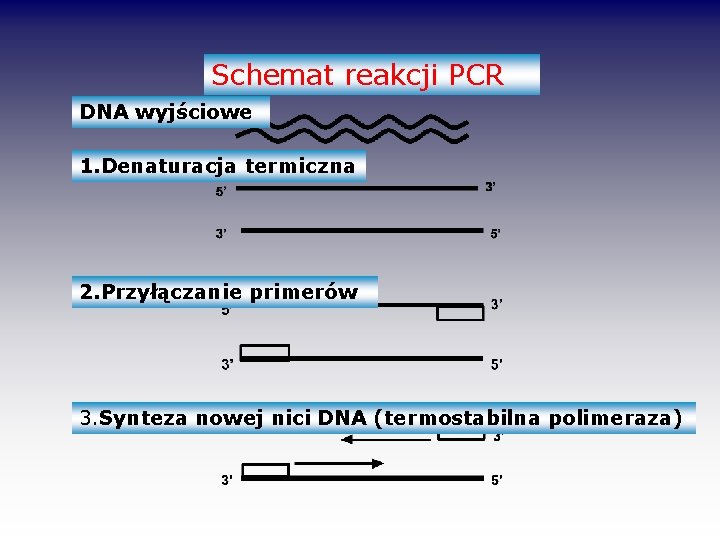
Schemat reakcji PCR DNA wyjściowe 1. Denaturacja termiczna 2. Przyłączanie primerów 3. Synteza nowej nici DNA (termostabilna polimeraza)
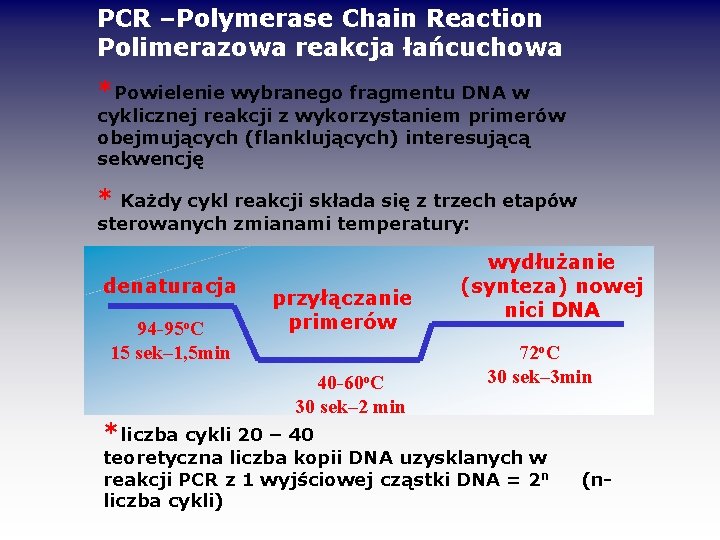
PCR –Polymerase Chain Reaction Polimerazowa reakcja łańcuchowa *Powielenie wybranego fragmentu DNA w cyklicznej reakcji z wykorzystaniem primerów obejmujących (flanklujących) interesującą sekwencję * Każdy cykl reakcji składa się z trzech etapów sterowanych zmianami temperatury: denaturacja 94 -95 o. C 15 sek– 1, 5 min przyłączanie primerów 40 -60 o. C 30 sek– 2 min wydłużanie (synteza) nowej nici DNA 72 o. C 30 sek– 3 min *liczba cykli 20 – 40 teoretyczna liczba kopii DNA uzysklanych w reakcji PCR z 1 wyjściowej cząstki DNA = 2 n liczba cykli) (n-

Wizualizacja wyników testu Amplicor - MTB opiera się na technice ELISA przy użyciu: • biotynylowanych primerów w reakcji PCR • sondy genetycznej wiążącej swoiste DNA • konjugatu awidyna - peroksydaza • substratu tetrametylobenzydyny –TMB • czas wykonania – 5 -8 godzin
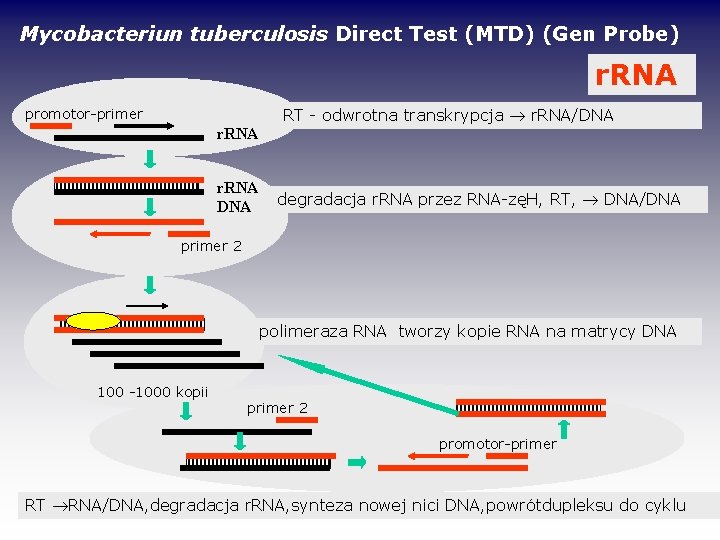
Mycobacteriun tuberculosis Direct Test (MTD) (Gen Probe) r. RNA promotor-primer r. RNA DNA RT - odwrotna transkrypcja r. RNA/DNA degradacja r. RNA przez RNA-zęH, RT, DNA/DNA primer 2 polimeraza RNA tworzy kopie RNA na matrycy DNA 100 -1000 kopii primer 2 promotor-primer RT RNA/DNA, degradacja r. RNA, synteza nowej nici DNA, powrótdupleksu do cyklu

Wizualizacja testu Mycobacteriun tuberculosis Direct Test (MTD) (Gen Probe) opiera się na: * stosowaniu sond DNA znakowanych estrem akrydyny, które wiążą amplikony RNA * odrzuceniu sond niezwiązanych z RNA * odczycie wyników w luminometrze * Czas wykonanie – 6 -8 godzin
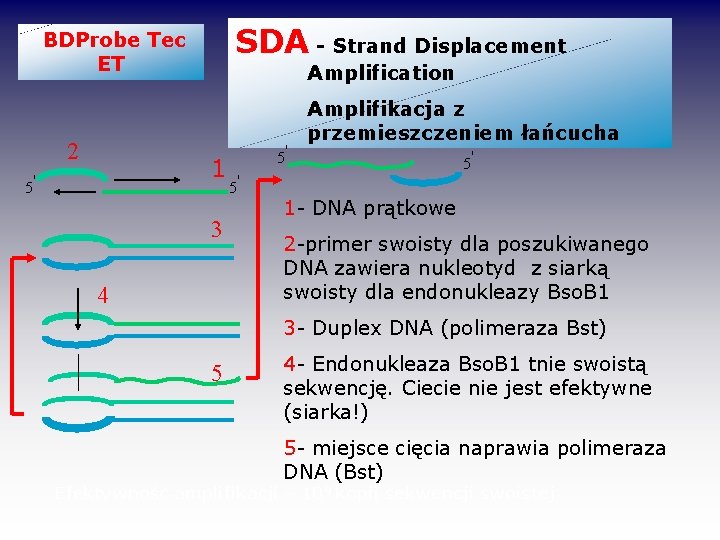
SDA - Strand Displacement BDProbe Tec ET 2 Amplification 1 5' 3 4 5' 5' Amplifikacja z przemieszczeniem łańcucha 5' 1 - DNA prątkowe 2 -primer swoisty dla poszukiwanego DNA zawiera nukleotyd z siarką swoisty dla endonukleazy Bso. B 1 3 - Duplex DNA (polimeraza Bst) 5 4 - Endonukleaza Bso. B 1 tnie swoistą sekwencję. Ciecie nie jest efektywne (siarka!) 5 - miejsce cięcia naprawia polimeraza DNA (Bst) Efektywność amplifikacji – 109 kopii sekwencji swoistej

BD Prob Tec ET(c. d. ) Detekcja produktów amplifikacji w teście odbywa się na zasadzie fluorescencji sonda F 1 +DNA swoiste separacja przestrzenna F 1 i F 2 emisja promieniowania czytnik F 2 przy braku wiązania ze swoistym DNA sygnał pobudzający F 1 przenoszony jest na F 2 (ET), który emituje światło o długości fali nie wykrywanej przez czytnik Zaletą systemu jest, że amplifikacja i detekcja (na zasadzie fluorescencji) odbywa się w stałej temperaturze * System ma wewnętrzną kontrolę pozytywną * Całkowity czas wykonania testu wynosi około 140 min. * Czułość 9 CFU/reakcję (125 CFU/ml)

Amplicor MTB W badaniu 900 próbek klinicznych, w których uzyskano wynik ujemny w badaniu molekularnym (PCR-MTB), w 12 przypadkach (1, 7 %) uzyskano wzrost prątków M. tuberculosis w hodowli na pożywce L-J 12 przypadków gruźlicy / 900 wyników PCR (-) Katedra i Klinika Chorób Wewnętrznych, Pneumonologii i Alergologii AM badania diagnostyczne w okresie: marzec 1999 - wrzesień 2003
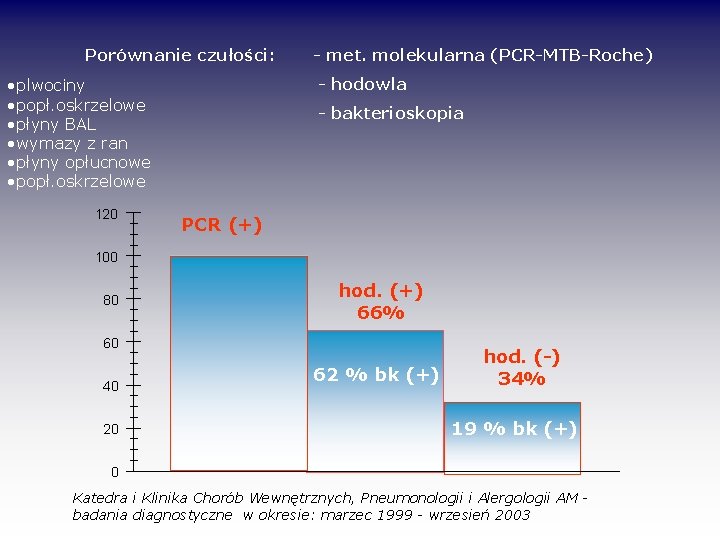
Porównanie czułości: - hodowla • plwociny • popł. oskrzelowe • płyny BAL • wymazy z ran • płyny opłucnowe • popł. oskrzelowe 120 - met. molekularna (PCR-MTB-Roche) - bakterioskopia PCR (+) 100 80 hod. (+) 66% 60 40 20 62 % bk (+) hod. (-) 34% 19 % bk (+) 0 Katedra i Klinika Chorób Wewnętrznych, Pneumonologii i Alergologii AM badania diagnostyczne w okresie: marzec 1999 - wrzesień 2003

czułość i swoistość testów molekularnych w diagnostyce gruźlicy czułość */ 70 – 90 % swoistość*/ 97 – 100 % */ w odniesieniu do hodowli dodatnich
- Slides: 77