Gorce Amandine Kervarec Elodie Perrier LiseMarine FHE Fivre




















- Slides: 23

Gorce Amandine Kervarec Elodie Perrier Lise-Marine FHE Fièvre Hémorragique Virus Ebola Travaux personnels P 4 Virologie

SOMMAIRE I. Caractères généraux – Structure II. Historique III. Épidémiologie IV. Pouvoir pathogène V. Diagnostic biologique VI. Traitement VII. Prévention VIII. Conclusion Bibliographie

• Ébola vient du nom d'une rivière passant près de la ville de Yambuku en République Démocratique du Congo. Lieu de la 1ère identification du filovirus lors d'une épidémie qui débuta en septembre 1976. • Fièvre Ébola = fièvre hémorragique foudroyante touchant l'homme et les primates. • Apparition récente chez l'homme (premier cas recensé en 1976) bien que l'on retrouve chez certaines populations africaines des traces d'anticorps.

I. Caractères généraux - structure A. Classification • Famille : Filoviridae • Ordre : mononegavirales • Genre : filovirus • Plusieurs sous-types : -Ebola Zaïre - Ebola Soudan - Ebola Reston - Ebola Cote d’Ivoire

I. Caractères généraux - structure B. Structure • Morphologie : ü Virions filamenteux quelques fois avec des ramifications : certains peuvent être en forme de U, de chiffres 6 ou circulaires ü 80 nm de diamètre, uniforme, et jusqu’à 14 000 nm de longueur, l’unité infectieuse est de 970 nm.

I. Caractères généraux - structure • B. Structure • Enveloppe : dérivée de la membrane cytoplasmique où est insérée la glycoprotéine • Nucléocapside : axe central entourée d’une capside tubulaire hélicoïdale Nucléocapside ARN enveloppe

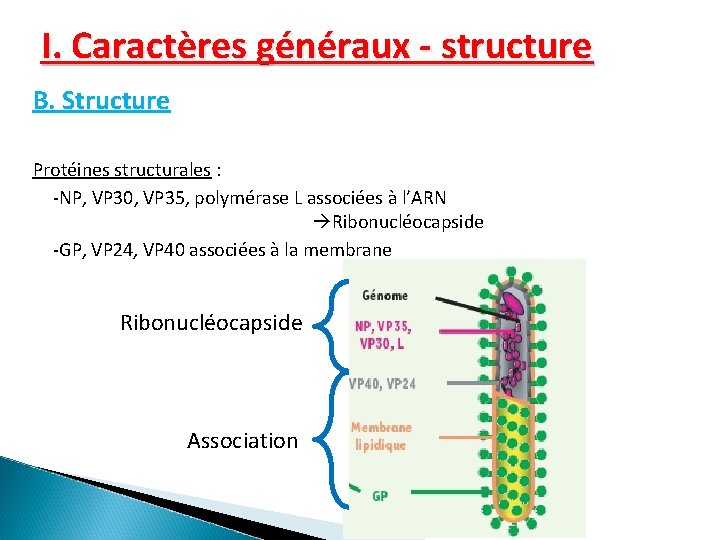
I. Caractères généraux - structure B. Structure Protéines structurales : -NP, VP 30, VP 35, polymérase L associées à l’ARN Ribonucléocapside -GP, VP 24, VP 40 associées à la membrane Ribonucléocapside Association

I. Caractères généraux - structure B. Structure • Génome ü GP=Glycoprotéine transmembranaire ü NP=Nucléoprotéine nécessaire à l’assemblage de la capside ü VP 24=Inhibiteur antiviral ü VP 35=Inhibe la production de IFN ü VP 30=Transcription anti-terminator ü VP 40=Nécessaire pour assemblage et bourgeonnement de la capside ü L-Viral Polymérase

I. Caractères généraux - structure B. Structure • Génome : ü ARN simple brin de polarité négative ü non segmenté et enveloppé ü 19, 1 kb ü la réplication n’est pas encore connue. • Multiplication : dans le cytoplasme, assemblage par bourgeonnement à travers les membranes intra cytoplasmiques et libération du virus par fusion, exocytose et lyse cellulaire.

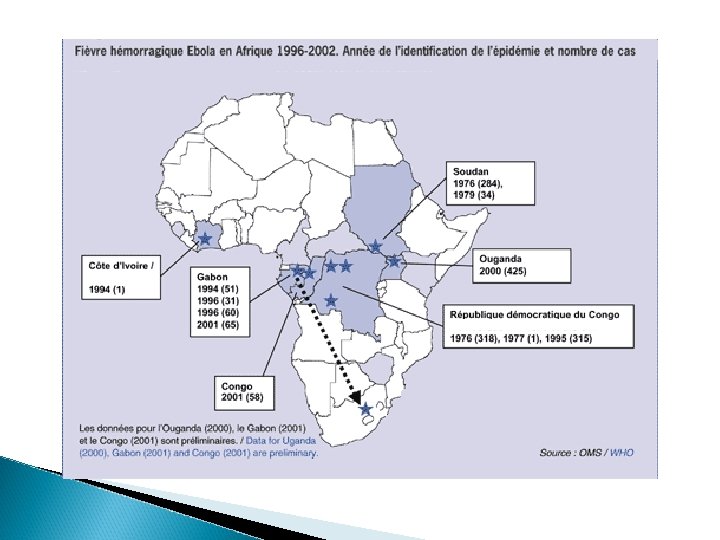
II. Historique • 1976 : 1ère épidémie (Zaïre: Yambuku) : 88 % mortalité • 1976 : épidémie au Soudan : 53% mortalité • 1979 : épidémie au Soudan • 1989 : isolement d’un virus apparenté • 1994 : contamination d’un primatologue avec un singe de Cote d’Ivoire • 1995 : épidémie au Zaïre • 1996 - 2008 : contaminations au Gabon, Ouganda, Zaïre, Soudan


III. Epidémiologie A. Habitat • • Zaïre, Soudan, Congo, Gabon Contagieux +++ B. Hôte • L’humain, singes, chimpanzés, cobayes domestiques

III. Epidémiologie C. Transmission • Contact direct avec singe infecté vivant ou mort • Interhumaine - Nosocomiale - Contact direct et non protégé : sang, urines, selles, vomissures, sueur - Contact direct: malade infecté ayant passé la phase d’incubation et présentant les signes cliniques

III. Epidémiologie D. Dissémination • Réservoir : le réservoir naturel est inconnu • Zoonose : probablement transmis par les animaux. Cause la maladie chez les primates non humains. • Vecteurs : inconnu

IV. Pouvoir pathogène Durée d'incubation : 2 21 jours Durée de la maladie : 6 10 jours (formes mortelles) • Quelques jours après l'infection la fièvre hémorragique d’Ebola se manifeste par : vune brusque montée de température vfatigue vdouleurs musculaires vcéphalées vdes maux de gorge.

IV. Pouvoir pathogène • Puis rapidement : vdouleurs abdominales, nausées, vomissements et diarrhée vpharyngite se compliquant d’ulcérations des lèvres et de la langue causant une dysphagie. • Malade rapidement asthénique avec amaigrissement

IV. Pouvoir pathogène • Au 5ème jour : éruptions maculopapuleuses sur tronc, face et bras manifestations hémorragiques atteinte foie, pancréas, reins par nécrose (+ SNC et cœur) ainsi que leucopénie, thrombocytopénie, élévation des transaminases. • La fièvre peut disparaître à la phase terminale 14ème jour. • Convalescence longue (+arthralgies, orchite, uvéite) • Décès dans les 5 à 8 jours précédé par tachypnée, hypotension, tachycardie, anurie.

V. Diagnostic biologique A. Diagnostic direct • • Culture virale (cellules Vero) - confirmer par IF Recherche du génome viral par RT-PCR Recherche d’antigènes viraux par ELISA (sang) Microscopie électronique B. Diagnostic indirect • Recherche d’Anticorps spécifiques par ELISA

VI. Traitement • Aucun traitement ni vaccin spécifique • Traitement symptomatique : dans les cas graves üréhydrater pour maintenir fonction rénale et équilibre électrolytique ücombattre hémorragie et état de choc üprévenir surinfections. • Sérothérapie non validée • Déclaration des fièvres hémorragiques obligatoire auprès des autorités sanitaires

VII. Prévention • Perspectives futures : immunité efficace sur des animaux vaccin à base de gènes du virus développer un vaccin chez les primates • Protections du niveau 4 + décontamination de l'air, habits imperméables, portes étanches à l'air, douches chimiques de décontamination • Prévention des épidémies (hospitalière) : détection précoce des cas initiaux + mise en place rapide des mesures d’isolement et de protection du personnel

VII. Prévention • Les morts doivent être rapidement enterrés ou incinérés. • L’absence de réservoir animal connu et identifiable rend impossible la prévention des cas primaires. • Mesures de quarantaine lors de l’importation des primates

VIII. Conclusion • Existe depuis des millions d'années • Ne peut vivre en milieu libre + impossibilité de coloniser aisément de nouvelles espèces d'hôtes • Risques faibles pour la population humaine sauf là où coexistent une possibilité de contamination primaire, de mauvaises conditions d'hygiène et des structures sociales perturbées. • Recherches avancent lentement • Structure moléculaire + mode de réplication du virus commence à être connus • Principal but: identifier dans la nature son hôte naturel

Bibliographie � Que sais-je ? les virus émergents de Antoine Gessain et Jean claude Manuguerra � Virologie médicale de R. Crainic et J. C. Nicolas � Classification et nomenclature des virus (Cinquième rapport du Comité International de Taxonomie des Virus) de R. I. B. Francki, C. M. Fauquet , D. L. Knudson, F. Brown � De la biologie à la clinique : Virologie de J-M. Huraux, J. C. Nicolas et Henri Agut � Traité de virologie médicale de J-M Huraux, J. C. Nicolas, Henri Agut et Hélène Peigue. Lafeuille � � Techniques de base : Virus et diagnostic virologique de P. Ardoin Abrégés : Virologie humaine de HJA Fleury