GOLONGAN IIA beryllium magnesium calcium strontium barium radium

GOLONGAN IIA beryllium magnesium calcium strontium barium radium

KELOMPOK 2 KELAS XII IPA 1 1. Fitra Turrizkiyah 2. Muhammad Miqdad 3. Nur’aini Diah Anisah 4. Rahmatia Miralena

A. Pengertian Alkali Tanah Unsur-unsur golongan IIA disebut juga Alkali Tanah sabab unsur tersebut bersifat basa dan banyak di temukan dalam mineral tanah. Logam alkali tanah umumnya relatif, tetapi kurang relatif jika dibandingkan dengan logam alkali. Namun dengan 2 elektron valensi yangdimilikinya logam alkali tanah pun mudah melepaskan elektronnya membentuk senyawa dengan tingkat oksidasi +2. Disebut logam karena memiliki sifat seperti logam. Disebt alkali karena mempunyai sifat alkai atau basa jika di reaksikan dengan air. Dan istilah tanah karena oksidasinya sukar larut dalam air, dan banyak di temukan dalam bebatuan di kerak bumi. Adapun elemen dalam golongan alkali tanah adalah logam yang mengilap, warna putih keperakan. Logam Alkali tanah yang tinggi dalam rangkaian reaktiitas logam, tapi tidak setinggi logam alkali.

B. Sifat Periodik Unsur 1. Jari-Jari Atom adalah jarak dari inti atom sampai ke elektron di kulit terluar. Besarnya jari-jari atom dipengaruhi oleh besarnya nomor atom unsur tersebut. Semakin besar nomor atom unsur-unsur segolongan, semakin banyak pula jumlah kulit elektronnya, sehingga semakin besar pula jari-jari atomnya. Jadi, dalam satu golongan (dari atas ke bawah), jari-jari atomnya semakin besar. Dalam satu periode (dari kiri ke kanan), nomor atomnya bertambah yang berarti semakin bertambahnya muatan inti, sedangkan jumlah kulit elektronnya tetap. Akibatnya tarikan inti terhadap elektron terluar makin besar, sehingga menyebabkan semakin kecilnya jari-jari atom. 2. Jari-Jari Ion mempunyai jari-jari yang berbeda secara nyata jika dibandingkan dengan jari-jari atom normalnya. Ion bermuatan positif (kation) mempunyai jari-jari yang lebih kecil, sedangkan ion bermuatan negatif (anion) mempunyai jari-jari yang lebih besar jika dibandingkan dengan jari-jari atom normalnya. 3. Energi Ionisasi (EI) adalah energi yang diperlukan atom dalam untuk melepaskan satu elektron sehingga membentuk ion bermuatan +1. Jika atom tersebut melepaskan elektronnya yang ke-2 maka akan diperlukan energi yang lebih besar, begitu juga pada pelepasan elektron yang ke-3 dan seterusnya. Maka EI 1<> 4. Afinitas Elektron adalah energi yang dilepaskan oleh atom apabila menerima sebuah elektron untuk membentuk ion negatif. Semakin negatif harga afinitas elektron, semakin mudah atom tersebut menerima elektron dan unsurnya akan semakin reaktif. Dalam satu golongan (dari atas ke bawah), harga afinitas elektronnya semakin kecil. Dan dalam satu periode (dari kiri ke kanan), harga afinitas elektronnya semakin besar. Unsur golongan utama memiliki afinitas elektron bertanda negatif, kecuali golongan IIA dan VIIIA. Afinitas elektron terbesar dimiliki oleh golongan VIIA.

5. Keelektronegatifan adalah kemampuan suatu unsur untuk menarik elektron dalam molekul suatu senyawa. Harga keelektronegatifan ini diukur dengan menggunakan skala Pauling yang besarnya antara 0, 7 sampai 4. Unsur yang mempunyai harga keelektronegatifan besar, cenderung menerima elektron dan akan membentuk ion negatif. Sedangkan unsur yang mempunyai harga keelektronegatifan kecil, cenderung melepaskan elektron dan akan membentuk ion positif. Dalam satu golongan (dari atas ke bawah), harga keelektronegatifan semakin kecil. Dan dalam satu periode (dari kiri ke kanan), harga keelektronegatifan semakin besar. 6. Sifat Logam dan Non Logam. Sifat logam berhubungan dengan keelektropositifan, yaitu kecenderungan atom untuk melepaskan elektron membentuk kation. Sifat logam bergantung pada besarnya energi ionisasi (EI). Makin besar harga EI, makin sulit bagi atom untuk melepaskan elektron dan makin berkurang sifat logamnya. Sifat non logam berhubungan dengan keelektronegatifan, yaitu kecenderungan atom untuk menarik elektron. Dalam satu periode (dari kiri ke kanan), sifat logam berkurang sedangkan sifat non logam bertambah. Dalam satu golongan (dari atas ke bawah), sifat logam bertambah sedangkan sifat non logam berkurang. Unsur logam terletak pada bagian kiri-bawah dalam sistem periodik unsur, sedangkan unsur non logam terletak pada bagian kanan-atas. Unsur-unsur yang terletak pada daerah peralihan antara unsur logam dengan non logam disebut unsur metaloid. Metalloid adalah unsur yang mempunyai sifat logam dan non logam. 7. Kereaktifan bergantung pada kecenderungan unsur untuk melepas atau menarik elektron. Dalam satu periode (dari kiri ke kanan), mula-mula kereaktifan menurun, tapi akan semakin bertambah hingga golongan alkali tanah (VIIA). Unsur golongan ini bersifat basa, sama seperti unsur golongan alkali, namun tingkat kebasaannya lebih lemah. Senyawa Be(OH)2 bersifat amfoter. Artinya bisa bersifat asam atau pun basa. Sedangkan unsur Ra bersifat Radioaktif. Semua logam alkali tanah merupakan logam yang tergolong reaktif, meskipun kurang reaktif dibandingkan dengan unsur alkali. Alkali tanah juga memiliki sifat relatif lunak dan dapat menghantarkan panas dan listrik dengan baik, kecuali Berilium. Logam ini juga memiliki kilapan logam.
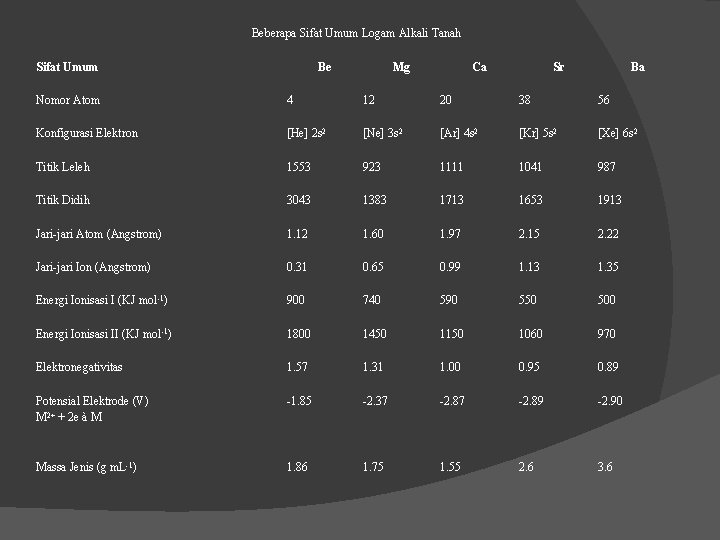
Beberapa Sifat Umum Logam Alkali Tanah Sifat Umum Be Mg Ca Sr Ba Nomor Atom 4 12 20 38 56 Konfigurasi Elektron [He] 2 s 2 [Ne] 3 s 2 [Ar] 4 s 2 [Kr] 5 s 2 [Xe] 6 s 2 Titik Leleh 1553 923 1111 1041 987 Titik Didih 3043 1383 1713 1653 1913 Jari-jari Atom (Angstrom) 1. 12 1. 60 1. 97 2. 15 2. 22 Jari-jari Ion (Angstrom) 0. 31 0. 65 0. 99 1. 13 1. 35 Energi Ionisasi I (KJ mol-1) 900 740 590 550 500 Energi Ionisasi II (KJ mol-1) 1800 1450 1150 1060 970 Elektronegativitas 1. 57 1. 31 1. 00 0. 95 0. 89 Potensial Elektrode (V) M 2+ + 2 e à M -1. 85 -2. 37 -2. 89 -2. 90 Massa Jenis (g m. L-1) 1. 86 1. 75 1. 55 2. 6 3. 6

Berdasarkan Tabel diatas dapat diamati juga hal-hal sebagai berikut : Ø Konfigurasi elektronnya menunjukan bahwa logam alkali tanah mempunyai elektron valensi ns 2. Selain jari-jari atomnya yang lebih kecil dibandingkan logam alkali, kedua elektron valensinya yang telah berpasangan mengakibatkan energi ionisasi logam alkali tanah lebih tinggi daripada alkali. Ø Meskipun energi ionisasinya tinggi, tetapi karena energi hidrasi dari ion M 2+ dari alkali tanah lebih besar daripada energi hidrasi ion M+ dari alkali, mengakibatkan logam alkali tetap mudah melepaskan kedua electron valensinya, sehingga lebih stabil sebagai ion M 2+. Ø Jari-jari atomnya yang lebih kecil dan muatan intinya yang lebih besar mengakibatkan logam alkali tanah membentuk kristal dengan susunan yang lebih rapat, sehingga mempunyai sifat yang lebih keras daripada logam alkali dan massa jenisnya lebih tinggi. Ø Berilium mempunyai energi ionisasi yang sangat tinggi dan keelektronegatifan yang cukup besar, kedua hal ini menyebabkan berilium dalam berikatan cenderung membentuk ikatan kovalen. Ø Potensial elektrode (reduki) standar logam alkali tanah menunjukkan harga yang rendah (negatif). Hal ini menunjukkan bahwa logam alkali tanah merupakan reduktor yang cukup kuat, bahkan kalsium, stronsium, dan barium mempunyai daya reduksi yang lebih kuat daripada natrium. Ø Titik didih dan titik leleh logam alkali tanah lebih tinggi daripada suhu ruangan. Oleh karena itu, unsur-unsur logam alkali tanah berwujud padat pada suhu ruangan.

SIFAT FISIKA ALKALI TANAH 1. Be (Berilium) Nama, Lambang, Nomor atom : Berilium, Be, 4 Deret kimia : Logam alkali tanah Golongan, Periode, Blok : 2, 2, s Penampilan : Putih-kelabu metalik Massa atom : 9, 012182(3) g/mol Konfigurasi electron : 1 s 2 2 s 2 Jumlah elektron tiap kulit : 2, 2 CIRI-CIRI FISIK Fase : padat Massa jenis (sekitar suhu kamar) : 1, 85 g/cm³ Massa jenis cair pada titik lebur : 1, 690 g/cm³ Titik lebur : 1560 K (1287 °C, 2349 °F) Titik didih : 2742 K (2469 °C, 4476 °F) Kalor peleburan : 7, 895 k. J/mol Kalor penguapan : 297 k. J/mol Kapasitas kalor : (25 °C) 16, 443 J/(mol • K) Tekanan uap : P/Pa 1 10 100 1 k 100 k pada T/K 1462 1608 1791 2023 2327 2742
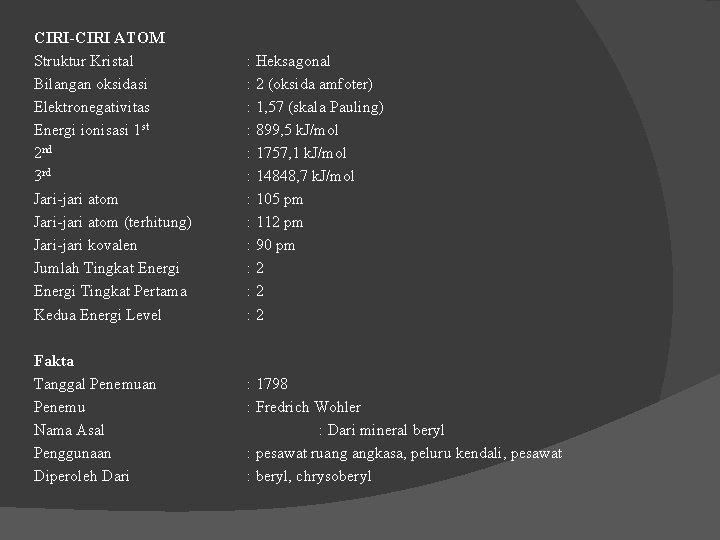
CIRI-CIRI ATOM Struktur Kristal Bilangan oksidasi Elektronegativitas Energi ionisasi 1 st 2 nd 3 rd Jari-jari atom (terhitung) Jari-jari kovalen Jumlah Tingkat Energi Tingkat Pertama Kedua Energi Level : Heksagonal : 2 (oksida amfoter) : 1, 57 (skala Pauling) : 899, 5 k. J/mol : 1757, 1 k. J/mol : 14848, 7 k. J/mol : 105 pm : 112 pm : 90 pm : 2 : 2 Fakta Tanggal Penemuan Penemu Nama Asal Penggunaan Diperoleh Dari : 1798 : Fredrich Wohler : Dari mineral beryl : pesawat ruang angkasa, peluru kendali, pesawat : beryl, chrysoberyl

2. Magnesium (Mg) Nama, Lambang, Nomor atom Deret kimia Golongan, Periode, Blok Penampilan Massa atom Konfigurasi electron Jumlah elektron tiap kulit : magnesium, Mg, 12 : alkali tanah : 2, 3, s : putih keperakan : 24. 3050(6) g/mol : [Ne] 3 s 2 : 2, 8, 2 CIRI-CIRI FISIK Fase : padat Massa jenis (sekitar suhu kamar) : 1. 738 g/cm³ Massa jenis cair pada titik lebur : 1. 584 g/cm³ Titik lebur : 923 K (650 °C, 1202 °F) Titik didih : 1363 K (1090 °C, 1994 °F) Kalor peleburan : 8. 48 k. J/mol Kalor penguapan : 128 k. J/mol Kapasitas kalor : (25 °C) 24. 869 J/(mol • K) Tekanan uap : P/Pa 1 10 100 1 k 100 k pada T/K 701 773 861 971 1132 1361
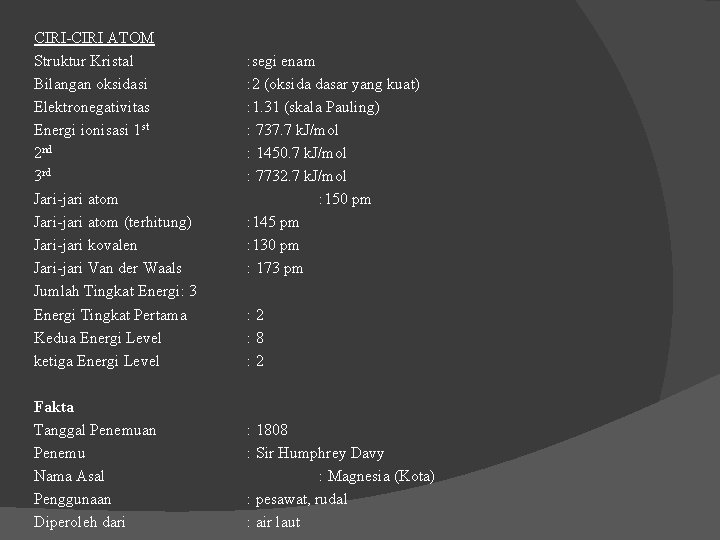
CIRI-CIRI ATOM Struktur Kristal Bilangan oksidasi Elektronegativitas Energi ionisasi 1 st 2 nd 3 rd Jari-jari atom (terhitung) Jari-jari kovalen Jari-jari Van der Waals Jumlah Tingkat Energi: 3 Energi Tingkat Pertama Kedua Energi Level ketiga Energi Level Fakta Tanggal Penemuan Penemu Nama Asal Penggunaan Diperoleh dari : segi enam : 2 (oksida dasar yang kuat) : 1. 31 (skala Pauling) : 737. 7 k. J/mol : 1450. 7 k. J/mol : 7732. 7 k. J/mol : 150 pm : 145 pm : 130 pm : 173 pm : 2 : 8 : 2 : 1808 : Sir Humphrey Davy : Magnesia (Kota) : pesawat, rudal : air laut
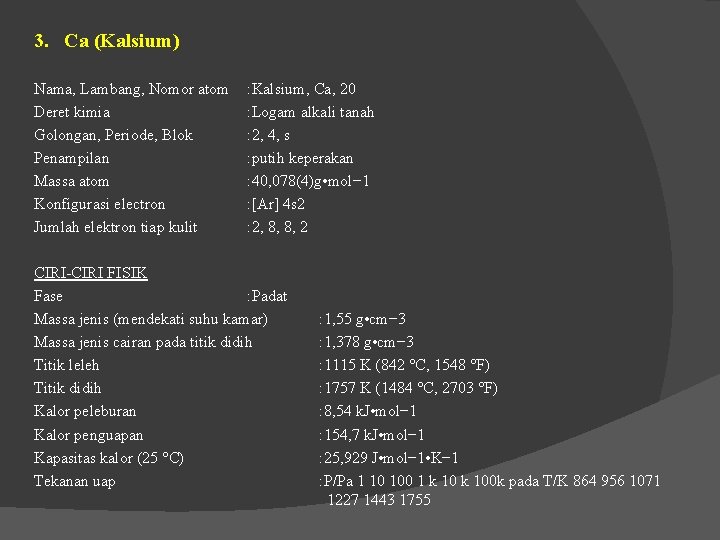
3. Ca (Kalsium) Nama, Lambang, Nomor atom Deret kimia Golongan, Periode, Blok Penampilan Massa atom Konfigurasi electron Jumlah elektron tiap kulit : Kalsium, Ca, 20 : Logam alkali tanah : 2, 4, s : putih keperakan : 40, 078(4)g • mol− 1 : [Ar] 4 s 2 : 2, 8, 8, 2 CIRI-CIRI FISIK Fase : Padat Massa jenis (mendekati suhu kamar) Massa jenis cairan pada titik didih Titik leleh Titik didih Kalor peleburan Kalor penguapan Kapasitas kalor (25 °C) Tekanan uap : 1, 55 g • cm− 3 : 1, 378 g • cm− 3 : 1115 K (842 °C, 1548 °F) : 1757 K (1484 °C, 2703 °F) : 8, 54 k. J • mol− 1 : 154, 7 k. J • mol− 1 : 25, 929 J • mol− 1 • K− 1 : P/Pa 1 10 100 1 k 100 k pada T/K 864 956 1071 1227 1443 1755
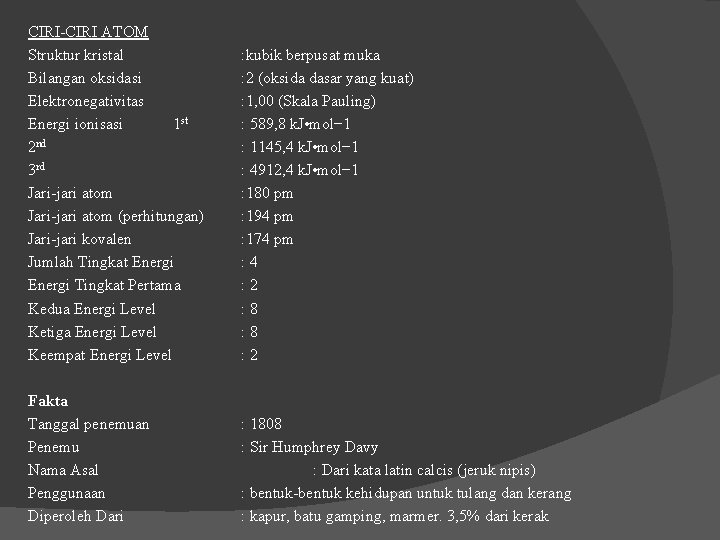
CIRI-CIRI ATOM Struktur kristal Bilangan oksidasi Elektronegativitas Energi ionisasi 1 st 2 nd 3 rd Jari-jari atom (perhitungan) Jari-jari kovalen Jumlah Tingkat Energi Tingkat Pertama Kedua Energi Level Ketiga Energi Level Keempat Energi Level : kubik berpusat muka : 2 (oksida dasar yang kuat) : 1, 00 (Skala Pauling) : 589, 8 k. J • mol− 1 : 1145, 4 k. J • mol− 1 : 4912, 4 k. J • mol− 1 : 180 pm : 194 pm : 174 pm : 4 : 2 : 8 : 2 Fakta Tanggal penemuan Penemu Nama Asal Penggunaan Diperoleh Dari : 1808 : Sir Humphrey Davy : Dari kata latin calcis (jeruk nipis) : bentuk-bentuk kehidupan untuk tulang dan kerang : kapur, batu gamping, marmer. 3, 5% dari kerak
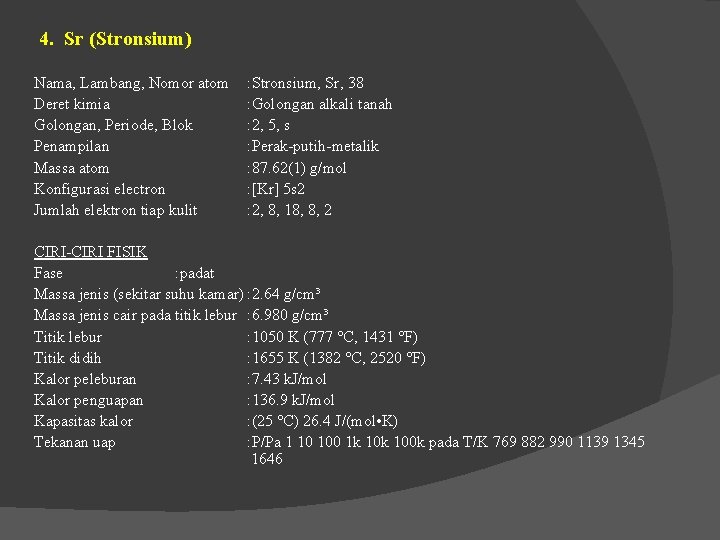
4. Sr (Stronsium) Nama, Lambang, Nomor atom Deret kimia Golongan, Periode, Blok Penampilan Massa atom Konfigurasi electron Jumlah elektron tiap kulit : Stronsium, Sr, 38 : Golongan alkali tanah : 2, 5, s : Perak-putih-metalik : 87. 62(1) g/mol : [Kr] 5 s 2 : 2, 8, 18, 8, 2 CIRI-CIRI FISIK Fase : padat Massa jenis (sekitar suhu kamar) : 2. 64 g/cm³ Massa jenis cair pada titik lebur : 6. 980 g/cm³ Titik lebur : 1050 K (777 °C, 1431 °F) Titik didih : 1655 K (1382 °C, 2520 °F) Kalor peleburan : 7. 43 k. J/mol Kalor penguapan : 136. 9 k. J/mol Kapasitas kalor : (25 °C) 26. 4 J/(mol • K) Tekanan uap : P/Pa 1 10 100 1 k 100 k pada T/K 769 882 990 1139 1345 1646
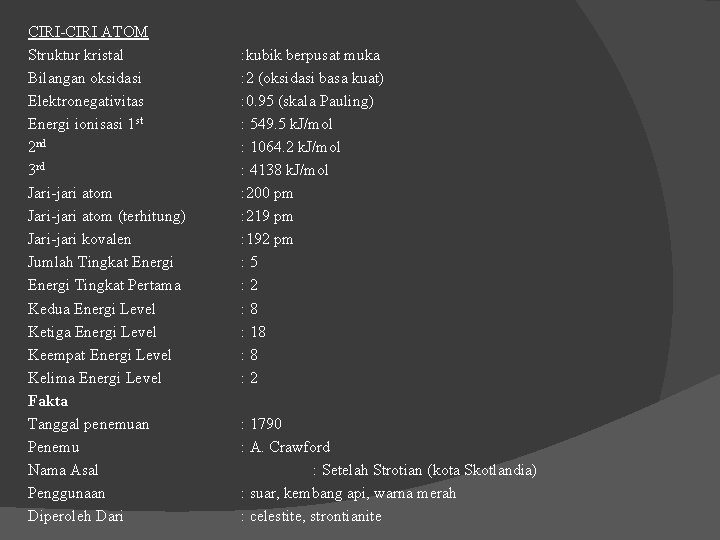
CIRI-CIRI ATOM Struktur kristal Bilangan oksidasi Elektronegativitas Energi ionisasi 1 st 2 nd 3 rd Jari-jari atom (terhitung) Jari-jari kovalen Jumlah Tingkat Energi Tingkat Pertama Kedua Energi Level Ketiga Energi Level Keempat Energi Level Kelima Energi Level Fakta Tanggal penemuan Penemu Nama Asal Penggunaan Diperoleh Dari : kubik berpusat muka : 2 (oksidasi basa kuat) : 0. 95 (skala Pauling) : 549. 5 k. J/mol : 1064. 2 k. J/mol : 4138 k. J/mol : 200 pm : 219 pm : 192 pm : 5 : 2 : 8 : 18 : 2 : 1790 : A. Crawford : Setelah Strotian (kota Skotlandia) : suar, kembang api, warna merah : celestite, strontianite
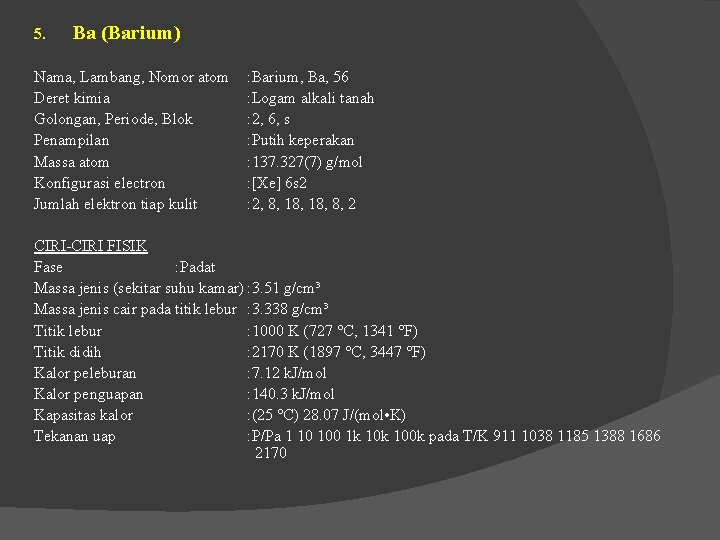
5. Ba (Barium) Nama, Lambang, Nomor atom Deret kimia Golongan, Periode, Blok Penampilan Massa atom Konfigurasi electron Jumlah elektron tiap kulit : Barium, Ba, 56 : Logam alkali tanah : 2, 6, s : Putih keperakan : 137. 327(7) g/mol : [Xe] 6 s 2 : 2, 8, 18, 8, 2 CIRI-CIRI FISIK Fase : Padat Massa jenis (sekitar suhu kamar) : 3. 51 g/cm³ Massa jenis cair pada titik lebur : 3. 338 g/cm³ Titik lebur : 1000 K (727 °C, 1341 °F) Titik didih : 2170 K (1897 °C, 3447 °F) Kalor peleburan : 7. 12 k. J/mol Kalor penguapan : 140. 3 k. J/mol Kapasitas kalor : (25 °C) 28. 07 J/(mol • K) Tekanan uap : P/Pa 1 10 100 1 k 100 k pada T/K 911 1038 1185 1388 1686 2170

CIRI-CIRI ATOM Struktur kristal Bilangan oksidasi Elektronegativitas Energi ionisasi 1 st 2 nd 3 rd Jari-jari atom (terhitung) Jari-jari kovalen Jumlah Tingkat Energi Tingkat Pertama Kedua Energi Level Ketiga Energi Level Keempat Energi Level Kelima Energi Level Keenam Energi Level Fakta Tanggal Discovery Penemu Nama Asal Penggunaan Diperoleh Dari : Kubik berpusat badan : 2 (oksidasi dasar yang kuat) : 0. 89 (skala Pauling) : 502. 9 k. J/mol : 965. 2 k. J/mol : 3600 k. J/mol : 215 pm : 253 pm : 198 pm : 6 : 2 : 8 : 18 : 2 : 1808 : Sir Humphrey Davy : Dari kata Yunani barys (berat) : Kedokteran aplikasi : barytine, whiterite

6. Ra (Radium) Nama, Lambang, Nomor atom Deret kimia Golongan, Periode, Blok Penampilan Massa atom Konfigurasi electron Jumlah elektron tiap kulit : Radium, Ra, 88 : alkali tanah : 2, 7, s : metalik putih keperak-perakan : 226 g/mol : [Rn] 7 s 2 : 2, 8, 18, 32, 18, 8, 2 CIRI-CIRI FISIK Fase : padat Massa jenis (sekitar suhu kamar) : 5, 5 g/cm³ Titik lebur : 973 K (700 °C, 1292 °F) Titik didih : 2010 K (1737 °C, 3159 °F) Kalor peleburan : 8, 5 k. J/mol Kalor penguapan : 113 k. J/mol Tekanan uap : P/Pa 1 10 100 1 k 100 k pada T/K 819 906 1037 1209 1446 1799
CIRI-CIRI ATOM Struktur kristal Bilangan oksidasi Elektronegativitas Energi ionisasi 1 st 2 nd 3 rd Jari-jari atom (terhitung) Jari-jari kovalen Jumlah Tingkat Energi Tingkat Pertama Kedua Energi Level Ketiga Energi Level Keempat Energi Level Kelima Energi Level Keenam Energi Level Fakta Tanggal Discovery Penemu Nama Asal Penggunaan Diperoleh Dari : Kubik berpusat badan : 2 (oksidasi dasar yang kuat) : 0. 89 (skala Pauling) : 502. 9 k. J/mol : 965. 2 k. J/mol : 3600 k. J/mol : 215 pm : 253 pm : 198 pm : 6 : 2 : 8 : 18 : 2 : 1808 : Sir Humphrey Davy : Dari kata Yunani barys (berat) : Kedokteran aplikasi : barytine, whiterite

SIFAT KIMIA ALKALI TANAH (REAKSI-REAKSI LOGAM ALKALI TANAH) Reaksi secara umum Reaksi-Reaksi Logam Alkali Tanah Keterangan 2 M(s) + O 2(g) à 2 MO(s) Reaksi selain Be dan Mg tak perlu Pemanasan M(s) + O 2(g) à MO 2 (s) Ba mudah, Sr dengan tekanan tinggi, Be, Mg, dan Ca, tidak terjadi M(s) + X 2(g) à MX 2 (s) X: F, Cl, Br, dan I M(s) + S(s) à MS (s) M(s) + 2 H 2 O (l) à M(OH)2 (aq) + H 2 (g) Be tidak dapat, Mg perlu pemanasan 3 M(s) + N 2 (g) à M 3 N 2 (s) Reaksi berlangsung pada suhu tinggi, Be tidak dapat berlangsung M(s) + 2 H+(aq) à M 2+(aq) + H 2 (g) Reaksi cepat berlangsung M(s) + H 2 (g) à MH 2 (s) Perlu pemanasan, Be dan Mg tidak dapat berlangsung

Sifat Kimia (reaksi-reaksi) unsur Alkali Tanah. 1. Reaksi dengan Air. Sifat reaksi dengan air dalam satu golongan dari atas ke bawah makin reaktif dan eksotermis (spt. gol I-A). Mg (s) + 2 H 2 O (l) → Mg(OH)2 (aq) + H 2 (g) , reaksinya lambat. Ca (s) + 2 H 2 O (l) → Ca(OH)2 (aq) + H 2 (g) , reaksi lebih cepat. Sr (s) + 2 H 2 O (l) → Sr(OH)2 (aq) + H 2 (g) , reaksi cepat. 2. Reaksi dengan Asam. Be (s) + HCl (aq) → Be. Cl 2 (aq) + H 2 (g) Mg (s) + H 2 SO 4 (aq) → Mg. SO 4 (aq) + H 2 (g) Ca (s) + HBr (aq) → Ca. Br 2 (aq) + H 2 (g) 3. Reaksi dengan basa, hanya Be sebagai logam amphoter yaitu : Be (s) + Na. OH (aq) → Na 2 Be. O 2 (aq) + H 2 (g)

4. Reaksi Logam Alkali Tanah ( M = Be s. d Ba ) dengan Udara. 2 M (s) + O 2 (g) → 2 MO (s) 3 M (s) + N 2 (g) → M 3 N 2 (s) 5. Reaksi Logam Alkali Tanah ( M ) dengan Halogen ( X 2 ). M (s) + X 2 (g) → MX 2 (s) Contoh : Mg (s) + Br 2 (g) → Mg. Br 2 (s) 6. Reaksi Logam Alkali Tanah ( M ) dengan Hidrogen ( H 2 ) M (s) + H 2 (g) → MH 2 (s) Contoh : Ca (s) + H 2 (g) → Ca. H 2 (s)

WUJUD DI ALAM PADA ALKALI TANAH Logam alkali tanah memilii sifat yang reaktif sehingga di alam hanya ditemukan dalam bentuk senyawanya. Berikut keberadaan senyawa yang mengandung logam alkali : Ø Berilium tidak begitu banyak terdapat di kerak bumi, bahkan hampir bisa dikatakan tidak ada. Sedangkan di alam berilium dapat bersenyawa menjadi Mineral beril [Be 3 Al 2(Si. O 6)3], dan Krisoberil [Al 2 Be. O 4]. Kadang-kadang mineral ini di temukan berupa Kristal murni yang besar, dan bila di gosok akan menjadi mutiara berwarna biru laut. Ø Magnesium berperingkat nomor 7 terbanyak yang terdapat di kerak bumi, dengan 1, 9% keberadaannya. Di alam magnesium bisa bersenyawa menjadi Magnesium Klorida [Mg. Cl 2], Senyawa Karbonat [Mg. CO 3], Dolomit [Mg. Ca(CO 3)2], dan Senyawa Epsomit [Mg. SO 4. 7 H 2 O] Magnesium dan Kalsium juga terdapat dalam organisme. Magnesium sangat penting dalam tumbuhan untuk membuat klorofil, yaitu senyawa penangkap energi cahaya matahari. Ø Kalsium adalah logam alkali yang paling banyak terdapat di kerak bumi. Bahkan kalsium menjadi nomor 5 terbanyak yang terdapat di kerak bumi, dengan 3, 4% keberadaanya. Di alam kalsium dapat membentuk senyawa karbonat [Ca. CO 3], Senyawa Fospat [Ca. PO 4], Senyawa Sulfat [Ca. SO 4], Senyawa Fourida [Ca. F] Kalsium sebagaian di pakai sebagai pembentuk tulang, binatang-binatang lunak, seperti siput, kerang, dan penyu. Strontium dan Barium sering di temukan sebagai Sr. SO 4 dan Ba. SO 4. Ø Stronsium berada di kerak bumi dengan jumlah 0, 03%. Di alam strontium dapat membuntuk senyawa Mineral Selesit [Sr. SO 4], dan Strontianit Ø Barium berada di kerak bumi sebanyak 0, 04%. Di alam barium dapat membentuk senyawa : Mineral Baritin [Ba. SO 4], dan Mineral Witerit [Ba. CO 3]

MANFAAT ALKALI TANAH 1. Berilium (Be) a) Berilium digunakan untuk memadukan logam agar lebih kuat, akan tetapi bermassa lebih ringan. Biasanya paduan ini digunakan pada kemudi pesawat Jet. b) Berilium digunakan pada kaca dari sinar X. c) Berilium digunakan untuk mengontrol reaksi fisi pada reaktor nuklir. d) Campuran berilium dan tembaga banyak dipakai pada alat listrik, maka Berilium sangat penting sebagai komponen televisi. 2. Magnesium (Mg) a) Magnesium digunakan untuk memberi warna putih terang pada kembang api dan pada lampu blitz. b) Senyawa Mg. O dapat digunakan untuk melapisi tungku, karena senyawa Mg. O memiliki titik leleh yang tinggi. c) Senyawa Mg(OH)2 digunakan dalam pasta gigi untuk mengurangi asam yang terdapat di mulut dan mencegah terjadinnya kerusakan gigi, sekaligus sebagai pencegah maag. d) Mirip dengan Berilium yang membuat campuran logam semakin kuat dan ringan sehingga bisa digunakan pada alat rumah tangga.

3. Kalsium (Ca) a) Kalsium digunakan pada obatan, bubuk pengembang kue dan plastik. b) Senyawa Ca. SO 4 digunakan untuk membuat gips yang berfungsi untuk membalut tulang yang patah. c) Senyawa Ca. CO 3 biasa digunakan untuk bahan bangunan seperti komponen semen dan cat tembok. Selain itu digunakan untuk membuat kapur tulis dan gelas. d) Kalsium Oksida (Ca. O) dapat mengikat air pada Etanol karena bersifat dehidrator, dapat juga mengeringkan gas dan mengikat Karbondioksida pada cerobong asap. e) Ca(OH)2 digunakan sebagai pengatur p. H air limbah dan juga sebagai sumber basa yang harganya relatif murah. f) Kalsium Karbida (Ca. C 2) disaebut juga batu karbit merupakan bahan untuk pembuatan gas asetilena (C 2 H 2) yang digunakan untuk pengelasan. g) Kalsium banyak terdapat pada susu dan ikan teri yang berfungsi sebagai pembentuk tulang dan gigi. 4. Stronsium (Sr) a) Stronsium dalam senyawa Sr(NO 3)2 memberikan warna merah apabila digunakan untuk bahan kembang api. b) Stronsium sebagai senyawa karbonat biasa digunakan dalam pembuatan kaca televisi berwarna dan komputer. c) Untuk pengoperasian mercusuar yang mengubah energi panas menjadi listrik dalam baterai nuklir RTG (Radiisotop Thermoelectric Generator). 5. Barium (Ba) a) Ba. SO 4 digunakan untuk memeriksa saluran pencernaan karena mampu menyerap sinar X meskipun beracun. b) Ba. SO 4 digunakan sebagai pewarna pada plastik karena memiliki kerapatan yang tinggi dan warna terang. c) Ba(NO 3)2 digunakan untuk memberikan warna hijau pada kembang api.

PENGOLAHAN ALKALI TANAH

PROSES EKSTRAKSI (PENGOLAHAN) LOGAM ALKALI TANAH Ekstraksi adalah pemisahan suatu unsur dari suatu senyawa. Logam alkali tanah dapat di ekstraksi dari senyawanya. Untuk mengekstraksinya kita dapat menggunakan dua cara, yaitu metode reduksi dan metode elektrolisis. Ekstraksi Berilium (Be) Metode reduksi Untuk mendapatkan Berilium, bisa didapatkan dengan mereduksi Be. F 2. Sebelum mendapatkan Be. F 2, kita harus memanaskan beril [Be 3 Al 2(Si. O 6)3] dengan Na 2 Si. F 6 hingga 700 0 C Karena beril adalah sumber utama berilium. Be. F 2 + Mg à Mg. F 2 + Be Metode Elektrolisis Untuk mendapatkan berilium juga kita dapat mengekstraksi dari lelehan Be. Cl 2 yang telah ditambah Na. Cl. Karena Be. Cl 2 tidak dapat mengahantarkan listrik dengan baik, sehingga ditambahkan Na. Cl. Reaksi yang terjadi adalah : Katoda : Be 2+ + 2 e à Be Anode : 2 Cl- à Cl 2 + 2 e-

� � � � � � � Ekstraksi Magnesium (Mg) Metode Reduksi Untuk mendapatkan magnesium kita dapat mengekstraksinya dari dolomit [Mg. Ca(CO 3)2] karena dolomite merupakan salah satu sumber yang dapat menhasilkan magnesium. Dolomite dipanaskan sehingga terbentuk Mg. O. Ca. O. lalu Mg. O. Ca. O. dipanaskan dengan Fe. Si sehingga menhasilkan Mg. 2[ Mg. O. Ca. O] + Fe. Si à 2 Mg + Ca 2 Si. O 4 + Fe Metode Elektrolisis Selain dengan ekstraksi dolomite magnesium juga bisa didapatkan dengan mereaksikan air alut dengan Ca. O. Reaksi yang terjadi : Ca. O + H 2 O à Ca 2+ + 2 OH Mg 2+ + 2 OH à Mg(OH)2 Selanjutnya Mg(OH)2 direaksikan dengan HCl Untuk membentuk Mg. Cl 2 Mg(OH)2 + 2 HCl à Mg. Cl 2 + 2 H 2 O Setelah mendapatkan lelehan Mg. Cl 2 kita dapat mengelektrolisisnya untuk mendapatkan magnesium Katode : Mg 2+ + 2 e à Mg Anode : 2 Cl à Cl 2 + 2 e Ekstraksi Kalsium (Ca) Metode Elektrolisis Batu kapur (Ca. CO 3) adalah sumber utama untuk mendapatkan kalsium (Ca). Untuk mendapatkan kalsium, kita dapat mereaksikan Ca. CO 3 dengan HCl agar terbentuk senyawa Ca. Cl 2. Reaksi yang terjadi : Ca. CO 3 + 2 HCl à Ca. Cl 2 + H 2 O + CO 2 Setelah mendapatkan Ca. Cl 2, kita dapat mengelektrolisisnya agar mendapatkan kalsium (Ca). Reaksi yang terjadi : Katoda ; Ca 2+ + 2 e à Ca Anoda ; 2 Cl à Cl 2 + 2 e Metode Reduksi Logam kalsium (Ca) juga dapat dihasilkan dengan mereduksi Ca. O oleh Al atau dengan mereduksi Ca. Cl 2 oleh Na. Reduksi Ca. O oleh Al 6 Ca. O + 2 Al à 3 Ca + Ca 3 Al 2 O 6 Reduksi Ca. Cl 2 oleh Na Ca. Cl 2 + 2 Na à Ca + 2 Na. Cl

Ekstraksi Strontium (Sr) Metode Elektrolisis Untuk mendapatkan Strontium (Sr), Kita bisa mendapatkannya dengan elektrolisis lelehan Sr. Cl 2. Lelehan Sr. Cl 2 bisa didapatkan dari senyawa selesit [Sr. SO 4]. Karena Senyawa selesit merupakan sumber utama Strontium (Sr). Reaksi yang terjadi ; � katode ; Sr 2+ +2 e à Sr � anoda ; 2 Cl à Cl 2 + 2 e � � � Ekstraksi Barium (Ba) Metode Elektrolisis Barit (Ba. SO 4) adalah sumber utama untuk memperoleh Barium (Ba). Setelah diproses menjadi Ba. Cl 2 barium bisa diperoleh dari elektrolisis lelehan Ba. Cl 2. Reaksi yang terjadi : katode ; Ba 2+ +2 e à Ba anoda ; 2 Cl à Cl 2 + 2 e Metode Reduksi Selain dengan elektrolisis, barium bisa kita peroleh dengan mereduksi Ba. O oleh Al. Reaksi yang terjadi : 6 Ba. O + 2 Al à 3 Ba + Ba 3 Al 2 O 6.
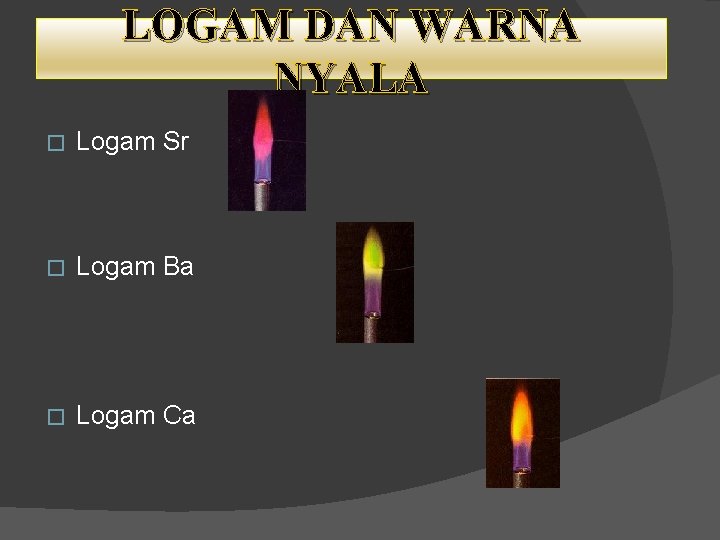
LOGAM DAN WARNA NYALA � Logam Sr � Logam Ba � Logam Ca
- Slides: 30