Glutamatergic and Aspartatergic Pathways Il Glutammato il NT










- Slides: 21

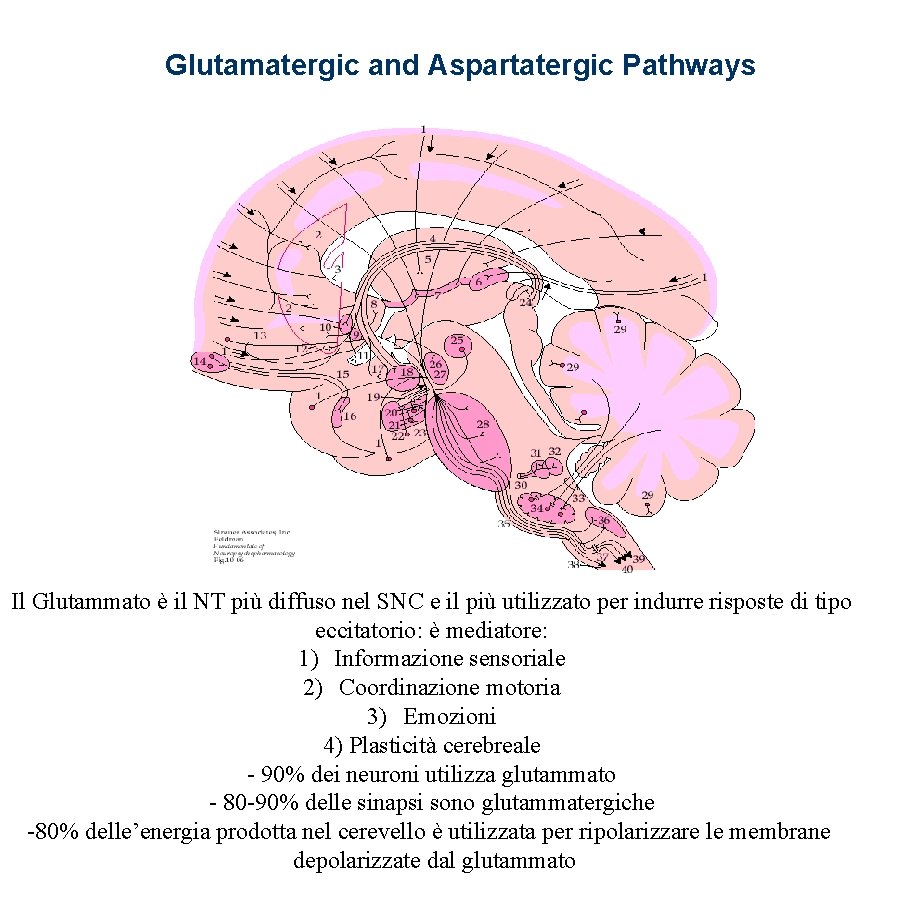
Glutamatergic and Aspartatergic Pathways Il Glutammato è il NT più diffuso nel SNC e il più utilizzato per indurre risposte di tipo eccitatorio: è mediatore: 1) Informazione sensoriale 2) Coordinazione motoria 3) Emozioni 4) Plasticità cerebreale - 90% dei neuroni utilizza glutammato - 80 -90% delle sinapsi sono glutammatergiche -80% delle’energia prodotta nel cerevello è utilizzata per ripolarizzare le membrane depolarizzate dal glutammato

Pathways of glutamate synthesis. Aa serici che passano la barriera LEU, ILE, VAL, poiché lo uptake di questi aminoacidi è << a quello del glucosio I gruppi NH 2 del glutammato devono essere riciclati quando lo scheletro del carbonio è degradato a CO 2 e H 20 Nelle cellule nervose il Glutammato è sintetizzato: 1) Dallo a-chetoglutarato, -un prodotto intermedio del ciclo degli acidi tricarbossilici – attraverso una reazione di transaminazione ad opera di un enzima che utilizza piridossal fosfato, 2) Dalla glutamina per azione della glutaminasi

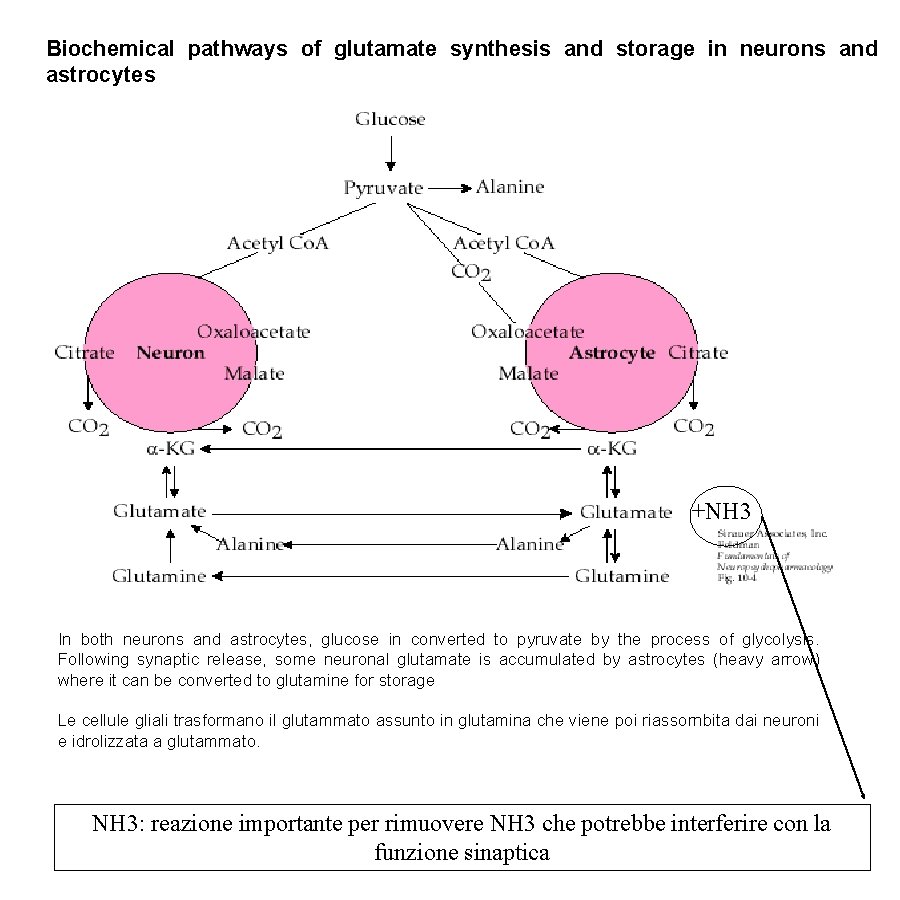
Biochemical pathways of glutamate synthesis and storage in neurons and astrocytes +NH 3 In both neurons and astrocytes, glucose in converted to pyruvate by the process of glycolysis. Following synaptic release, some neuronal glutamate is accumulated by astrocytes (heavy arrow) where it can be converted to glutamine for storage Le cellule gliali trasformano il glutammato assunto in glutamina che viene poi riassornbita dai neuroni e idrolizzata a glutammato. NH 3: reazione importante per rimuovere NH 3 che potrebbe interferire con la funzione sinaptica

Glutamate catabolism. One route of glutamate catabolism is oxidative deamination by the enzyme glutamate dehydrogenase (GDH).

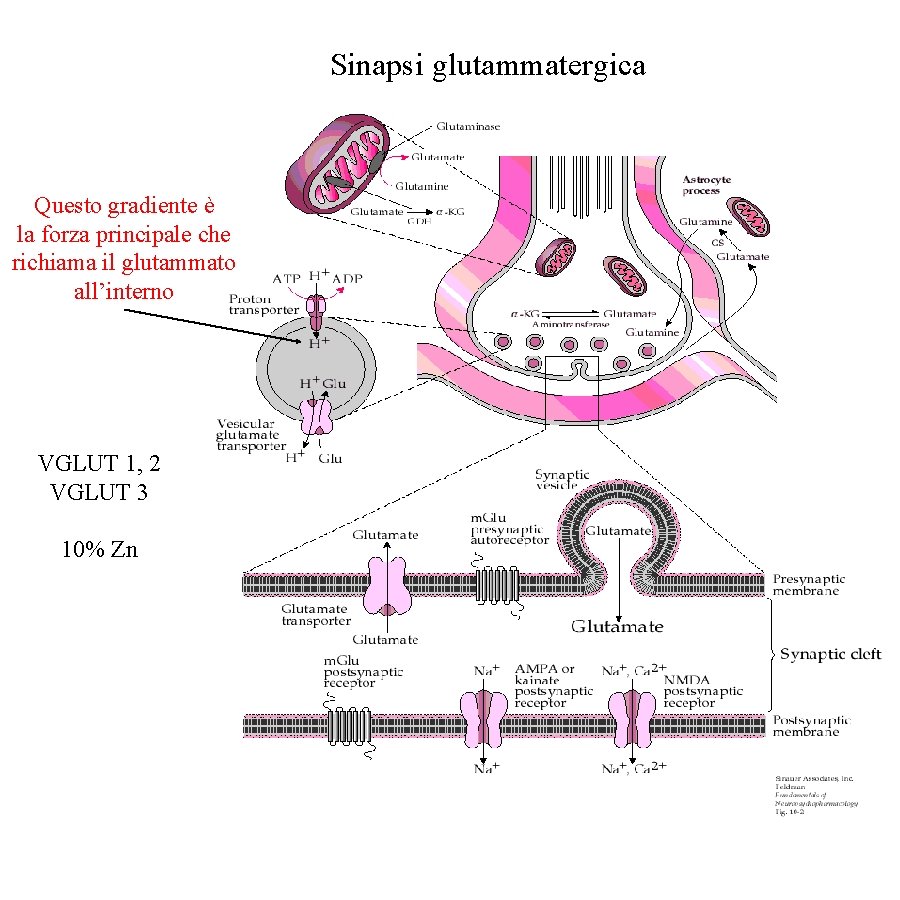
Sinapsi glutammatergica Questo gradiente è la forza principale che richiama il glutammato all’interno VGLUT 1, 2 VGLUT 3 10% Zn

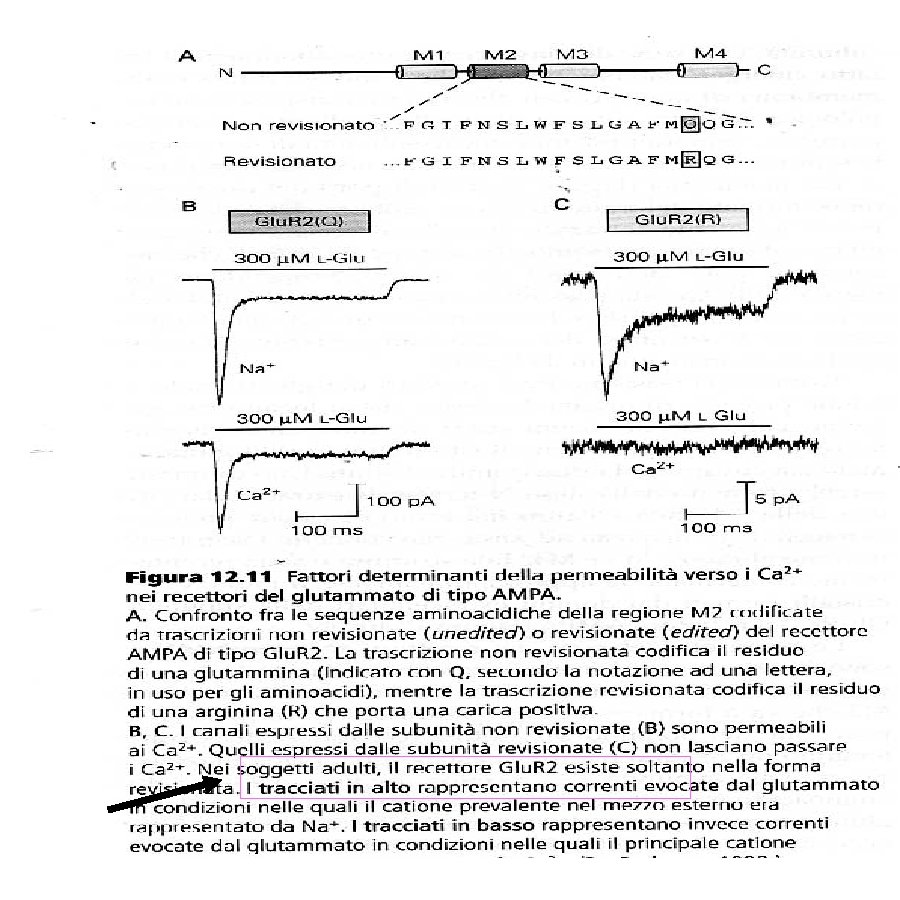
Recettori del glutamato 1) recettori ionotropici : recettore canale - tre tipi in rapporto agli agonisti sonda -NMDA R: selettivo per il ligando N-methyl-D-aspartato (bloccato da APV: acido amino-5 - fosfovalerianico) -AMPA R : selettivo per il ligando a-amino-3 -idrossi-5 - methyl-4 proprionato e per il quisqualato isossiazol -Kainate R: selettivo per il ligando acido kainico. (bloccati dal CNQX : 6 ciano-7 nitrochinossalina-2, 3 -dione) 2) recettori metabotropici: ne esistono almeno 6 sottotipi. Sono associati a G-proteins. Alcuni stimolano la via del IP 3 e dell’acido arachidonico, altri riducono le concentrazioni di c. AMP. Funzioni: cervello: regolano l’eccitabilità sopprimendo le correnti del K (ippocampo). Inducono depressione sinaptica protratta nelle Purkinje del cervelletto, sopprimono in via presinaptica la neurotrasmissione bloccando la formazione di c. AMP (c. Golgi del cervelletto), iperpolarizzano le cellule bipolari della retina


Stessa famiglia di geni


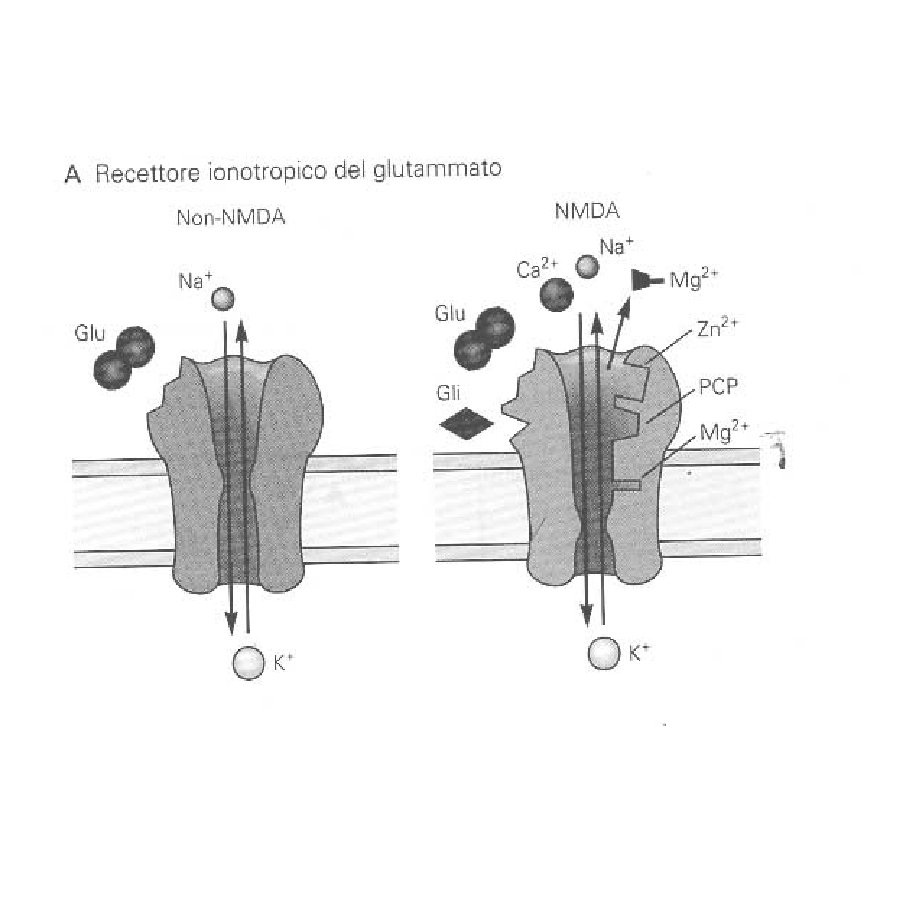
Excitatory Amino Acid Receptors non. NMDA



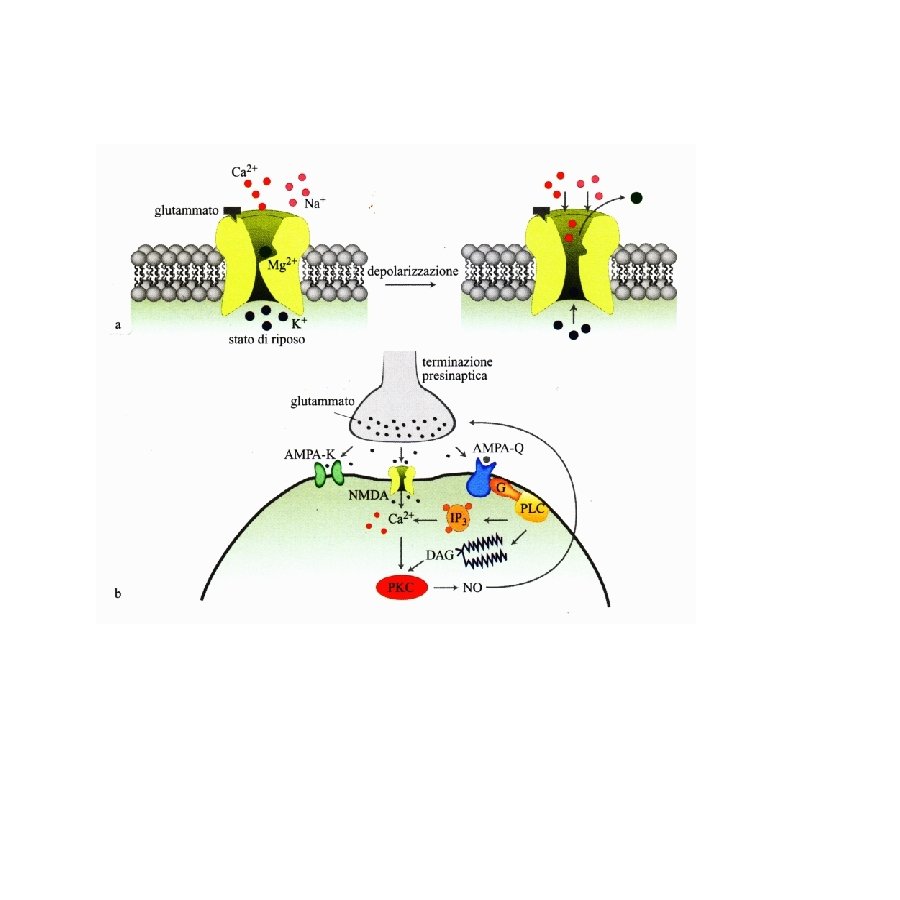
I recettori di tipo non NMDA danno origine, ad es. nei motoneuroni, alla componente precoce del EPSP in risposta alla stimolazione delle fibre afferenti sensitive primarie. Questi recettori attivano canali cationici a conduttanza bassa ( <<20 ps) permebaili al Na+ e K+ I recettori di tipo NMDA intervengono e sono resposabili della componenente tardiva del EPSP. Tre caratteristiche: 1) Controllano un canale cationico a conduttanza elevata (50 ps), permebile al Na+, K+ e Ca+ 2) L’apertura del canale richiede anche la glicina o la D-serina (D-serine racemase) 3) L’apertura dipende dal voltaggio della membrana (che rimuove la molecola del Mg++ che si trova all’interno del canale) E’ inibito dalla FENICICLINA o PCP o polvere degli angeli una sostanza allucinogena che si lega a un sito localizzato all’interno del poro-canale aperto. Il blocco dei recettori NMDA dà origine a sintomi che richimano le allucinazioni che si osservano nei pazienti affetti da schizofrenia


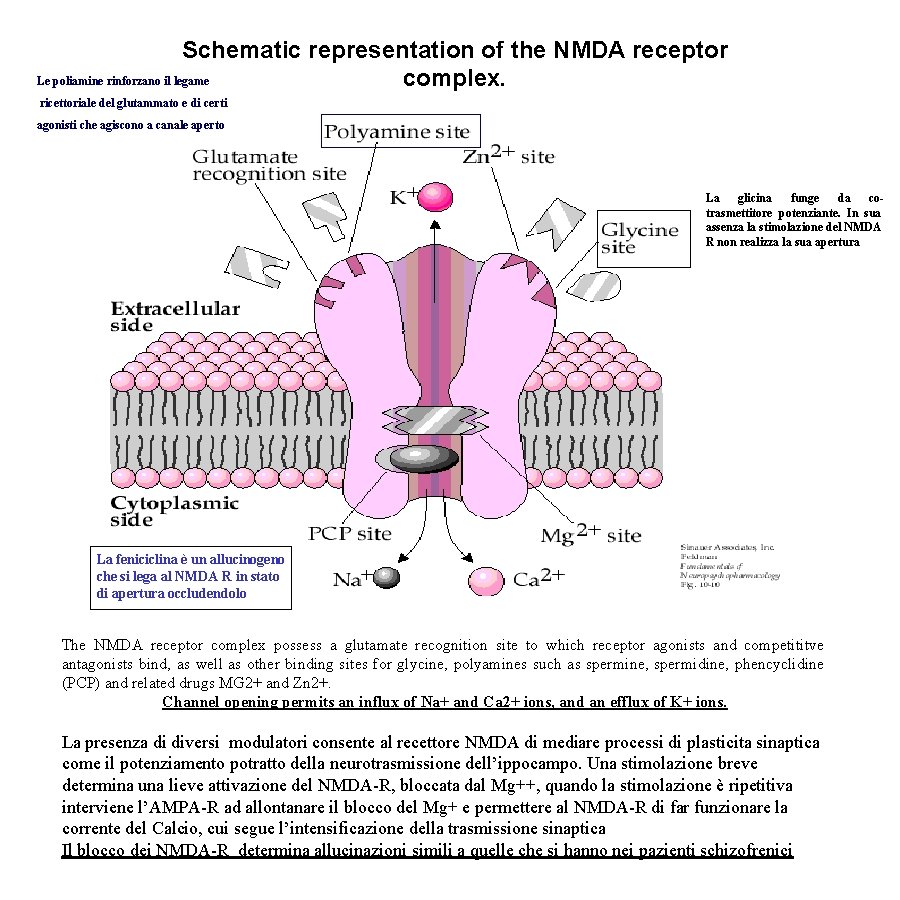
Schematic representation of the NMDA receptor Le poliamine rinforzano il legame complex. ricettoriale del glutammato e di certi agonisti che agiscono a canale aperto La glicina funge da cotrasmettitore potenziante. In sua assenza la stimolazione del NMDA R non realizza la sua apertura La feniciclina è un allucinogeno che si lega al NMDA R in stato di apertura occludendolo The NMDA receptor complex possess a glutamate recognition site to which receptor agonists and competititve antagonists bind, as well as other binding sites for glycine, polyamines such as spermine, spermidine, phencyclidine (PCP) and related drugs MG 2+ and Zn 2+. Channel opening permits an influx of Na+ and Ca 2+ ions, and an efflux of K+ ions. La presenza di diversi modulatori consente al recettore NMDA di mediare processi di plasticita sinaptica come il potenziamento potratto della neurotrasmissione dell’ippocampo. Una stimolazione breve determina una lieve attivazione del NMDA-R, bloccata dal Mg++, quando la stimolazione è ripetitiva interviene l’AMPA-R ad allontanare il blocco del Mg+ e permettere al NMDA-R di far funzionare la corrente del Calcio, cui segue l’intensificazione della trasmissione sinaptica Il blocco dei NMDA-R determina allucinazioni simili a quelle che si hanno nei pazienti schizofrenici

All’effetto citotossico della stimolazione dei recettori del glutammato sono state attribuite anche patologie psichiatriche: 1) la demenza pugilistica 2) la sindronme di Korsakoff negli alcolisti 3) la schizofrenia da danno cerebrale intrauterino ( ipofunzione dei Glu-R) 4) l’autismo infantile 5) la epilettogenesi , specie il processo di generalizzazione delle convulsioni Tossine alimentari: 1) ACIDO DOMOICO: veleno prodotto da alcune conchiglie di mare attiva i recettori del kainato, provoca MORTE o GRAVI DEFICIT MEMORIA 2) CYCAS CIRCINALIS: (cicade originaria dell'India meridionale. ) contiene BMAA (b-N-methylamino-L-alanine) che in presenza di bicarbonato attiva AMPAR e NMDAR (isola di Guam nel Pacifico: ALS) 3) LATHYRIUS SATIVUS: (è un legume, comunemente chiamato Cicerchia) causa il LATIRISMO provoca 1) disturbi degli arti inferiori dopo lunghi periodi di assunzione, dovuta all'aminoacido 2) β-N-Oxalyl-L-α, β-diaminopropionico acido, è diffusa soprattutto nel continente asiatico Il Glutammato, lo NMDA e il Kainato sono delle potenti neuro-tossine 1970: somministrati per via orale negli animali immaturi: acuta neurodegenrazione nelle zone non protette da barriera ematoencefalica (nucleo arcuato, ipotalamo) Acido kainico: selettiva lesione dei neuroni ippocampali area CA 3 e crisi epilettiche

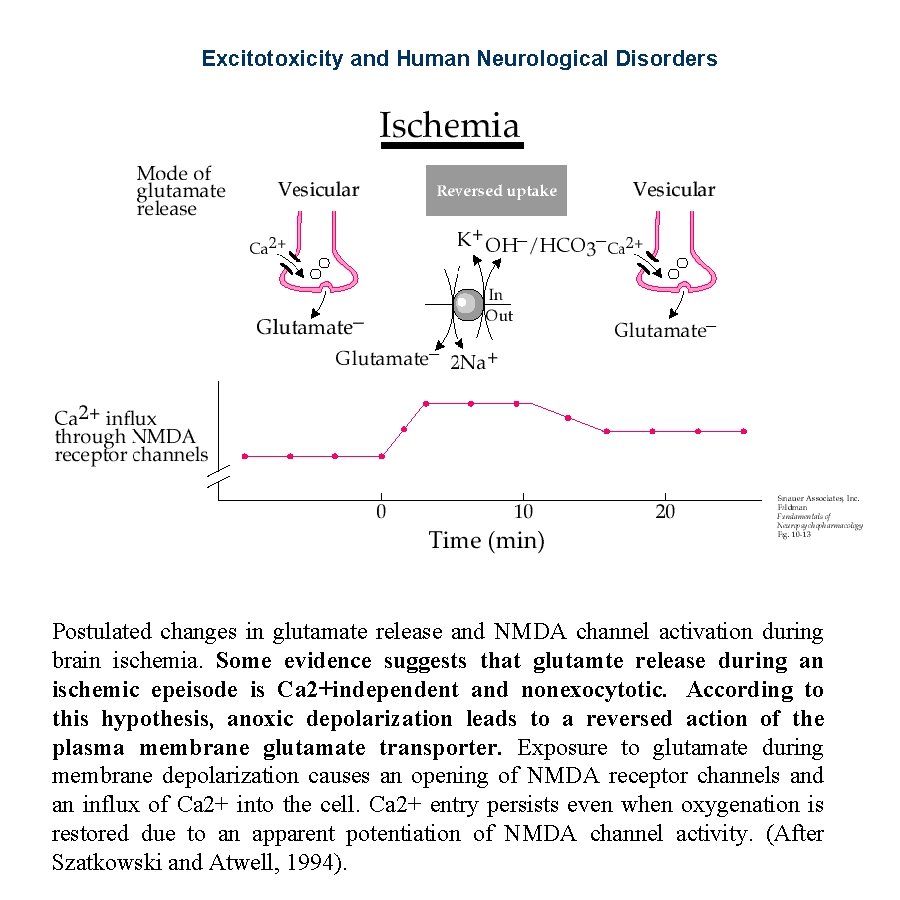
Excitotoxicity and Human Neurological Disorders Postulated changes in glutamate release and NMDA channel activation during brain ischemia. Some evidence suggests that glutamte release during an ischemic epeisode is Ca 2+independent and nonexocytotic. According to this hypothesis, anoxic depolarization leads to a reversed action of the plasma membrane glutamate transporter. Exposure to glutamate during membrane depolarization causes an opening of NMDA receptor channels and an influx of Ca 2+ into the cell. Ca 2+ entry persists even when oxygenation is restored due to an apparent potentiation of NMDA channel activity. (After Szatkowski and Atwell, 1994).

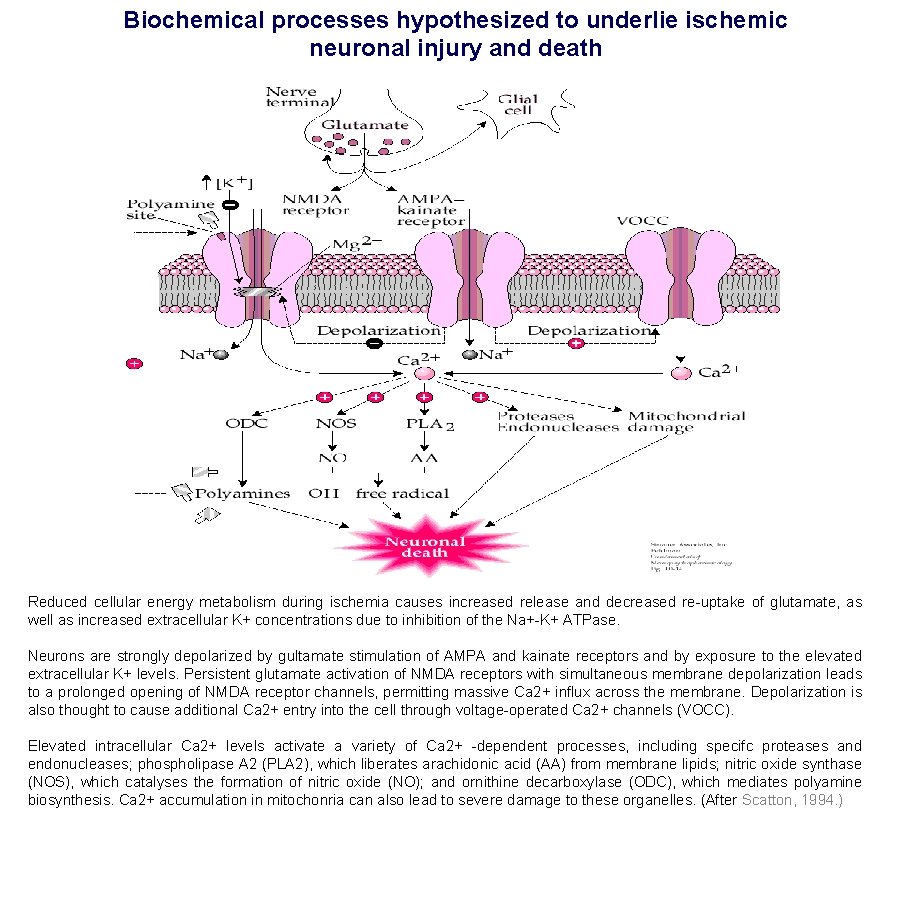
Biochemical processes hypothesized to underlie ischemic neuronal injury and death Reduced cellular energy metabolism during ischemia causes increased release and decreased re-uptake of glutamate, as well as increased extracellular K+ concentrations due to inhibition of the Na+-K+ ATPase. Neurons are strongly depolarized by gultamate stimulation of AMPA and kainate receptors and by exposure to the elevated extracellular K+ levels. Persistent glutamate activation of NMDA receptors with simultaneous membrane depolarization leads to a prolonged opening of NMDA receptor channels, permitting massive Ca 2+ influx across the membrane. Depolarization is also thought to cause additional Ca 2+ entry into the cell through voltage-operated Ca 2+ channels (VOCC). Elevated intracellular Ca 2+ levels activate a variety of Ca 2+ -dependent processes, including specifc proteases and endonucleases; phospholipase A 2 (PLA 2), which liberates arachidonic acid (AA) from membrane lipids; nitric oxide synthase (NOS), which catalyses the formation of nitric oxide (NO); and ornithine decarboxylase (ODC), which mediates polyamine biosynthesis. Ca 2+ accumulation in mitochonria can also lead to severe damage to these organelles. (After Scatton, 1994. )

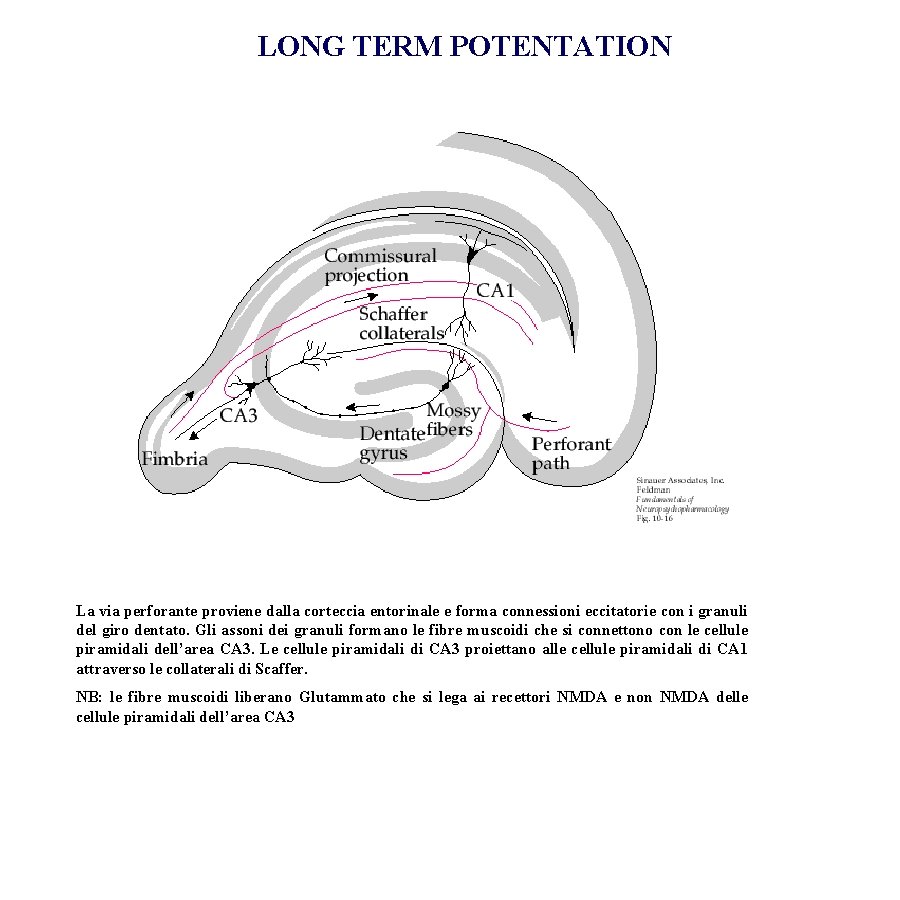
LONG TERM POTENTATION La via perforante proviene dalla corteccia entorinale e forma connessioni eccitatorie con i granuli del giro dentato. Gli assoni dei granuli formano le fibre muscoidi che si connettono con le cellule piramidali dell’area CA 3. Le cellule piramidali di CA 3 proiettano alle cellule piramidali di CA 1 attraverso le collaterali di Scaffer. NB: le fibre muscoidi liberano Glutammato che si lega ai recettori NMDA e non NMDA delle cellule piramidali dell’area CA 3

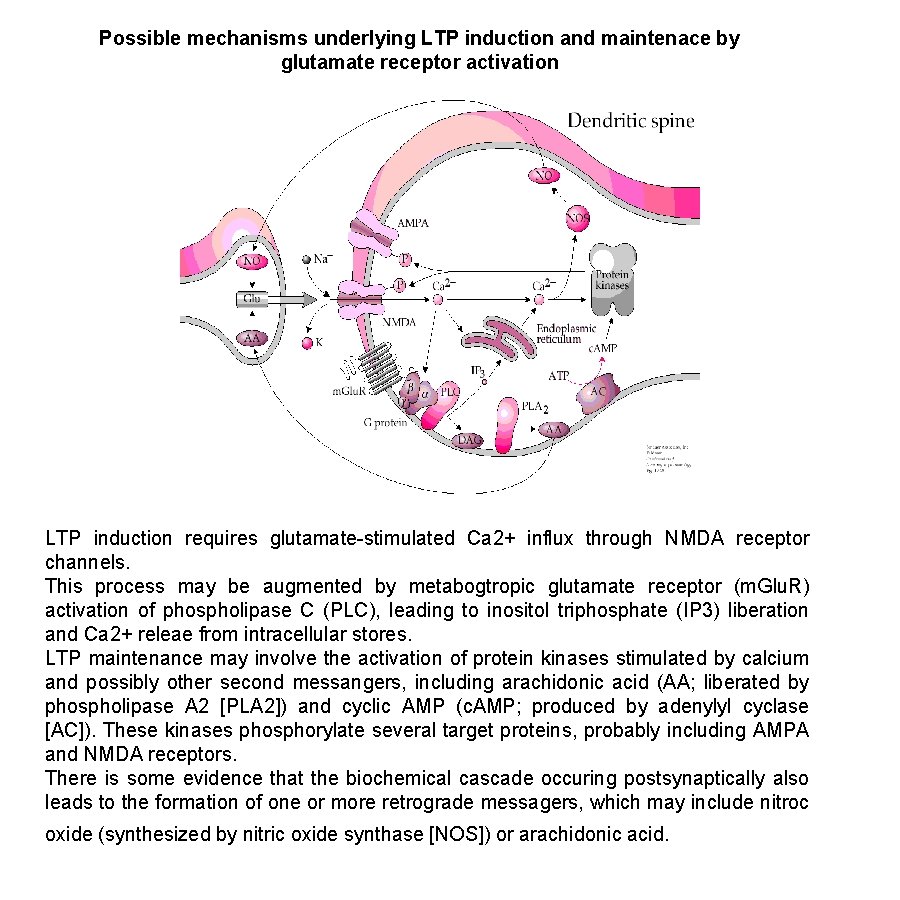
Possible mechanisms underlying LTP induction and maintenace by glutamate receptor activation LTP induction requires glutamate-stimulated Ca 2+ influx through NMDA receptor channels. This process may be augmented by metabogtropic glutamate receptor (m. Glu. R) activation of phospholipase C (PLC), leading to inositol triphosphate (IP 3) liberation and Ca 2+ releae from intracellular stores. LTP maintenance may involve the activation of protein kinases stimulated by calcium and possibly other second messangers, including arachidonic acid (AA; liberated by phospholipase A 2 [PLA 2]) and cyclic AMP (c. AMP; produced by adenylyl cyclase [AC]). These kinases phosphorylate several target proteins, probably including AMPA and NMDA receptors. There is some evidence that the biochemical cascade occuring postsynaptically also leads to the formation of one or more retrograde messagers, which may include nitroc oxide (synthesized by nitric oxide synthase [NOS]) or arachidonic acid.
