GLOBALTRAINING IMPLANON NXT Informao Clnica e Workshop de

GLOBALTRAINING IMPLANON NXT® Informação Clínica e Workshop de Formação 1

Bem-vindo ► Bem-vindo ao Programa de Formação Clínica de IMPLANON NXT® (implante de etonogestrel). Este Workshop foi concebido para lhe apresentar o IMPLANON NXT®. ► A MSD recomenda que todos os profissionais de saúde que tencionem inserir IMPLANON NXT® recebam formação sobre este procedimento. Como acontece em todos os dispositivos médicos, a formação não significa que o profissional de saúde registado possua competências nos procedimentos de inserção e remoção. Como tal, cada profissional de saúde deve decidir de forma independente sobre a sua competência antes de efetuar qualquer procedimento de inserção ou remoção. ► A MSD recomenda também que verifique com a sua associação profissional e seguradora os requisitos que estas possam ter antes de inserir ou remover IMPLANON NXT®. 2

Agenda ► ► ► Informação Clínica. Aconselhamento. Procedimento e Prática de Inserção. Localização antes da Remoção. Procedimento para a Remoção e Prática de Reinserção. Conclusão. 3

Informação importante ► A participação nesta formação não substitui a necessidade de consultar o RCM do produto aprovado relativamente às instruções de inserção, remoção e substituição de IMPLANON NXT® (implante de etonogestrel) e de outras informações ► Estes materiais educativos são disponibilizados para auxiliar a formação dos profissionais de saúde, nos países fora dos EUA, nos procedimentos de inserção e remoção de IMPLANON NXT®. Estes materiais não substituem a revisão do RCM do produto que deve ser revisto antes da administração ou remoção do produto. 4

IMPLANON NXT® (implante de etonogestrel) ► ► ► Contracetivo hormonal, subcutâneo, de ação prolongada, eficaz até 3 anos. Implante contendo apenas progestagénio, pré-carregado num aplicador descartável. IMPLANON NXT® é radiopaco e comparável ao IMPLANON® (implante de etonogestrel). Ensaios clínicos com IMPLANON® em 17 países, incluindo os E. U. A. Ensaios clínicos com IMPLANON NXT® em 6 países. 5
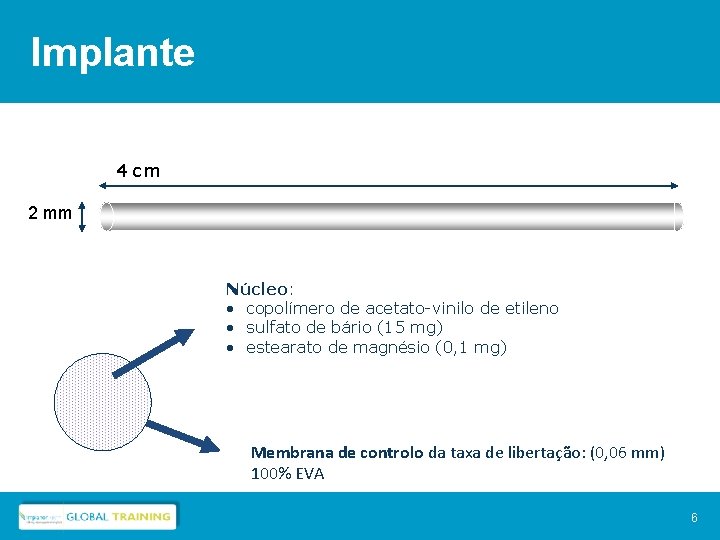
Implante 4 cm 2 mm Núcleo: • copolímero de acetato-vinilo de etileno • sulfato de bário (15 mg) • estearato de magnésio (0, 1 mg) Membrana de controlo da taxa de libertação: (0, 06 mm) 100% EVA 6

Aplicador de IMPLANON NXT® (implante de etonogestrel) ► ► Aplicador pré-carregado, estéril Uso único e descartável. Apenas deve ser utilizado segundo as instruções de inserção por profissionais de saúde autorizados para realização destes procedimentos Os clínicos familiarizados com o aplicador do IMPLANON® (implante de etonogestrel) necessitam de se familiarizar com IMPLANON NXT®. 7

GLOBALTRAINING Informação Clínica 8

Eficácia ► ► A eficácia de IMPLANON® (implante de etonogestrel) é superior a 99% – O efeito contracetivo de IMPLANON NXT® (implante de etonogestrel) está relacionado com os níveis plasmáticos de etonogestrel, que possuem uma relação inversa com o peso corporal e diminuem ao longo do tempo após a inserção. É limitada a experiência clínica em mulheres mais pesadas no terceiro ano de utilização. Não se pode excluir que o efeito contracetivo nestas mulheres, durante o terceiro ano de utilização, possa ser mais baixo do que nas mulheres com peso normal. Os profissionais de saúde poderão considerar a substituição antecipada do implante em mulheres mais pesadas. Os medicamentos que reduzem a eficácia dos contracetivos orais também reduzem a eficácia de IMPLANON NXT® 1. Graesslin O et al. Eur J Contracept Reprod Health Care. 2008; 13(S 1): 4– 12. 9

Mecanismos de ação ► ► Inibição da ovulação Alterações da viscosidade do muco cervical. 10

Farmacocinética ► ► O etonogestrel é rapidamente absorvido na circulação após a inserção As concentrações de inibição da ovulação são atingidas no espaço de 1 dia Concentrações séricas máximas nos Dias 1 a 13: 472 a 1270 pg/ml A taxa de libertação do impante diminui ao longo do tempo – Final do Ano 1: ~200 pg/ml – Final do Ano 3: ~156 pg/ml 11
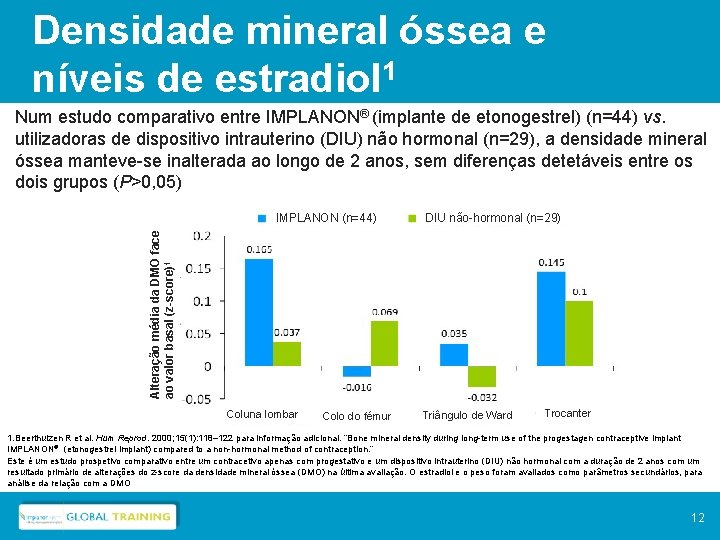
Densidade mineral óssea e níveis de estradiol 1 Num estudo comparativo entre IMPLANON® (implante de etonogestrel) (n=44) vs. utilizadoras de dispositivo intrauterino (DIU) não hormonal (n=29), a densidade mineral óssea manteve-se inalterada ao longo de 2 anos, sem diferenças detetáveis entre os dois grupos (P>0, 05) DIU não-hormonal (n=29) Alteração média da DMO face 1 1 ao valor basal (z-score) IMPLANON (n=44) Coluna lombar Colo do fémur Triângulo de Ward Trocanter 1. Beerthuizen R et al. Hum Reprod. 2000; 15(1): 118– 122 para informação adicional. “Bone mineral density during long-term use of the progestagen contraceptive implant IMPLANON® (etonogestrel implant) compared to a non-hormonal method of contraception. ” Este é um estudo prospetivo comparativo entre um contracetivo apenas com progestativo e um dispositivo intrauterino (DIU) não hormonal com a duração de 2 anos com um resultado primário de alterações do z-score da densidade mineral óssea (DMO) na última avaliação. O estradiol e o peso foram avaliados como parâmetros secundários, para análise da relação com a DMO 12
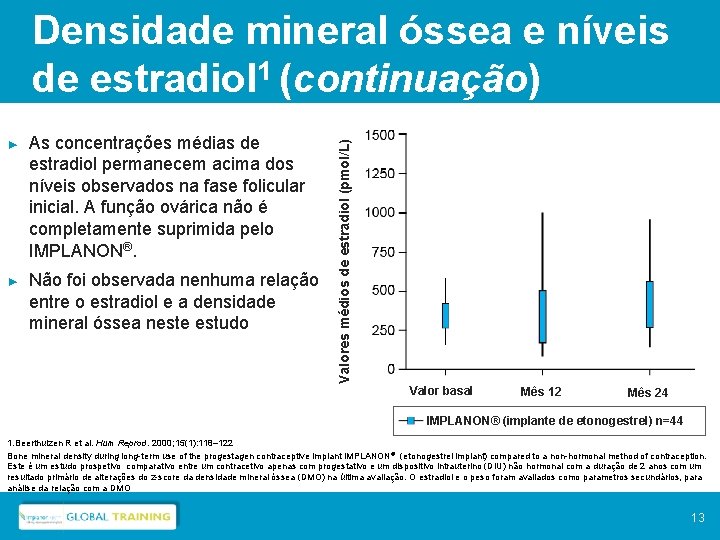
► As concentrações médias de estradiol permanecem acima dos níveis observados na fase folicular inicial. A função ovárica não é completamente suprimida pelo IMPLANON®. ► Não foi observada nenhuma relação entre o estradiol e a densidade mineral óssea neste estudo Valores médios de estradiol (pmol/L) Densidade mineral óssea e níveis de estradiol 1 (continuação) Valor basal Mês 12 Mês 24 IMPLANON® (implante de etonogestrel) n=44 1. Beerthuizen R et al. Hum Reprod. 2000; 15(1): 118– 122 Bone mineral density during long-term use of the progestagen contraceptive implant IMPLANON® (etonogestrel implant) compared to a non-hormonal method of contraception. Este é um estudo prospetivo comparativo entre um contracetivo apenas com progestativo e um dispositivo intrauterino (DIU) não hormonal com a duração de 2 anos com um resultado primário de alterações do z-score da densidade mineral óssea (DMO) na última avaliação. O estradiol e o peso foram avaliados como parametros secundários, para análise da relação com a DMO 13

Padrões de hemorragia – Desenho do estudo ► ► Desenho do estudo: dados de 11 ensaios clínicos realizados em vários países (n=923, 18– 40 anos de idade). Os ensaios tiveram um desenho aberto e foram não-comparativos ou comparativos. A maioria dos ensaios durou, pelo menos, 2 anos com esquema de visitas de 3 em 3 meses incluindo até 3 meses após a remoção do implante. Todas as participantes registaram os dados relativos à hemorragia em períodos de referência de 90 dias. Definições-chave usadas no estudo: – O dia de hemorragia foi definido como qualquer dia com corrimento vaginal contendo sangue que necessitou, por dia, de mais de um penso higiénico ou tampão. – Dia de spotting foi definido como qualquer dia com corrimento vaginal contendo sangue que necessitou, por dia, no máximo, de um penso higiénico ou tampão. – Dia sem hemorragia foi definido como um dia em que não foram introduzidos no diário nem hemorragia nem spotting. 1. Mansour D et al. Eur J Contracept Reprod Health Care. 2008; 13(suppl 1): 13– 28. 14

Padrões de hemorragia ► ► Durante a utilização de IMPLANON NXT® (implante de etonogestrel), é provável que as mulheres possam referir alterações no seu padrão de hemorragia. As alterações podem estar relacionadas com a frequência (ausente, menor, maior ou contínua), intensidade (reduzida ou aumentada) ou duração. Em muitas mulheres, o padrão de hemorragia observado durante os primeiros três meses é largamente indicador do padrão hemorrágico futuro. Foi relatada amenorreia em cerca de 1 em cada 5 mulheres, sendo que também 1 em cada 5 mulheres referiu hemorragia frequente e/ou prolongada. ► A informação, aconselhamento e utilização de um diário de hemorragias podem melhorar a aceitação do padrão hemorrágico pela mulher ► Pode ser indicada a avaliação da hemorragia vaginal ou da sua ausência, para excluir patologia ginecológica ou gravidez numa base ad-hoc 15

Hemorragia/Spotting (H/S) durante o uso do IMPLANON NXT® (implante de etonogestrel)1 Por períodos de referência de 90 dias para todos as participantes Número médio de dias com H/S 17, 7 Número médio de episódios com H/S 2, 4 Desenho do estudo: dados de 11 ensaios clínicos realizados em diversos países (n=923, 18– 40 anos de idade). Todos os ensaios tiveram um desenho aberto e foram não comparativos ou comparativos com Norplant ou um dispositivo intrauterino não hormonal. A maioria dos ensaios durou, pelo menos, 2 anos, tendo parâmetros de avaliação de eficácia contracetiva e hemorragia e apresentavam um esquema de visitas de 3 em 3 meses incluindo até 3 meses após a remoção do implante, Todas as participantes registaram os dados relativos a hemorragia em períodos de referência de 90 dias. Período de referência de 90 dias – Conforme definido nas diretrizes da Organização Mundial de Saúde (OMS), a análise do período de referência do estudo dividiu a informação relativa à hemorragia das participantes em segmentos de 90 dias. Cada segmento representou um período de referência, começando no dia de inserção do implante como o primeiro dia do período de referência. Dia H/S= qualquer dia com hemorragia vaginal com utilização ≥ 1 penso higiénico ou tampão Episódio H/S = um ou mais dias consecutivos com hemorragia/spotting. Períodos de referência 2– 6. Número de mulheres = 780. 1. Mansour D et al. Eur J Contracept Reprod Health Care. 2008; 13(suppl 1): 13– 28. 16

Dismenorreia 1 ► ► ► No início do estudo, 315 das 647 mulheres referiram dismenorreia ligeira, moderada ou grave (48, 7%). Durante a utilização de IMPLANON® (implante de etonogestrel), 77% referiram que os seus sintomas tinham desaparecido e 6% referiram redução da sua gravidade. Houve desenvolvimento ou agravamento da dismenorreia em 5, 5% das mulheres tendo sido relatado como um efeito adverso frequente (≥ 1% e <10%) nos ensaios clínicos. Desenho do estudo Mansour: Dados de 11 ensaios clínicos realizados em diversos países (n=923, 18– 40 anos de idade). Todos os ensaios tiveram um desenho aberto e eram não comparativos ou comparativos com Norplant ou um dispositivo intrauterino não medicado. A maioria dos ensaios durou, pelo menos, 2 anos, tendo parâmetros de avaliação de eficácia contracetiva e hemorragia e apresentavam um esquema de visitas de 3 em 3 meses incluindo até 3 meses após a remoção do implante, Todas as participantes registaram os dados relativos a hemorragia em períodos de referência de 90 dias. 1 1. Mansour D et al. Eur J Contracept Reprod Health Care. 2008; 13(suppl 1): 13– 28. 17

Reações adversas que levam a descontinuação de tratamento 1 ►Em ensaios clínicos de IMPLANON® (implante de etonogestrel) envolvendo 942 mulheres, os efeitos adversos foram a causa mais frequente para descontinuação do tratamento Causa para a descontinuação Todos os estudos (N=942) Eventos adversos 13, 9% Hemorragias irregulares 10, 4% Gravidez planeada 4. 1% Outras causas 3, 5% Perda para seguimento 2, 4% Amenorreia 0, 7% Desenho do estudo: análise de segurança integrada baseada nos 11 ensaios clínicos internacionais (n=942), mulheres a usar IMPLANON® para 24. 679 ciclos durante 1 -5 anos. 1. Blumenthal PD et al. Eur J Contracept Reprod Health Care. 2008; 13(Suppl 1): 29– 36. 18
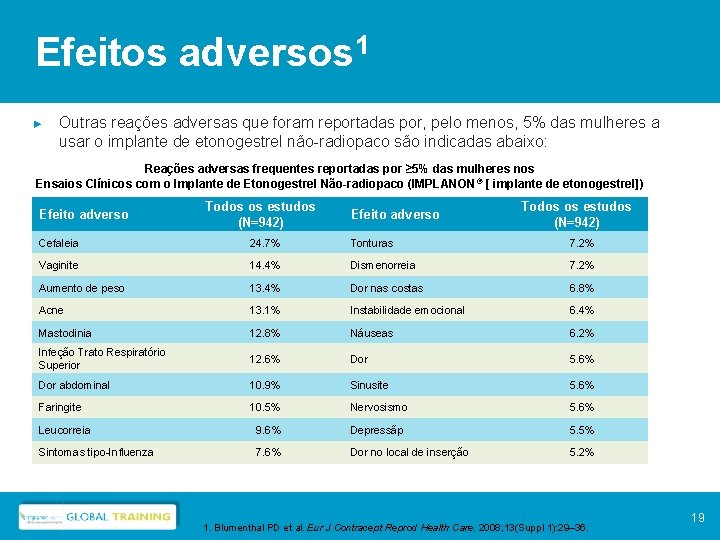
Efeitos adversos 1 ► Outras reações adversas que foram reportadas por, pelo menos, 5% das mulheres a usar o implante de etonogestrel não-radiopaco são indicadas abaixo: Reações adversas frequentes reportadas por ≥ 5% das mulheres nos Ensaios Clínicos com o Implante de Etonogestrel Não-radiopaco (IMPLANON ® [ implante de etonogestrel]) Efeito adverso Todos os estudos (N=942) Cefaleia 24. 7% Tonturas 7. 2% Vaginite 14. 4% Dismenorreia 7. 2% Aumento de peso 13. 4% Dor nas costas 6. 8% Acne 13. 1% Instabilidade emocional 6. 4% Mastodinia 12. 8% Náuseas 6. 2% Infeção Trato Respiratório Superior 12. 6% Dor 5. 6% Dor abdominal 10. 9% Sinusite 5. 6% Faringite 10. 5% Nervosismo 5. 6% Leucorreia 9. 6% Depressãp 5. 5% Sintomas tipo-Influenza 7. 6% Dor no local de inserção 5. 2% 1. Blumenthal PD et al. Eur J Contracept Reprod Health Care. 2008; 13(Suppl 1): 29– 36. 19

Complicações da inserção e remoção ► ► ► A inserção e remoção do implante podem causar algum hematoma, ligeira irritação local, dor ou prurido. Pode ocorrer fibrose no local da inserção, formar‑se uma cicatriz ou desenvolver‑se um abcesso. Pode ocorrer parestesia ou sintomas do tipo parestesia. Foram notificados casos de migração do implante no interior do braço a partir do local de inserção, o que poderá estar relacionado com inserções profundas ou fatores externos (por ex. , manipulação do implante ou desportos de contacto). Foram também notificados casos raros, pós-introdução no mercado, de implantes localizados nos vasos do braço e artéria pulmonar, o que poderá estar relacionado com inserções profundas ou inserções intravasculares. Nos casos de implantes encontrados no interior da artéria pulmonar foi relatada dor torácica e/ou alterações respiratórias (tais como dispneia, tosse ou hemoptise). 20

Complicações da inserção e remoção (continuação) ► ► Nos casos em que o implante migrou do local de inserção no interior do braço, a localização do implante pode ser mais difícil e a remoção pode requerer um procedimento cirúrgico minor com uma incisão maior ou um procedimento cirúrgico numa sala de operações. Nos casos em que o implante migrou para a artéria pulmonar, poderão ser necessários procedimentos endovasculares ou cirúrgicos para a remoção Se, a qualquer momento, o implante não for palpável, este deverá ser localizado e recomenda-se a sua remoção. Se o implante não for removido, a contraceção e o risco de efeitos indesejáveis relacionados com o progestagénio poderão prolongar-se para além do tempo desejado pela mulher. 21

Utilização durante o aleitamento ► ► ► São excretadas pequenas quantidades de etonogestrel no leite materno (~ 0, 2% da dose materna absoluta estimada). Estudo comparativo: DIU - cobre (n=33) vs. IMPLANON® (implante de etonogestrel) (n= 38), lactentes seguidos até 36 meses: – Não foi detetado qualquer efeito na qualidade ou quantidade do leite – Não se observou diferença no crescimento e desenvolvimento do lactente entre IMPLANON® e um DIU Para mais informação consultar a Informação de produto aprovada DIU = Dispositivo intrauterino 22

Contraindicações ► ► ► ► Conhecimento ou suspeita de gravidez Doença tromboembólica venosa ativa Neoplasias malignas conhecidas ou suspeitas sensíveis aos esteroides sexuais Presença ou antecedentes de tumores hepáticos (benignos ou malignos) Presença ou antecedente de doença hepática grave enquanto o caso os valores da função hepática não tenham normalizado. Hemorragia vaginal não diagnosticada. Hipersensibilidade à substância ativa ou a qualquer dos excipientes de IMPLANON NXT®(implante de etonogestrel). 23

Exposição ao IMPLANON NXT® (implante de etonogestrel) durante a gravidez ► ► Caso ocorra uma gravidez durante a utilização de IMPLANON NXT®, deve remover-se o implante. A vigilância pós-introdução no mercado desde o lançamento mundial de IMPLANON® (implante de etonogestrel) (1998) não indica efeitos adversos para o feto. Estudos epidemiológicos extensivos revelaram não existir um risco aumentado de malformações fetais em crianças nascidas de mulheres que utilizaram contracetivos orais (CO) antes de engravidar, nem de efeitos teratogénicos quando foram tomados inadvertidamente CO durante a gravidez Embora isto se aplique provavelmente a todos os CO, não é claro se isto também se aplica a IMPLANON NXT. 24

Advertências e precauções especiais de utilização ► Risco de cancro de mama ► Distúrbios da função hepática ► Eventos tromboembólicos arteriais e venosos ► Hipertensão ► Resistência à insulina e tolerância à glucose ► Hiperlipidemia ► Cloasma 25

Advertências e precauções especiais de utilização (continuação) ► Peso corporal ► Migração do implante ► Implante partido ou dobrado in situ ► Desenvolvimento folicular ► Gravidez ectópica ► Doenças relacionadas com a utilização de esteroides sexuais 26

Interações Podem ocorrer interações com medicamentos ou produtos à base de plantas que induzem as enzimas microssomais, especificamente as do grupo do Citocromo P 450, que podem resultar numa eliminação das hormonas sexuais e reduzir a eficácia de IMPLANON NXT ® (implante de etonogestrel): ► ► Ex. fenitoína, fenobarbital, primidona, bosentano, carbamazepina, rifampicina ► Medicamentos para o tratamento do VIH (ex. ritonavir, nelfinavir, nevirapina, efavirenz) ► possivelmente, também oxcarbazepina, topiramato, felbamato, griseofulvina e produtos medicinais à base de erva de S. João Muitas combinações de inibidores da protease do VIH (por ex. , nelfinavir) e inibidores da transcriptase reversa não nucleósidos (por ex. , nevirapina) e/ou associações com medicamentos para o tratamento do VHC (ex. boceprevir, telaprevir) podem aumentar ou diminuir as concentrações plasmáticas dos progestagénios, incluindo o etonogestrel. O efeito global destas alterações pode ser clinicamente relevante em alguns casos VHC = vírus da hepatite C; VIH= vírus da imunodeficiência humana. 27

Interações (continuação) ► As mulheres a fazer tratamento com qualquer um dos medicamentos ou produtos à base de ervas indutores de enzimas hepáticas indicados devem ser avisadas de que a eficácia do IMPLANON NXT ® (implante de etonogestrel) pode estar reduzida. ► Caso seja decido continuar a usar o IMPLANON NXT deve aconselhar -se a mulher a usar também um método contracetivo não hormonal durante o tempo da administração concomitante e nos 28 dias após a suspensão. 28

GLOBALTRAINING Aconselhamento 29

Pontos de aconselhamento Discutir os benefícios, riscos e possíveis efeitos colaterais: ► Eficácia elevada. ► Nenhum método contracetivo é 100% eficaz. ► Retorno ao ciclo menstrual normal. ► Se inserido corretamente, pode ser removido a qualquer momento. ► Não deve ser usado durante mais de 3 anos e terá de ser removido no final desse período de tempo. ► Contraindicações. ► Efeitos colaterais, salientando a alteração do padrão de hemorragia. ► Ausência de proteção contra IST e VIH = virus da imunodeficiência humana; IST = infeções sexualmente transmitssíveis 30

Pontos de aconselhamento (continuação) Alterações no padrão de hemorragia e dismenorreia 1: ► ► Durante a utilização de IMPLANON NXT® (implante de etonogestrel), é provável que as mulheres apresentem alterações no seu padrão de hemorragia menstrual. Cerca de 20% das mulheres tiveram amenorreia. Cerca de 20% das mulheres tiveram hemorragias frequentes e/ou prolongadas. Houve uma tendência para a melhoria da dismenorreia. 1. Mansour D et al. Eur J Contracept Reprod Health Care. 2008; 13(suppl 1): 13– 28. 31

Pontos de aconselhamento (continuação) ► ► ► Informe as mulheres que, nos ensaios clínicos, as alterações hemorrágicas foram a causa mais frequente para a interrupção do tratamento com IMPLANON NXT® (implante de etonogestrel) (11%). Explique os procedimentos da inserção e remoção – O implante deve ser palpável. – Pode haver remoções difíceis e cicatrizes/complicações Conceda à mulher tempo suficiente para rever, considerar e fazer perguntas. 32

GLOBALTRAINING Inserção com aplicador, localização, remoção e reinserção 33

Antes da inserção de IMPLANON NXT® (Implante de etonogestrel) ► O profissional de saúde deverá confirmar o seguinte: – Foi recolhida a história clínica completa da mulher e foi realizado um exame físico – A mulher não está grávida e não tem outras contraindicações relativas ao IMPLANON NXT® – A mulher compreende os riscos e benefícios do IMPLANON NXT® – A mulher recebeu uma cópia da informação do produto contido na embalagem – A mulher analisou e completou o formulário de consentimento que deverá ser guardado no seu processo clínico. – A mulher não tem alergias ao antisséptico ou anestésico que será usado durante a inserção 34

Materiais para inserção ► Insira o IMPLANON NXT ® sob condições assépticas ► O seguinte material é necessário para a inserção do implante: – Uma marquesa para deitar a mulher – Campo cirúrgico estéril – Luvas esterilizadas – Solução antisséptica – Marcador esterilizado – Anestésico local – Agulhas e seringa – Gaze esterilizada – Penso adesivo – Penso compressivo Imagem fornecida para efeito de demonstração 35

Posicione a mulher antes da inserção Para ajudar a garantir que o implante é inserido imediatamente sob a pele, o profissional de saúde deve estar posicionado de forma a ver o avanço da agulha ao olhar lateralmente para o aplicador e não por cima do braço. Desta forma, o local de inserção e o movimento da agulha imediatamente sob a pele são claramente visíveis. 36
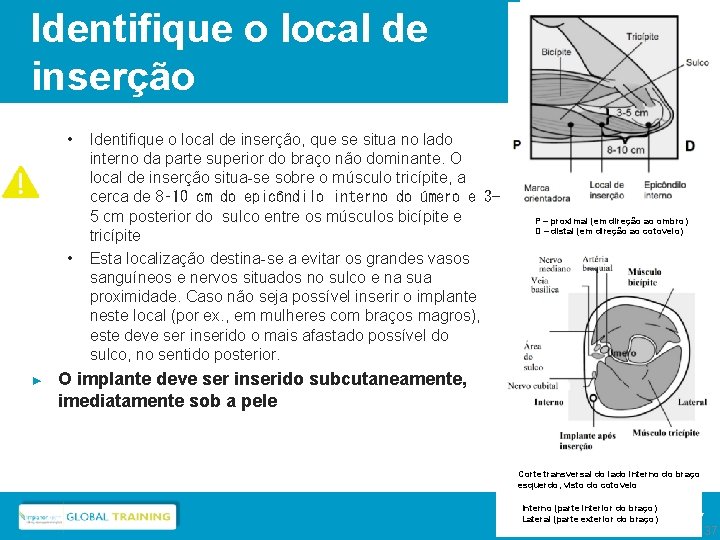
Identifique o local de inserção • • ► Identifique o local de inserção, que se situa no lado interno da parte superior do braço não dominante. O local de inserção situa-se sobre o músculo tricípite, a cerca de 8‑ 10 cm do epicôndilo interno do úmero e 35 cm posterior do sulco entre os músculos bicípite e tricípite Esta localização destina-se a evitar os grandes vasos sanguíneos e nervos situados no sulco e na sua proximidade. Caso não seja possível inserir o implante neste local (por ex. , em mulheres com braços magros), este deve ser inserido o mais afastado possível do sulco, no sentido posterior. P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) O implante deve ser inserido subcutaneamente, imediatamente sob a pele Corte transversal do lado interno do braço esquerdo, visto do cotovelo Interno (parte interior do braço) Lateral (parte exterior do braço) 37 37
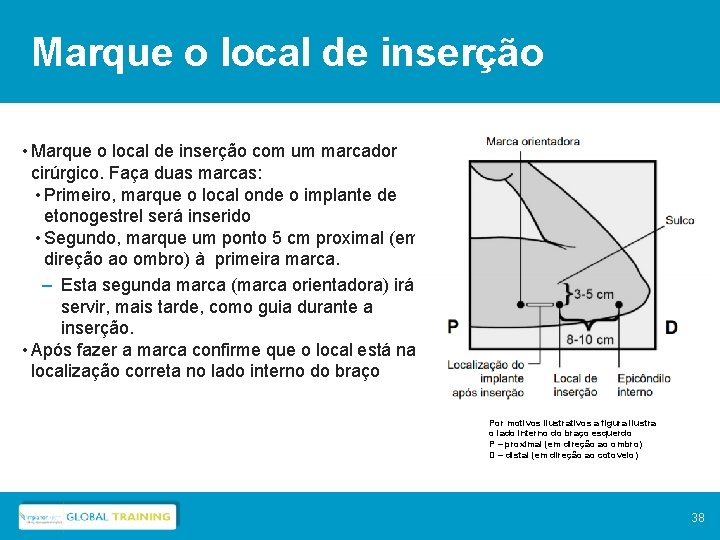
Marque o local de inserção • Marque o local de inserção com um marcador cirúrgico. Faça duas marcas: • Primeiro, marque o local onde o implante de etonogestrel será inserido • Segundo, marque um ponto 5 cm proximal (em direção ao ombro) à primeira marca. – Esta segunda marca (marca orientadora) irá servir, mais tarde, como guia durante a inserção. • Após fazer a marca confirme que o local está na localização correta no lado interno do braço Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 38

Inserção do IMPLANON NXT ® (implante de etonogestrel) ► ► ► Limpe a pele desde o local de inserção até à marca guia com uma solução antisséptica. Anestesie a área de inserção (por exemplo, com um spray anestésico ou com uma injeção de 2 ml de lidocaína a 1 %, imediatamente sob a pele ao longo do canal de inserção planeado) Retire da saqueta o aplicador pré-carregado estéril e descartável de IMPLANON NXT® que contém o implante. O aplicador não deve ser usado se a sua esterilidade estiver em causa. Segure o aplicador imediatamente acima da agulha, na área de superfície com textura. Retire a tampa transparente de proteção fazendo-a deslizar horizontalmente na direção da seta no sentido oposto à agulha. Deverá ver o implante de cor branca no interior da ponta da agulha Se a tampa não sair facilmente, o aplicador não deve ser utilizado Não toque na patilha roxa até ter inserido completamente a agulha subcutaneamente, pois isso irá retrair a agulha e libertar prematuramente o implante do aplicador Se a patilha roxa se libertar prematuramente, reinicie o procedimento com um aplicador novo 39

Inserção do IMPLANON NXT ® (implante de etonogestrel) (continuação) ►Para ajudar a garantir que o implante é inserido imediatamente sob a pele, o profissional de saúde deve estar posicionado de forma a ver o avanço da agulha ao olhar lateralmente para o aplicador e não por cima do braço. Desta forma, observa claramente o local de inserção e o movimento da agulha imediatamente sob a pele ►Com a sua mão livre, estique a pele à volta do local de inserção em direção ao cotovelo • O implante deve ser inserido subcutaneamente, imediatamente sob a pele • Perfure a pele com a ponta da agulha, num ângulo ligeiramente inferior a 30º Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 40 40
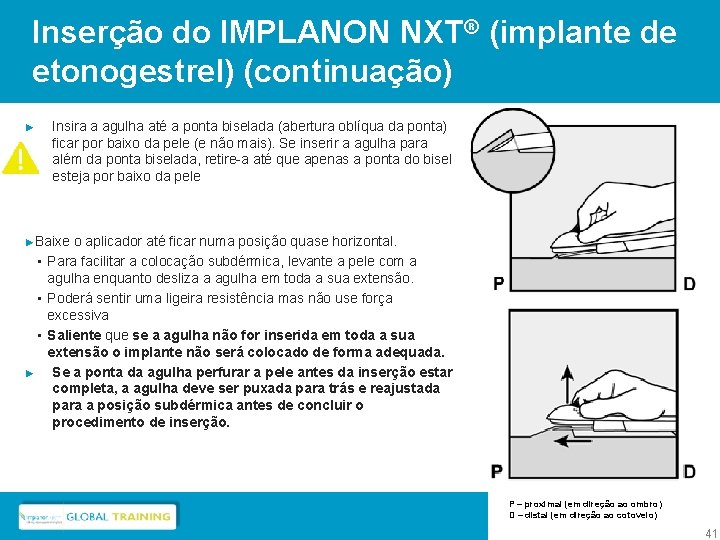
Inserção do IMPLANON NXT® (implante de etonogestrel) (continuação) ► Insira a agulha até a ponta biselada (abertura oblíqua da ponta) ficar por baixo da pele (e não mais). Se inserir a agulha para além da ponta biselada, retire-a até que apenas a ponta do bisel esteja por baixo da pele ►Baixe o aplicador até ficar numa posição quase horizontal. • Para facilitar a colocação subdérmica, levante a pele com a agulha enquanto desliza a agulha em toda a sua extensão. • Poderá sentir uma ligeira resistência mas não use força excessiva • Saliente que se a agulha não for inserida em toda a sua extensão o implante não será colocado de forma adequada. ► Se a ponta da agulha perfurar a pele antes da inserção estar completa, a agulha deve ser puxada para trás e reajustada para a posição subdérmica antes de concluir o procedimento de inserção. P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 41 41
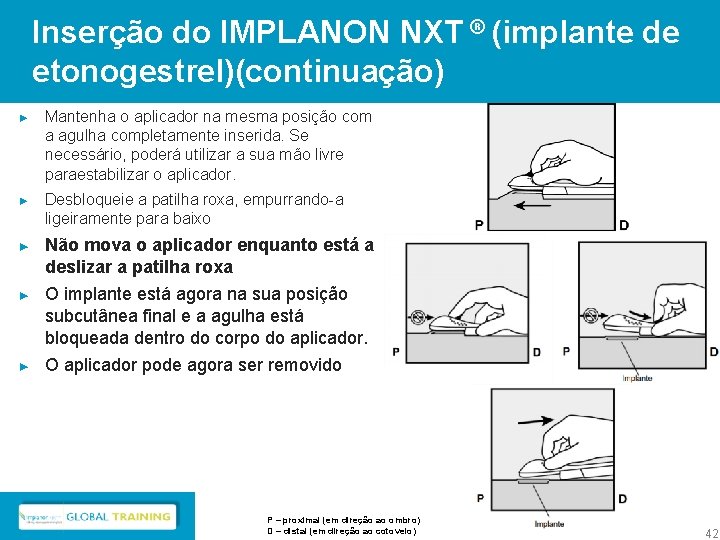
Inserção do IMPLANON NXT ® (implante de etonogestrel)(continuação) ► Mantenha o aplicador na mesma posição com a agulha completamente inserida. Se necessário, poderá utilizar a sua mão livre paraestabilizar o aplicador. ► Desbloqueie a patilha roxa, empurrando-a ligeiramente para baixo ► Não mova o aplicador enquanto está a deslizar a patilha roxa ► O implante está agora na sua posição subcutânea final e a agulha está bloqueada dentro do corpo do aplicador. ► O aplicador pode agora ser removido P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 42 42

Inserção do IMPLANON NXT ® (implante de etonogestrel) (continuação) ► Se o aplicador não se mantiver na mesma posição durante este procedimento ou se a patilha roxa não for estiver toda puxada para trás, o implante não será inserido de forma adequada e pode sair do local de inserção. ► Se o implante estiver a sair do local de inserção, retire o implante e efetue um novo procedimento no mesmo local de inserção usando um novo aplicador. Não empurre o implante saliente novamente para dentro da incisão ► 43
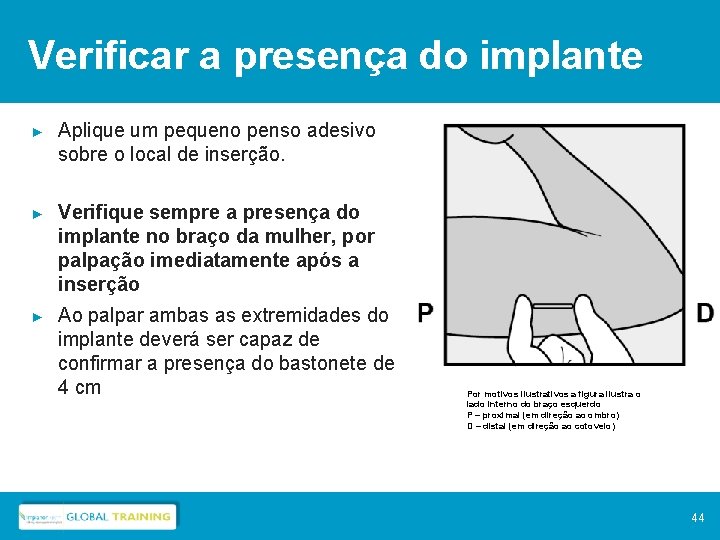
Verificar a presença do implante ► Aplique um pequeno penso adesivo sobre o local de inserção. ► Verifique sempre a presença do implante no braço da mulher, por palpação imediatamente após a inserção ► Ao palpar ambas as extremidades do implante deverá ser capaz de confirmar a presença do bastonete de 4 cm Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 44

Passos pós-inserção ► Peça à mulher que palpe o implante ► Aplique uma compressa estéril com um penso compressivo para minimizar equimoses ► A mulher poderá retirar o penso compressivo ao fim de 24 horas e o pequeno penso adesivo colocado sobre o local de inserção ao fim de 3‑ 5 dias ► Preencha o Cartão de Alerta da Doente e dê-o à mulher para guardar ► Preencha também as etiquetas autocolantes e cole-as no registo clínico da mulher. O aplicador destina-se a utilização única e deve ser eliminado de forma adequada, de acordo com as exigências locais para o manuseamento de resíduos com potencial risco biológico. ► ► 45

Se o implante não for palpável após a inserção ► Se não conseguir palpar o implante ou em caso de dúvida relativamente à sua presença, o implante pode não ter sido inserido ou pode ter sido inserido profundamente: – Verifique o aplicador. A agulha deve estar totalmente retraída e apenas deve ser visível a patilha roxa do obturador. – Utilize outros métodos para confirmar a sua presença. Devido à natureza radiopaca do implante, os métodos adequados para a sua localização são: • Radiografia bidimensional • Tomografia computorizada por radiografia (TC) • Ecografia com um transdutor linear de alta frequência (10 MHz ou superior) • Ressonância magnética (RM) 46

Se o implante não for palpável após a inserção (continuação) ► Caso estes métodos de imagiologia falhem, aconselha‑se a confirmação da presença do implante no braço através da medição do nível (doseamento) de etonogestrel numa amostra de sangue da mulher. Neste caso, o representante local da MSD irá indicar‑lhe o protocolo apropriado. ► Até que tenha confirmado a presença do implante, terá de ser utilizado um método contracetivo não hormonal ► Os implantes localizados profundamente devem ser localizados e removidos assim que possível de modo a evitar o potencial de migração à distância 47

Vídeo sobre a inserção http: //www. implanonnxtvideos. eu 48

GLOBALTRAINING Questões 49

GLOBALTRAINING Localização 50

A localização é essencial ► ► Um implante não palpável deve sempre ser localizado antes da tentativa de remoção A localização começa com a palpação Se o implante não for palpável após a inserção, confirme a sua presença no braço com técnicas de imagiologia – Radiografia bidimensional – Tomografia computorizada por radiografia (TC) – Ecografia com um transdutor linear de alta frequência (10 MHz ou superior) – Ressonância magnética Caso a mulher tenha dúvidas quanto à presença do implante (não é capaz de sentir o implante), esta deve utilizar um método contracetivo alternativo até que a presença do implante possa ser confirmada. TC- tomografia computorizada 51

A localização é essencial (continuação) ► ► Têm sido notificados casos de migração do implante; habitualmente esta ocorrência envolve uma pequena deslocação relativamente à posição inicial mas poderá levar a que o implante não seja palpável na localização em que foi inserido. Um implante que tenha sido inserido profundamente ou que tenha migrado pode não ser palpável e por isso, podem ser necessários procedimentos de imagiologia, como os descritos, para a sua localização. 52

A localização é essencial (continuação) ► ► ► Se o implante não for detetado no braço após tentativas de localização exaustivas, considere aplicar as técnicas de imagiologia ao tórax uma vez que foram notificados casos de migração para a vasculatura pulmonar. Se o implante for localizado no tórax, poderão ser necessários procedimentos cirúrgicos ou endovasculares para a remoção; devem ser consultados profissionais de saúde familiarizados com a anatomia do tórax. Caso estes métodos de imagiologia falhem na localização do implante, a presença do implante poderá ser verificada através da medição do nível (doseamento) de etonogestrel numa amostra de sangue. Contacte o representante local da MSD para instruções adicionais. Caso a mulher tenha dúvidas quanto à presença do implante (não é capaz de sentir o implante), esta deve utilizar um método contracetivo alternativo até que a presença do implante possa ser confirmada. 53

Na altura da remoção pode estar presente 1 dos 2 implantes ► ► ► Deve estar ciente de que pode encontrar doentes com implantes de etonogestrel não rádio-opacos (IMPLANON ® [implante de etonogestrel]) O cartão da doente deve identificar de forma clara qual o tipo de implante que foi utilizado – IMPLANON ® (Não-radiopaco) – IMPLANON NXT ® (Radiopaco) As técnicas de imagiologia a utilizar para localizar um implante não palpável dependem do tipo de implante 54
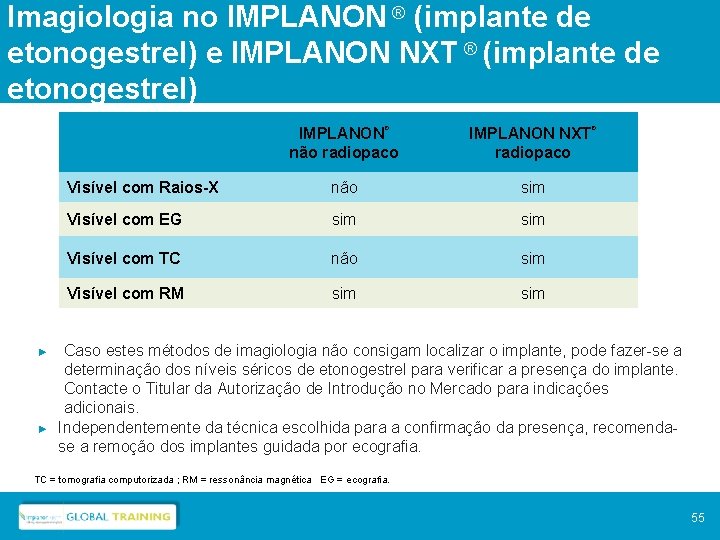
Imagiologia no IMPLANON ® (implante de etonogestrel) e IMPLANON NXT ® (implante de etonogestrel) ► ► IMPLANON® não radiopaco IMPLANON NXT® radiopaco Visível com Raios-X não sim Visível com EG sim Visível com TC não sim Visível com RM sim Caso estes métodos de imagiologia não consigam localizar o implante, pode fazer-se a determinação dos níveis séricos de etonogestrel para verificar a presença do implante. Contacte o Titular da Autorização de Introdução no Mercado para indicações adicionais. Independentemente da técnica escolhida para a confirmação da presença, recomendase a remoção dos implantes guidada por ecografia. TC = tomografia computorizada ; RM = ressonância magnética EG = ecografia. 55
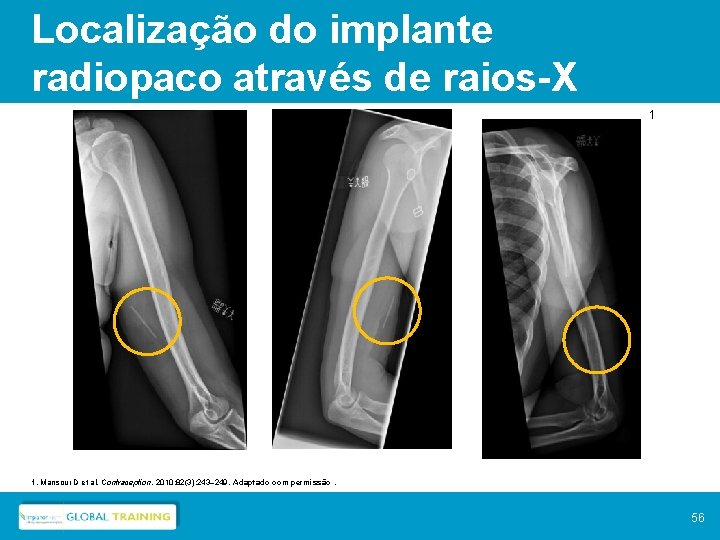
Localização do implante radiopaco através de raios-X 1 1. Mansour D et al. Contraception. 2010; 82(3): 243– 249. Adaptado com permissão. 56

Localização por ecografia 1, 2 Ecografia ► Deve ser realizada por um profissional de saúde familiarizado com os procedimentos de localização de implantes e com equipamento de ecografia adequado: • Com um transdutor linear • Com uma frequência igual ou superior a 10 MHz ► – Regule a focagem da ecografia para visualização superficial (aumenta a visibilidade da sombra) e desligue o software de otimização de imagem – Com uma técnica e transdutores adequados: é possível localizar os implantes – Idealmente deve proceder à remoção pouco depois/durante a localização, para aumentar precisão da remoção Características ecográficas – Sombra acústica bem definida por baixo do implante em posição transversal. – O implante é um pequeno ponto ecogénico (2 mm) quando observado transversalmente 1. Shulman LP et al. Contraception. 2006; 73(4): 325– 330. 2. Walling M. J Fam Plann Reprod Health Care. 2005; 31(4): 320– 321. 57
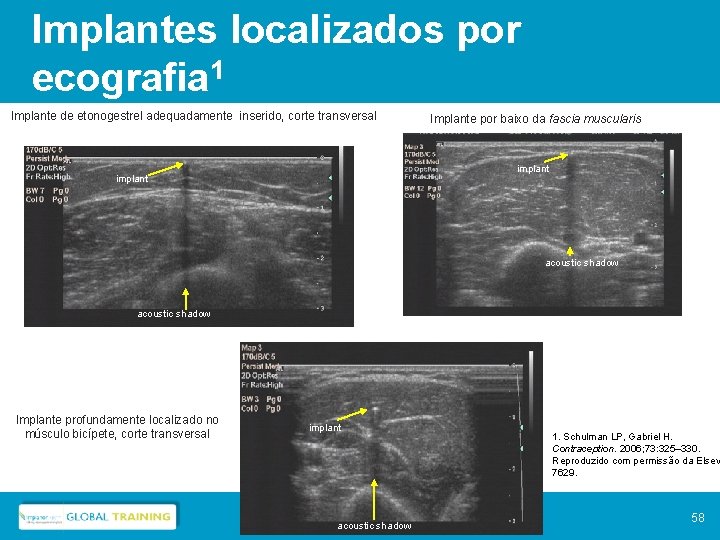
Implantes localizados por ecografia 1 Implante de etonogestrel adequadamente inserido, corte transversal Implante por baixo da fascia muscularis implant acoustic shadow Implante profundamente localizado no músculo bicípete, corte transversal implant acoustic shadow 1. Schulman LP, Gabriel H. Contraception. 2006; 73: 325– 330. Reproduzido com permissão da Elsev 7629. 58

Localização por RM 1 ► ► ► O implante surge como uma área hipodensa É importante distinguilo dos vasos sanguíneos. Pode ser acompanhado em imagem sequenciais até aos 40 mm. RM= ressonância magnética. 1. Merki-Feld GS, et al. Contraception. 2001; 63(6): 325 -328; 2. Westerway SC, et al. Aust N Z J Obstet Gynaecol. 2003; 43(5): 346 -350. 3. Shulman LP, Gabriel H. Contraception. 2006; 73(4): 325 -330. Reproduzido com permissão da Elsevier, 7629 59
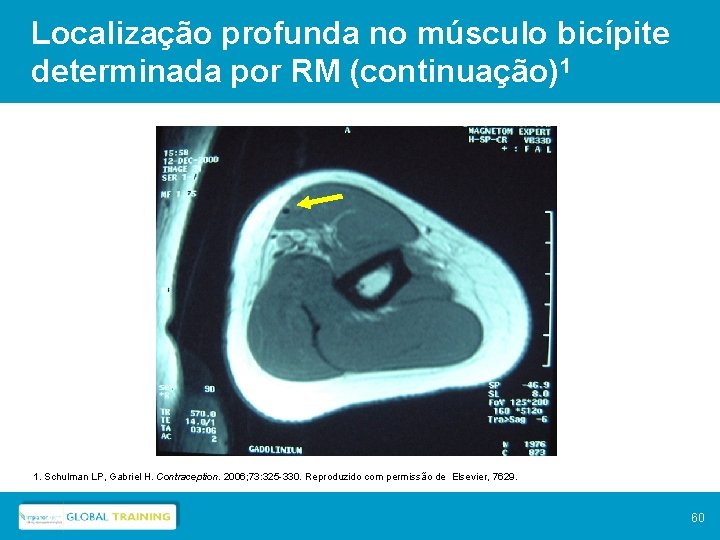
Localização profunda no músculo bicípite determinada por RM (continuação)1 1. Schulman LP, Gabriel H. Contraception. 2006; 73: 325 -330. Reproduzido com permissão de Elsevier, 7629. 60

Caso os métodos de imagem não permitam identificar o implante ► Pode requisitar-se um doseamento de etonogestrel para confirmar a presença do IMPLANON NXT® (implante de etonogestrel) mas não a sua localização ► Contacte o representante local da MSD para assistência adicional 61

GLOBALTRAINING Questões 62

GLOBALTRAINING Remoção e Reinserção 63

Preparação ► ► ► A remoção do implante deve ser feita apenas sob condições assépticas por um profissional de saúde familiarizado com a técnica de remoção. Caso não esteja familiarizado com a técnica de remoção contacte o representante local da MSD. Antes de iniciar o processo de remoção, o prestador de cuidados de saúde deve avaliar a localização do implante e ler cuidadosamente as instruções de remoção. A localização exata do implante no braço deve ser verificada por palpação Se o implante não for palpável consulte o cartão da utilizadora ou o registo médico para verificar qual o braço que contém o implante Se o implante não for palpável pode estar localizado profundamente ou ter migrado. Considere que pode estar perto de vasos e nervos A remoção de implantes não palpáveis deve ser realizada apenas por profissionais de saúde com experiência na remoção de implantes profundos e familiarizado com a localização do implante e com a anatomia do braço. Contacte o representante local da MSD para informações adicionais 64

Procedimento de remoção de um implante palpável ► Confirme que a mulher não tem alergias ao antisséptico ou ao anestésico que vai ser usado. 65

Equipamento necessário para a remoção do IMPLANON NXT® (implante de etonogestrel) ► O seguinte material é necessário para a remoção do implante: – Uma marquesa para a mulher se deitar – Campo cirúrgico estéril – Luvas esterilizadas – Solução antisséptica – Marcador esterilizado – Anestésico local – Agulhas e seringa – Bisturi esterilizado – Pinças (reta e mosquito curvo) – Material para encerramento da pele – Gaze esterilizada – Penso compressivo Imagem fornecida para efeito de demonstração 66

Remoção do IMPLANON NXT® (implante de etonogestrel) ► ► Peça à mulher que se deite de costas na marquesa. O braço deve ser posicionado com o cotovelo fletido e a mão por baixo da cabeça (ou o mais perto possível) Localize o implante por palpação. Empurre para baixo a extremidade do implante mais próxima do ombro de modo a estabilizá-lo; deve aparecer uma saliência, indicando a ponta do implante mais próxima do cotovelo. Se a ponta não aparecer, a remoção do implante pode ser difícil e deve ser realizada por profissionais com experiência em remover implantes mais profundos. Contacte o representante local da MSD para informação adicional Marque a extremidade distal (a extremidade mais próxima do cotovelo), utilizando, por exemplo, um marcador cirúrgico Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo 67 P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 67

Remoção do IMPLANON NXT® (implante de etonogestrel) (continuação) ► ► Limpe o local com uma solução antisséptica. Anestesie o local com, por exemplo, 0, 5 a 1 ml de lidocaína a 1% no local onde será feita a incisão – Certifique-se de que injeta o anestésico local por baixo do implante, de modo a mantê-lo próximo da superfície da pele. – A injeção de anestésico local sobre o implante pode tornar a remoção mais difícil. Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 68

Remoção do IMPLANON NXT® (implante de etonogestrel) (continuação) ► ► ► Empurre para baixo a extremidade do implante mais próxima do ombro para o estabilizar durante o procedimento Começando pela extremidade do implante mais próxima do cotovelo, faça uma incisão longitudinal (paralela ao implante) de 2 mm em direção ao cotovelo Tenha cuidado para não cortar a ponta do implante. Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 69
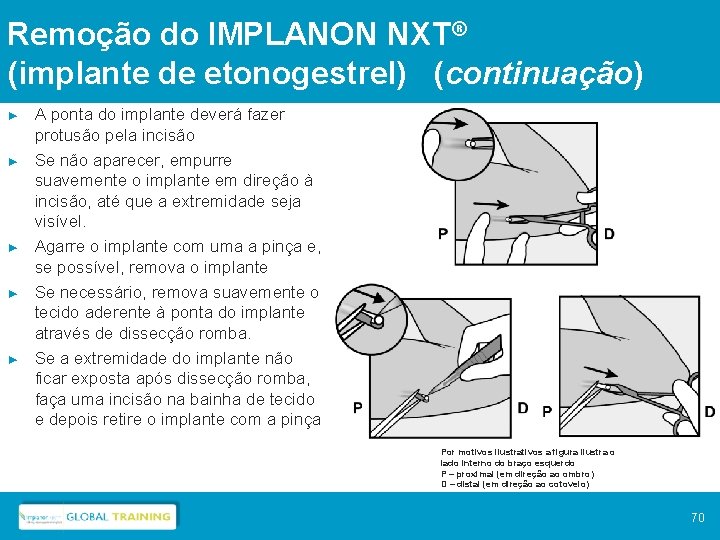
Remoção do IMPLANON NXT® (implante de etonogestrel) (continuação) ► ► ► A ponta do implante deverá fazer protusão pela incisão Se não aparecer, empurre suavemente o implante em direção à incisão, até que a extremidade seja visível. Agarre o implante com uma a pinça e, se possível, remova o implante Se necessário, remova suavemente o tecido aderente à ponta do implante através de dissecção romba. Se a extremidade do implante não ficar exposta após dissecção romba, faça uma incisão na bainha de tecido e depois retire o implante com a pinça Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 70

Remoção do IMPLANON NXT ® (continuação) ► ► Se a extremidade do implante não ficar visível no local da incisão, insira uma pinça (de preferência um mosquito curvo com as pontas viradas para cima) superficialmente na incisão Agarre suavemente o implante e gire a pinça até à sua outra mão. Com uma segunda pinça, disseque cuidadosamente o tecido à volta do implante e agarre o implante. O implante pode então ser removido. Se não for possível agarrar o implante, interrompa o procedimento e encaminhe a mulher para um profissional de saúde com experiência em remoções complexas ou contacte o representante local da MSD Por motivos ilustrativos a figura ilustra o lado interno do braço esquerdo P – proximal (em direção ao ombro) D – distal (em direção ao cotovelo) 71 71

Remoção do IMPLANON NXT® (implante de etonogestrel) (continuação) ► ► ► Confirme que a totalidade do bastonete, que tem 4 cm de comprimento, foi removida medindo o seu comprimento. Têm sido notificados casos de implantes partidos enquanto estão inseridos no braço da mulher Em alguns casos, foi notificada uma difícil remoção do implante partido Caso seja removido um implante parcial (menos de 4 cm) a restante porção deverá ser removida Se a mulher pretender continuar a utilizar IMPLANON NXT®, pode ser inserido um novo implante imediatamente após a remoção do implanterior, utilizando a mesma incisão, desde que o local seja o correto 72

Após a remoção do implante ► ► Feche a incisão com um adesivo estéril para fechar feridas Aplique uma compressa esterilizada estéril para minimizar hematomas – A mulher poderá retirar o penso compressivo após 24 horas e o adesivo estéril para fechar feridas ao fim de 3 - 5 dias ► A mulher deve retomar a contraceção imediatamente após a remoção do implante caso deseje manter uma proteção contracetiva 73

Vídeo de remoção 74

Fatores que podem complicar a remoção ► ► ► Implante não inserido corretamente Implante inserido demasiado profundamente Implante não palpável Implante encapsulado em tecido fibroso Migração do implante 75

Remoção de um implante não palpável ► ► ► Um implante não palpável deve ser sempre localizado antes de qualquer tentativa de remoção. A cirurgia exploratória sem o conhecimento da localização exata do implante é fortemente desaconselhada. Após a localização do implante no braço, o implante deverá ser removido por um profissional de saúde experiente na remoção de implantes localizados profundamente e familiarizado com a anatomia do braço, devendo considerar-se o uso de ecografia 76

Remoção de um implante não palpável (continuação) ► ► ► Se o implante não for detetado no braço após tentativas de localização exaustivas, considere aplicar as técnicas de imagiologia ao tórax uma vez que foram notificados casos de migração para a vasculatura pulmonar. Se o implante for localizado no tórax, poderão ser necessários procedimentos cirúrgicos ou endovasculares para a remoção; devem ser consultados profissionais de saúde familiarizados com a anatomia do toráx. Se o implante migrar dentro do braço, a remoção poderá exigir obrigar a um procedimento cirúrgico minor com uma incisão maior ou um procedimento cirúrgico numa sala de operações 77

Remoção de um implante não palpável (continuação) ► ► A remoção de implantes inseridos profundamente deve ser efetuada com precaução de forma a prevenir a lesão de estruturas neurais e vasculares profundas do braço e deve ser realizada por profissionais de saúde familiarizados com a anatomia do braço Se não estiver familiarizado ou se sentir desconfortável com a remoção de implantes inseridos profundamente contacte por favor o representante local da MSD para instruções adicionais 78

GLOBALTRAINING Questões 79

GLOBALTRAINING Reinserção 80

Substituição do IMPLANON NXT® (implante de etonogestrel) ► ► ► A substituição imediata pode ser realizada após a remoção do implanterior e é semelhante ao procedimento de inserção descrito nas instruções de inserção O novo implante pode ser inserido no mesmo braço e através da mesma incisão que serviu para a remoção do implanterior, desde que se situe no local correto, ou seja, 8‑ 10 cm do epicôndilo mediano do úmero e 3 -5 cm posterior do sulco (abaixo). Se a mesma incisão for usada para inserir o novo implante, anestesie o local de inserção (por exemplo 2 ml de lidocaína a 1%), imediatamente sob a pele, começando na incisão da remoção ao longo “do canal de inserção”, e siga as etapas subsequentes das instruções de inserção 81

GLOBALTRAINING Questões 82

GLOBALTRAINING Muito obrigado Copyright © 2019 Merck Sharp & Dohme B. V. , a subsidiary of Merck & Co. , Inc. , Kenilworth, NJ, USA. All rights reserved. HQ-XPL-00036 04/20 83
- Slides: 83