Glicsidos Nombre general para un aglicn unido covalentemente

Glicósidos • Nombre general para un aglicón unido covalentemente a un residuo glicosilo. • En plantas: acumulación, almacenamiento y transporte de substancias hidrofóbicas.
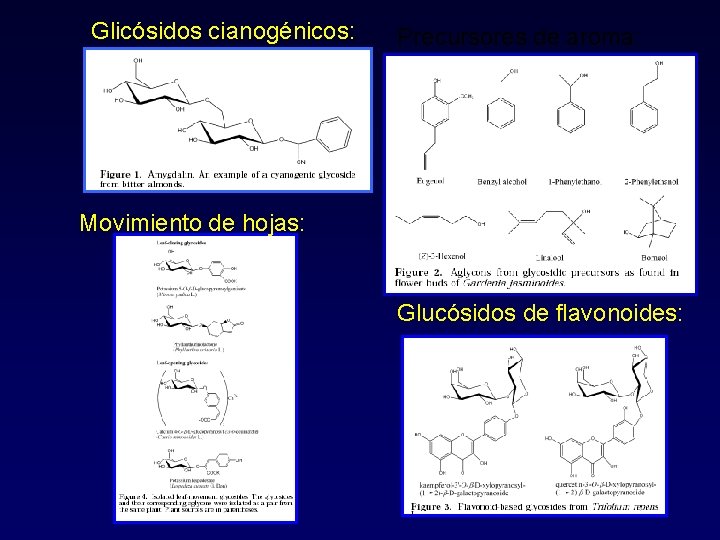
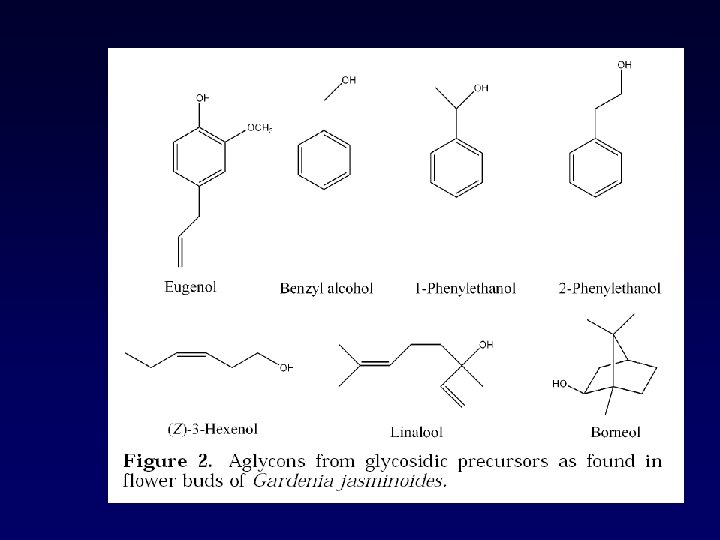
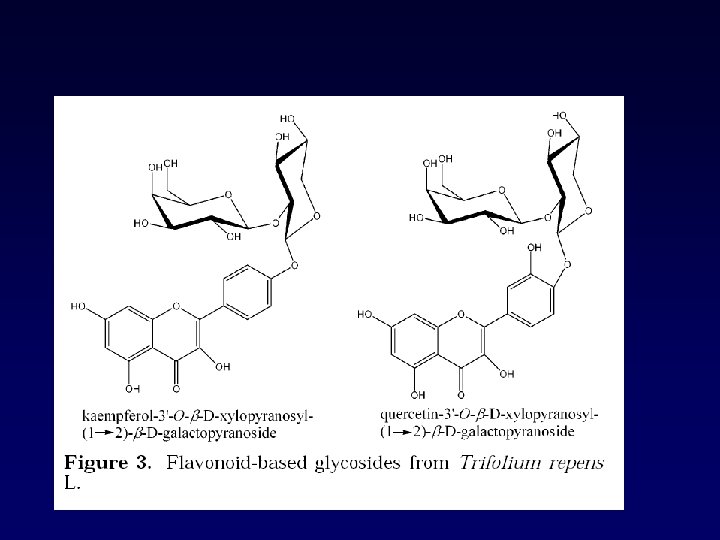
Glicósidos cianogénicos: Precursores de aroma: Movimiento de hojas: Glucósidos de flavonoides:

Aplicación industrial de glicósidos Residuos glicosilo conectado a: • Cadenas alquilo largas: propiedades surfactantes y emulsificantes; aplicación en detergentes y cosméticos. • Cadenas alquilo insaturadas (ej. terpenos): actividad antimicrobiana y antifúngica. • Péptidos y esteroides: formulaciones antitumorales y drogas para enfermedades cardiacas, respectivamente. • Glicósidos de aroma y sabor: compuestos controladores de la liberación de aroma y sabor en alimentos.

Preparación de glicósidos. Síntesis química: • Buenos rendimientos. • Necesidad de pasos de protección y desprotección de los sustratos y productos. • Uso de catalizadores y solventes tóxicos. • Excepción: síntesis de Fischer, pero sólo aplicable a un rango limitado de aglicones.

Preparación de glicósidos. Síntesis enzimática: Glicosil-transferasas • Transferencia selectiva de un residuo glicosilo de un intermediario activado a un aglicón. • Síntesis en bioreactores sólo posible con un sistema de regeneración de nucleótidos glicosilados. • Su alta selectividad las hace inflexibles en su aplicación. Glicosil-hidrolasas • Generalmente utilizadas en las reacciones de glicosilación. • Función natural: hidrólisis de glucósidos. • En 1914, Bourquelot demostró que es posible usar b-glicosidasa en reacciones de glicosilación.

Preparación de glicósidos. Síntesis enzimática: Glicosil-transferasas • Generalmente no disponibles comercialmente o muy caras. • Alta especificidad hacia sustrato y aglicón. • Sustratos: oligosacáridos, nucleótidos difosfato glicosilados. • Se sabe poco de su estabilidad. Glicosil-hidrolasas • Muy disponibles, baratas. • Baja especificidad hacia el aceptor de residuos glicosilo. • Sustratos: mono y disacáridos, alquil y aril glicósidos. • Generalmente estables, algunas especies termoestables están disponibles comercialmente.

Síntesis de glicósidos con glicosidasas: Transglicosilación: Hidrólisis inversa: • Control temodinámico. • Control cinético. • Menores rendimientos de • Mayores rendimientos en reacción. tiempos cortos de reacción. • Monosacáridos como • Algunas veces, los donadores de residuos glicosilo, son caros.

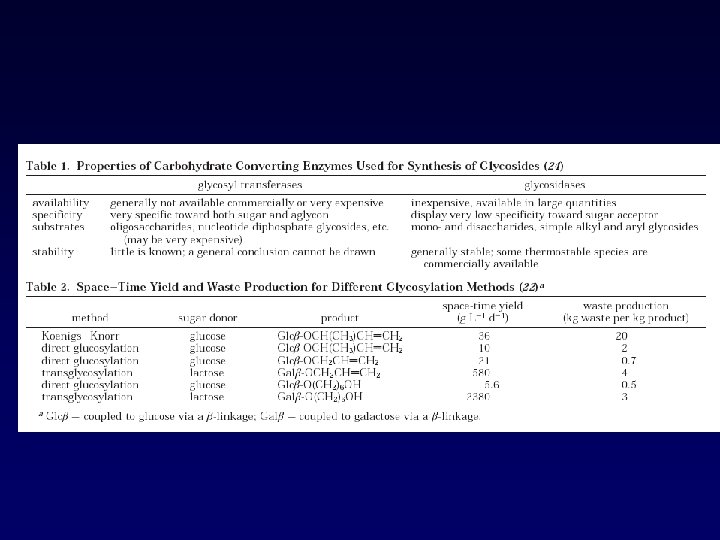
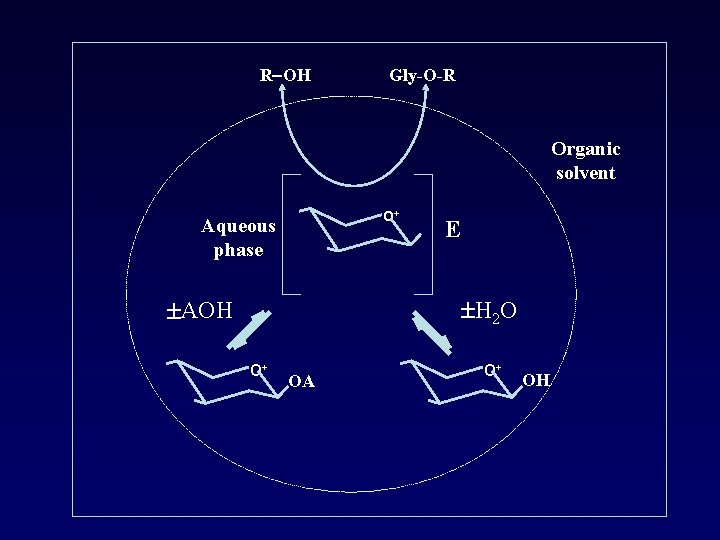
R-OH Gly-O-R Organic solvent O+ Aqueous phase E ±H 2 O ±AOH O+ OA O+ OH
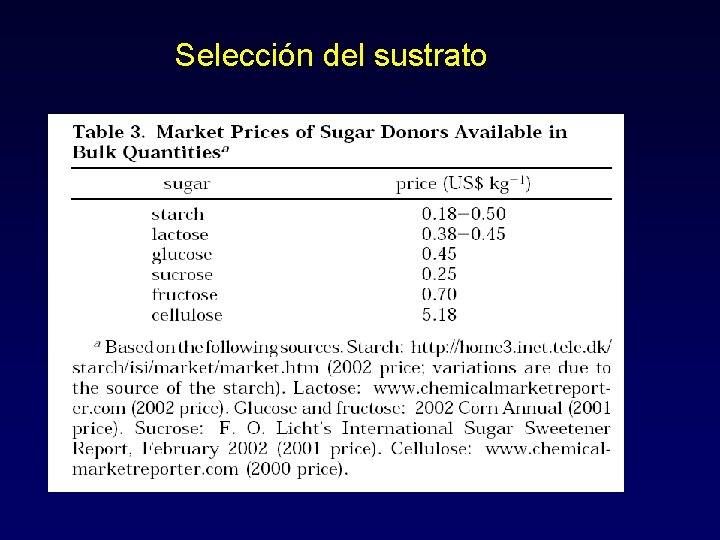
Selección del sustrato

Selección de la enzima.

Selección de la enzima. • • • a- glucosidasa b- glucosidasa a-amilasa b-galactosidasa

Reactores para glicosilación. • La mayor parte de los estudios enfocados a reacciones de hidrólisis. • Najakima et al. : producción de b-thujaplicin 2 -Ob-D-glucósido con UDP-glucosil transferasa libre en un reactor de tanque agitado con membrana: 0. 11 mg/g de enzima h en cuatro “batches” sin pérdida de actividad

Reactores para glicosilación. • Yi et al. : reactor de tanque agitado con b-glucosidasa inmovilizada para la producción de hexyl glucósido.
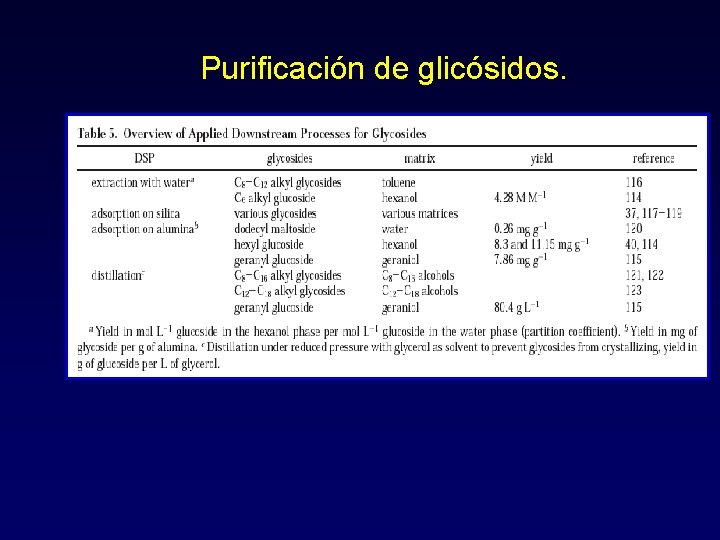
Purificación de glicósidos.

Glicosidasas en reacciones de transglicosilación. Necesidades: Hidrolasas con mayor relación transferencia/hidrólisis para la obtención de altos rendimientos de síntesis. Uso de enzimas termoestables (las altas temperaturas permiten una mayor concentración de sustrato y evitan la contaminación).
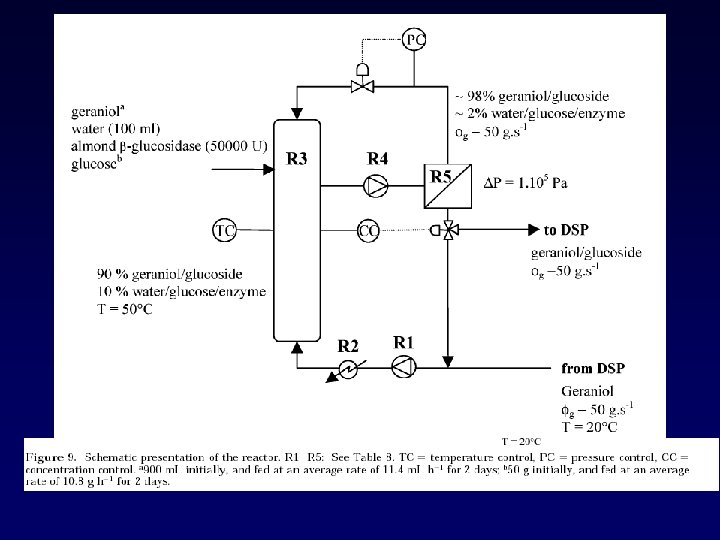
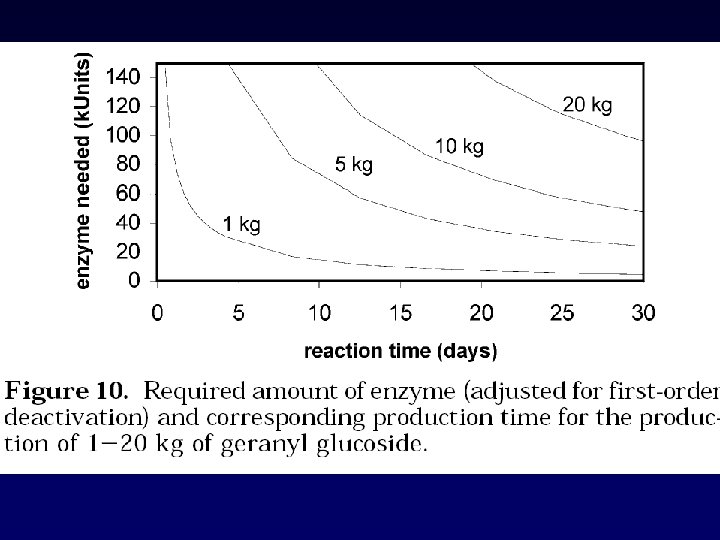
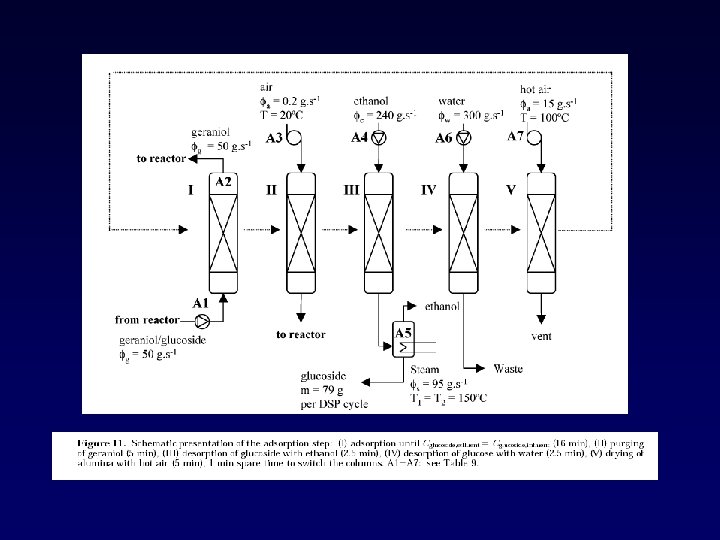

En varios estudios se han reportado rendimientos máximos de 40 -42% para la síntesis de oligosacáridos a partir de lactosa con b-glicosidasa. Objetivo: aumentar el rendimiento de oligosacáridos a partir de lactosa de la b-glicosidasa hipertermoestable de P. furiusus por ingeniería de proteínas en el sitio activo.

Familia 1 de las glicosil-hidrolasas. • b-glicosidasas, 6 -fosfo-b-glicosidasas. • Hidrólisis con retención de la configuración del carbono anomérico. b-glucosidasa de P. furiusus: • Homotetrámero • Monómero: barril (b/a)8 • Subunidades de 58 KDa;

b-glucosidasa de P. furiusus: Cel B • Hidrólisis de b-glucósidos (100%) • Actividad de b-galactosidasa (61%) • Actividad manosidasa (9. 5%)
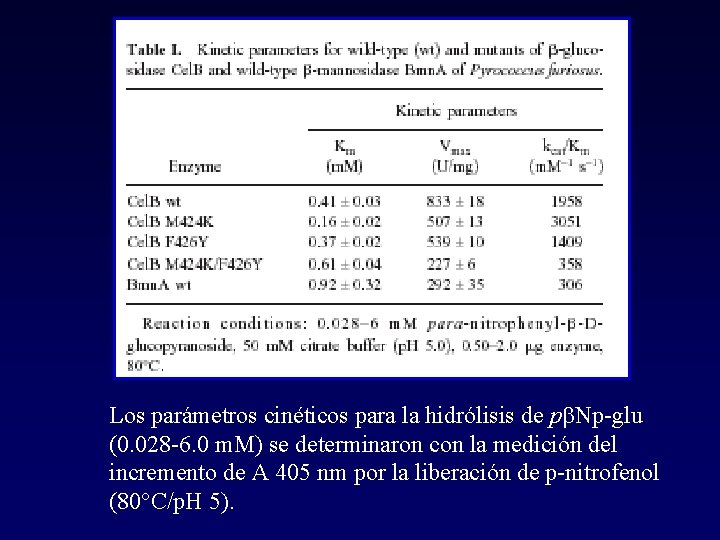
Los parámetros cinéticos para la hidrólisis de pb. Np-glu (0. 028 -6. 0 m. M) se determinaron con la medición del incremento de A 405 nm por la liberación de p-nitrofenol (80°C/p. H 5).
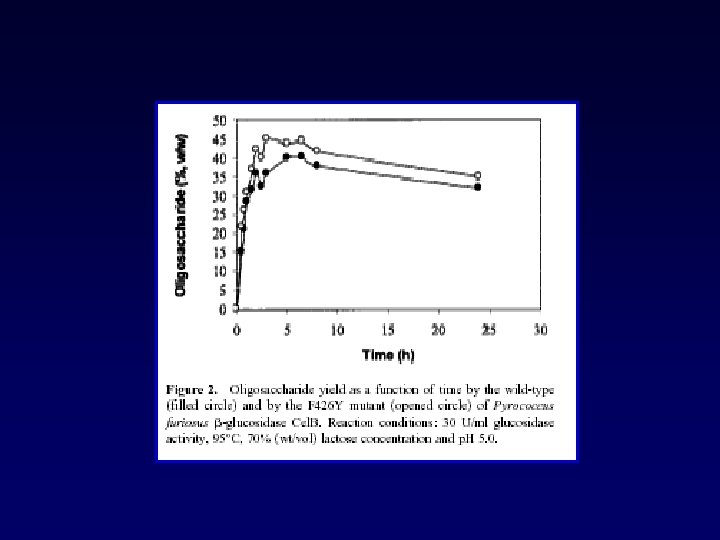
- Slides: 29