Gli acidi e le basi Acidi e basi

Gli acidi e le basi

Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un’altra specie. Base di Lewis = specie che può cedere in compartecipazione una coppia di elettroni ad un’altra sostanza. F F B F H + N H H F F F B N H H H

Secondo la teoria di Arrhenius Sono acide le sostanze che dissociandosi in acqua producono ioni H+ HCl H 2 O H+ + Cl- Sono basiche le sostanze che dissociandosi in acqua producono ioni OHNa. OH H 2 O Na+ + OH-

Secondo la teoria di Brönsted-Lowry : Un acido è una qualunque sostanza che è capace di donare uno ione H+ ad un altra sostanza in una reazione chimica Una base è una sostanza che accetta lo ione H+ dall'acido Questa definizione non è vincolata alla presenza del solvente; una reazione acido-base può avvenire quindi in un solvente qualunque, in assenza di solvente ed in qualunque stato di aggregazione delle sostanze.
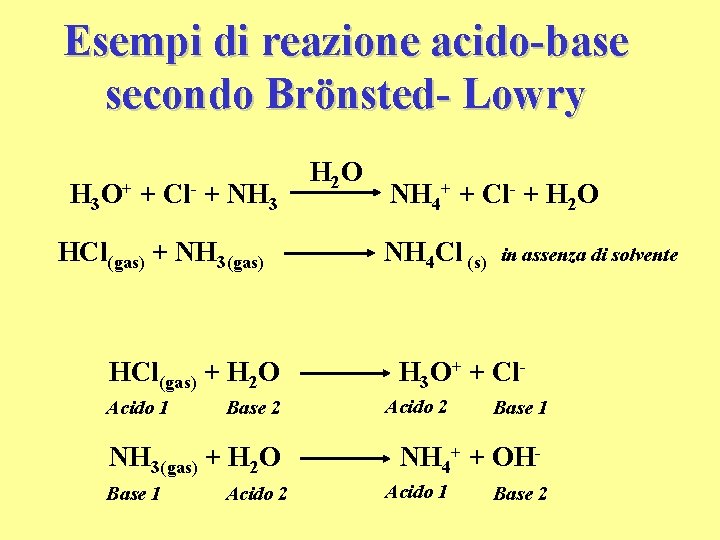
Esempi di reazione acido-base secondo Brönsted- Lowry H 3 O+ + Cl- + NH 3 HCl(gas) + NH 3(gas) HCl(gas) + H 2 O Acido 1 Base 2 NH 3(gas) + H 2 O Base 1 Acido 2 H 2 O NH 4+ + Cl- + H 2 O NH 4 Cl (s) in assenza di solvente H 3 O+ + Cl. Acido 2 Base 1 NH 4+ + OHAcido 1 Base 2

L’autoprotolisi dell’acqua Il prodotto della concentrazione di OH- per quella dello ione H 3 O+ in una qualunque soluzione acquosa è costante a temperatura costante. Esso corrisponde alla costante dell'equilibrio di autoprotolisi dell'acqua che a 25°C è uguale a 1. 0 x 10 -14. H 2 O + H 2 O H 3 O+ + OH- Equilibrio spostato fortemente verso sinistra; concentrazione dell’H 2 O molto elevata ([H 2 O] = 55. 3 M!!!) d = 0, 997 g/m. L a 25°C
![L’autoprotolisi dell’acqua Kw = [ H 3 O+ ] [ OH-] = 1. 0 L’autoprotolisi dell’acqua Kw = [ H 3 O+ ] [ OH-] = 1. 0](http://slidetodoc.com/presentation_image/27203a6ff046f77161d7c121c8b205db/image-7.jpg)
L’autoprotolisi dell’acqua Kw = [ H 3 O+ ] [ OH-] = 1. 0 x 10 -14 Kw = prodotto ionico dell’acqua In assenza di sostanze che perturbino l’equilibrio (acidi o basi): [ H 3 O+ ] = [ OH-] = 1. 0 x 10 -7 [ H 3 O+ ] = [ OH-] soluzione NEUTRA [ H 3 O+ ] > [ OH-] soluzione ACIDA [ H 3 O+ ] < [ OH-] soluzione BASICA Tramite Kw si possono sempre calcolare [H+] e [OH-]
![Calcolare [OH-] in una soluzione in cui [H 3 O+] = 4. 52· 10 Calcolare [OH-] in una soluzione in cui [H 3 O+] = 4. 52· 10](http://slidetodoc.com/presentation_image/27203a6ff046f77161d7c121c8b205db/image-8.jpg)
Calcolare [OH-] in una soluzione in cui [H 3 O+] = 4. 52· 10 -3 M Sapendo che in una soluzione [H 3 O+] è 7. 9· 10 -10 M, calcolare la [OH-] nella stessa soluzione
![Il p. H e la sua scala p. H = -log [H 3 O+] Il p. H e la sua scala p. H = -log [H 3 O+]](http://slidetodoc.com/presentation_image/27203a6ff046f77161d7c121c8b205db/image-9.jpg)
Il p. H e la sua scala p. H = -log [H 3 O+] p. OH = -log [OH-] p. H + p. OH = p. Kw = 14 Soluzioni basiche p. H 0 1 2 3 basicità crescente 4 5 6 7 8 9 10 11 12 13 14 14 13 12 11 10 9 8 7 6 5 4 acidità crescente Soluzioni acide 3 2 1 0 p. OH
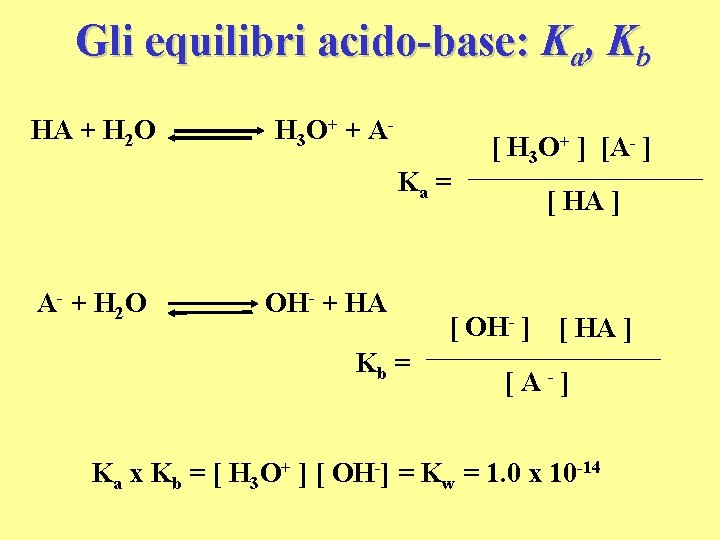
Gli equilibri acido-base: Ka, Kb HA + H 2 O H 3 O+ + AKa = A- + H 2 O OH- + HA Kb = [ H 3 O+ ] [A- ] [ HA ] [ OH- ] [ HA ] [A-] Ka x Kb = [ H 3 O+ ] [ OH-] = Kw = 1. 0 x 10 -14
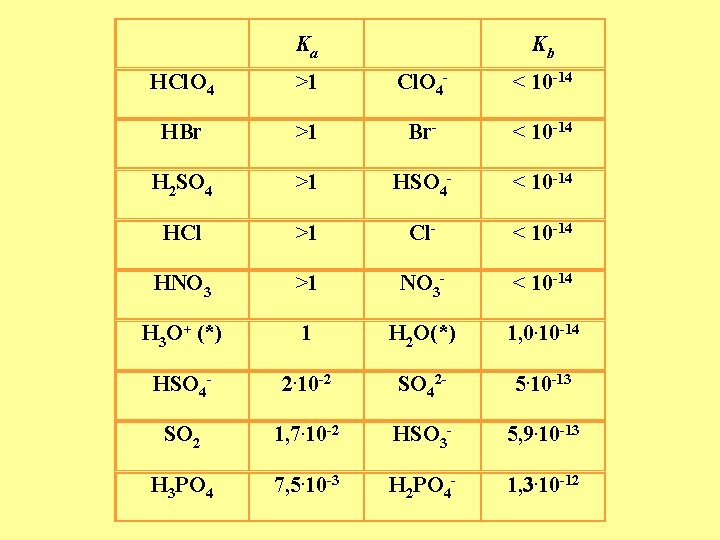
Ka Kb HCl. O 4 >1 Cl. O 4 - < 10 -14 HBr >1 Br- < 10 -14 H 2 SO 4 >1 HSO 4 - < 10 -14 HCl >1 Cl- < 10 -14 HNO 3 >1 NO 3 - < 10 -14 H 3 O+ (*) 1 H 2 O(*) 1, 0. 10 -14 HSO 4 - 2. 10 -2 SO 42 - 5. 10 -13 SO 2 1, 7. 10 -2 HSO 3 - 5, 9. 10 -13 H 3 PO 4 7, 5. 10 -3 H 2 PO 4 - 1, 3. 10 -12
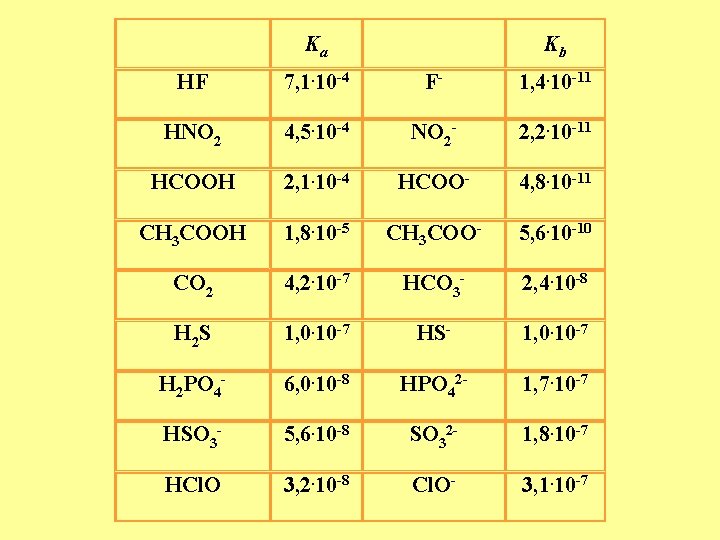
Ka Kb HF 7, 1. 10 -4 F- 1, 4. 10 -11 HNO 2 4, 5. 10 -4 NO 2 - 2, 2. 10 -11 HCOOH 2, 1. 10 -4 HCOO- 4, 8. 10 -11 CH 3 COOH 1, 8. 10 -5 CH 3 COO- 5, 6. 10 -10 CO 2 4, 2. 10 -7 HCO 3 - 2, 4. 10 -8 H 2 S 1, 0. 10 -7 HS- 1, 0. 10 -7 H 2 PO 4 - 6, 0. 10 -8 HPO 42 - 1, 7. 10 -7 HSO 3 - 5, 6. 10 -8 SO 32 - 1, 8. 10 -7 HCl. O 3, 2. 10 -8 Cl. O- 3, 1. 10 -7
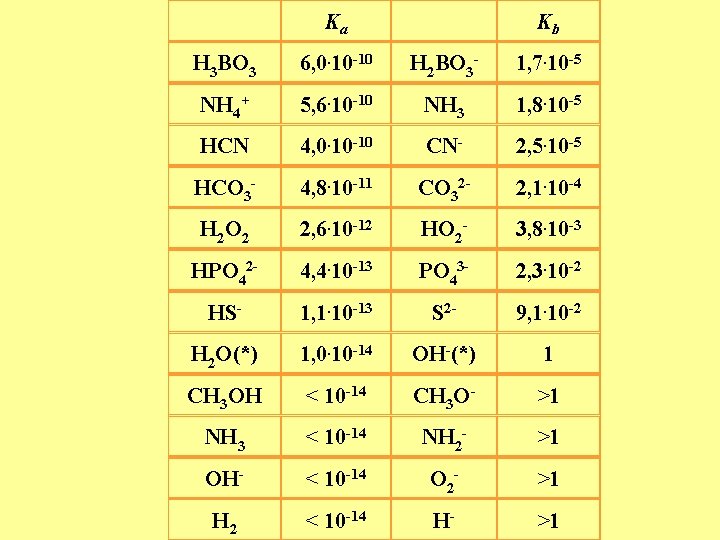
Ka Kb H 3 BO 3 6, 0. 10 -10 H 2 BO 3 - 1, 7. 10 -5 NH 4+ 5, 6. 10 -10 NH 3 1, 8. 10 -5 HCN 4, 0. 10 -10 CN- 2, 5. 10 -5 HCO 3 - 4, 8. 10 -11 CO 32 - 2, 1. 10 -4 H 2 O 2 2, 6. 10 -12 HO 2 - 3, 8. 10 -3 HPO 42 - 4, 4. 10 -13 PO 43 - 2, 3. 10 -2 HS- 1, 1. 10 -13 S 2 - 9, 1. 10 -2 H 2 O(*) 1, 0. 10 -14 OH-(*) 1 CH 3 OH < 10 -14 CH 3 O- >1 NH 3 < 10 -14 NH 2 - >1 OH- < 10 -14 O 2 - >1 H 2 < 10 -14 H- >1

Il calcolo del p. H: acidi forti Si calcoli il p. H di una soluzione 0. 100 M di HNO 3

Il calcolo del p. H: acidi forti Si calcoli il p. H di una soluzione 0. 100 M di HNO 3 è un acido forte con Ka > 1 quindi in H 2 O si dissocia completamente: [H 3 O+] derivante dall’acido = CHNO 3= 0. 100 M p. H = -log 0. 100 = 1 Il p. H risultante è acido

Si calcolino il p. H ed il p. OH di una soluzione acquosa 1. 00 x 10 -4 M di HCl. O 4

Si calcolino il p. H ed il p. OH di una soluzione acquosa 1. 00 x 10 -4 M di HCl. O 4 è un acido forte con Ka > 1 quindi in H 2 O si dissocia completamente: [H 3 O+] derivante dall’acido = CHCl. O 4= 1. 00 x 10 -4 M p. H = -log 1. 00 x 10 -4 = 4 poiché [H 3 O+] [OH-] = 1. 0 x 10 -14 M risulta che: [OH-] = 1. 0 x 10 -14/1. 0 x 10 -4 = 1. 0 x 10 -10 M p. OH = 10. 0 Si noti che p. H + p. OH = p. Kw= 14

Nel problema non si è tenuto conto del contributo degli ioni H 3 O+ derivanti dalla dissociazione dell’H 2 O Si verifica a posteriori che l’approssimazione fatta sia lecita: dato che la [OH-] = 10 -10 M deriva dalla dissociazione delle molecole di H 2 O, la [H 3 O+] derivante dalla medesima dissociazione sarà uguale, cioè pari a 10 -10 M Questa concentrazione è trascurabile rispetto alla concentrazione di [H 3 O+] derivante dall’acido (10 -4 M)

Si calcoli il p. H di una soluzione 1. 00 x 10 -7 M di HCl. O 4

Si calcoli il p. H di una soluzione 1. 00 x 10 -7 M di HCl. O 4 è un acido forte con Ka > 1 quindi in H 2 O si dissocia completamente: CH 3 O+ derivante dall’acido = CHCl. O 4= 1. 00 x 10 -7 M tale concentrazione è paragonabile alla dissociazione delle molecole di H 2 O che quindi contribuirà al p. H della soluzione: [H 3 O+] = 1. 00 x 10 -7 + x dove x è la concentrazione di H 3 O+ , e quindi anche di OH-, derivante dalla dissociazione del solvente

quindi: Kw = (1. 00 x 10 -7 + x) x = 1. 0 x 10 -14 x = 0. 62 x 10 -7 M la concentrazione totale di [H 3 O+] = 1. 62 x 10 -7 M p. H = 6. 79 Si noti che il p. H è acido come atteso

Solo quando gli ioni H 3 O+ derivanti da un acido sono in concentrazione < 10 -6 M occorre tenere conto del contributo della dissociazione dell’acqua al p. H

Il calcolo del p. H: acidi deboli Si calcoli il p. H di una soluzione 0. 100 M di CH 3 COOH

Si calcoli il p. H di una soluzione 0. 100 M di CH 3 COOH è un acido debole con Ka = 1. 8 x 10 -5, quindi in H 2 O non si dissocia completamente: La concentrazione di H 3 O+ derivante dalla sua dissociazione si può ricavare dalla Ka. -5 [ H 3 O+ ][ CH 3 COO- ] Ka = __________ = 1. 8 x 10 [ CH 3 COOH ] x 2 _______ Ka = = 1. 8 x 10 -5 0. 100 -x 0. 100 x = 1. 34 x 10 -3 p. H = 2. 9 molto meno acido di quello di un acido forte della stessa concentrazione

La x al denominatore risulta generalmente trascurabile quando siano contemporaneamente soddisfatte le condizioni: a) Ka è minore o dell’ordine di 10 -5 b) la concentrazione dell’acido è maggiore di 10 -2 M

Il calcolo del p. H di basi forti e deboli si effettua in maniera analoga

Grado di dissociazione HA + H 2 O α= Ka = H 3 O+ + A- [A-] c 0 [ H 3 O+ ] [A- [ H 3 O+ ] c 0 α ] = [ HA ] c 0 α 2 c 0 (1 - α) = c 0 (1 - α) c 0 α 2 (1 - α) =

Un acido debole in concentrazione 0. 1 M è dissociato per lo 0. 0063%. Calcolare il p. H della soluzione e la Ka dell’acido

Un acido debole in concentrazione 0. 1 M è dissociato per lo 0. 0063%. Calcolare il p. H della soluzione e la Ka dell’acido α= [A-] Ka = c 0 α 2 (1 - α) [H 3 O+] = [A-] = c 0 α = 0. 1 x 6. 3· 10 -5 = 6. 3· 10 -6 p. H = - log [H 3 O+] = - log 6. 3· 10 -6 = 5. 20 Ka = c 0 α 2 (1 - α) 0. 1(6. 3· 10 -5)2 = (1 - 6. 3· 10 -5 ) -10 = 4. 0· 10

Acidi e basi polifunzionali Acido poliprotico = acido che ha la possibilità di cedere più di uno ione H+. H 3 PO 4 + H 2 O H 2 PO 4 - + H 3 O+ Ka = 7. 5 x 10 -3 H 2 PO 4 - + H 2 O HPO 42 - + H 3 O+ Ka = 6. 0 x 10 -8 HPO 42 - + H 2 O PO 43 - + H 3 O+ Ka = 4. 4 x 10 -13 Base poliacida = base che può accettare più di un protone: PO 43 - + H 2 O HPO 42 - + OHKb = 2. 3 x 10 -2 HPO 42 - + H 2 O H 2 PO 4 - + OH- Kb = 1. 7 x 10 -7 H 2 PO 4 - + H 2 O H 3 PO 4 + OH- Kb = 1. 3 x 10 -12

H 2 A + H 2 O H 3 O+ + HA- + H 2 O H 3 O+ + A 2 - Ci sono 4 incognite da calcolare K 1 = [ H 2 A ] [HA-] [ H 3 O+] [A 2 - ] [ H 3 O+] [HA-] [ H 2 A ] Da queste due equazioni ricaviamo K 2 = [ H 3 O+ ] [A 2 - ] [ HA-] [A 2 - ] Se CA è la concentrazione iniziale dell’acido: CA = [ H 2 A ] + [HA-] + [A 2 - ] +] = -] + [HA-] + 2 [A 2 - ] [ H O [OH Condizione di elettroneutralità = 3 Normalmente K 1 >>K 2 quindi gli equilibri possono essere trattati separatamente

Calcolare la concentrazione delle specie all’equilibrio in una soluzione 0. 100 M di acido solfidrico sapendo che K 1 = 1. 1· 10 -7 e K 2 = 1. 0· 10 -14

L’idrolisi Sali derivanti da un acido debole e una base forte HA + OH- A- + H 2 O Kib = [ HA ] [ OH- ] [ A- ] Sali derivanti da un acido forte e una base debole HB + H 2 O Kia = B- + H 3 O+ [ B - ] [ H 3 O + ] [ HB ]

Calcolare il p. H di una soluzione di acetato di sodio 0. 1 M sapendo che La costante di dissociazione dell’acido acetico vale 1. 76 10 -5 Calcolare il p. H di una soluzione di cloruro d’ammonio 0. 2 M sapendo che la costante di dissociazione dell’ammoniaca vale 1. 8 10 -5

Le soluzioni tampone Se in una soluzione acquosa sono presenti un acido ed una base coniugata (CH 3 COOH e CH 3 COO-; NH 4+ e NH 3, etc. ) si ha una soluzione tampone quando il rapporto fra le concentrazioni stechiometriche dell’acido e della base è compreso tra 0. 1 e 10 Le soluzioni tampone hanno proprietà chimiche peculiari: • Il p. H non varia al variare della diluizione • Il p. H tende a rimanere costante per piccole aggiunte di acidi e basi forti
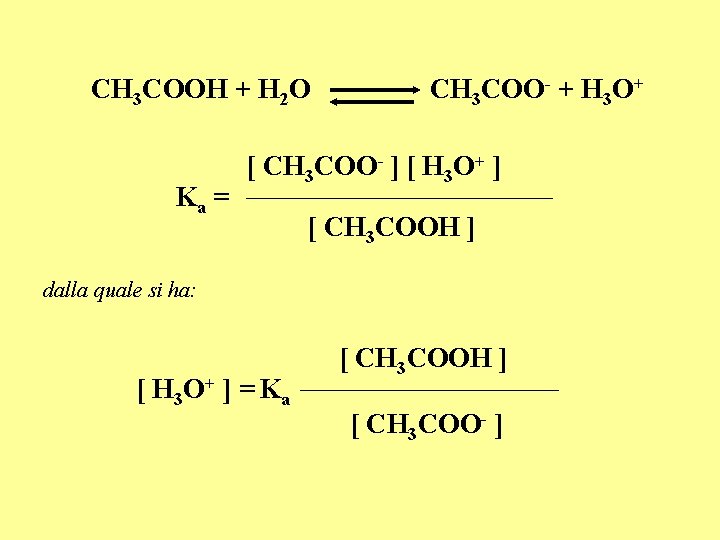
CH 3 COOH + H 2 O Ka = CH 3 COO- + H 3 O+ [ CH 3 COO- ] [ H 3 O+ ] [ CH 3 COOH ] dalla quale si ha: [ H 3 O + ] = K a [ CH 3 COOH ] [ CH 3 COO- ]
![e quindi: p. H = p. Ka - log [ CH 3 COOH ] e quindi: p. H = p. Ka - log [ CH 3 COOH ]](http://slidetodoc.com/presentation_image/27203a6ff046f77161d7c121c8b205db/image-37.jpg)
e quindi: p. H = p. Ka - log [ CH 3 COOH ] [ CH 3 COO- ] Se le concentrazioni delle due specie CH 3 COOH e CH 3 COO- sono uguali, p. H = p. Ka. Le concentrazioni dell’acido e della base coniugata all’equilibrio sono prese uguali a quelle iniziali per effetto dello ione a comune

Il calcolo del p. H: soluzioni tampone Si calcoli il p. H di una soluzione 0. 321 M di CH 3 COOH e 0. 281 M di CH 3 COO-.

Si calcoli il p. H di una soluzione 0. 321 M di CH 3 COOH e 0. 281 M di CH 3 COO-. Si tratta di una soluzione tampone (0. 321/0. 281= 1. 14). [ CH 3 COOH ] [ CH 3 COO- ] [ H 3 O+ ] = Ka [ H 3 O+ ] = 1. 8 x 10 -5 p. H = 4. 69 0. 321 0. 281 = 2. 06 x 10 -5

Effetto tampone Il p. H varia poco per piccole aggiunte di acidi e basi, anche forti, purché in quantità piccole rispetto a quelle delle specie che costituiscono la soluzione tampone. Es. Calcolare la variazione di p. H che si verifica per aggiunta di 6. 25 x 10 -3 mol di HCl alla soluzione tampone dell’esempio precedente. L’aggiunta di HCl fa avvenire la reazione: CH 3 COO- + H 3 O+ CH 3 COOH + H 2 O Con aumento di [CH 3 COOH] e diminuzione di [CH 3 COO-]. -3) (0. 321 + 6. 25 x 10 -5 = 2. 14 x 10 [ H 3 O+ ] = 1. 8 x 10 -5 (0. 281 - 6. 25 x 10 -3) p. H = 4. 67 L’effetto di un’analoga aggiunta di HCl in H 2 O è di portare il p. H a 2. 2.

Alcuni sistemi tampone Coppia HA/A- Ka Intervallo di p. H CH 3 COOH/CH 3 COO- 1. 8 x 10 -5 3. 75 -5. 75 H 2 CO 3/HCO 3 - 4. 3 x 10 -7 5. 37 -7. 37 H 2 S/HS- 9. 1 x 10 -8 6. 04 -8. 04 H 2 PO 4 -/HPO 42 - 6. 2 x 10 -8 6. 21 -8. 21 NH 4+/NH 3 5. 6 x 10 -10 8. 25 -10. 25

Titolazioni acido-base Titolazione = è una operazione il cui scopo è la determinazione del titolo di una soluzione. Consiste nell’aggiungere volumi noti di una soluzione a concentrazione nota di un titolante ad un volume noto di una soluzione a concentrazione ignota. Il titolante deve reagire in modo rapido, completo e con stechiometria ben definita con la sostanza da titolare. Nel caso delle titolazioni acido-base, il titolante è costituito quindi da acidi e basi forti. La sostanza da titolare può essere una base o un acido qualsiasi.

Punto equivalente • Una titolazione termina quando le moli di titolante uguagliano quelle della sostanza da titolare: M AV A = M B V B

Gli indicatori Indicatore = sostanza organica che cambia colore tra la sua forma acida e quella basica HIn + H 2 O In- + H 3 O+ Il p. H di viraggio è il p. H in corrispondenza del quale la concentrazione della forma protonata è uguale alla concentrazione della forma non protonata [H 3 O+] = KHIn Indicatori universali Cartina tornasole

L’intervallo di viraggio dell’indicatore indica l’entità della variazione di p. H che si deve produrre perché l’occhio apprezzi la differenza di colore tra la forma acida e quella basica e viceversa. E’ necessario che una della due forme sia presente rispetto all’altra con un eccesso di 10 volte. si ricava considerando che: [Hin]/[In-] 10 [H 3 O+] = Ka(ind) [Hin]/[In-] ed è compreso fra Ka(ind)/10 e 10 Ka(ind)

A 100 m. L di acido acetico 0. 5 M vengono aggiunti 0. 8 g di Na. OH Calcolare il p. H della soluzione sapendo che la costante di dissociazione Dell’acido acetico è 1. 76 E-5.
- Slides: 47