Glcidos Prcticas resumidas Bonifacio San Milln IES Muriedas
Glúcidos Prácticas (resumidas) Bonifacio San Millán IES Muriedas 2º Bachillerato - Biología

RECONOCIMIENTO DE AZÚCARES REDUCTORES FUNDAMENTO Reacción de Fehling “ojo, simplificada” q + rojo ladrillo (cambio de color) q - azul verdoso (no cambio de color) R-CHO + 2 Cu. O R-COOH + Cu 2 O (Cu 2+) al reducirse pasa a (Cu +) PROCEDIMIENTO: Añadir a diluciones (3 ml) , reactivos de Fehling A (Cu. SO 4) y B (Na. OH) (1 ml) Calentar baño María

IDENTIFICACION DEL ALMIDÓN CON LUGOL FUNDAMENTO: proceso físico: El efecto óptico del yodo cuando se introduce o fija en las hélices de la amilosa , proceso que solo ocurre en frío. PROCEDIMIENTO Pipeteamos (+) 3 ml + 2 gotas lugol : Contiene almidón, virará a color violeta o azul oscuro ( - ): No contiene almidón no cambiará de color IMPORTANTE: COMBINANDO LAS DOS PRÁCTICAS ANTERIORES PODEMOS IDENTIFICAR DIFERENTES MUESTRAS DE: EJ. GLUCOSA (MONOS.

DIGESTION DE ALMIDÓN CON AMILASA SALIVAL (PTIALINA) FUNDAMENTO: Hidrólisis enzimática ALMIDÓN --- enzimas desramificadores + amilasa ----> MAL TOSA ---- maltasa ----> GLUCOSA PROCEDIMIENTO: Un poco de almidón en un tubo de ensayo. Añadimos un poco de saliva (contiene amilasa) Para agilizar el proceso, calentamos a menos de 37ºC Dejamos reposar el tubo, agitándolo de vez en cuando. 5´ Reacción de Fehling A y 1 ml de Fehling B. IMPORTANTE: EL REACTIVO FEHLING NOS PERMITE COMPROBAR QUE SE HA PRODUCIDO LA HIDRÓLISIS, YA QUE EL ALMIDON NO PRESENTA PODER REDUCTOR, PERO UNA VEZ SE HA PRODUCIDO LA HIDRÓLISIS, TENDREMOS GLUCOSAS LIBRES O MALTOSA QUE, COMO TODOS LOS MONOSACÁRIDOS Y LA MAYORÍA DE LOS DISACÁRIDOS (LA MALTOSA SI), SI PRESENTAN PODER REDUCTOR. EL COLOR

B) Porque la amilosa (20% del almidón fija el Iodo del lugol entre sus hélices, se trata de una AMILASA que hidroliza el almidón dando principalmente Maltosa. C) Glándulas salivales: Parótidas sublingual y submandibular. Si, el jugo pancreático D) Temperatura y cambios de p. H, ambos implican desnaturalización de la amilasa D) Físico, efecto óptico del Yodo entre las hélices de amilosa, hélices que se desestructuran con el calor.
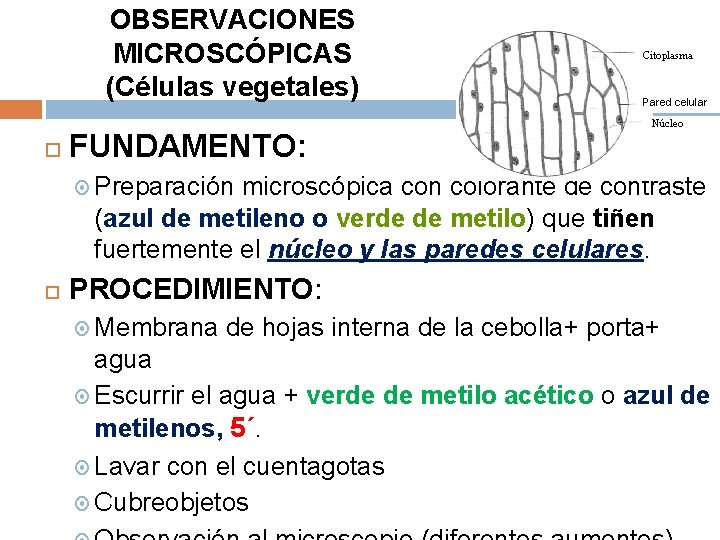
OBSERVACIONES MICROSCÓPICAS (Células vegetales) FUNDAMENTO: Citoplasma Pared celular Núcleo Preparación microscópica con colorante de contraste (azul de metileno o verde de metilo) que tiñen fuertemente el núcleo y las paredes celulares. PROCEDIMIENTO: Membrana de hojas interna de la cebolla+ porta+ agua Escurrir el agua + verde de metilo acético o azul de metilenos, 5´. Lavar con el cuentagotas Cubreobjetos

S MICROSCÓPICA S (Células animales) FUNDAMENTO: Preparación microscópica con colorante de contraste (azul de metileno o verde de metilo) que tiñen fuertemente el núcleo con menos color el citoplasma (granuloso). PROCEDIMIENTO: Raspado del interior del carrillo+ porta (extensión) Calentar + verde de metilo acético o azul de metilenos, 3´. Lavar con el cuentagotas Cubreobjetos
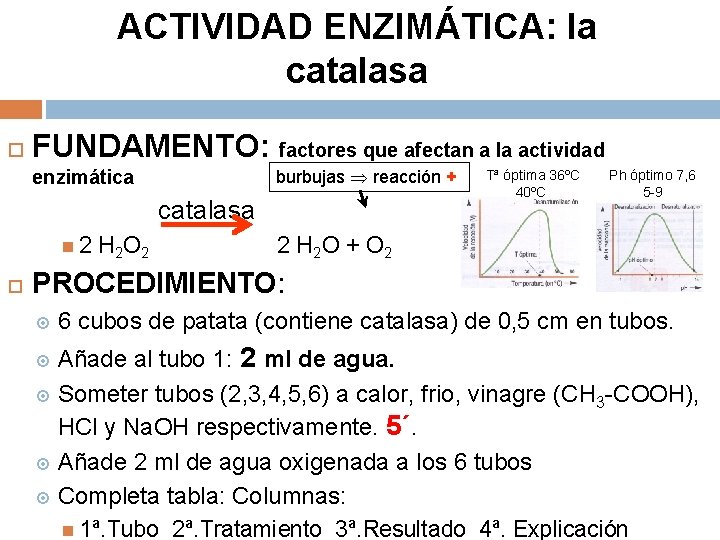
ACTIVIDAD ENZIMÁTICA: la catalasa FUNDAMENTO: factores que afectan a la actividad burbujas reacción + enzimática catalasa 2 H 2 O 2 Tª óptima 36ºC 40ºC Ph óptimo 7, 6 5 -9 2 H 2 O + O 2 PROCEDIMIENTO: 6 cubos de patata (contiene catalasa) de 0, 5 cm en tubos. Añade al tubo 1: 2 ml de agua. Someter tubos (2, 3, 4, 5, 6) a calor, frio, vinagre (CH 3 -COOH), HCl y Na. OH respectivamente. 5´. Añade 2 ml de agua oxigenada a los 6 tubos Completa tabla: Columnas: 1ª. Tubo 2ª. Tratamiento 3ª. Resultado 4ª. Explicación
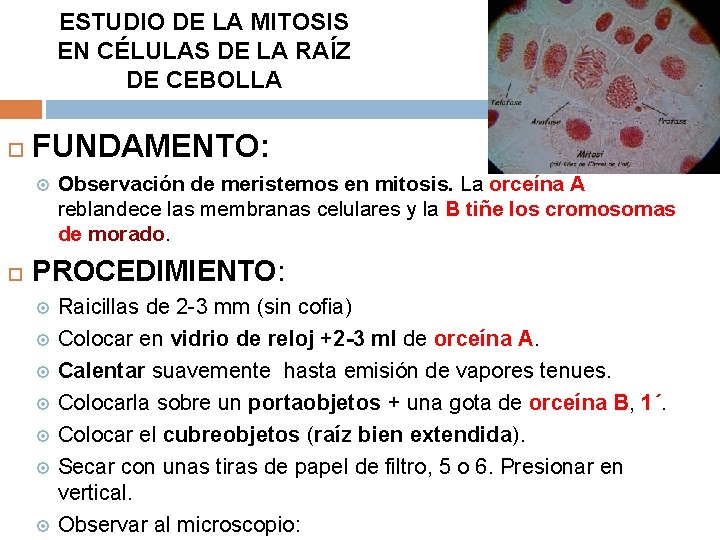
ESTUDIO DE LA MITOSIS EN CÉLULAS DE LA RAÍZ DE CEBOLLA FUNDAMENTO: Observación de meristemos en mitosis. La orceína A reblandece las membranas celulares y la B tiñe los cromosomas de morado. PROCEDIMIENTO: Raicillas de 2 -3 mm (sin cofia) Colocar en vidrio de reloj +2 -3 ml de orceína A. Calentar suavemente hasta emisión de vapores tenues. Colocarla sobre un portaobjetos + una gota de orceína B, 1´. Colocar el cubreobjetos (raíz bien extendida). Secar con unas tiras de papel de filtro, 5 o 6. Presionar en vertical. Observar al microscopio:
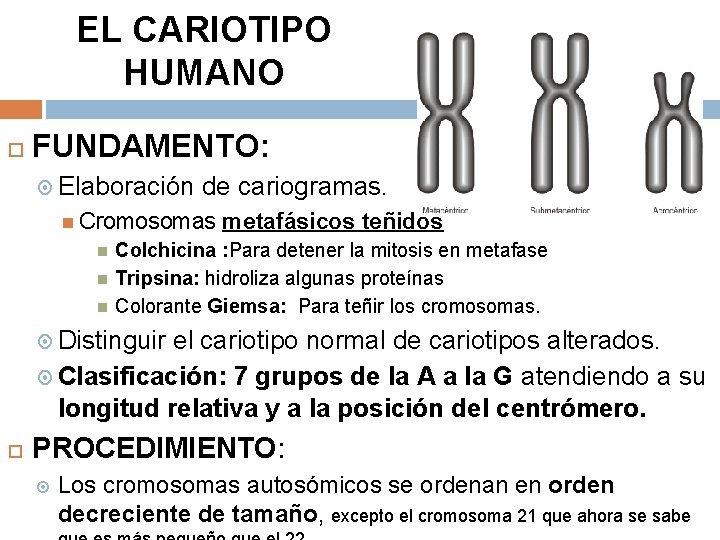
EL CARIOTIPO HUMANO FUNDAMENTO: Elaboración de cariogramas. Cromosomas metafásicos teñidos Colchicina : Para detener la mitosis en metafase Tripsina: hidroliza algunas proteínas Colorante Giemsa: Para teñir los cromosomas. Distinguir el cariotipo normal de cariotipos alterados. Clasificación: 7 grupos de la A a la G atendiendo a su longitud relativa y a la posición del centrómero. PROCEDIMIENTO: Los cromosomas autosómicos se ordenan en orden decreciente de tamaño, excepto el cromosoma 21 que ahora se sabe
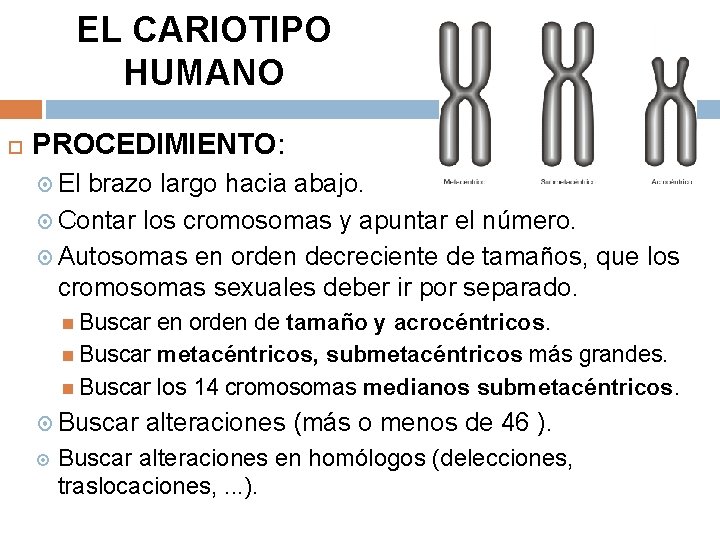
EL CARIOTIPO HUMANO PROCEDIMIENTO: El brazo largo hacia abajo. Contar los cromosomas y apuntar el número. Autosomas en orden decreciente de tamaños, que los cromosomas sexuales deber ir por separado. Buscar en orden de tamaño y acrocéntricos. Buscar metacéntricos, submetacéntricos más grandes. Buscar los 14 cromosomas medianos submetacéntricos. Buscar alteraciones (más o menos de 46 ). Buscar alteraciones en homólogos (delecciones, traslocaciones, . . . ).
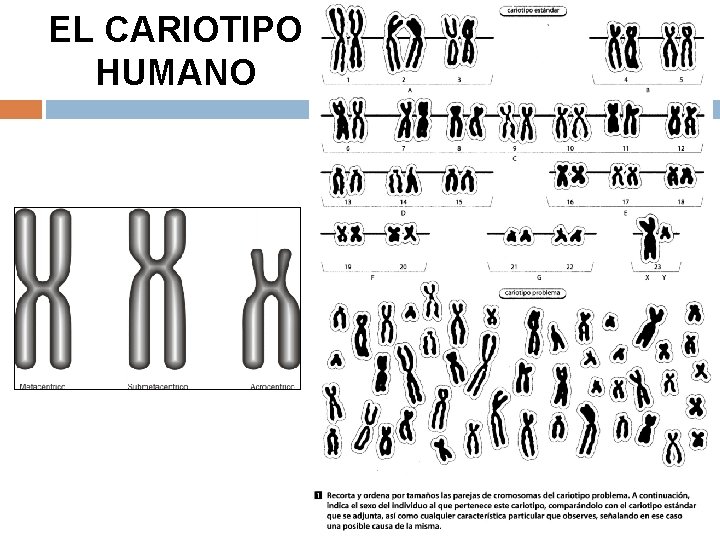
EL CARIOTIPO HUMANO
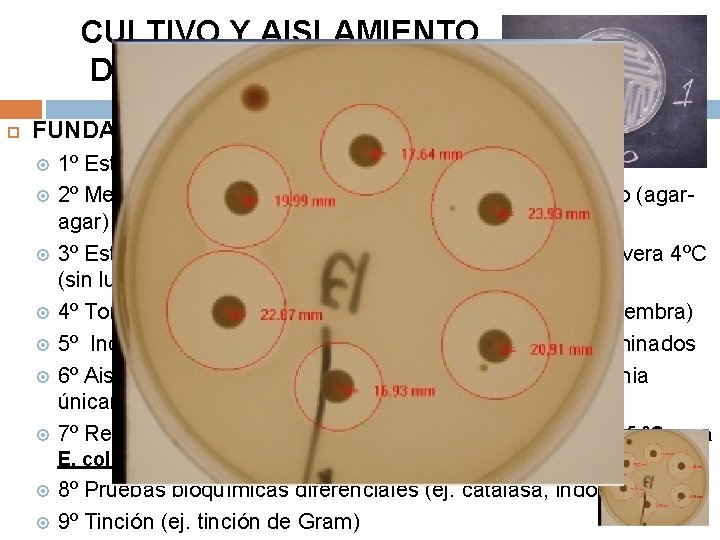
CULTIVO Y AISLAMIENTO DE MICROORGANISMOS FUNDAMENTO Y PROCEDIMIENTOS: 1º Esterilización y técnicas asépticas 2º Medio de cultivo (genérico o específico): líquido o sólido (agar) 3º Esterilización y conservación del medio: autoclave y nevera 4ºC (sin luz) 4º Toma de muestras (ej. bastoncillo) y siembra (asa de siembra) 5º Incubación (estufa), durante periodos de tiempo determinados 6º Aislamiento (toma de muestra monoclonal, de una colonia únicamente) 7º Resiembra en medio genérico o selectivo (ej. Lactosa, 45 ºC para E. coli) 8º Pruebas bioquímicas diferenciales (ej. catalasa, indol, …) 9º Tinción (ej. tinción de Gram)

CULTIVO Y AISLAMIENTO DE MICROORGANISMOS Autoclave microscopio óptico Medio de cultivo (líquido y sólido) siembra (asa de siembra) Incubación (estufa) Tinción (ej. tinción de Gram) y observación Halo de inhibición - +

TINCIÓN DE GRAM + FUNDAMENTO _ Colorantes cristal violeta y safranina las bacterias Gram + se tiñen de morado (fijan el cristal violeta que es el colorante fundamental) las Gram – se tiñen de rosa con safranina, colorante de contraste (no fijan el cristal violeta). PROCEDIMIENTO Fijar la muestra con metanol durante un minuto o al calor Añadir azul violeta (cristal violeta) , 1´ Todas las células gram + y - se tiñen de color azul-purpura. Agregar lugol (intensifica el cristal violeta) Lavar con acetona y/o alcohol , elimina el c. violeta de las Gram. Tinción de contraste agregando safranina. 1 -2´ Observar al microscopio óptico a 1000 x con aceite de inmersión

Tema 14. Prácticas Almidón : lugol (+) violeta, en frío AZÚCARES REDUCTORES: ESTUDIO DE LA MITOSIS EN CÉLULAS DE LA RAÍZ DE CEBOLLA: Observación de meristemos en mitosis. La orceína A reblandece las membranas celulares y la B tiñe los cromosomas de morado. Reacción de Fehling simplificada R-CHO + 2 Cu. O R-COOH + Cu 2 O (Cu 2+) al reducirse pasa a (Cu +) RF (+) : Rojo ladrillo RF (-) : Azul verdoso FUNDAMENTO: factores que afectan a la Ph óptimo 7, 6 actividad enzimática burbujas reacción (+) 5 -9 catalasa Tª óptima 36ºC - 40ºC 2 H 2 O 2 2 H 2 O + O 2 CULTIVO Y AISLAMIENTO DE MICROORGANISMOS 1. Esterilización y técnicas asépticas. 2. Medio de cultivo (genérico o específico): líquido o sólido (agar). 3. Esterilización y conservación del medio: autoclave y nevera 4ºC (sin luz). 4. Toma de muestras (ej. bastoncillo) y siembra (asa de siembra). 5. Incubación (estufa), durante periodos de tiempo determinados. 6. Aislamiento (toma de muestra monoclonal, de una colonia únicamente). 7. Resiembra en medio genérico o selectivo (ej. Lactosa, 45 ºC para E. coli). 8. Pruebas bioquímicas diferenciales (ej. catalasa, indol, …). 9. Tinción (ej. tinción de Gram: (+) azul, (-) rojo. 10. Observación con microscopio (mínimo 1000 x). Estudio de cariotipos anómalos
- Slides: 16