Glcidos Hidratos de Carbono Carbohidratos Nora Sosa 2015

Glúcidos, Hidratos de Carbono, Carbohidratos. Nora Sosa 2015 1

Concepto Los glúcidos, derivan su nombre de la glucosa, el glúcido de mayor significación biológica. También se los denomina carbohidratos, debido a que muchos de ellos, responden a una fórmula general Cn(H 2 O)n Por ejemplo la glucosa tiene fórmula global: C 6 H 12 O 6 2
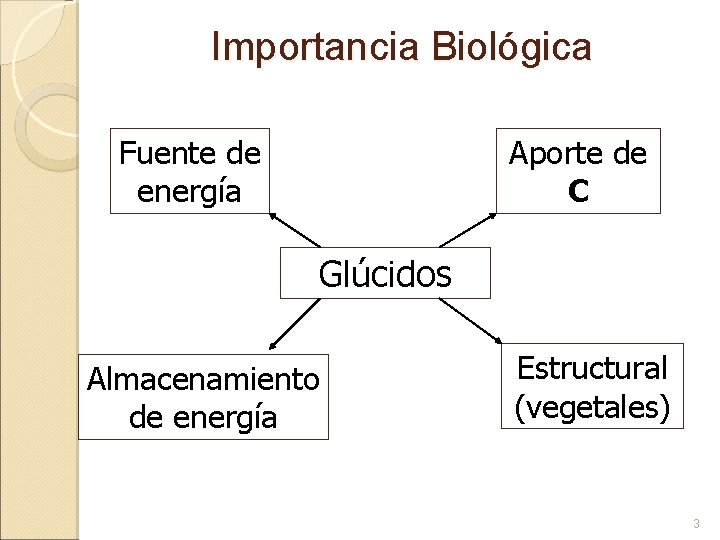
Importancia Biológica Fuente de energía Aporte de C Glúcidos Almacenamiento de energía Estructural (vegetales) 3
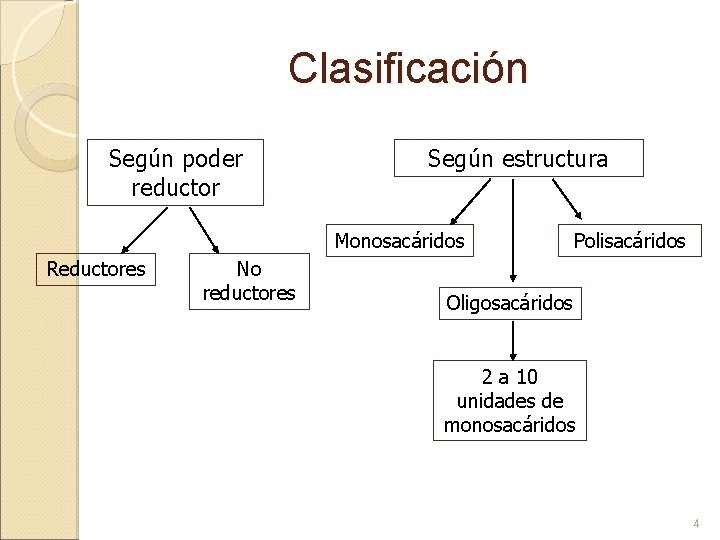
Clasificación Según poder reductor Según estructura Monosacáridos Reductores No reductores Polisacáridos Oligosacáridos 2 a 10 unidades de monosacáridos 4
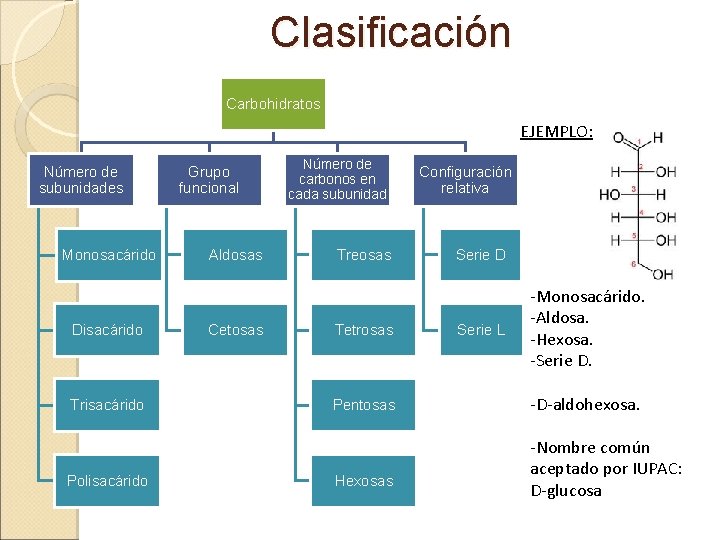
Clasificación Carbohidratos EJEMPLO: Número de subunidades Monosacárido Disacárido Trisacárido Polisacárido Grupo funcional Aldosas Cetosas Número de carbonos en cada subunidad Treosas Tetrosas Pentosas Hexosas Configuración relativa Serie D Serie L -Monosacárido. -Aldosa. -Hexosa. -Serie D. -D-aldohexosa. -Nombre común aceptado por IUPAC: D-glucosa

Concepto Químicamente, los glúcidos son polihidroxialdehídos, polihidroxicetonas o uniones poliméricas de éstos. 6
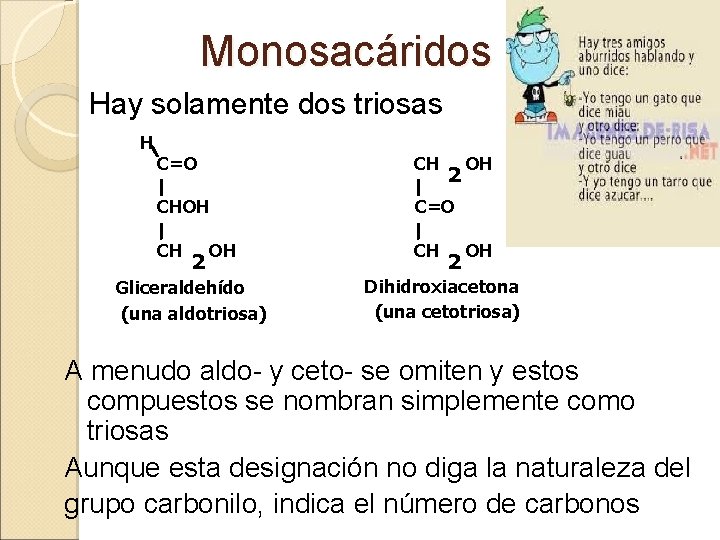
Monosacáridos Hay solamente dos triosas H C=O CH CHOH C=O CH CH 2 OH Gliceraldehído (una aldotriosa) 2 2 OH OH Dihidroxiacetona (una cetotriosa) A menudo aldo- y ceto- se omiten y estos compuestos se nombran simplemente como triosas Aunque esta designación no diga la naturaleza del grupo carbonilo, indica el número de carbonos
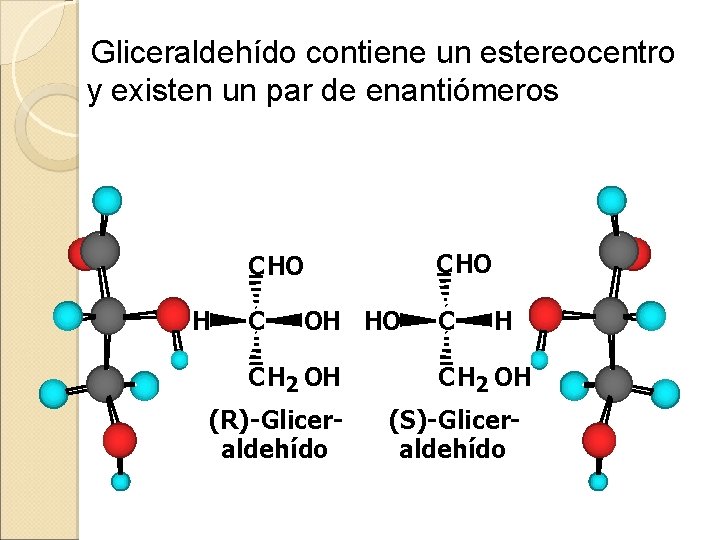
Gliceraldehído contiene un estereocentro y existen un par de enantiómeros CHO H C OH HO CH 2 OH (R)-Gliceraldehído C H CH 2 OH (S)-Gliceraldehído
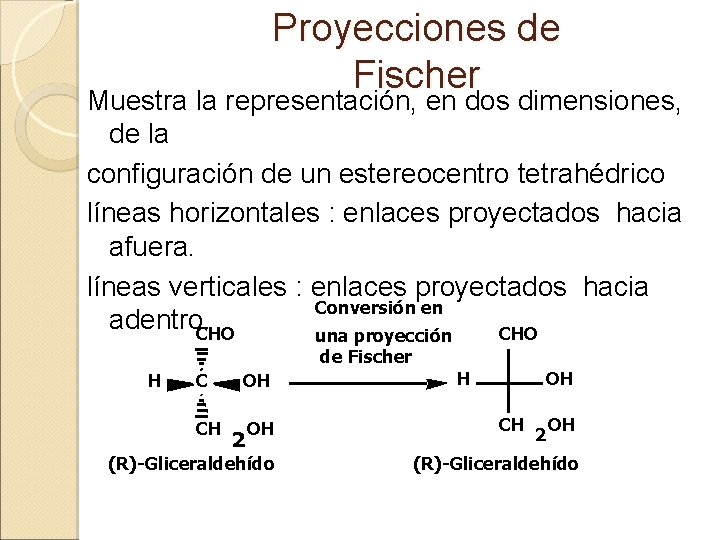
Proyecciones de Fischer Muestra la representación, en dos dimensiones, de la configuración de un estereocentro tetrahédrico líneas horizontales : enlaces proyectados hacia afuera. líneas verticales : enlaces proyectados hacia Conversión en adentro. CHO una proyección de Fischer H C OH CH OH 2 (R)-Gliceraldehído H OH CH 2 OH (R)-Gliceraldehído
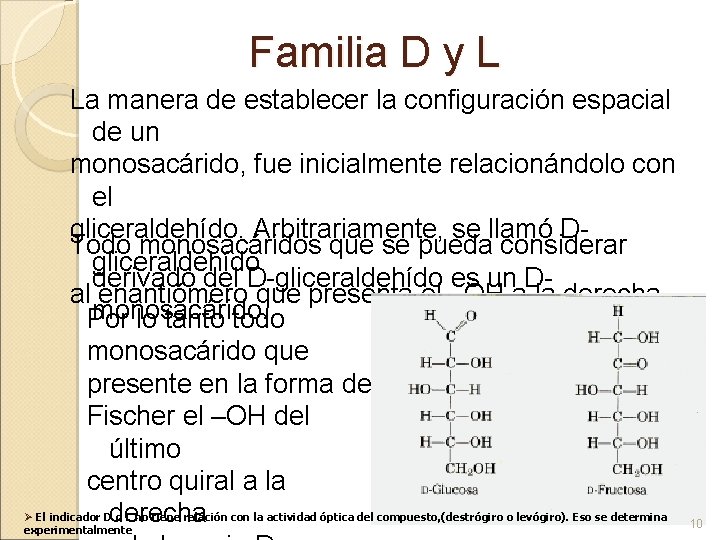
Familia D y L La manera de establecer la configuración espacial de un monosacárido, fue inicialmente relacionándolo con el gliceraldehído. Arbitrariamente, se llamó DTodo monosacáridos que se pueda considerar gliceraldehído derivado del D-gliceraldehído es un Dal enantiómero que presenta el –OH a la derecha. monosacárido. Por lo tanto todo monosacárido que presente en la forma de Fischer el –OH del último centro quiral a la Ø El indicador Dderecha o L no tiene relación con la actividad óptica del compuesto, (destrógiro o levógiro). Eso se determina experimentalmente 10
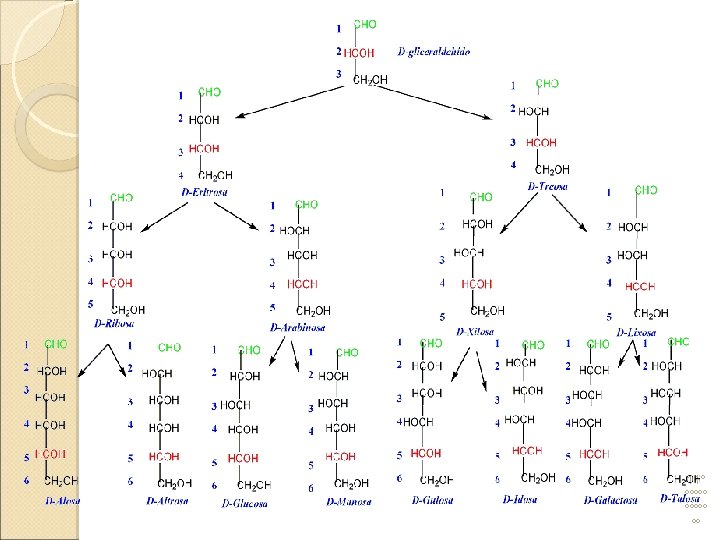

Monosacáridos El monosacárido más abundante es la glucosa. Prácticamente todo lo que es necesario saber acerca de la estructura de los monosacáridos, es posible conocerlo estudiando la glucosa. La glucosa es una aldohexosa Debido a que presenta 4 carbonos quirales, tiene actividad óptica, teniendo 8 pares de enantiómeros 12

Diasterómeros y enantiómeros De acuerdo con la regla de Van’t Hoff, la glucosa al tener 4 centros quirales, y por lo tanto 24=16 isómeros espaciales diferentes. 13

Epímeros Azúcares que se diferencian por la estereoquímica de un único átomo de carbono. Así la manosa y la glucosa son epímeros en C 2. Si no se especifíca el carbono se asume C 2.

Estructura Cíclica Los monosacáridos presentan grupos hidroxilo y carbonilo en la misma molécula, encontrándose en la naturaleza normalmente como hemiacetales cíclicos de cinco y seis Miembros Carbono anomérico : el nuevo estereocentro que resulta de la formación del hemiacetal cíclico.

Proyecciones de Haworth La representación más común es con el carbono anomérico a la derecha del oxígeno hemiacetálico que se encuentra detrás. La designación β- cuando el -OH del carbono anomérico es cis respecto al -CH 2 OH terminal; α- cuando es trans O O Furano Pirano Anillos de hemiacetal de seis-miembros son nombrados por el sufijo -piranosa Anillos de hemiacetal de cinco-miembros son
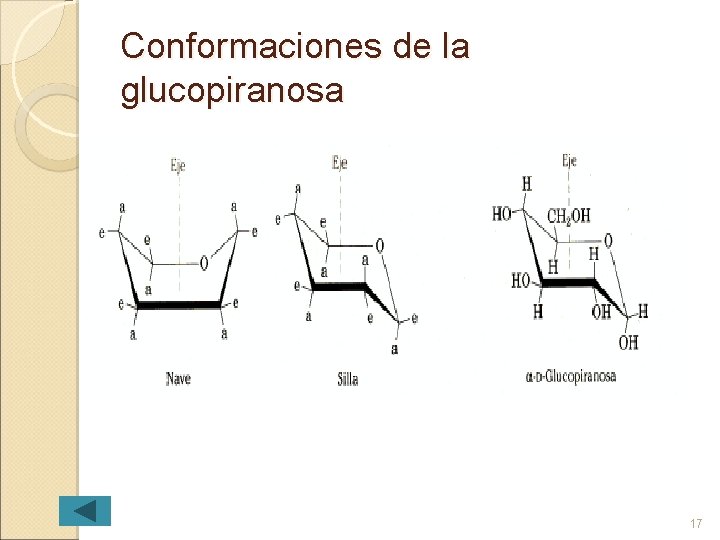
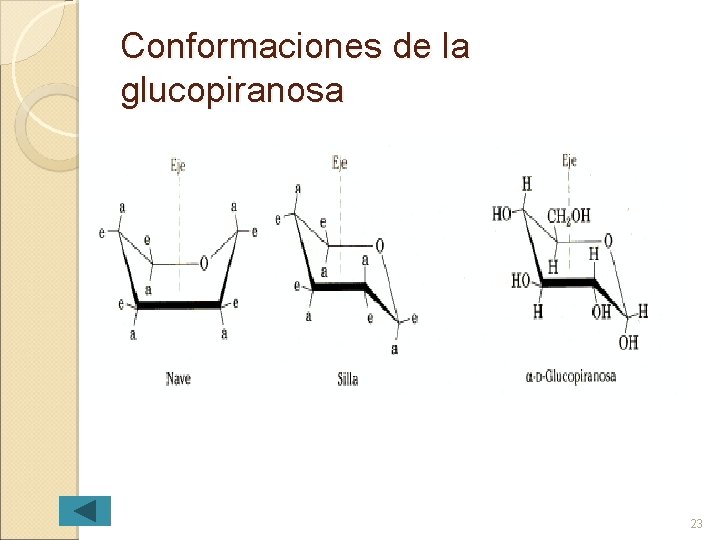
Conformaciones de la glucopiranosa 17
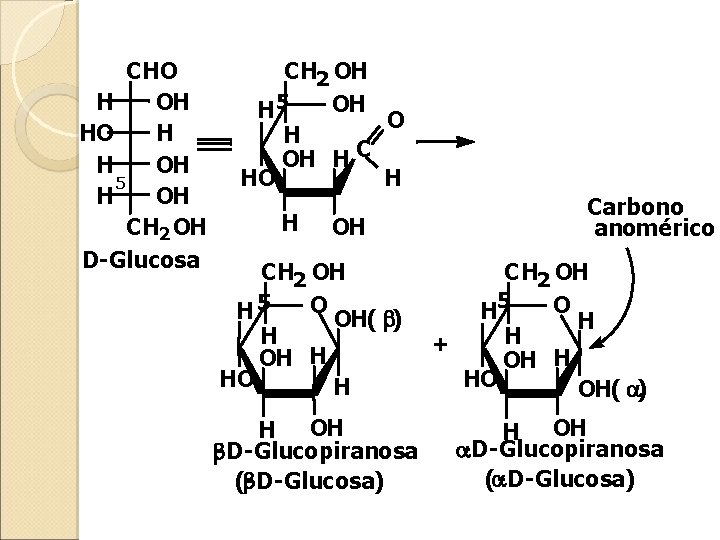
CHO H OH HO H H OH 5 H OH CH 2 OH D-Glucosa CH 2 OH OH H 5 O H OH H C H HO H OH CH 2 OH O H 5 OH( ) H OH H HO H H OH -D-Glucopiranosa ( -D-Glucosa) Carbono anomérico CH 2 OH O H 5 H H + OH H HO OH( ) H OH -D-Glucopiranosa ( -D-Glucosa)
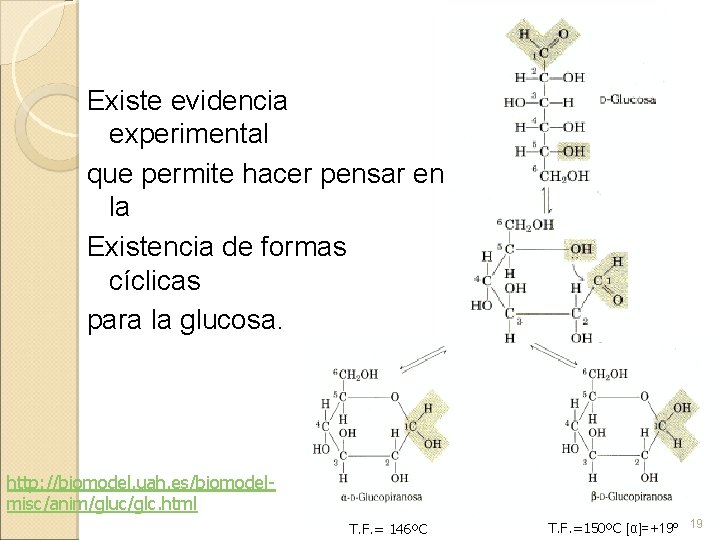
Existe evidencia experimental que permite hacer pensar en la Existencia de formas cíclicas para la glucosa. http: //biomodel. uah. es/biomodelmisc/anim/gluc/glc. html T. F. = 146ºC T. F. =150ºC [α]=+19º 19
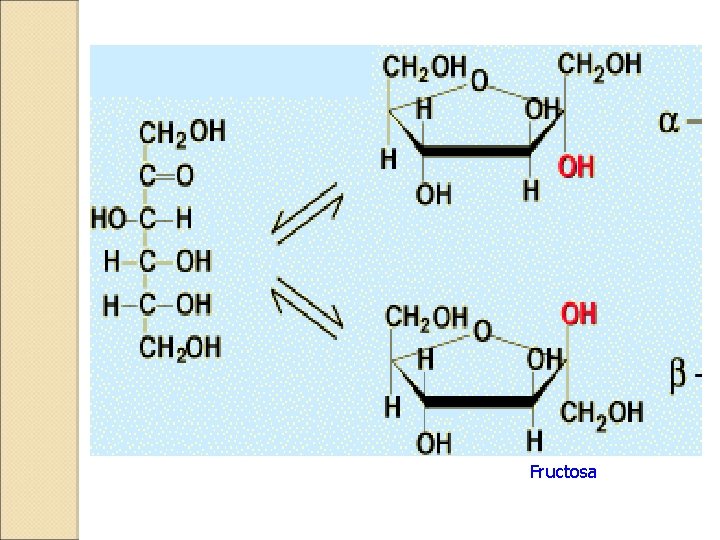
Fructosa
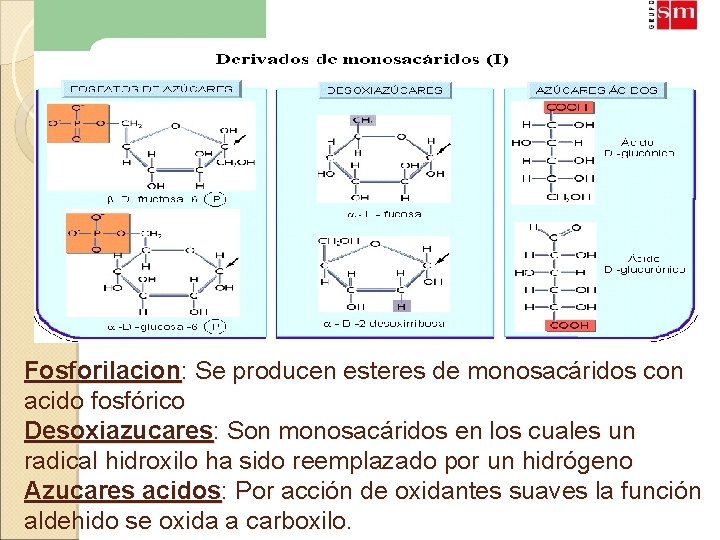
Fosforilacion: Se producen esteres de monosacáridos con acido fosfórico Desoxiazucares: Son monosacáridos en los cuales un radical hidroxilo ha sido reemplazado por un hidrógeno Azucares acidos: Por acción de oxidantes suaves la función aldehido se oxida a carboxilo.

Conformacionales Al comparar las orientaciones de los grupos de los carbonos 1 -5 en la proyecciones de Haworth y en la representación de -D-glucopiranosa se constata que los grupos CH 2 OH-OH están alternados a cada lado del plano. Para anillos de seis O OH los CH 2 miembros, OH H ( ) O H HO piranosas, la OH H HO HO conformación silla es la más adecuada OH ( ) H H OH -D-Glucopiranosa (proyección Haworth) OH -D-Glucopiranosa (conformación silla)
Conformaciones de la glucopiranosa 23

Mutarrotación El cambio en la [ rotación especifica que ocurre con las formas o de los carbohidratos se debe a la existencia de un equilibrio entre ambas [ ] después formas. Monosacárido -D-glucosa mutarrotación % presente en [ ] (grados ) (grados) el equilibrio +112. 0 +52. 7 36 +18. 7 +52. 7 64 -D-galactosa +150. 7 +80. 2 28 -D-galactosa +52. 8 +80. 2 72 -D-glucosa
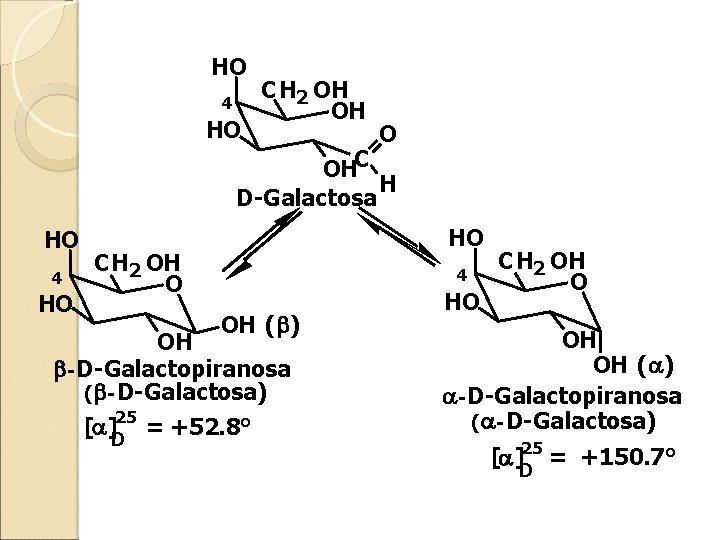
HO 4 HO CH 2 OH OH O OHC H D-Galactosa HO 4 HO HO CH 2 OH O 4 OH ( ) OH - D-Galactopiranosa ( - D-Galactosa) 25 [ ]D = +52. 8° HO CH 2 OH OH ( ) - D-Galactopiranosa ( - D-Galactosa) 25 [ ]D = +150. 7°
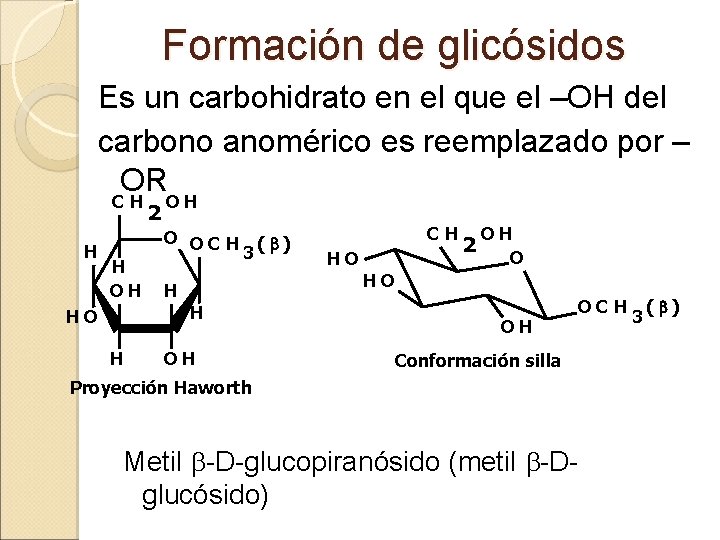
Formación de glicósidos Es un carbohidrato en el que el –OH del carbono anomérico es reemplazado por – OR CH H 2 OH O OC H H OH 3 H CH HO 2 OH O HO H H HO ( ) OH OH OC H Conformación silla Proyección Haworth Metil -D-glucopiranósido (metil -Dglucósido) 3 ( )
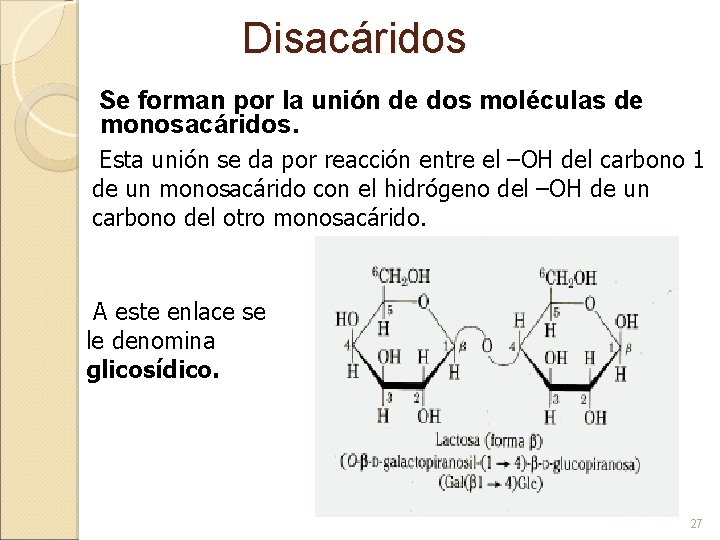
Disacáridos Se forman por la unión de dos moléculas de monosacáridos. Esta unión se da por reacción entre el –OH del carbono 1 de un monosacárido con el hidrógeno del –OH de un carbono del otro monosacárido. A este enlace se le denomina glicosídico. 27
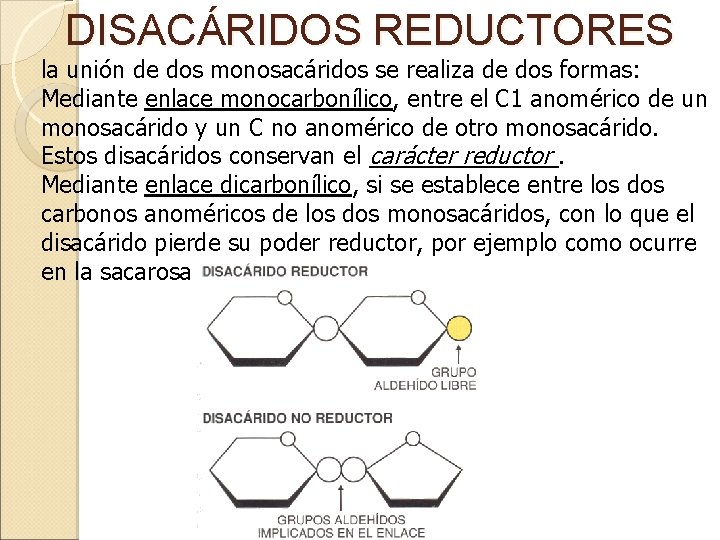
DISACÁRIDOS REDUCTORES la unión de dos monosacáridos se realiza de dos formas: Mediante enlace monocarbonílico, entre el C 1 anomérico de un monosacárido y un C no anomérico de otro monosacárido. Estos disacáridos conservan el carácter reductor. Mediante enlace dicarbonílico, si se establece entre los dos carbonos anoméricos de los dos monosacáridos, con lo que el disacárido pierde su poder reductor, por ejemplo como ocurre en la sacarosa
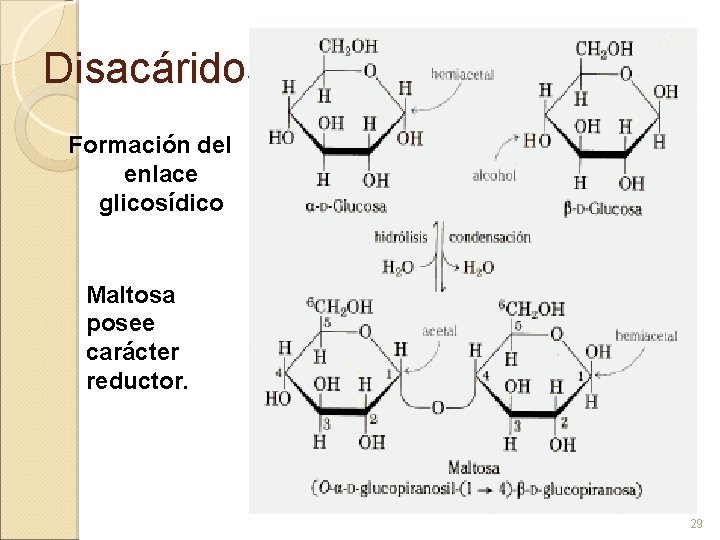
Disacáridos Formación del enlace glicosídico Maltosa posee carácter reductor. 29
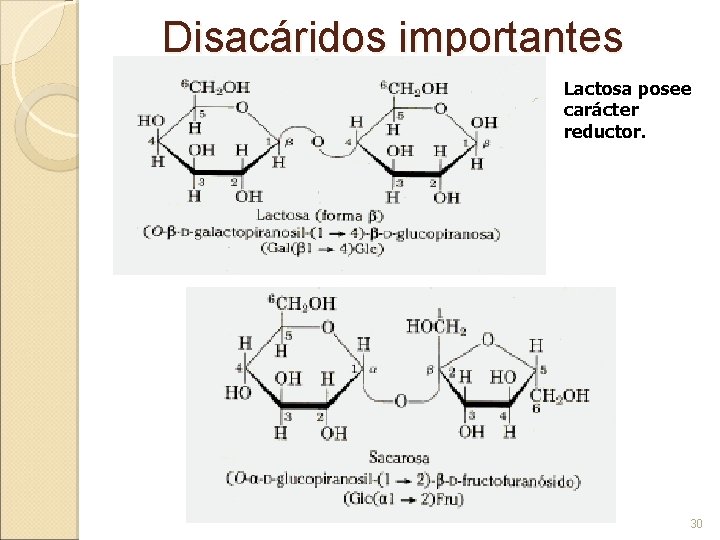
Disacáridos importantes Lactosa posee carácter reductor. 30

Polisacáridos Se forman por la unión mediante enlace glicosídico de cerca de 100 o más unidades de monosacáridos. Los polisacáridos más importantes son: el 31
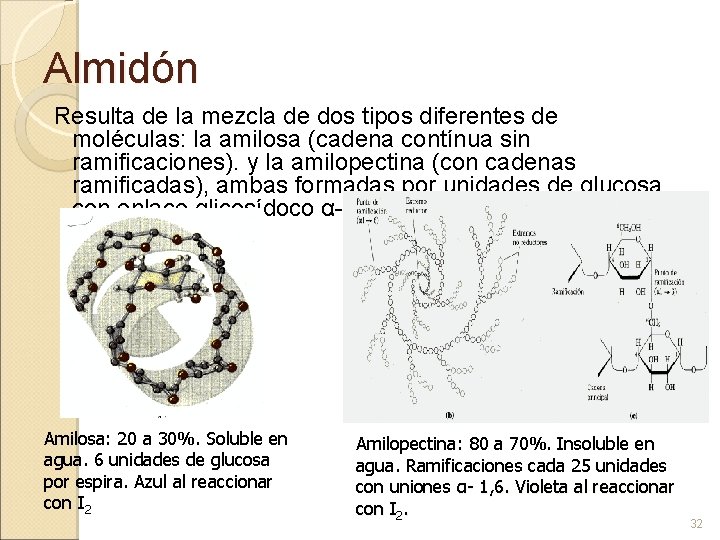
Almidón Resulta de la mezcla de dos tipos diferentes de moléculas: la amilosa (cadena contínua sin ramificaciones). y la amilopectina (con cadenas ramificadas), ambas formadas por unidades de glucosa con enlace glicosídoco α-1, 4. Amilosa: 20 a 30%. Soluble en agua. 6 unidades de glucosa por espira. Azul al reaccionar con I 2 Amilopectina: 80 a 70%. Insoluble en agua. Ramificaciones cada 25 unidades con uniones α- 1, 6. Violeta al reaccionar con I 2. 32
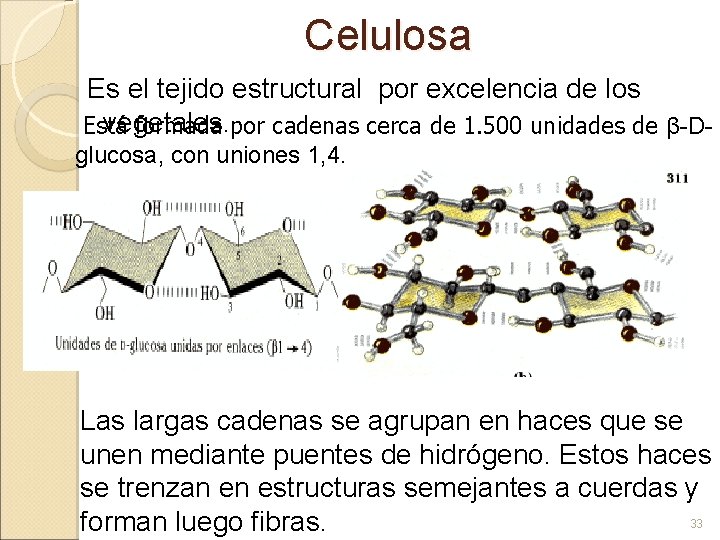
Celulosa Es el tejido estructural por excelencia de los vegetales. Está formada por cadenas cerca de 1. 500 unidades de β-Dglucosa, con uniones 1, 4. Las largas cadenas se agrupan en haces que se unen mediante puentes de hidrógeno. Estos haces se trenzan en estructuras semejantes a cuerdas y 33 forman luego fibras.

Los alimentos con mas azucares 34

Imágenes tomadas de: “ Principios de Bioquímica” Albert L. Lehninger 1992 35
- Slides: 35