Glcidos Concepto Los glcidos son biomolculas formadas bsicamente

Glúcidos

Concepto. • Los glúcidos son biomoléculas formadas básicamente por carbono (C), hidrógeno (H) y oxígeno (O). Los átomos de carbono están unidos a grupos alcohólicos (-OH), llamados también radicales hidroxilo y a radicales hidrógeno (-H). • En todos los glúcidos siempre hay un grupo carbonilo, es decir, un carbono unido a un oxígeno mediante un doble enlace (C=O). El grupo carbonilo puede ser un grupo aldehído (CHO), o un grupo cetónico (-CO-). Así pues, los glúcidos pueden definirse como polihidroxialdehídos o polihidroxicetonas

• El nombre de glúcido deriva de la palabra "glucosa" que proviene del vocablo griego glykys que significa dulce, aunque solamente lo son algunos monosacáridos y disacáridos. • Su fórmula general suele ser (CH 2 O)n
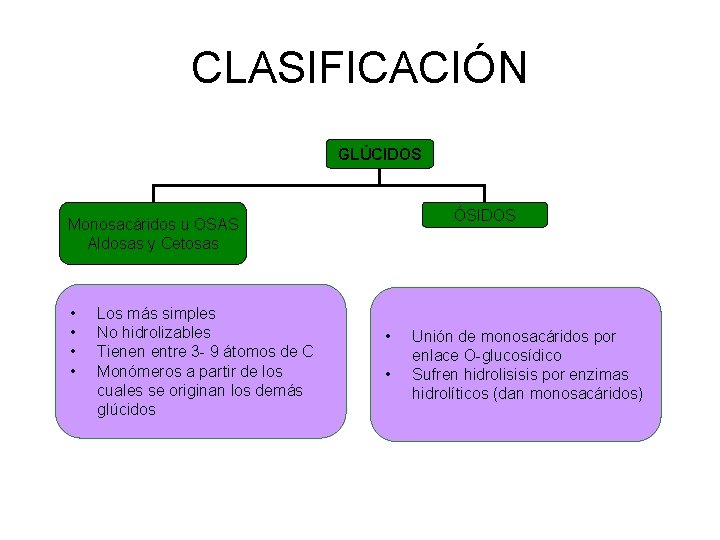
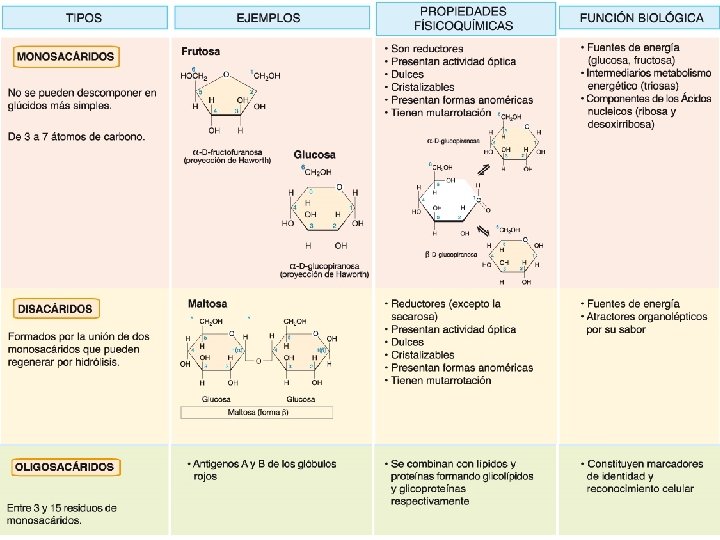
CLASIFICACIÓN GLÚCIDOS ÓSIDOS Monosacáridos u OSAS Aldosas y Cetosas • • Los más simples No hidrolizables Tienen entre 3 - 9 átomos de C Monómeros a partir de los cuales se originan los demás glúcidos • • Unión de monosacáridos por enlace O-glucosídico Sufren hidrolisisis por enzimas hidrolíticos (dan monosacáridos)
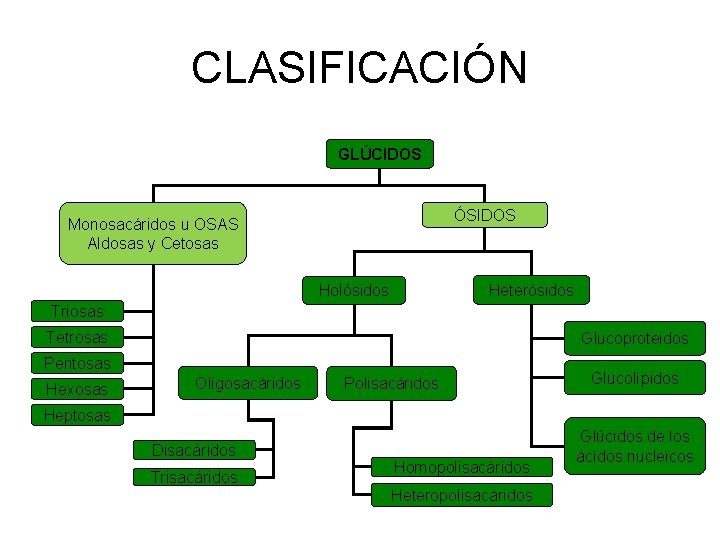
CLASIFICACIÓN GLÚCIDOS ÓSIDOS Monosacáridos u OSAS Aldosas y Cetosas Heterósidos Holósidos Triosas Tetrosas Glucoproteidos Pentosas Hexosas Oligosacáridos Polisacáridos Glucolípidos Heptosas Disacáridos Trisacáridos Homopolisacáridos Heteropolisacáridos Glúcidos de los ácidos nucleicos
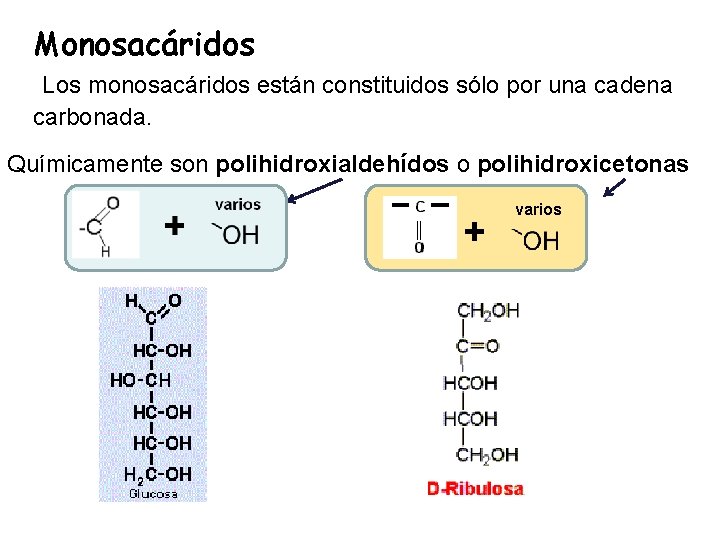
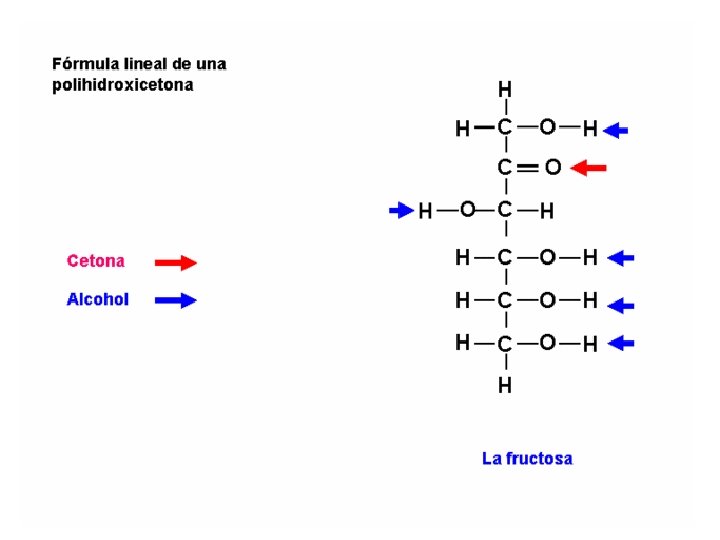
Monosacáridos Los monosacáridos están constituidos sólo por una cadena carbonada. Químicamente son polihidroxialdehídos o polihidroxicetonas + varios
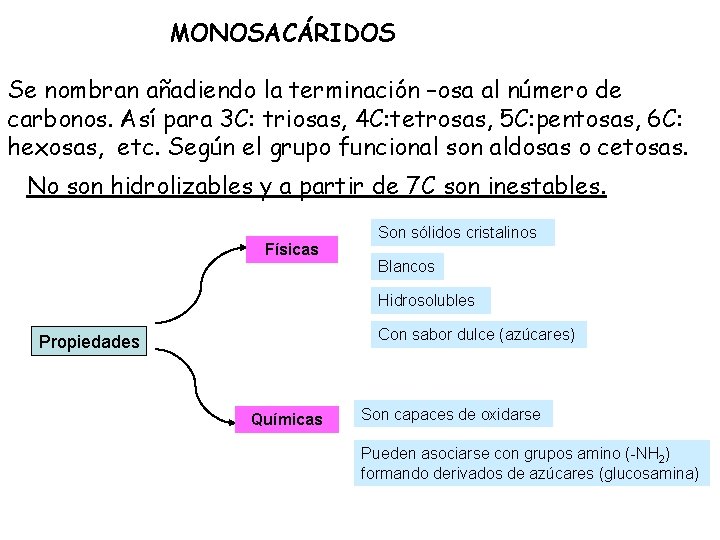
MONOSACÁRIDOS Se nombran añadiendo la terminación –osa al número de carbonos. Así para 3 C: triosas, 4 C: tetrosas, 5 C: pentosas, 6 C: hexosas, etc. Según el grupo funcional son aldosas o cetosas. No son hidrolizables y a partir de 7 C son inestables. Físicas Son sólidos cristalinos Blancos Hidrosolubles Con sabor dulce (azúcares) Propiedades Químicas Son capaces de oxidarse Pueden asociarse con grupos amino (-NH 2) formando derivados de azúcares (glucosamina)
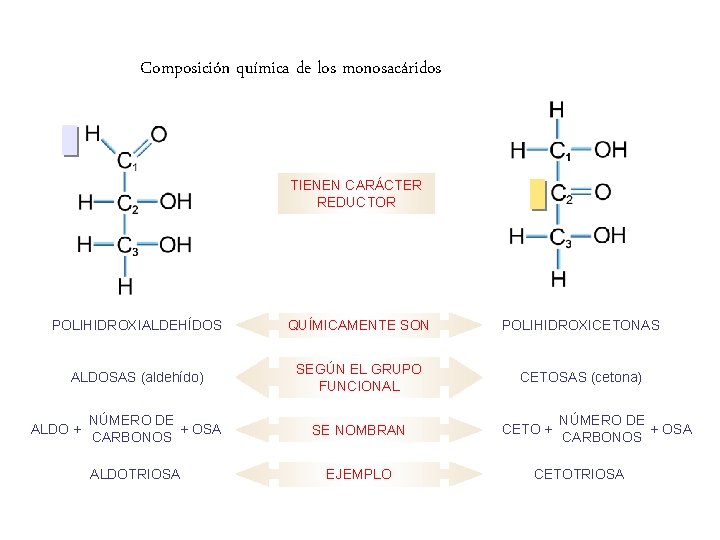
Composición química de los monosacáridos TIENEN CARÁCTER REDUCTOR POLIHIDROXIALDEHÍDOS QUÍMICAMENTE SON POLIHIDROXICETONAS ALDOSAS (aldehído) SEGÚN EL GRUPO FUNCIONAL CETOSAS (cetona) ALDO + NÚMERO DE + OSA CARBONOS ALDOTRIOSA SE NOMBRAN EJEMPLO CETO + NÚMERO DE + OSA CARBONOS CETOTRIOSA
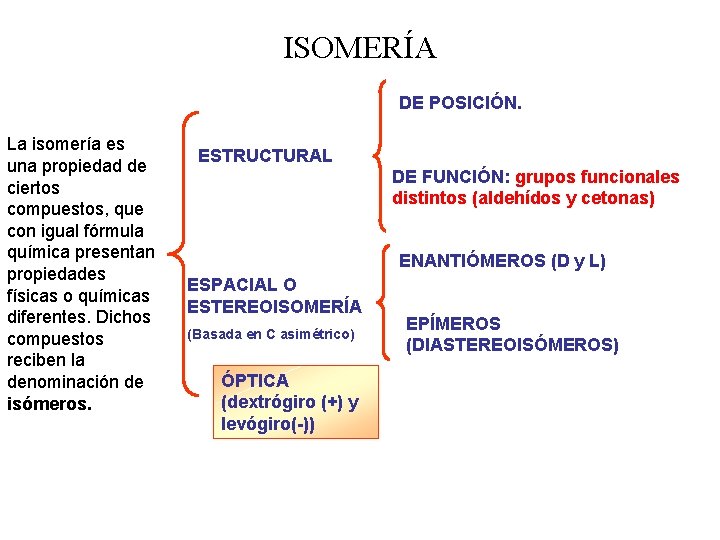
ISOMERÍA DE POSICIÓN. La isomería es una propiedad de ciertos compuestos, que con igual fórmula química presentan propiedades físicas o químicas diferentes. Dichos compuestos reciben la denominación de isómeros. ESTRUCTURAL DE FUNCIÓN: grupos funcionales distintos (aldehídos y cetonas) ENANTIÓMEROS (D y L) ESPACIAL O ESTEREOISOMERÍA (Basada en C asimétrico) ÓPTICA (dextrógiro (+) y levógiro(-)) EPÍMEROS (DIASTEREOISÓMEROS)
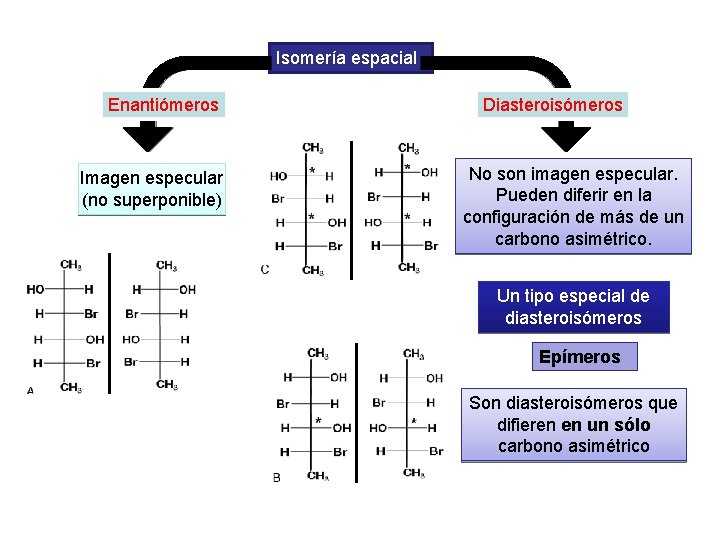
Isomería espacial Enantiómeros Imagen especular (no superponible) Diasteroisómeros No son imagen especular. Pueden diferir en la configuración de más de un carbono asimétrico. Un tipo especial de diasteroisómeros Epímeros Son diasteroisómeros que difieren en un sólo carbono asimétrico
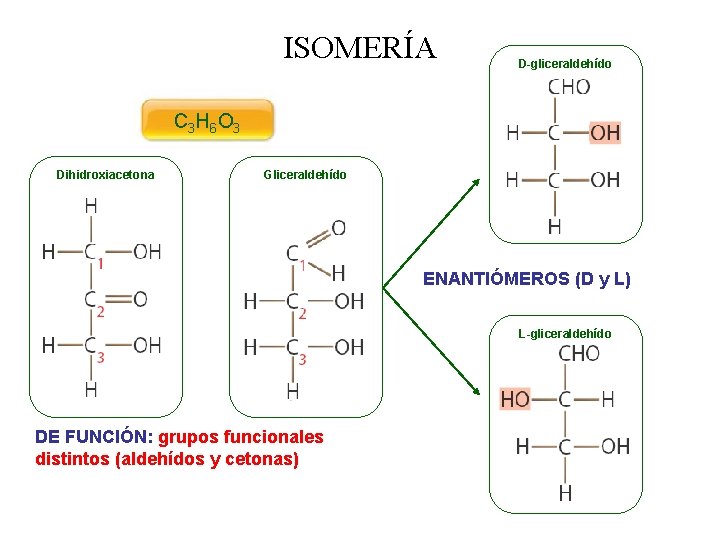
ISOMERÍA D-gliceraldehído C 3 H 6 O 3 Dihidroxiacetona Gliceraldehído ENANTIÓMEROS (D y L) L-gliceraldehído DE FUNCIÓN: grupos funcionales distintos (aldehídos y cetonas)
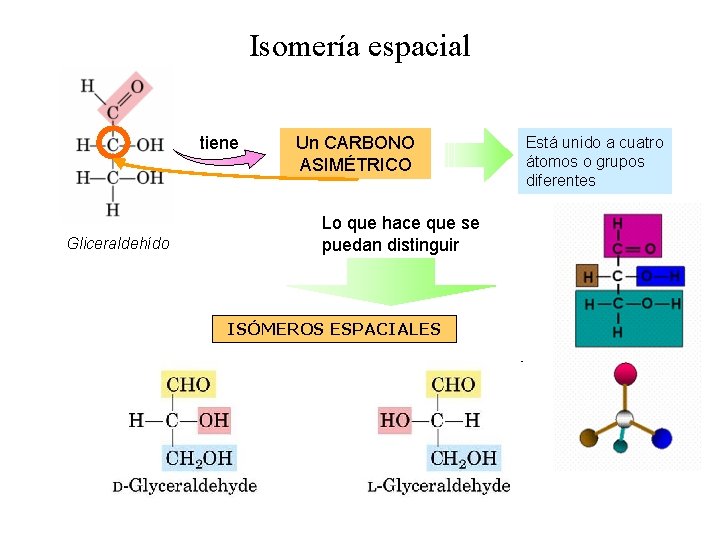
Isomería espacial tiene Gliceraldehído Un CARBONO ASIMÉTRICO Lo que hace que se puedan distinguir ISÓMEROS ESPACIALES Está unido a cuatro átomos o grupos diferentes
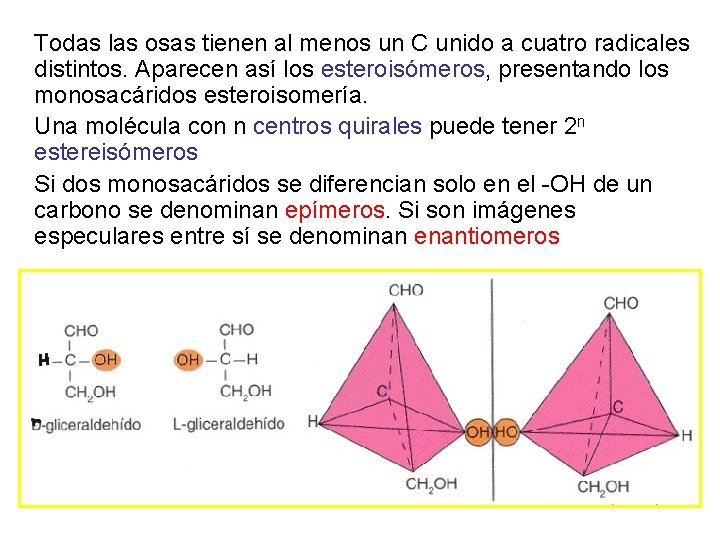
Todas las osas tienen al menos un C unido a cuatro radicales distintos. Aparecen así los esteroisómeros, presentando los monosacáridos esteroisomería. Una molécula con n centros quirales puede tener 2 n estereisómeros Si dos monosacáridos se diferencian solo en el -OH de un carbono se denominan epímeros. Si son imágenes especulares entre sí se denominan enantiomeros
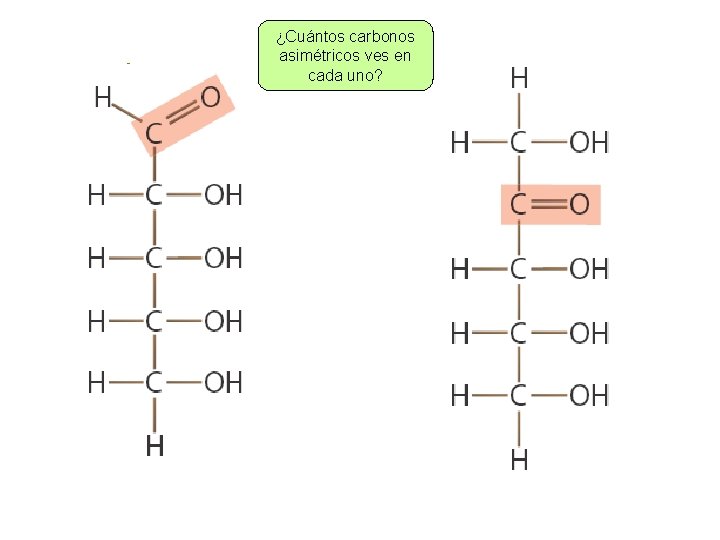
Los glúcidos ¿Cuántos carbonos asimétricos ves en cada uno?
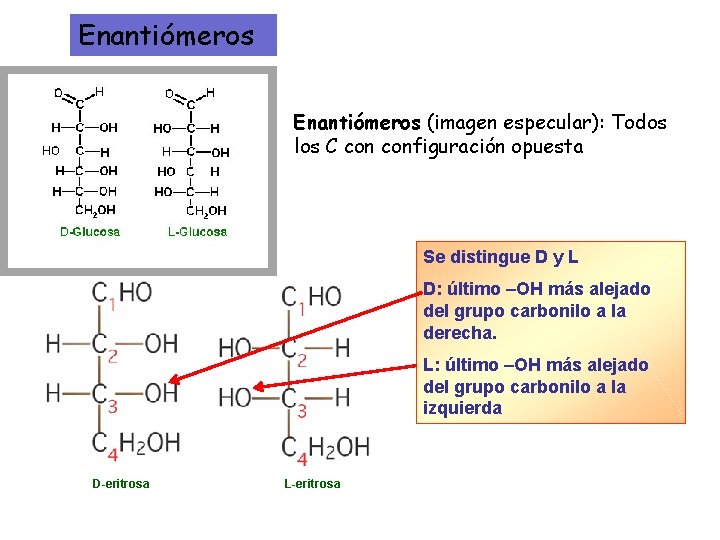
Enantiómeros (imagen especular): Todos los C configuración opuesta Se distingue D y L D: último –OH más alejado del grupo carbonilo a la derecha. L: último –OH más alejado del grupo carbonilo a la izquierda D-eritrosa L-eritrosa
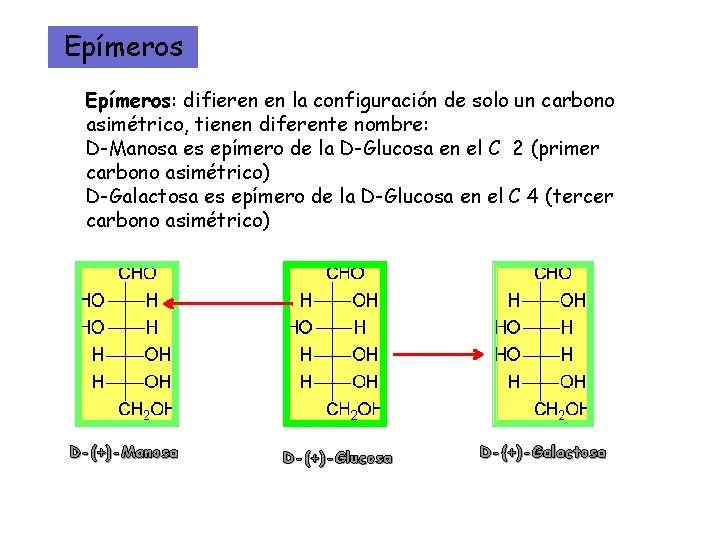
Epímeros: difieren en la configuración de solo un carbono asimétrico, tienen diferente nombre: D-Manosa es epímero de la D-Glucosa en el C 2 (primer carbono asimétrico) D-Galactosa es epímero de la D-Glucosa en el C 4 (tercer carbono asimétrico) D-(+)-Manosa D-(+)-Glucosa D-(+)-Galactosa
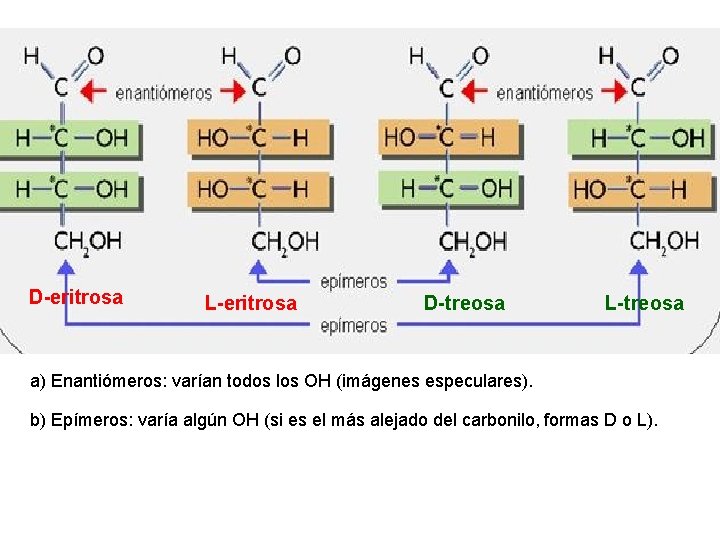
D-eritrosa L-eritrosa D-treosa L-treosa a) Enantiómeros: varían todos los OH (imágenes especulares). b) Epímeros: varía algún OH (si es el más alejado del carbonilo, formas D o L).
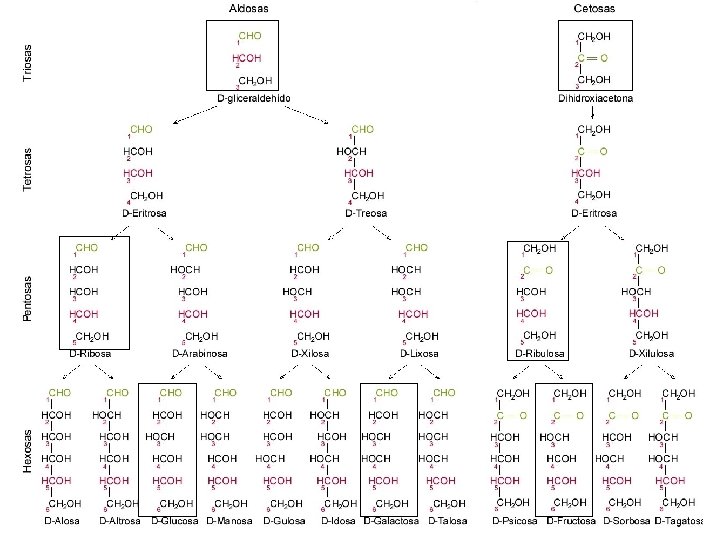
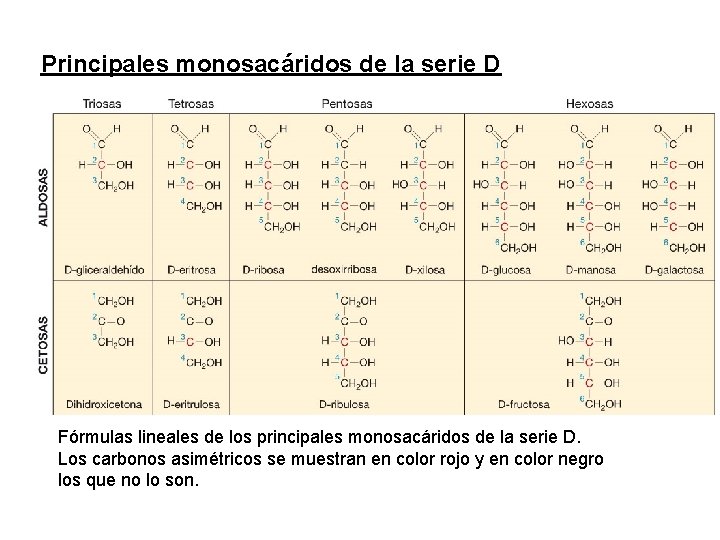
Principales monosacáridos de la serie D 2. Monosacáridos Fórmulas lineales de los principales monosacáridos de la serie D. Los carbonos asimétricos se muestran en color rojo y en color negro los que no lo son.
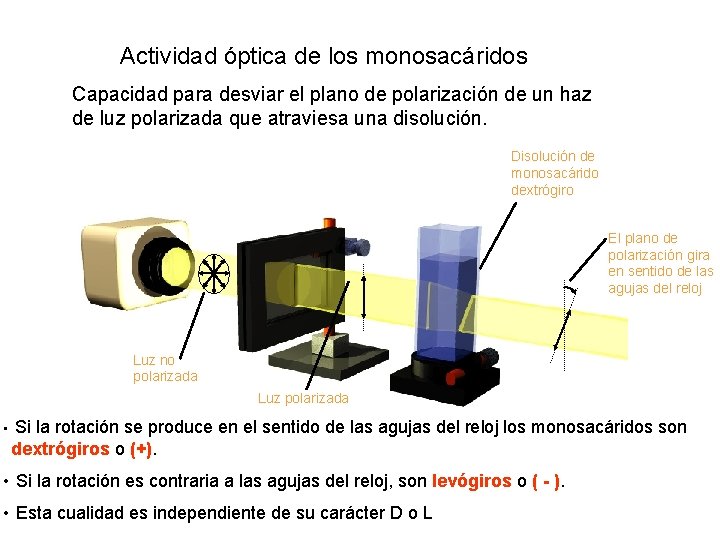
Actividad óptica de los monosacáridos Capacidad para desviar el plano de polarización de un haz de luz polarizada que atraviesa una disolución. Disolución de monosacárido dextrógiro El plano de polarización gira en sentido de las agujas del reloj Luz no polarizada Luz polarizada • Si la rotación se produce en el sentido de las agujas del reloj los monosacáridos son dextrógiros o (+). • Si la rotación es contraria a las agujas del reloj, son levógiros o ( - ). • Esta cualidad es independiente de su carácter D o L
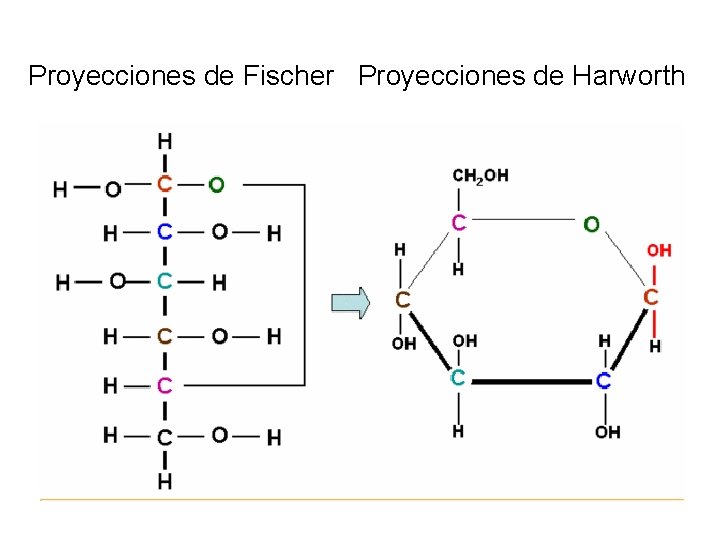
Proyecciones de Fischer Proyecciones de Harworth
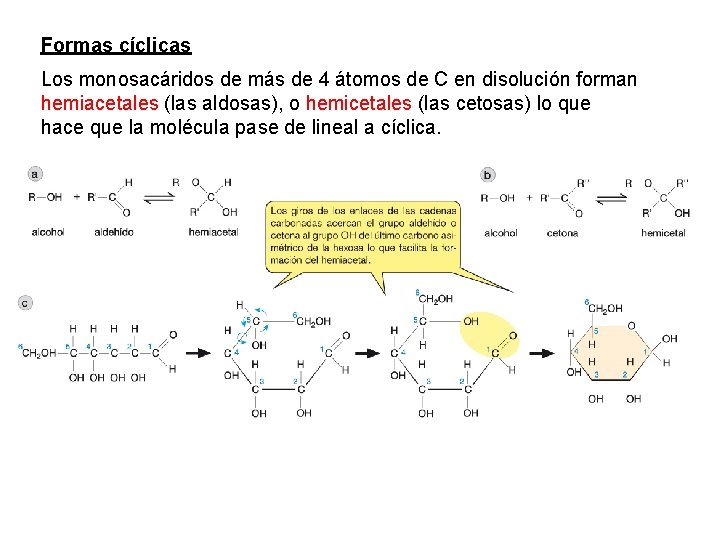
Formas cíclicas Los monosacáridos de más de 4 átomos de C en disolución forman hemiacetales (las aldosas), o hemicetales (las cetosas) lo que hace que la molécula pase de lineal a cíclica.
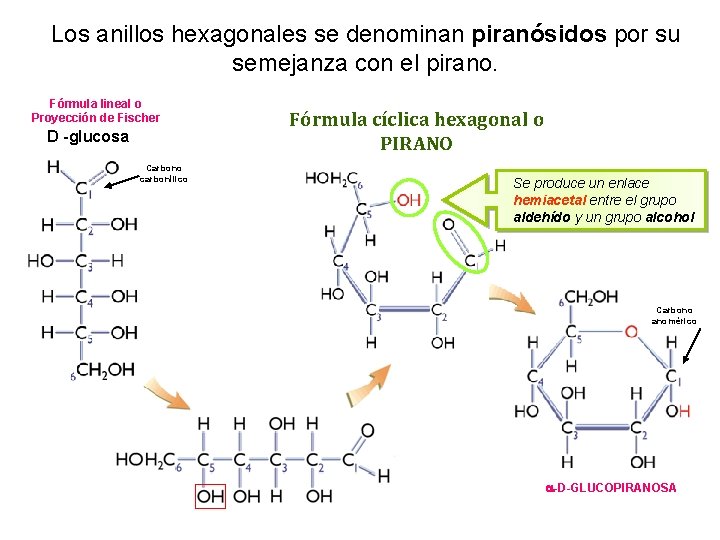
Los anillos hexagonales se denominan piranósidos por su semejanza con el pirano. Fórmula lineal o Proyección de Fischer D -glucosa Carbono carbonílico Fórmula cíclica hexagonal o PIRANO Se produce un enlace hemiacetal entre el grupo aldehído y un grupo alcohol Carbono anomérico a-D-GLUCOPIRANOSA
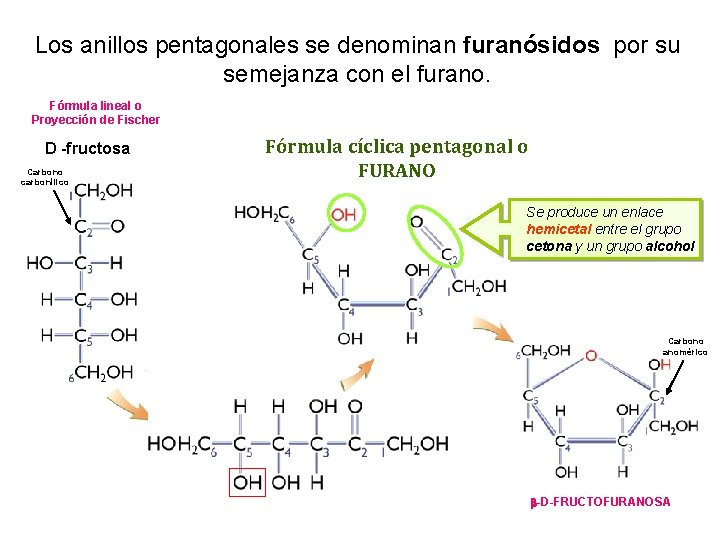
Los anillos pentagonales se denominan furanósidos por su semejanza con el furano. Fórmula lineal o Proyección de Fischer D -fructosa Carbono carbonílico Fórmula cíclica pentagonal o FURANO Se produce un enlace hemicetal entre el grupo cetona y un grupo alcohol Carbono anomérico b-D-FRUCTOFURANOSA
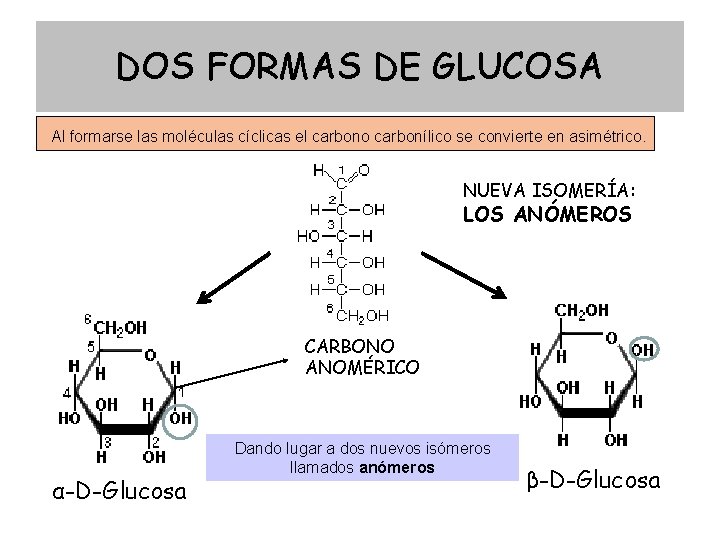
DOS FORMAS DE GLUCOSA Al formarse las moléculas cíclicas el carbono carbonílico se convierte en asimétrico. NUEVA ISOMERÍA: LOS ANÓMEROS CARBONO ANOMÉRICO α-D-Glucosa Dando lugar a dos nuevos isómeros llamados anómeros β-D-Glucosa
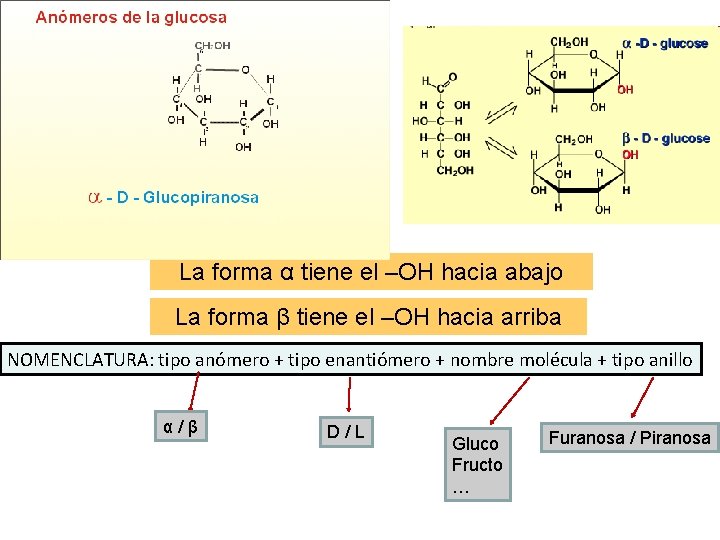
La forma α tiene el –OH hacia abajo La forma β tiene el –OH hacia arriba NOMENCLATURA: tipo anómero + tipo enantiómero + nombre molécula + tipo anillo α / β D / L Gluco Fructo … Furanosa / Piranosa
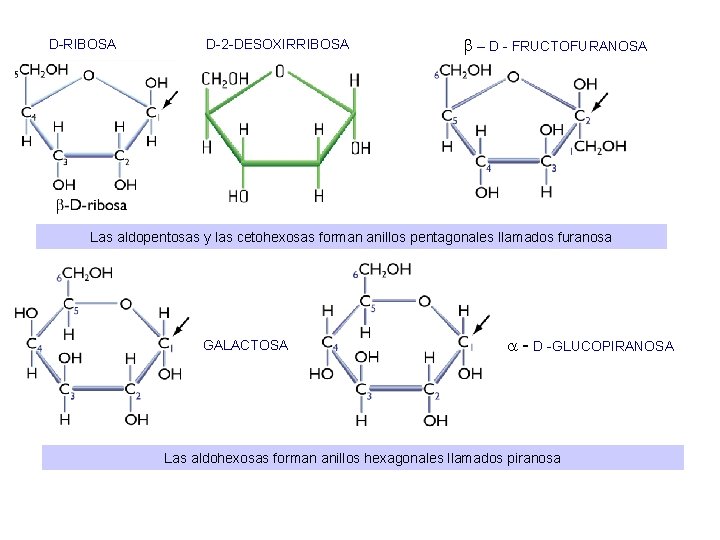
D-RIBOSA D-2 -DESOXIRRIBOSA – D - FRUCTOFURANOSA Las aldopentosas y las cetohexosas forman anillos pentagonales llamados furanosa GALACTOSA - D -GLUCOPIRANOSA Las aldohexosas forman anillos hexagonales llamados piranosa
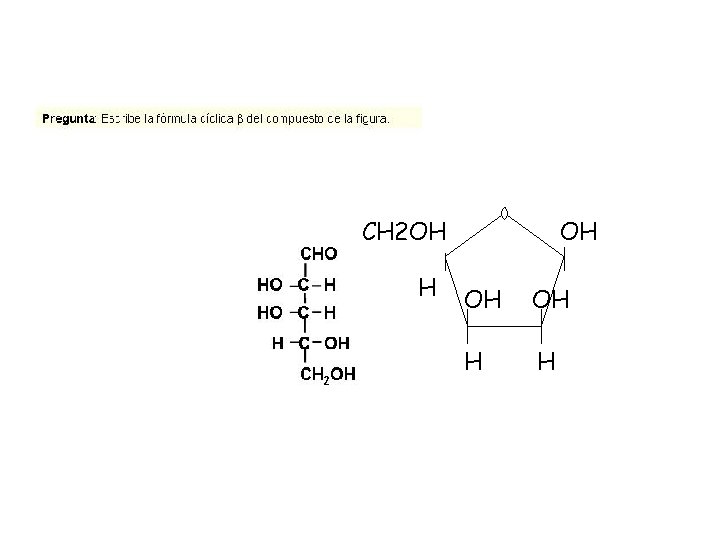
CH 2 OH H OH OH OH H H
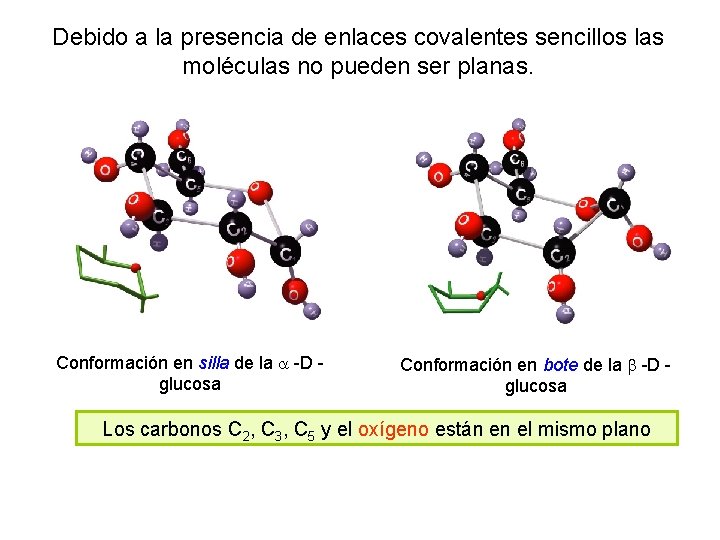
Debido a la presencia de enlaces covalentes sencillos las moléculas no pueden ser planas. Conformación en silla de la -D - glucosa Conformación en bote de la -D - glucosa Los carbonos C 2, C 3, C 5 y el oxígeno están en el mismo plano
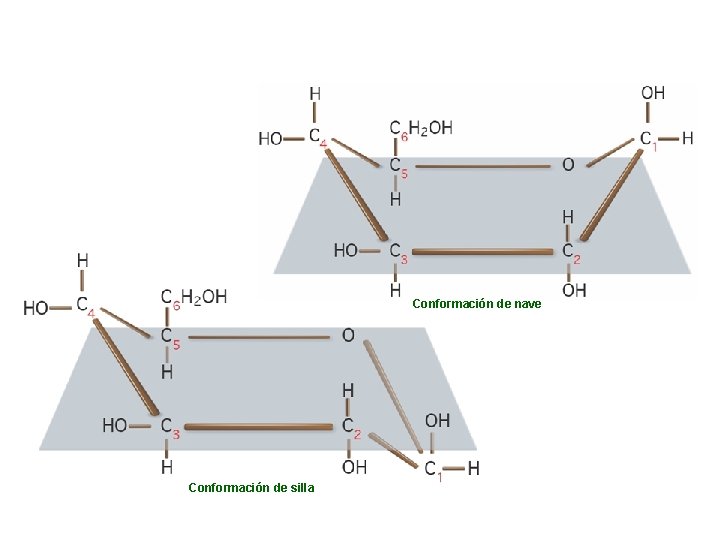
Conformación de nave Conformación de silla
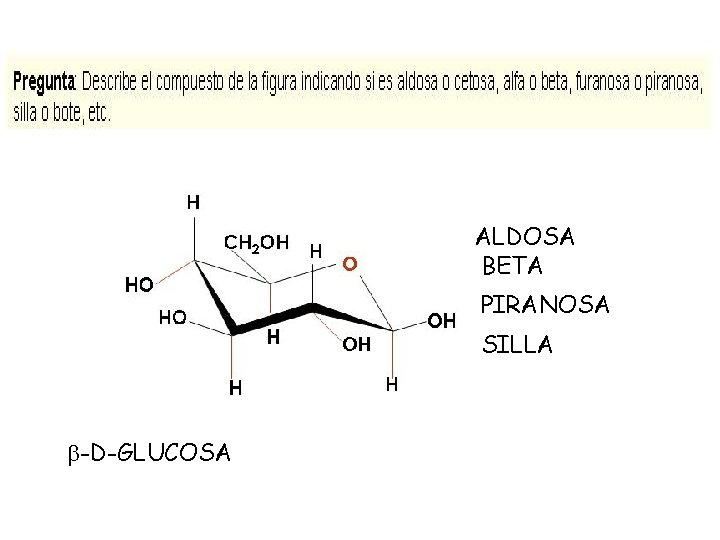
ALDOSA BETA PIRANOSA SILLA -D-GLUCOSA
![IMPORTANCIA BIOLÓGICA 1. Triosas [ C 3 H 6 O 3 ]: intermediarios metabolismo. IMPORTANCIA BIOLÓGICA 1. Triosas [ C 3 H 6 O 3 ]: intermediarios metabolismo.](http://slidetodoc.com/presentation_image/4adecf21c5394fa892221e25b5a16632/image-33.jpg)
IMPORTANCIA BIOLÓGICA 1. Triosas [ C 3 H 6 O 3 ]: intermediarios metabolismo. 2. Pentosas [ C 5 H 10 O 5 ] Ribosa: forma parte del ATP y del ARN Gliceraldehído Dihidroxiacetona Ribulosa: se une al CO 2 en la fotosíntesis
![IMPORTANCIA BIOLÓGICA (2) 3. Hexosas [ C 6 H 12 O 6 ]: las IMPORTANCIA BIOLÓGICA (2) 3. Hexosas [ C 6 H 12 O 6 ]: las](http://slidetodoc.com/presentation_image/4adecf21c5394fa892221e25b5a16632/image-34.jpg)
IMPORTANCIA BIOLÓGICA (2) 3. Hexosas [ C 6 H 12 O 6 ]: las más importantes y abundantes. Fructosa: también combustible metabólico. Glucosa: principal combustible metabólico Galactosa: forma parte de la lactosa
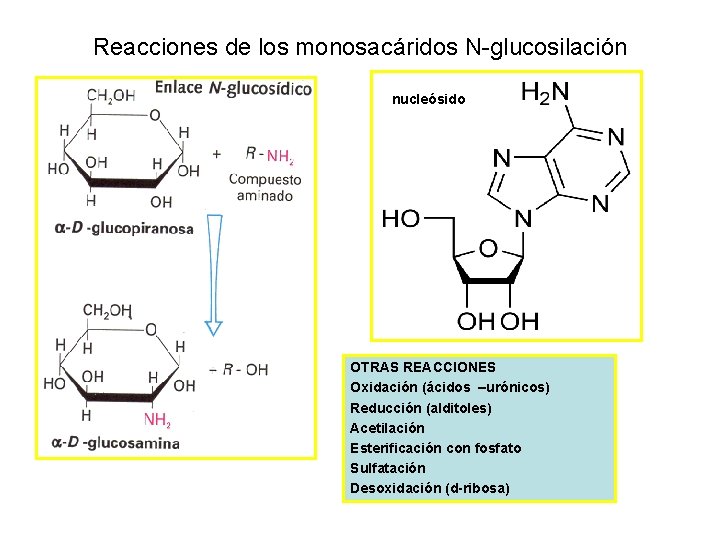
Reacciones de los monosacáridos N-glucosilación nucleósido OTRAS REACCIONES Oxidación (ácidos –urónicos) Reducción (alditoles) Acetilación Esterificación con fosfato Sulfatación Desoxidación (d-ribosa)
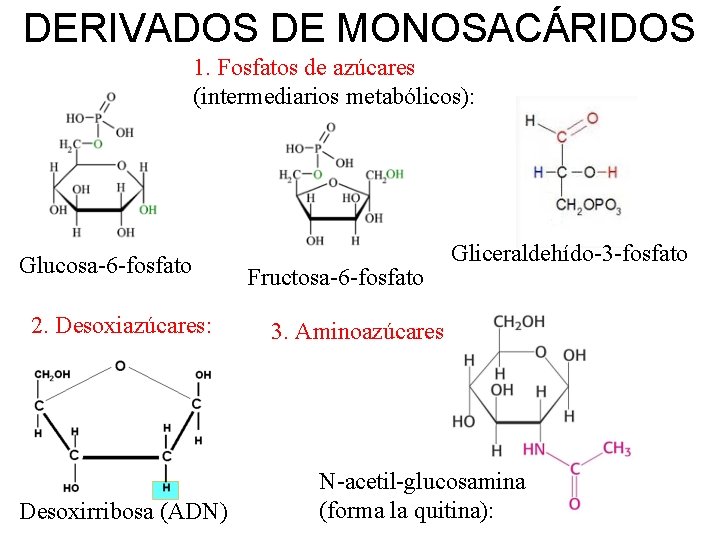
DERIVADOS DE MONOSACÁRIDOS 1. Fosfatos de azúcares (intermediarios metabólicos): Glucosa-6 -fosfato 2. Desoxiazúcares: Desoxirribosa (ADN) Fructosa-6 -fosfato Gliceraldehído-3 -fosfato 3. Aminoazúcares N-acetil-glucosamina (forma la quitina):
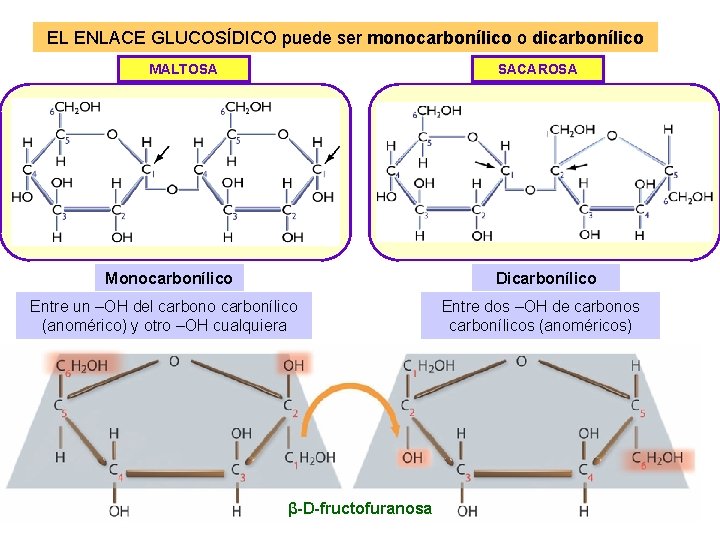
EL ENLACE GLUCOSÍDICO puede ser monocarbonílico o dicarbonílico MALTOSA SACAROSA Monocarbonílico Dicarbonílico Entre un –OH del carbono carbonílico (anomérico) y otro –OH cualquiera Entre dos –OH de carbonos carbonílicos (anoméricos) β-D-fructofuranosa
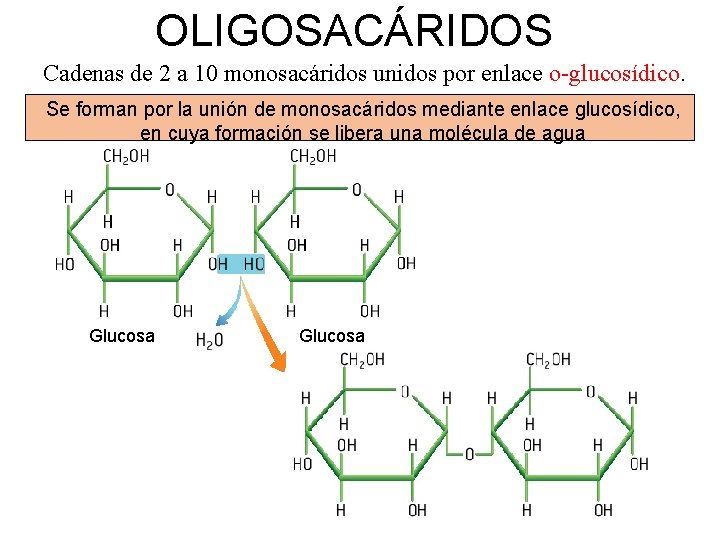
OLIGOSACÁRIDOS Cadenas de 2 a 10 monosacáridos unidos por enlace o-glucosídico. Se forman por la unión de monosacáridos mediante enlace glucosídico, en cuya formación se libera una molécula de agua Glucosa
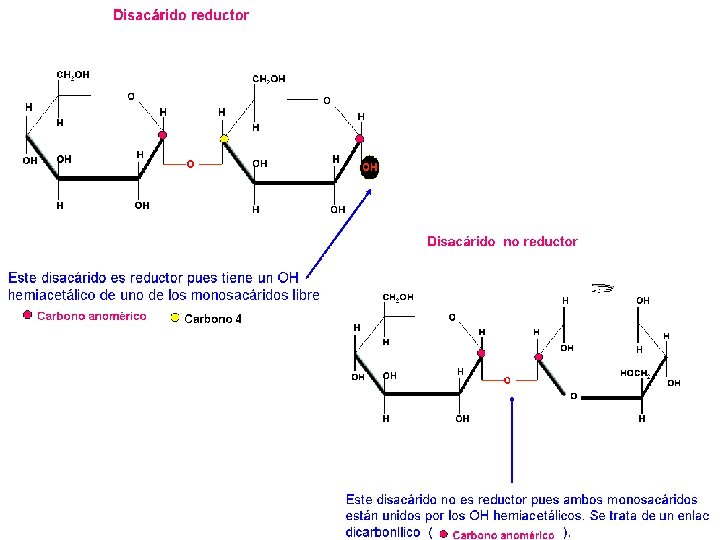
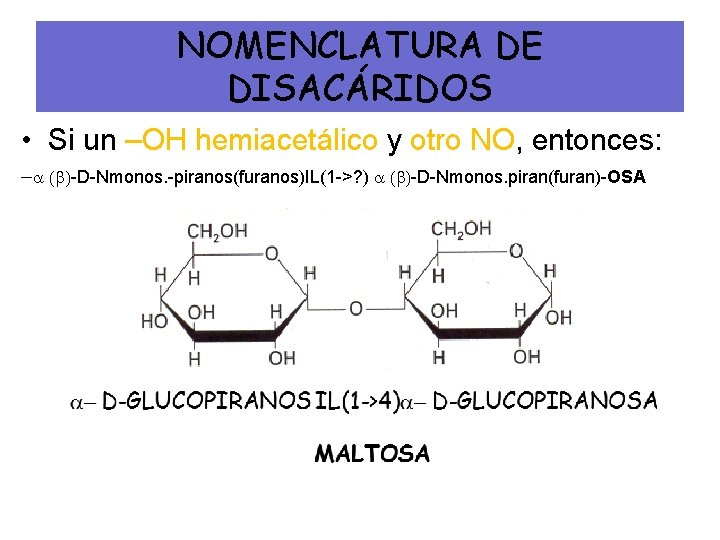
NOMENCLATURA DE DISACÁRIDOS • Si un –OH hemiacetálico y otro NO, entonces: - ( )-D-Nmonos. -piranos(furanos)IL(1 ->? ) ( )-D-Nmonos. piran(furan)-OSA
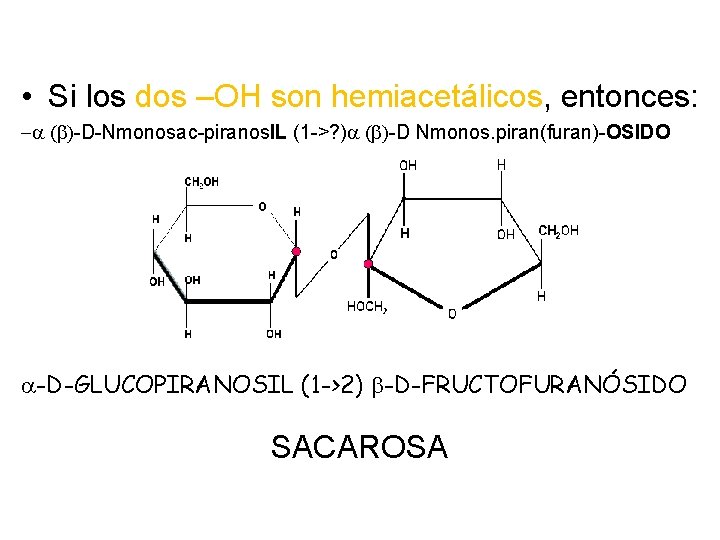
• Si los dos –OH son hemiacetálicos, entonces: - ( )-D-Nmonosac-piranos. IL (1 ->? ) ( )-D Nmonos. piran(furan)-OSIDO -D-GLUCOPIRANOSIL (1 ->2) -D-FRUCTOFURANÓSIDO SACAROSA
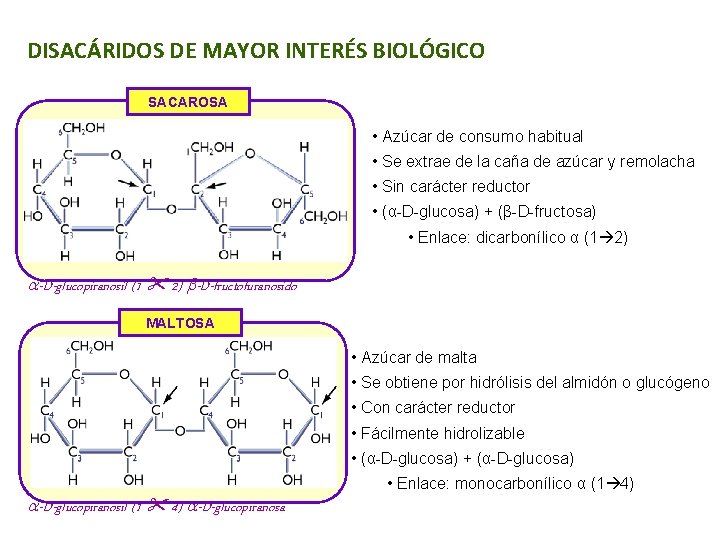
DISACÁRIDOS DE MAYOR INTERÉS BIOLÓGICO SACAROSA • Azúcar de consumo habitual • Se extrae de la caña de azúcar y remolacha • Sin carácter reductor • (α-D-glucosa) + (β-D-fructosa) • Enlace: dicarbonílico α (1 2) a-D-glucopiranosil (1 2) b-D-fructofuranosido MALTOSA • Azúcar de malta • Se obtiene por hidrólisis del almidón o glucógeno • Con carácter reductor • Fácilmente hidrolizable • (α-D-glucosa) + (α-D-glucosa) a-D-glucopiranosil (1 4) a-D-glucopiranosa • Enlace: monocarbonílico α (1 4)
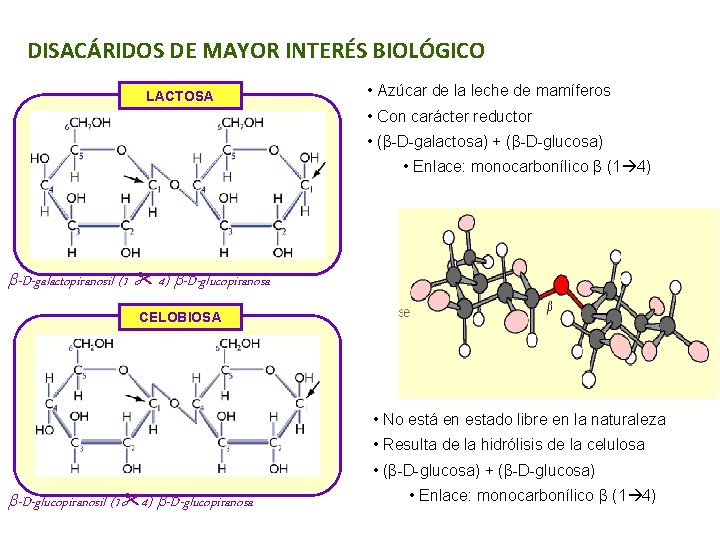
DISACÁRIDOS DE MAYOR INTERÉS BIOLÓGICO LACTOSA • Azúcar de la leche de mamíferos • Con carácter reductor • (β-D-galactosa) + (β-D-glucosa) • Enlace: monocarbonílico β (1 4) b-D-galactopiranosil (1 4) b-D-glucopiranosa CELOBIOSA • No está en estado libre en la naturaleza • Resulta de la hidrólisis de la celulosa • (β-D-glucosa) + (β-D-glucosa) b-D-glucopiranosil (1 4) b-D-glucopiranosa • Enlace: monocarbonílico β (1 4)
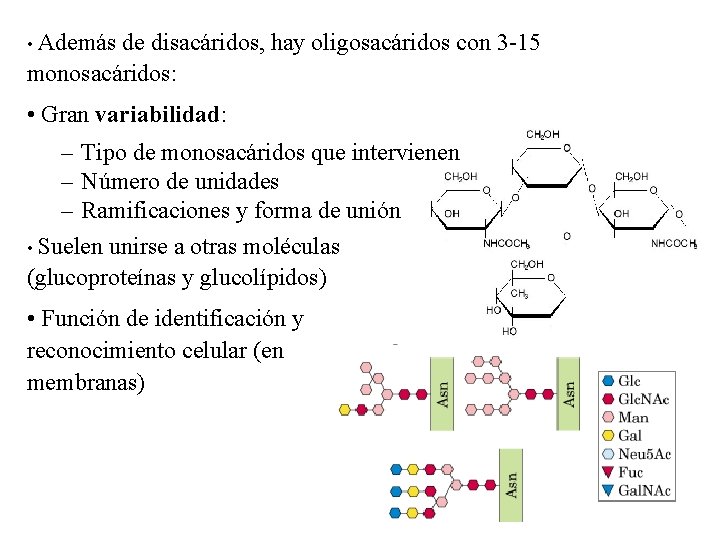
• Además de disacáridos, hay oligosacáridos con 3 -15 monosacáridos: • Gran variabilidad: – Tipo de monosacáridos que intervienen – Número de unidades – Ramificaciones y forma de unión • Suelen unirse a otras moléculas (glucoproteínas y glucolípidos) • Función de identificación y reconocimiento celular (en membranas)
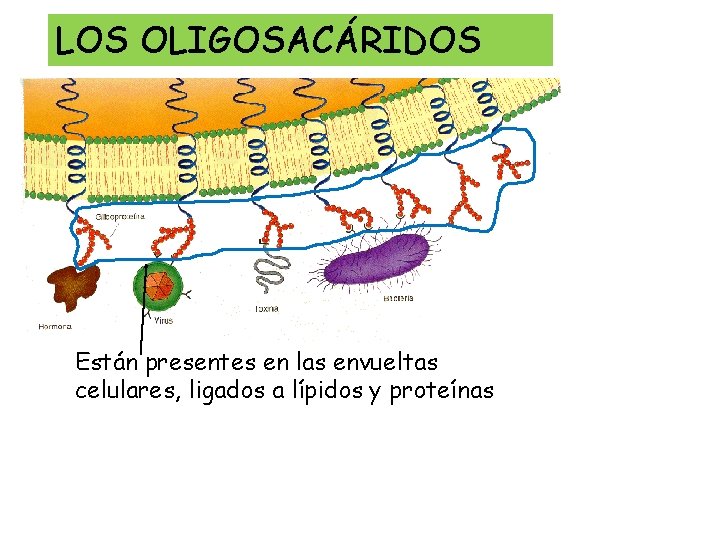
LOS OLIGOSACÁRIDOS Están presentes en las envueltas celulares, ligados a lípidos y proteínas

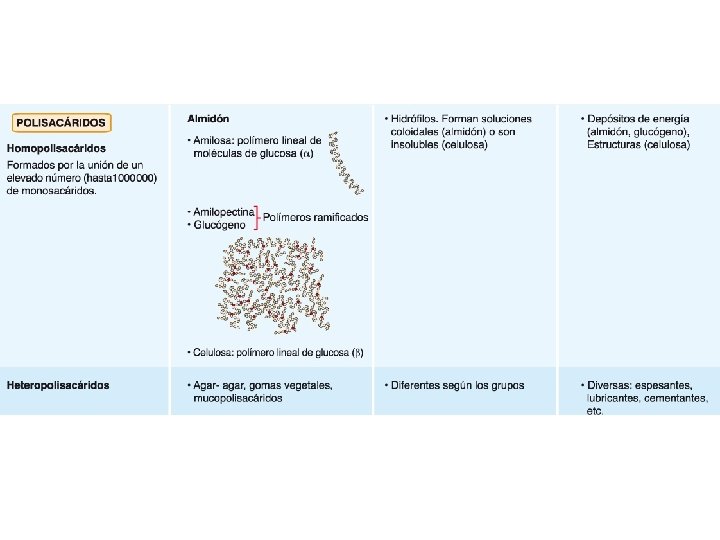
LOS POLISACÁRIDOS Unión de muchos monosacáridos mediante enlace o-glucosídico. Peso molecular muy elevado. No son dulces, ni tienen poder reductor. Son insolubles o forman dispersiones coloidales Su función depende del tipo de enlace: - Enlace α Débil - Enlace β Resistente Función de Reserva (almidón o glucógeno). Función Estructural (celulosa).
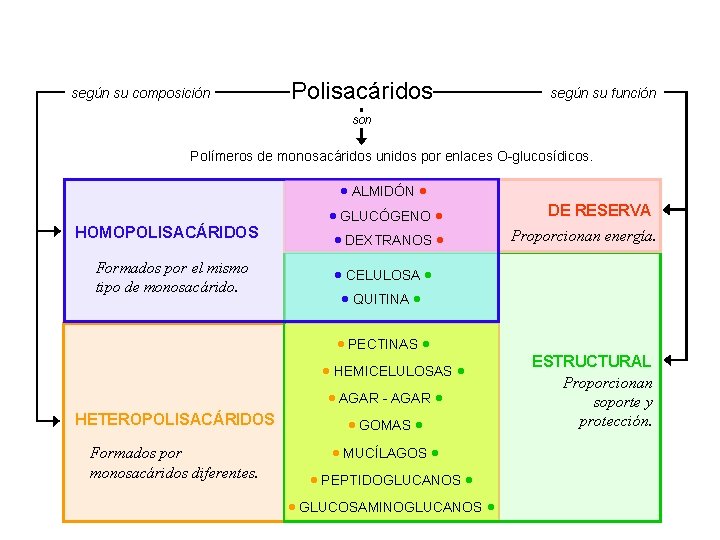
según su composición Polisacáridos según su función son Polímeros de monosacáridos unidos por enlaces O-glucosídicos. ALMIDÓN HOMOPOLISACÁRIDOS Formados por el mismo tipo de monosacárido. GLUCÓGENO DEXTRANOS DE RESERVA Proporcionan energía. CELULOSA QUITINA PECTINAS HEMICELULOSAS AGAR - AGAR HETEROPOLISACÁRIDOS GOMAS Formados por monosacáridos diferentes. MUCÍLAGOS PEPTIDOGLUCANOS GLUCOSAMINOGLUCANOS ESTRUCTURAL Proporcionan soporte y protección.
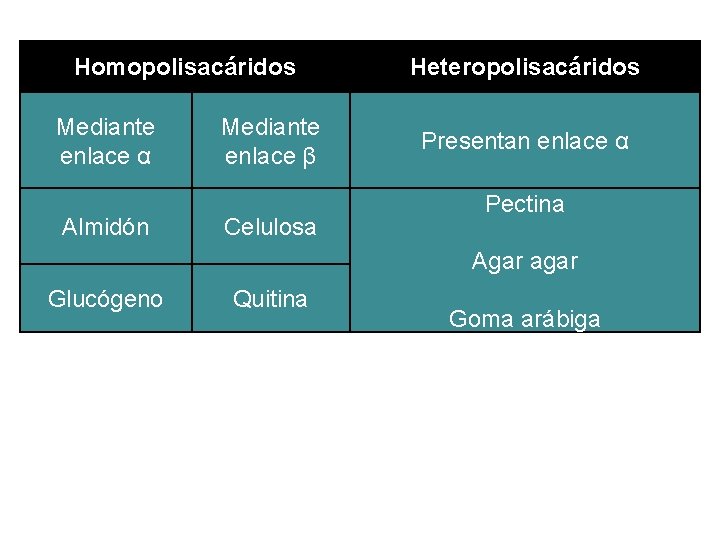
Homopolisacáridos Mediante enlace α Almidón Mediante enlace β Celulosa Heteropolisacáridos Presentan enlace α Pectina Agar agar Glucógeno Quitina Goma arábiga
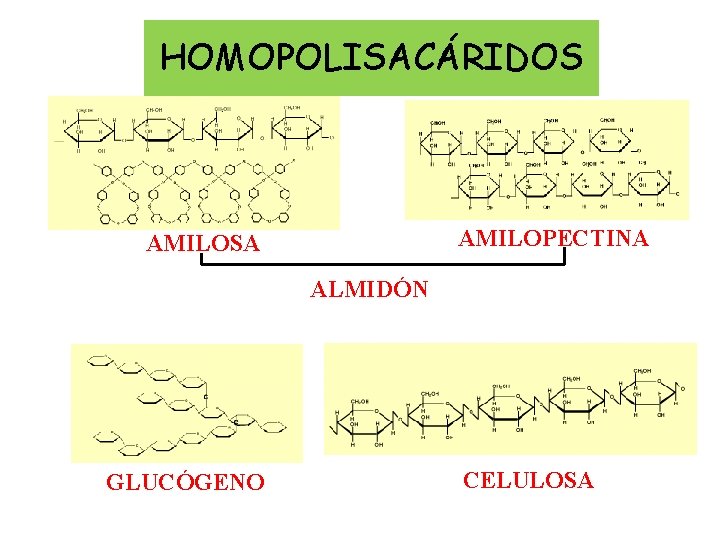
HOMOPOLISACÁRIDOS AMILOPECTINA AMILOSA ALMIDÓN GLUCÓGENO CELULOSA
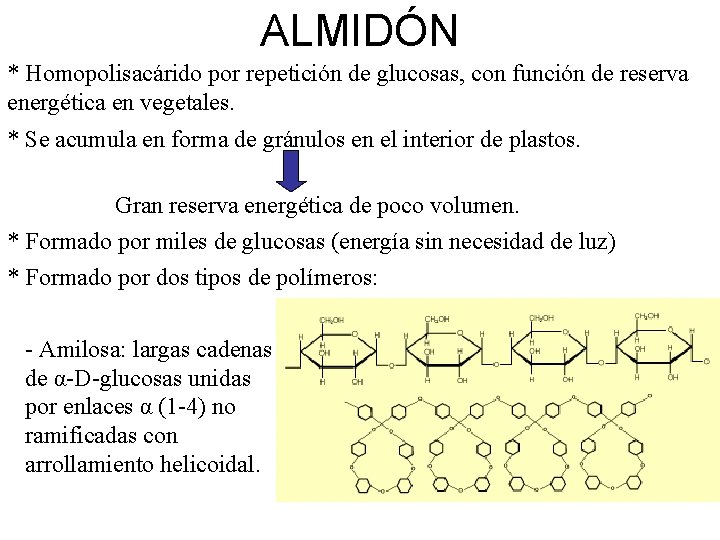
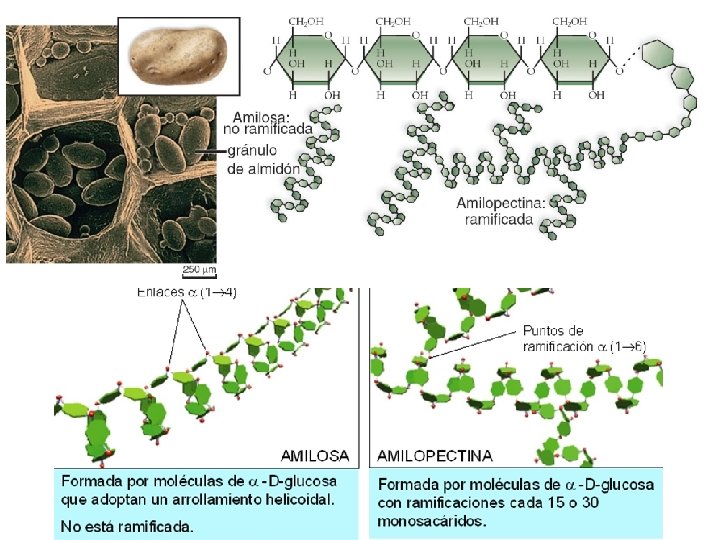
ALMIDÓN * Homopolisacárido por repetición de glucosas, con función de reserva energética en vegetales. * Se acumula en forma de gránulos en el interior de plastos. Gran reserva energética de poco volumen. * Formado por miles de glucosas (energía sin necesidad de luz) * Formado por dos tipos de polímeros: - Amilosa: largas cadenas de α-D-glucosas unidas por enlaces α (1 -4) no ramificadas con arrollamiento helicoidal.
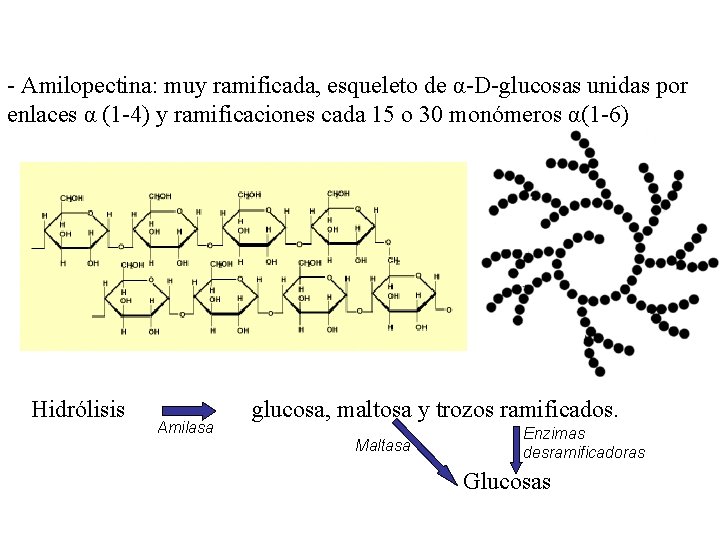
- Amilopectina: muy ramificada, esqueleto de α-D-glucosas unidas por enlaces α (1 -4) y ramificaciones cada 15 o 30 monómeros α(1 -6) Hidrólisis Amilasa glucosa, maltosa y trozos ramificados. Maltasa Enzimas desramificadoras Glucosas
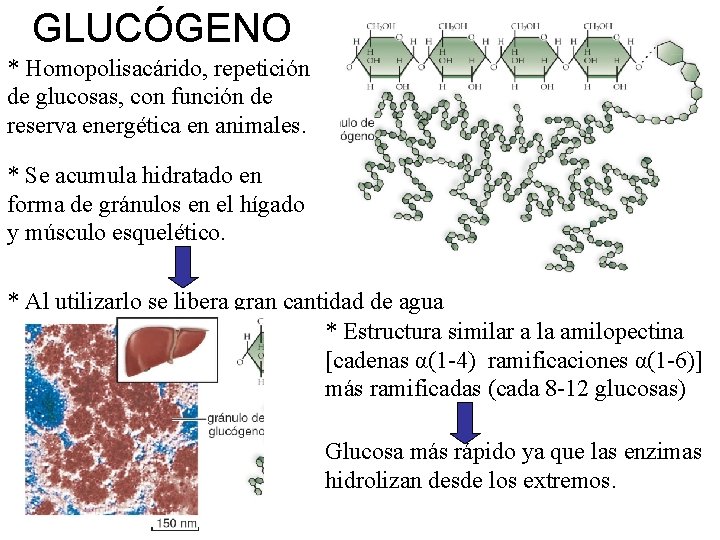
GLUCÓGENO * Homopolisacárido, repetición de glucosas, con función de reserva energética en animales. * Se acumula hidratado en forma de gránulos en el hígado y músculo esquelético. * Al utilizarlo se libera gran cantidad de agua * Estructura similar a la amilopectina [cadenas α(1 -4) ramificaciones α(1 -6)] más ramificadas (cada 8 -12 glucosas) Glucosa más rápido ya que las enzimas hidrolizan desde los extremos.
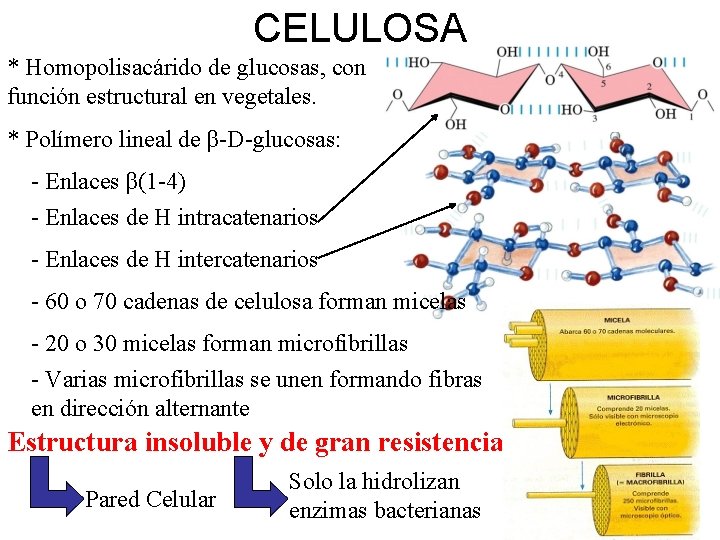
CELULOSA * Homopolisacárido de glucosas, con función estructural en vegetales. * Polímero lineal de β-D-glucosas: - Enlaces β(1 -4) - Enlaces de H intracatenarios - Enlaces de H intercatenarios - 60 o 70 cadenas de celulosa forman micelas - 20 o 30 micelas forman microfibrillas - Varias microfibrillas se unen formando fibras en dirección alternante Estructura insoluble y de gran resistencia Pared Celular Solo la hidrolizan enzimas bacterianas
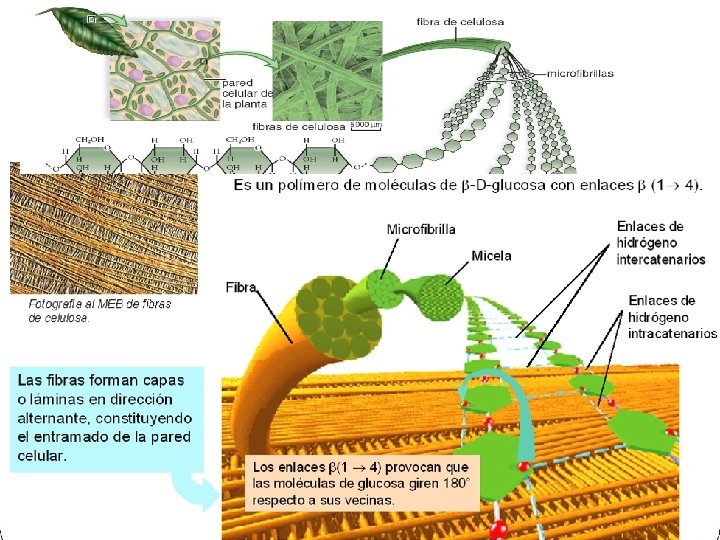

• La peculiaridad del enlace β hace a la celulosa inatacable por las enzimas digestivas humanas; por ello, este polisacárido no tiene interés alimentario para el hombre. • Muchos microorganismos y ciertos invertebrados como el pececillo de plata o el molusco taladrador de la madera son capaces de segregar celulasas. • Los insectos xilófagos, como las termitas, y los herbívoros rumiantes aprovechan la celulosa gracias a los microorganismos simbióticos del tracto digestivo, que producen celulasas. • Los rumiantes, como la oveja, tienen un voluminoso estómago que les sirve como tanque de fermentación; por ello en sus heces no hay restos celulósicos. En los herbívoros no rumiantes, como el caballo, sí hay.
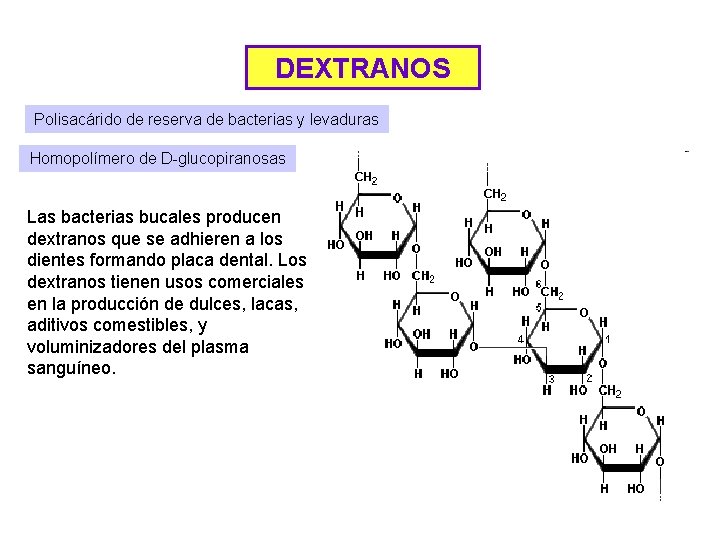
DEXTRANOS Polisacárido de reserva de bacterias y levaduras Homopolímero de D-glucopiranosas Las bacterias bucales producen dextranos que se adhieren a los dientes formando placa dental. Los dextranos tienen usos comerciales en la producción de dulces, lacas, aditivos comestibles, y voluminizadores del plasma sanguíneo.
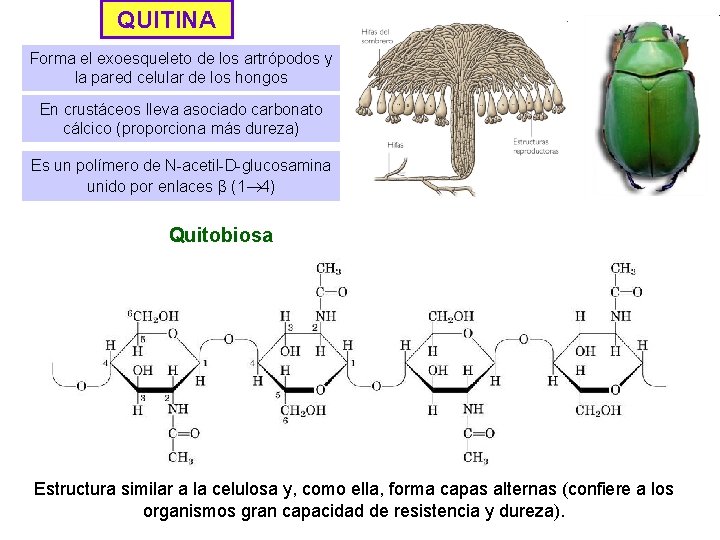
QUITINA Forma el exoesqueleto de los artrópodos y la pared celular de los hongos En crustáceos lleva asociado carbonato cálcico (proporciona más dureza) Es un polímero de N-acetil-D-glucosamina unido por enlaces β (1 4) Quitobiosa Estructura similar a la celulosa y, como ella, forma capas alternas (confiere a los organismos gran capacidad de resistencia y dureza).
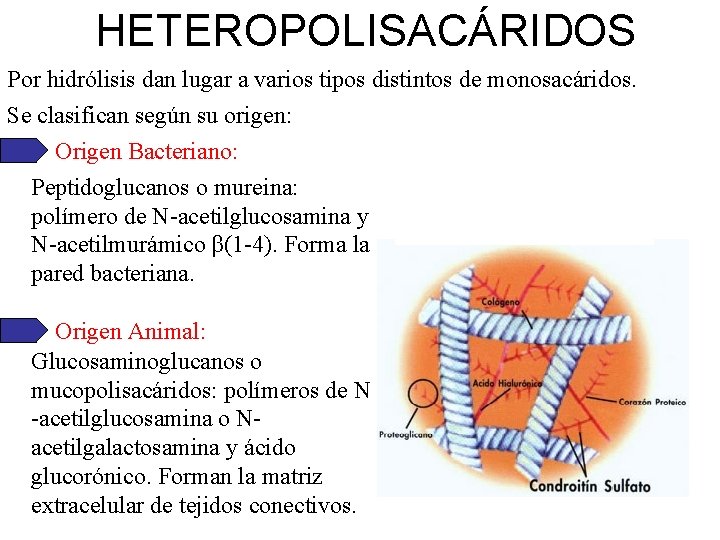
HETEROPOLISACÁRIDOS Por hidrólisis dan lugar a varios tipos distintos de monosacáridos. Se clasifican según su origen: Origen Bacteriano: Peptidoglucanos o mureina: polímero de N-acetilglucosamina y N-acetilmurámico β(1 -4). Forma la pared bacteriana. Origen Animal: Glucosaminoglucanos o mucopolisacáridos: polímeros de N -acetilglucosamina o Nacetilgalactosamina y ácido glucorónico. Forman la matriz extracelular de tejidos conectivos.
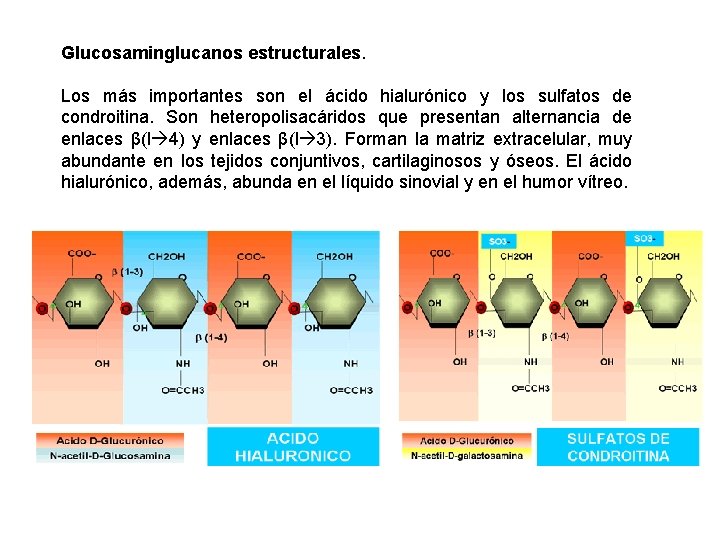
Glucosaminglucanos estructurales. Los más importantes son el ácido hialurónico y los sulfatos de condroitina. Son heteropolisacáridos que presentan alternancia de enlaces β(l 4) y enlaces β(l 3). Forman la matriz extracelular, muy abundante en los tejidos conjuntivos, cartilaginosos y óseos. El ácido hialurónico, además, abunda en el líquido sinovial y en el humor vítreo.
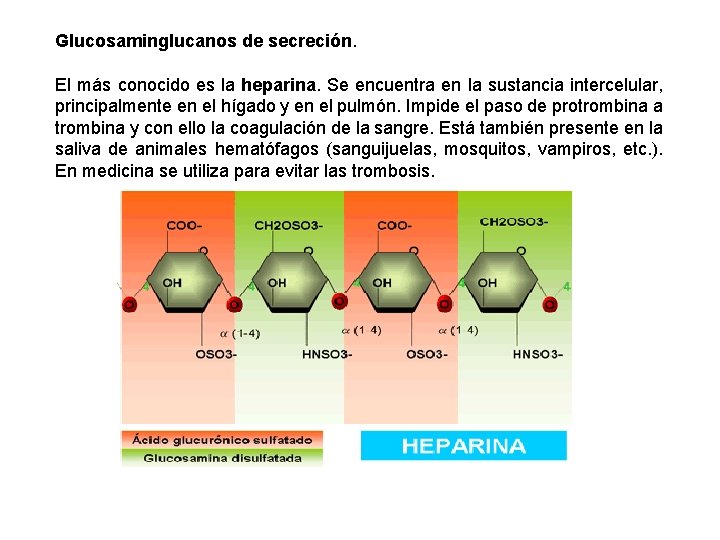
Glucosaminglucanos de secreción. El más conocido es la heparina. Se encuentra en la sustancia intercelular, principalmente en el hígado y en el pulmón. Impide el paso de protrombina a trombina y con ello la coagulación de la sangre. Está también presente en la saliva de animales hematófagos (sanguijuelas, mosquitos, vampiros, etc. ). En medicina se utiliza para evitar las trombosis.
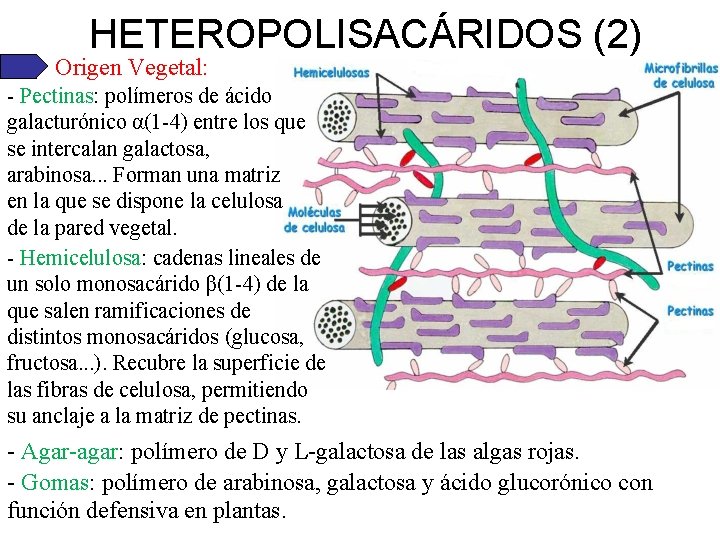
HETEROPOLISACÁRIDOS (2) Origen Vegetal: - Pectinas: polímeros de ácido galacturónico α(1 -4) entre los que se intercalan galactosa, arabinosa. . . Forman una matriz en la que se dispone la celulosa de la pared vegetal. - Hemicelulosa: cadenas lineales de un solo monosacárido β(1 -4) de la que salen ramificaciones de distintos monosacáridos (glucosa, fructosa. . . ). Recubre la superficie de las fibras de celulosa, permitiendo su anclaje a la matriz de pectinas. - Agar-agar: polímero de D y L-galactosa de las algas rojas. - Gomas: polímero de arabinosa, galactosa y ácido glucorónico con función defensiva en plantas.

q AGAR-AGAR: se extrae de algas rojas (Rodofíceas) espesante de líquidos en la industria alimentaria medios de cultivo de microorganismos q GOMAS: función defensiva en plantas goma arábiga tiene interés industrial q MUCÍLAGOS: saciantes en dietas hipocalóricas
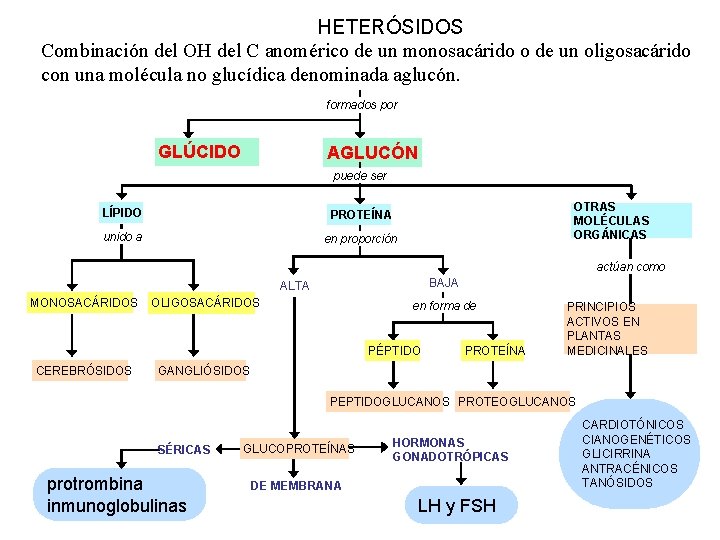
HETERÓSIDOS Combinación del OH del C anomérico de un monosacárido o de un oligosacárido con una molécula no glucídica denominada aglucón. formados por GLÚCIDO AGLUCÓN puede ser LÍPIDO PROTEÍNA unido a en proporción OTRAS MOLÉCULAS ORGÁNICAS actúan como BAJA ALTA MONOSACÁRIDOS OLIGOSACÁRIDOS en forma de PÉPTIDO CEREBRÓSIDOS PROTEÍNA PRINCIPIOS ACTIVOS EN PLANTAS MEDICINALES GANGLIÓSIDOS PEPTIDOGLUCANOS PROTEOGLUCANOS SÉRICAS protrombina inmunoglobulinas GLUCOPROTEÍNAS HORMONAS GONADOTRÓPICAS DE MEMBRANA LH y FSH CARDIOTÓNICOS CIANOGENÉTICOS GLICIRRINA ANTRACÉNICOS TANÓSIDOS

FUNCIONES DE CARBOHIDRATOS Función energética fuente de energía inmediata para la célula C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + energía electrones Función estructural por algunos polisacáridos entre los que destacan: Celulosa Quitina principal componente de exoesqueleto de artrópodos

Otras funciones específicas de determinados glúcidos son: § antibiótico (estreptomicina) § vitamina (vitamina C) § anticoagulante (heparina) § hormonal (hormonas gonadotropas) § enzimática (junto con proteínas forman las ribonucleasas) § inmunológica (las glucoproteínas de la membrana constituyen antígenos y, por otro lado, las inmunoglobulinas o anticuerpos están formadas en parte por glúcidos) § protectora (goma arábiga) § marcadores de membrana, ya que algunos glúcidos (oligosacáridos unidos a lípidos y proteínas de membrana) sirven de seña de identidad celular, actuando de marcadores de membrana, receptores de señales, etc.
- Slides: 68