Gio vin Nguyn Th Bnh Nm hc 2020

Giáo viên: Nguyễn Thị Bình Năm học: 2020 – 2021

Kiểm tra bài cũ 1/ Thế nào là dung dịch? Dung môi? Chất tan? - Dung dịch là hỗn hợp đồng nhất của dung môi và chất tan. - Dung môi là chất có khả năng hòa tan chất khác để tạo thành dung dịch. Chất tan là chất bị hòa tan trong dung môi. 2/ Thế nào là độ tan của một chất trong nước? Độ tan của một chất trong nước là số gam chất đó hòa tan trong 100 g nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định

Bài 42: NỒNG ĐỘ DUNG DỊCH v Nội dung bài học: I. Nồng độ phần trăm của dung dịch II. Nồng độ mol của dung dịch

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa 2. Công thức 3. Bài tập áp dụng
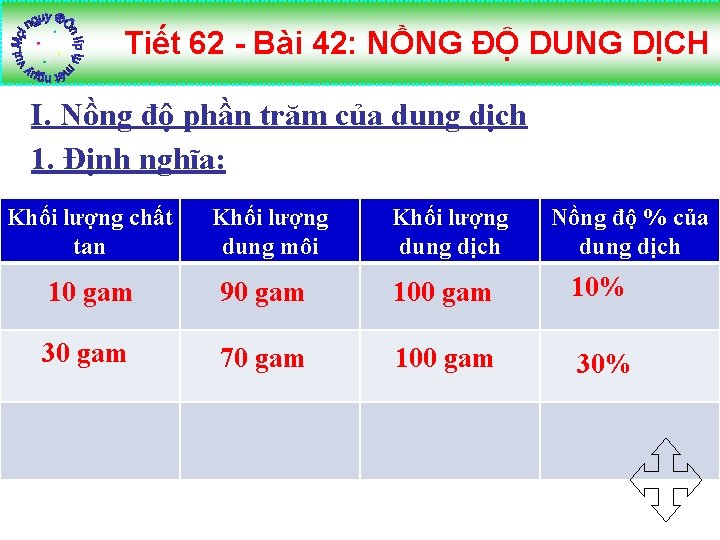
Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa: Khối lượng chất tan Khối lượng dung môi Khối lượng dung dịch Nồng độ % của dung dịch 10 gam 90 gam 10% 30 gam 70 gam 100 gam 30%
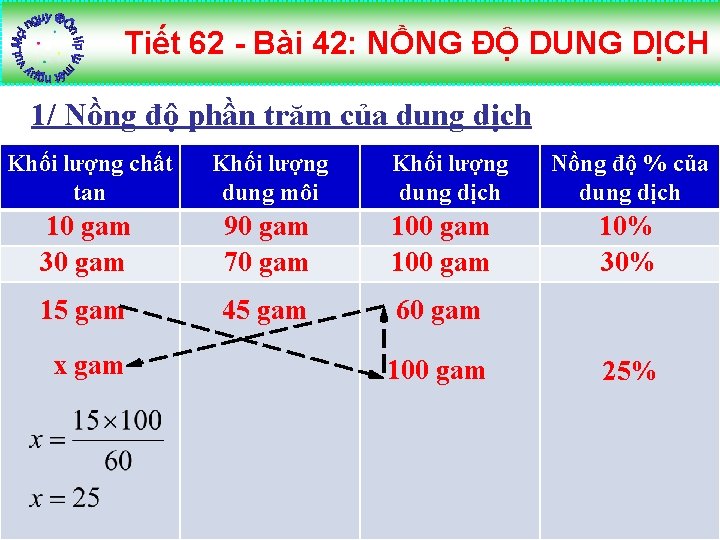
Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH 1/ Nồng độ phần trăm của dung dịch Khối lượng chất tan Khối lượng dung môi 10 gam 30 gam 90 gam 70 gam 100 gam 15 gam 45 gam 60 gam x gam Khối lượng dung dịch 100 gam Nồng độ % của dung dịch 10% 30% 25%

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa: Nồng độ phần trăm (C%) của một dung dịch cho ta biết số gam chất tan có trong 100 g dung dịch VD: Dung dịch axit HCl có nồng độ 96% cho ta biết trong ……. . g dung dịch có ……. g axit HCl 2. Công thức:

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa 2. Công thức - C%: Nồng độ phần trăm của dung dịch ( %) (1) - mdd: khối lượng dung dịch (g) - mct : khối lượng chất tan (g) (2) - mdm: khối lượng dung môi (g) Từ (1) suy ra: (3) (4)

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa 2. Công thức 3. Bài tập BT 1: Hòa tan 15 g Na. Cl vào 45 g nước. Tính nồng độ phần trăm của dung dịch Tóm tắt: mct=15 g mdm=45 g mdd=? C%=? Giải: Khối lượng dung dịch Na. Cl là: mdd= mct+mdm= 15+45=60(g) Nồng độ phần trăm của dung dịch Na. Cl là: = 25%

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa 2. Công thức 3. Bài tập BT 2: Một dung dịch H 2 SO 4 có nồng độ 14%. Tính khối lượng H 2 SO 4 có trong 150 g dung dịch. Tóm tắt: C% =14% mdd =150 g mct=? Giải: Khối lượng chất tan H 2 SO 4 là:

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH I. Nồng độ phần trăm của dung dịch 1. Định nghĩa 2. Công thức 3. Bài tập 0’ 55 0’ 45 1’ 55 1’ 00 0’ 35 0’ 10 1’ 25 1’ 30 1’ 35 1’ 10 0’ 25 0’ 05 1’ 40 1’ 50 2’ 00 1’ 15 1’ 20 1’ 05 0’ 50 0’ 30 0’ 40 0’ 15 0’ 20 0’ 00 Tóm tắt: mct =50 g C% =25% a) mdd=? b) mdm=? Giải: Khối lượng dung dịch đường là: BT 3: Hòa tan 50 g đường vào nước, được dung dịch đường có nồng độ Khối lượng nước cần dùng là: 25%. Hãy tính: a/ Khối lượng dung dịch đường pha chế được b/ Khối lượng nước cần dùng cho sự pha chế

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH Củng cố: v Tính C% của 200 g dung dịch chứa 10 g Ba. Cl 2 A. 10% B. 5% C. 15% D. 20% Giải:

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH Củng cố: v Tính số gam muối ăn của 50 g dung dịch muối ăn 4% A. 5(g) B. 2(g) C. 4(g) D. 7(g) Giải:

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH Phân biệt giữa độ tan và nồng độ phần trăm của dung dịch I. Độ tan: 1. Kí hiệu: S 2. Định nghĩa: Là số gam chất tan hòa tan trong 100 g nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định II. Nồng độ phần trăm 1. Kí hiệu: C% 2. Định nghĩa: Là số gam chất tan có trong 100 g dung dịch (không phụ thuộc vào nhiệt độ)
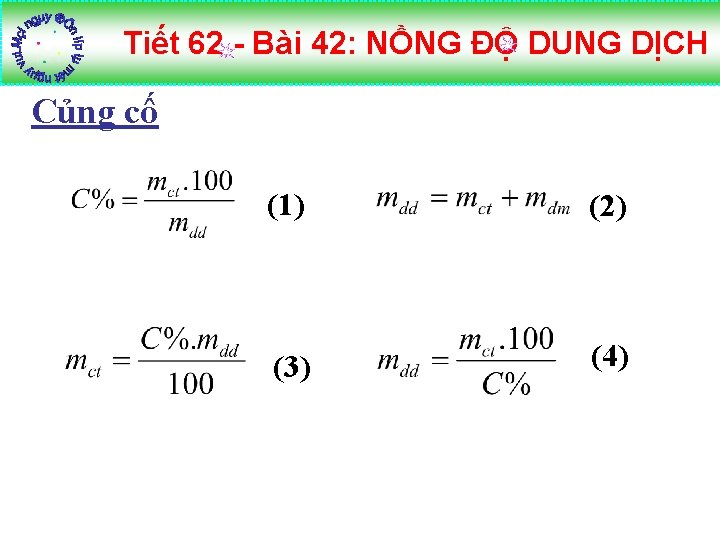
Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH Củng cố (1) (2) (3) (4)
Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH Nước oxi già (Hidro peoxit) ở nồng độ thấp (3%) được sử dụng trong y học để sát trùng vết thương, với nồng độ cao hơn nó có thể làm cháy da khi tiếp xúc, với nồng độ đậm đặc (35%) sẽ gây tử vong nếu uống phải. Ngay cả nước oxi già có nồng độ thấp mua từ các hiệu thuốc ta cũng không được uống vì chúng có chứa các hóa chất có tính độc hại

Tiết 62 - Bài 42: NỒNG ĐỘ DUNG DỊCH Hướng dẫn về nhà: - Học bài trong vở kết hợp SGK - Làm bài tập 1; 5; 6 b (SGK) - Chuẩn bị phần II. Nồng độ mol của dung dịch

- Slides: 18