Gii thiu UBND TNH IN BIN S GIO

Giới thiệu UBND TỈNH ĐIỆN BIÊN SỞ GIÁO DỤC VÀ ĐÀO TẠO Cuộc thi: Thiết kế bài giảng điện tử E - learning --------Bài giảng: Tiết 6, 7 : PHẢN ỨNG TRAO ĐỔI ION TRONG DUNG DỊCH CÁC CHẤT ĐIỆN LI Chương trình Hóa học, lớp 11 ban cơ bản Giáo viên: Phạm Văn Toản phamtoandtnttuachua@gmail. com Điện thoại di động: 01659309908 Trường PTDTNT THPT Tủa Chùa huyện: Tủa Chùa, tỉnh: Điện Biên Tủa Chùa, tháng 01 năm 2015
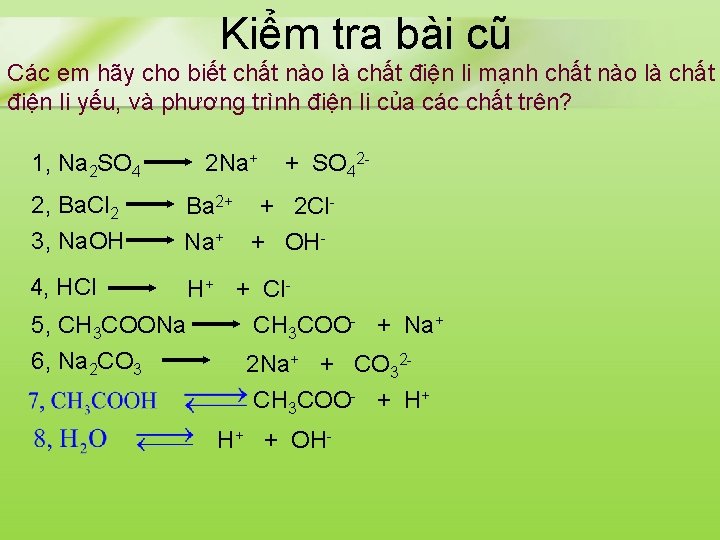
Kiểm tra bài cũ Các em hãy cho biết chất nào là chất điện li mạnh chất nào là chất điện li yếu, và phương trình điện li của các chất trên? 1, Na 2 SO 4 2, Ba. Cl 2 3, Na. OH 2 Na+ + SO 42 - Ba 2+ + 2 Cl. Na+ + OH- 4, HCl H+ + Cl 5, CH 3 COONa CH 3 COO- + Na+ 6, Na 2 CO 3 2 Na+ + CO 32 CH 3 COO- + H+ H+ + OH-

Bài 4 : PHẢN ỨNG TRAO ĐỔI ION TRONG DUNG DỊCH CÁC CHẤT ĐIỆN LI Nội dungchính của bài I. ĐIÊ U KIÊ N XA Y RA PHA N Ư NG TRAO ĐÔ I ION TRONG DUNG DI CH CA C CH T ĐIÊ N LI 1, Phản ứng tạo thành chất kết tủa 2, Phản ứng tạo thành chất điện li yếu 3, Phản ứng tạo thành chất khí II. KÊ T LU N ĐIÊ U KIÊ N XA Y RA PHA N Ư NG TRONG DUNG DI CH CA C CH T ĐIÊ N LI

I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 1, phảnứng tạo thànhchất kết tủa 1. Phản ứng tạo thành chất kết tủa Thí nghiệm : Cho 2 dung dịch Na 2 SO 4 và Ba. Cl 2 phản ứng với nhau Các em hãy quan sát cho biết hiện tượng, giải thích?
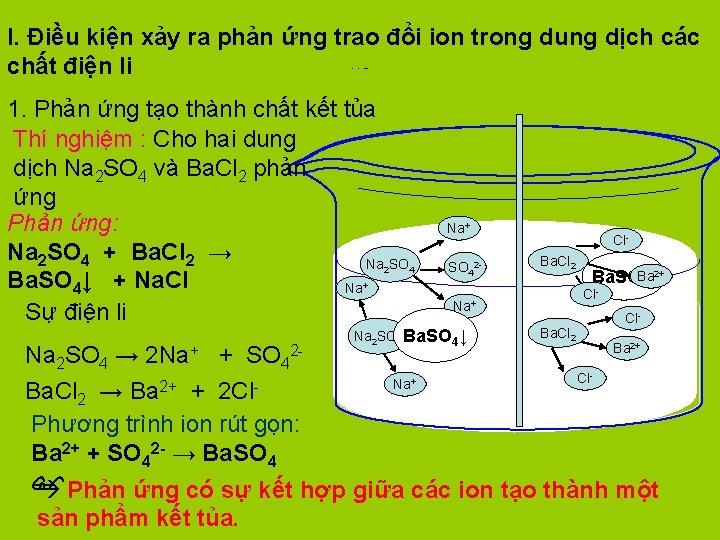
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li Giải thích thí nghiệm tạo kết tủa Ba. SO 4 1. Phản ứng tạo thành chất kết tủa Thí nghiệm : Cho hai dung dịch Na 2 SO 4 và Ba. Cl 2 phản ứng Phản ứng: Na 2 SO 4 + Ba. Cl 2 → Na SO Ba. SO 4↓ + Na. Cl Na Sư điê n li 2 Na+ 4 SO 42 - Cl. Ba. Cl 2 + Cl- Na+ Na 2 SO 4 Ba. SO SO 44↓ 2 - 2+ Ba. SOBa 4↓ Cl- Ba. Cl 2 Ba Na 2 SO 4 → 2 Na+ + SO 42 Cl Na 2+ Ba. Cl 2 → Ba + 2 Cl Phương trình ion rút gọn: Ba 2+ + SO 42 - → Ba. SO 4 Phản ứng có sự kết hợp giữa các ion tạo thành một + sản phẩm kết tủa. 2+ -
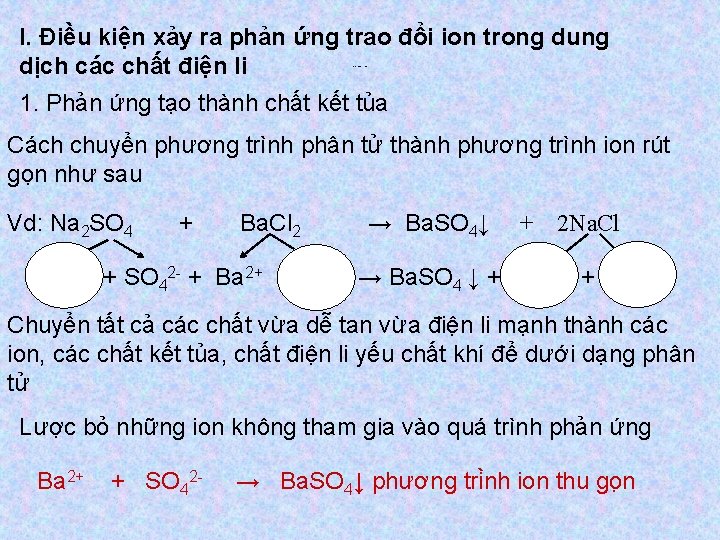
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li Cách viết phươngtrình ion thu gọn 1. Phản ứng tạo thành chất kết tủa Cách chuyển phương trình phân tử thành phương trình ion rút gọn như sau Vd: Na 2 SO 4 + Ba. Cl 2 → Ba. SO 4↓ + 2 Na. Cl 2 Na+ + SO 42 - + Ba 2+ + 2 Cl- → Ba. SO 4 ↓ + 2 Na+ + 2 Cl. Chuyển tất cả các chất vừa dễ tan vừa điện li mạnh thành các ion, các chất kết tủa, chất điện li yếu chất khí để dưới dạng phân tử Lược bỏ những ion không tham gia vào quá trình phản ứng Ba 2+ + SO 42 - → Ba. SO 4↓ phương tri nh ion thu go n
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 2. Phản ứng tạo thành chất điện li yếu a. Phản ứng tạo thành nước Thí nghiệm: Cho dd HCl tác dụng với dd Na. OH có pha sẵn phenolphtalein 2, phảnứng tạo thànhchất điện li yếu là nước
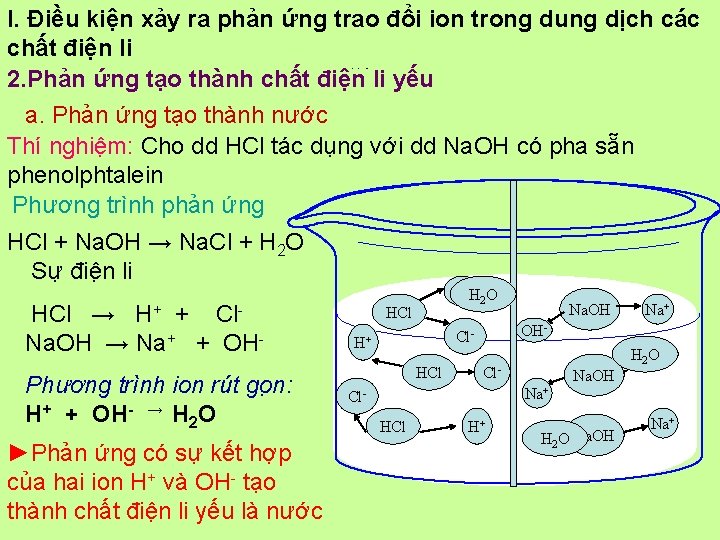
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 2. Phản ứng tạo thành chất điện li yếu a. Phản ứng tạo thành nước Thí nghiệm: Cho dd HCl tác dụng với dd Na. OH có pha sẵn phenolphtalein Phương trình phản ứng Giải thích thí nghiệm tạo thànhnước HCl + Na. OH → Na. Cl + H 2 O Sư điê n li HCl → H+ + Cl. Na. OH → Na+ + OHPhương trình ion rút go n: H+ + OH- → H 2 O ►Phản ứng có sự kết hợp của hai ion H+ và OH- tạo thành chất điện li yếu là nước H+H 2 O HCl Na+ OH- Cl- H+ Na. OH H 2 OH O - Cl- Na. OH Na+ Cl. HCl H+ H-2 O OH Na+

I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 2. Phản ứng tạo thành chất điện li yếu b, Phản ứng tạo thành axit yếu Thí nghiệm: Nhỏ dd HCl vào ống nghiệm đựng dd CH 3 COONa Phản ứng tạo thànhaxit yếu Hiện tượng: Thấy có mùi giấm chua Giải thích: Có mùi giấm chua chính tỏ axit CH 3 COOH là chất điện li yếu được tạo thành từ phản ứng HCl + CH 3 COONa → CH 3 COOH + Na. Cl : ptpt H+ + Cl- + CH 3 COO- + Na+ → CH 3 COOH + Na+ + Cl: pt ion đầy đủ H+ + CH 3 COO- → CH 3 COOH : pt ion thu go n
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 3, Phản ứng tạo thành chất khí Thí nghiệm: Cho dd HCl phản ứng với dd Na 2 CO 3 3. Phảnứng tạo thànhchất khí
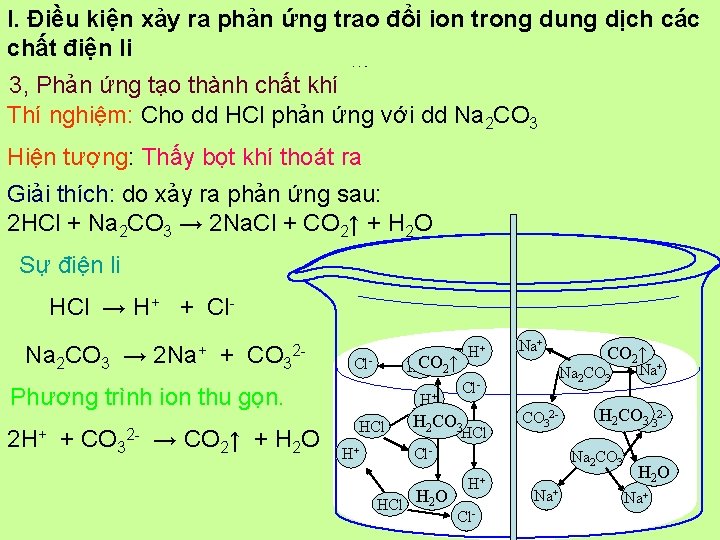
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li Giải thích thí nghiệm tạo khí CO 2 3, Phản ứng tạo thành chất khí Thí nghiệm: Cho dd HCl phản ứng với dd Na 2 CO 3 Hiện tượng: Thấy bọt khí thoát ra Giải thích: do xảy ra phản ứng sau: 2 HCl + Na 2 CO 3 → 2 Na. Cl + CO 2↑ + H 2 O Sự điện li HCl → H+ + Cl. Na 2 CO 3 → 2 Na+ + CO 3 2 - CO 2↑ HCl Cl- Phương trình ion thu gọn. 2 H+ + CO 32 - → CO 2↑ + H 2 O H+ H+ HCl H+ Na 2 CO 3 Cl- H 2 CO 3 HCl CO 32 - Cl. HCl H 2 O CO 2↑ 2 H 2 CO CO 33 Na 2 CO 3 H+ Cl- Na+ H 2 O Na+
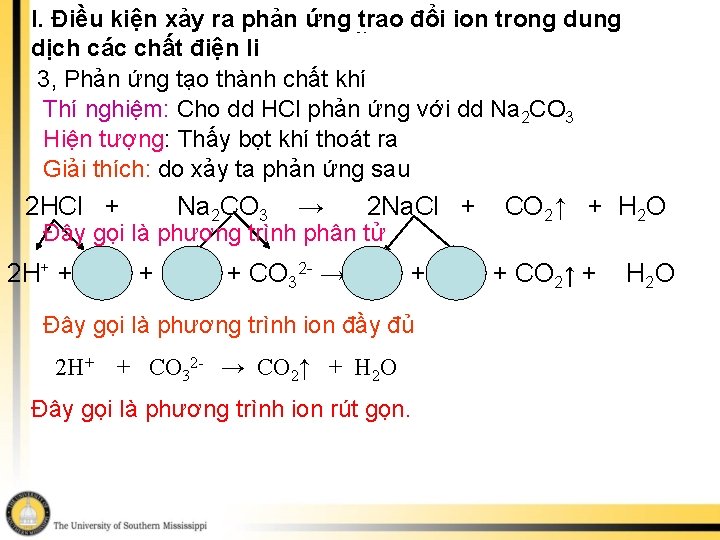
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 3, Phản ứng tạo thành chất khí Thí nghiệm: Cho dd HCl phản ứng với dd Na 2 CO 3 Hiện tượng: Thấy bọt khí thoát ra Giải thích: do xảy ta phản ứng sau Viết phươngtrình ion thu gọn 2 HCl + Na 2 CO 3 → 2 Na. Cl + Đây gọi là phương trình phân tử CO 2↑ + H 2 O 2 H+ + 2 Cl- + 2 Na+ + CO 32 - → 2 Na+ + 2 Cl- + CO 2↑ + Đây gọi là phương trình ion đầy đủ 2 H+ + CO 32 - → CO 2↑ + H 2 O Đây gọi là phương trình ion rút gọn. H 2 O

I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 3, Phản ứng tạo thành chất khí Em hãy quan sát thí nghiệm sau Phản ứng tạo chất khí

I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li 3, Phản ứng tạo thành chất khí. Các em hãy hoàn thành yêu cầu sau Viết phươngtrình ion của phảnứng Thí nghiệm: Cho đá vôi( Ca. CO 3) phản ứng với dd HCl thấy có hiện tượng gì. Hãy viết phương trình phân tử và phương trình ion đầy đủ, phương trình ion thu gọn của phản ứng trên? Sau khi làm xong các em hãy kiểm tra lại kết quả Hiện tượng: có khí CO 2 thoát ra Phương trình phân tử Ca. CO 3 + 2 HCl → Ca. Cl 2 + CO 2↑ + H 2 O Phương trình ion đầy đủ Ca. CO 3 + 2 H+ + 2 Cl- → Ca 2+ + 2 Cl- + CO 2 ↑ + H 2 O Phương trình ion thu gọn Ca. CO 3 + 2 H+ → Ca 2+ + CO 2↑ + H 2 O

II. KÊ T LU N II. Kết luận 1. Phản ứng trao đổi ion trong dung dịch các chất điện li là phản ứng giữa các ion 2. Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp với nhau tạo thành ít nhất một trong các điều kiện sau - Chất kết tủa Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch các chất điện li - Chất điện li yếu - Chất khí
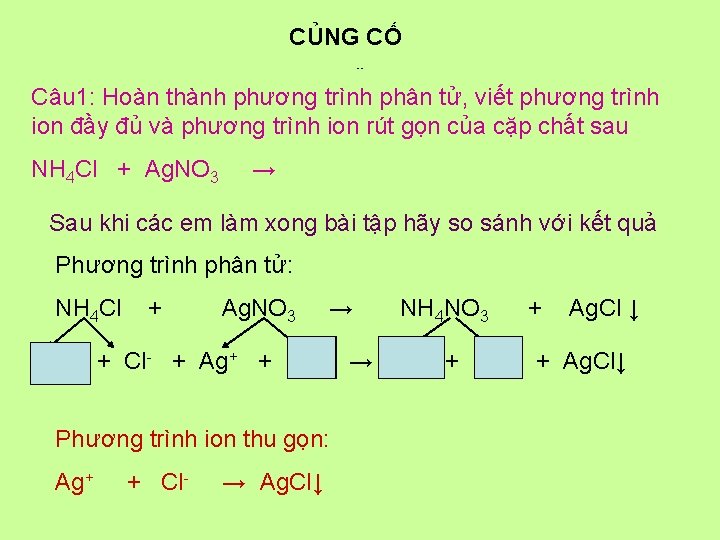
CỦNG CỐ Củng cố, Câu 1: Hoàn thành phương trình phân tử, viết phương trình ion đầy đủ và phương trình ion rút gọn của cặp chất sau NH 4 Cl + Ag. NO 3 → Sau khi các em làm xong bài tập hãy so sánh với kết quả Phương trình phân tử: NH 4 Cl + Ag. NO 3 → NH 4 NO 3 + Ag. Cl ↓ NH 4+ + Cl- + Ag+ + NO 3 - → NH 4+ + NO 3 - + Ag. Cl↓ Phương trình ion thu gọn: Ag+ + Cl- → Ag. Cl↓

Câu 2 : Phản ứng nào sau đây xảy ra trong dung dịch tạo được kết tủa Fe(OH)3 A) Fe(NO 3)3 + KOH B) Fe 2(SO 4)3 + KI C) Fe(NO 3)3 + Fe D) Fe. SO 4 + KMn. O 4 + H 2 SO 4 Đu ng rô i - Em đa hiê u đươ c kiê n thư c trong Câu ba tra i lơ i cu a em la : Sai rô i - Em ha y xem la i kiê n thư c trong ba i Em chưa hoa n tha nh câu tra lơ i cho Em đa tra lơ i đu ng! Câu Em tra lơ i đu ncg câu la : ho nih câu tra lơ i pha ica hoa n tha trươ c khi tiê p tu c Tra lơ i i Xo aa Xo

Câu 3: Những ion nào sau đây không thể tồn tại trong cùng một dung dịch? A) Na+, SO 42 -, Cu 2+, Cl. B) Ba 2+, K+, NO 3 -, SO 42 C) Mg 2+, Ca 2+, NO 3 -, Cl. D) Al 3+, Na+, SO 42 -, ClĐu ng rô i - Em đa hiê u đươ c kiê n thư c trong Câuba tra i lơ i cu a em la : Sai rô i - Em ha y xem la i kiê n thư c trong ba i Em chưa hoa n tha nh câu tra lơ i cho Em đa tra lơ i đu ng! Câu Em tra lơ i đu ncg câu la : ho nih câu tra lơ i pha ica hoa n tha trươ c khi tiê p tu c Tra lơ i i Xo aa Xo

Câu 4: Phương trình ion rút gọn của phản ứng cho biết? A) Những ion nào tồn tại trong dung dịch B) Nồng độ ion nào trong dung dịch lớn nhất Không tồn tại phân tử trong dung dịch các chất C) điện li Bản chất của phản ứng trong dung dịch các chất D) điện li Đu ng rô i - Em đa hiê u đươ c kiê n thư c trong Câu ba tra i lơ i cu a em la : Sai rô i - Em ha y xem la i kiê n thư c trong ba i Em chưa hoa n tha nh câu tra lơ i cho Em đa tra lơ i đu ng! Câu Em tra lơ i đu ncg câu la : ho nih câu tra lơ i pha ica hoa n tha trươ c khi tiê p tu c Tra lơ i i Xo aa Xo

Củng cố Your Score {score} Max Score {max-score} Number of Quiz {total-attempts} Attempts Question Feedback/Review Information Will Appear Here Continue Review Quiz

Tài liệu tham khảo Sách giáo khoa lớp 11 cơ bản Sách giáo viên lớp 11 cơ bản Chẩn kiến thức kĩ năng lớp 11 cơ bản Một số tranh ảnh, hình nền, thí nghiệm trên các trang mạng youtube. com, google

Kết thúc bài giảng XIN CH N TRO NG CA M ƠN QUY TH Y CÔ CU NG CA C EM HO C SINH ĐA CHU Y LĂ NG NGE
- Slides: 22