GFP Ouest SFGP Ouest 2013 Microparticules antibactriennes base

GFP Ouest / SFGP Ouest 2013 Microparticules antibactériennes à base de polysaccharides Jiang CHANGa, Laurent LEBRUNa, Claire HELLIOb, Rozenn TREPOSb, Carole KARAKASYAN-DIAa a: Laboratoire "Polymères, Biopolymères, Surfaces"UMR 6270 - Université de ROUEN / INSA / CNRS b: Ecole de sciences biologiques, Université de Portsmouth 16/05/2013 1

Problématique : • Algue alimentaire • Biomasse • Déchets marins Alges vertes / brunes 2

Tests antibactériens menés sur les ulvanes en solution Rozenn TREPOS, Claire HELLIO - Université de Portsmouth Extrait Test d’inhibition de Croissance de • Bactéries (marines, terrestres) • Microalgues Ulva compressa Ulvane Bilan des tests d’inhibition de croissance des bactéries et microalgues Valeurs des CMI (concentration minimale d’inhibition) en µg/m. L Source Ulvane Bactéries Marines V. a. V. h. U 1 -1 0, 01 U 1 -2 1 U 1 -3 U 1 -5 0, 01 U 1 -7 0, 01 U. clathrata U 2 0, 01 U. compressa U 3 0, 01 U. armoricana V. aestuarianus V. harveyi V. n. H. a. P. e. P. i. S. p. E. c. S. a 0, 01 0, 01 0, 01 0, 1 1 0, 01 0, 1 0, 01 V. P. Bactéries Terrestres 0, 01 V. P. H. a. V. V. natriegens H. aquamarina proteolyticus 0, 01 Microalgues P. r. P. p. 10 0, 01 0, 1 1 0, 01 10 10 0, 1 0, 01 C. c 0, 01 P. e. P. i. S. p. E. c. S. a P. elyakovii P. irgensii S. putrefaciens E. coli S. aureus 0, 01 C. c P. r. P. p. Cylindrothecca Pleurochrysis Porphyridium closterium roscoffensis purpureum 3

Nano, micro-particules d’Ulvanes → Propriétés biocides ? Domaines d’ application : • Peinture « antifouling » • Industrie agroalimentaire (films d’emballage) • Domaine biomédical o formulation de solutions antimicrobiennes o surfaces antimicrobiennes (hydrogels, surfaces métalliques) Intérêts des nano, microparticules : Ø Possibilité de séquestration d’un principe actif Ø Protection du principe actif vis-à-vis du milieu environnemental Ø Contrôle de la libération dans le temps du principe actif 4
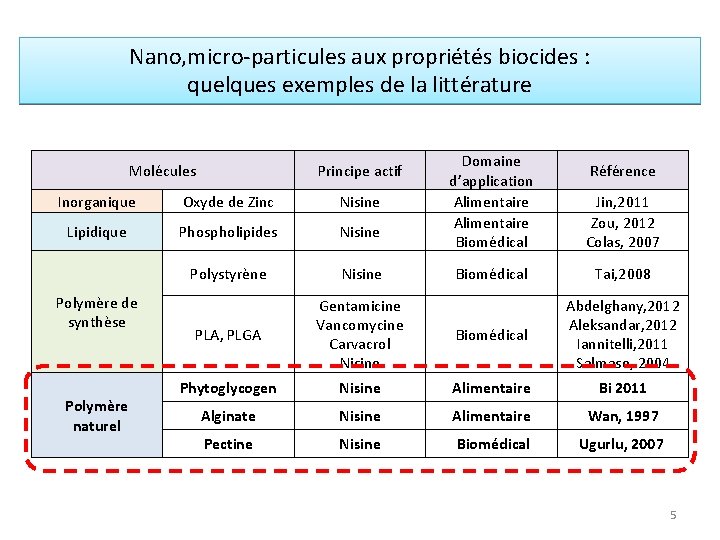
Nano, micro-particules aux propriétés biocides : quelques exemples de la littérature Molécules Principe actif Domaine d’application Alimentaire Biomédical Jin, 2011 Zou, 2012 Colas, 2007 Biomédical Tai, 2008 Référence Inorganique Oxyde de Zinc Nisine Lipidique Phospholipides Nisine Polystyrène Nisine PLA, PLGA Gentamicine Vancomycine Carvacrol Nisine Biomédical Abdelghany, 2012 Aleksandar, 2012 Iannitelli, 2011 Salmaso, 2004 Phytoglycogen Nisine Alimentaire Bi 2011 Alginate Nisine Alimentaire Wan, 1997 Pectine Nisine Biomédical Ugurlu, 2007 Polymère de synthèse Polymère naturel 5
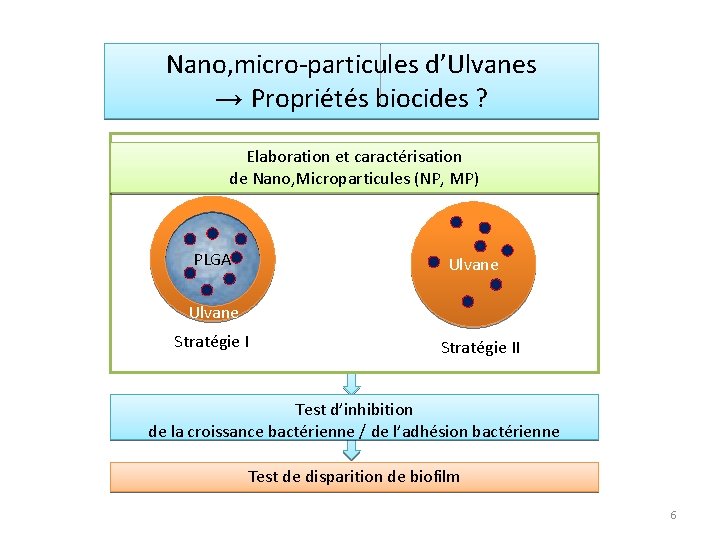
Nano, micro-particules d’Ulvanes → Propriétés biocides ? Elaboration et caractérisation de Nano, Microparticules (NP, MP) PLGA Ulvane Stratégie II Test d’inhibition de la croissance bactérienne / de l’adhésion bactérienne Test de disparition de biofilm 6
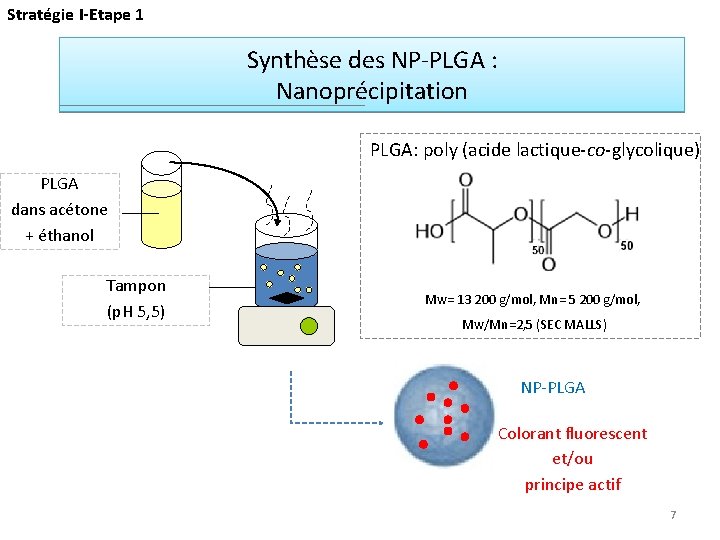
Stratégie I-Etape 1 Synthèse des NP-PLGA : Nanoprécipitation PLGA: poly (acide lactique-co-glycolique) PLGA dans acétone + éthanol Tampon (p. H 5, 5) Mw= 13 200 g/mol, Mn= 5 200 g/mol, Mw/Mn=2, 5 (SEC MALLS) NP-PLGA Colorant fluorescent et/ou principe actif 7
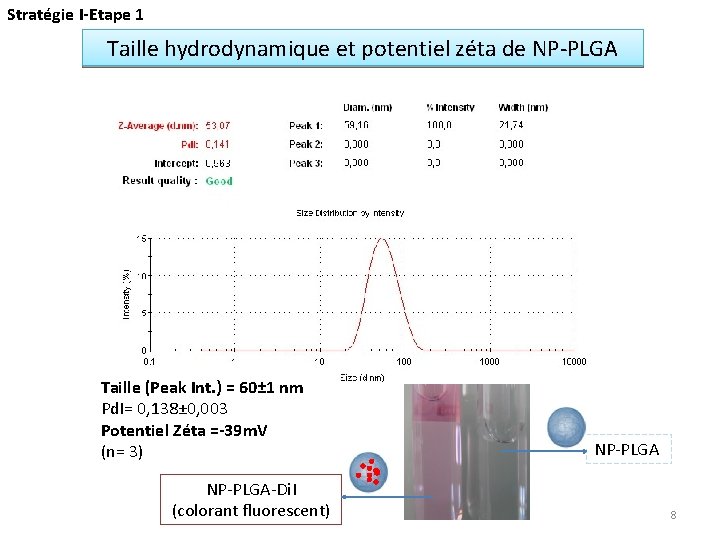
Stratégie I-Etape 1 Taille hydrodynamique et potentiel zéta de NP-PLGA Taille (Peak Int. ) = 60± 1 nm Pd. I= 0, 138± 0, 003 Potentiel Zéta =-39 m. V (n= 3) NP-PLGA-Di. I (colorant fluorescent) NP-PLGA 8

Stratégie I-Etape 1 NP-PLGA sous microscope électronique PLGA 2 µm AFM 300 nm MEB 9
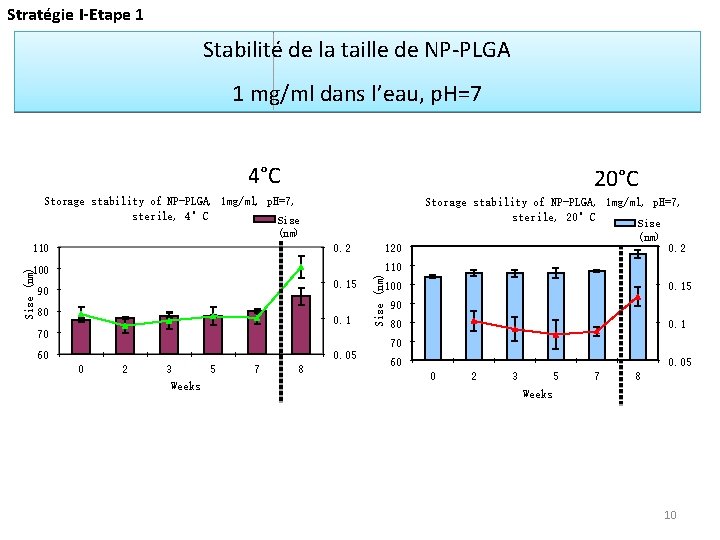
Stratégie I-Etape 1 Stabilité de la taille de NP-PLGA 1 mg/ml dans l’eau, p. H=7 4°C 20°C Storage stability of NP-PLGA, 1 mg/ml, p. H=7, sterile, 4°C Size Storage stability of NP-PLGA, 1 mg/ml, p. H=7, sterile, 20°C Size (nm) 110 0. 2 0. 15 90 80 0. 1 70 Size (nm) 110 100 Size (nm) 120 100 0. 15 90 80 0. 1 70 60 0. 05 0 2 3 5 Weeks 7 8 60 0. 05 0 2 3 5 7 8 Weeks 10
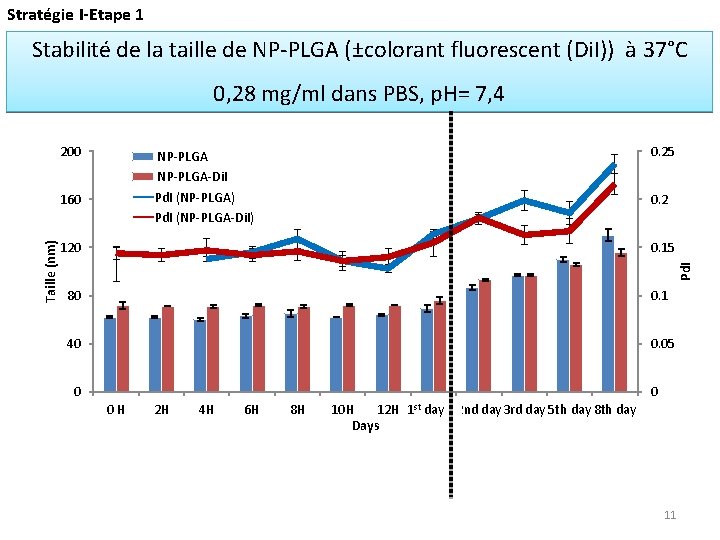
Stratégie I-Etape 1 Stabilité de la taille de NP-PLGA (±colorant fluorescent (Di. I)) à 37°C 0, 28 mg/ml dans PBS, p. H= 7, 4 200 160 0. 2 120 0. 15 80 0. 1 40 0. 05 Pd. I Taille (nm) 0. 25 NP-PLGA-Di. I Pd. I (NP-PLGA) Pd. I (NP-PLGA-Di. I) 0 0 0 H 2 H 4 H 6 H 8 H 10 H 12 H Days st day 5 th day 8 th day 12 nd day 3 rd day 11
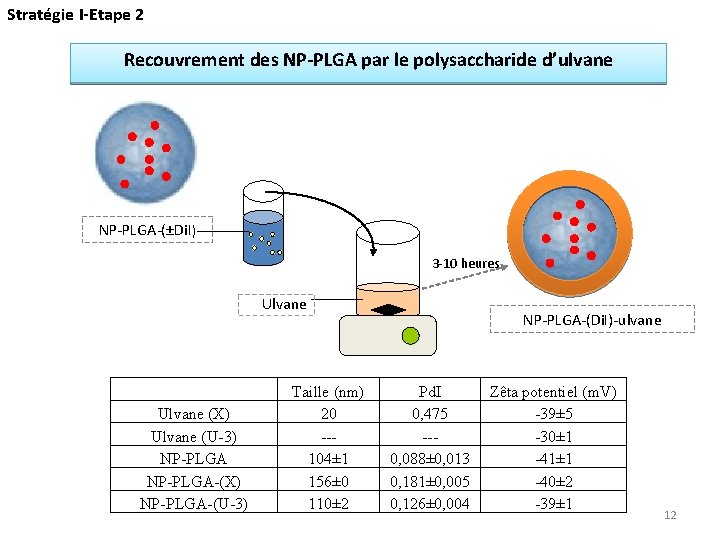
Stratégie I-Etape 2 Recouvrement des NP-PLGA par le polysaccharide d’ulvane NP-PLGA-(±Di. I) 3 -10 heures Ulvane (X) Ulvane (U-3) NP-PLGA-(X) NP-PLGA-(U-3) Taille (nm) 20 --104± 1 156± 0 110± 2 NP-PLGA-(Di. I)-ulvane Pd. I 0, 475 --0, 088± 0, 013 0, 181± 0, 005 0, 126± 0, 004 Zêta potentiel (m. V) -39± 5 -30± 1 -41± 1 -40± 2 -39± 1 12
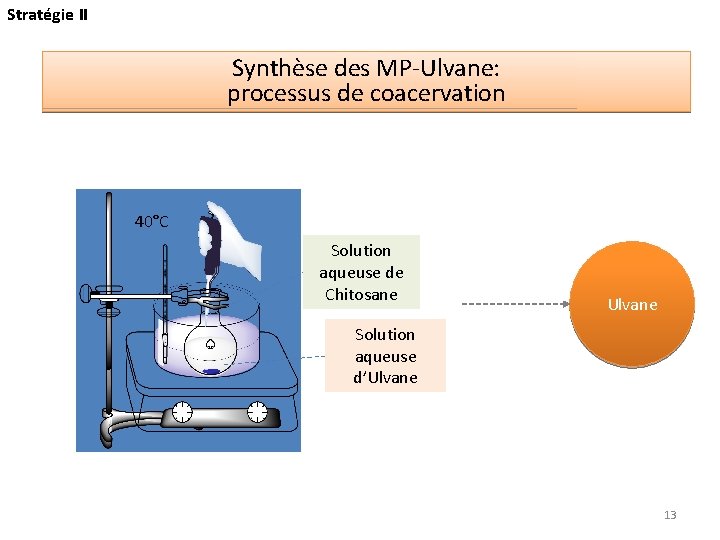
Stratégie II Synthèse des MP-Ulvane: processus de coacervation 40°C Solution aqueuse de Chitosane Ulvane Solution aqueuse d’Ulvane 13
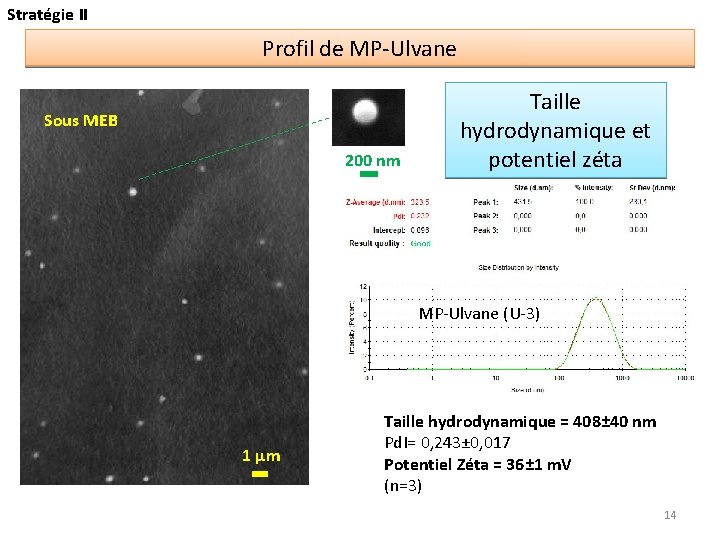
Stratégie II Profil de MP-Ulvane Sous MEB 200 nm Taille hydrodynamique et potentiel zéta MP-Ulvane (U-3) 1 µm Taille hydrodynamique = 408± 40 nm Pd. I= 0, 243± 0, 017 Potentiel Zéta = 36± 1 m. V (n=3) 14
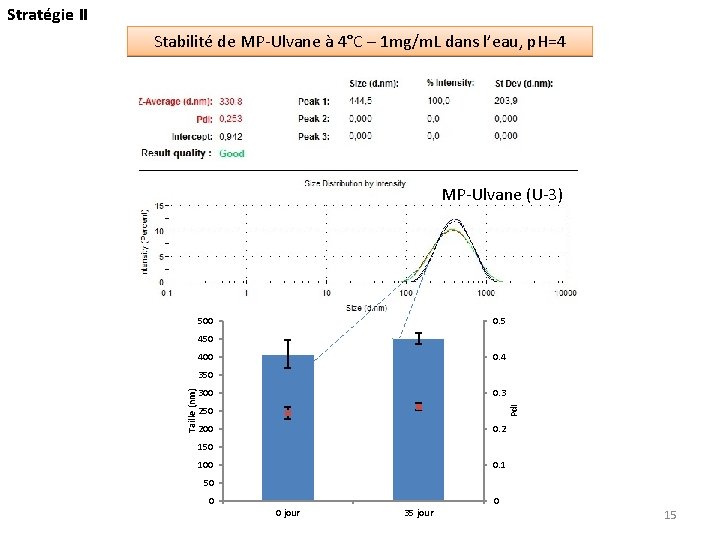
Stratégie II Stabilité de MP-Ulvane à 4°C – 1 mg/m. L dans l’eau, p. H=4 MP-Ulvane (U-3) 500 0. 5 450 400 0. 4 300 0. 3 Pd. I Taille (nm) 350 200 0. 2 150 100 0. 1 50 0 jour 35 jour 15
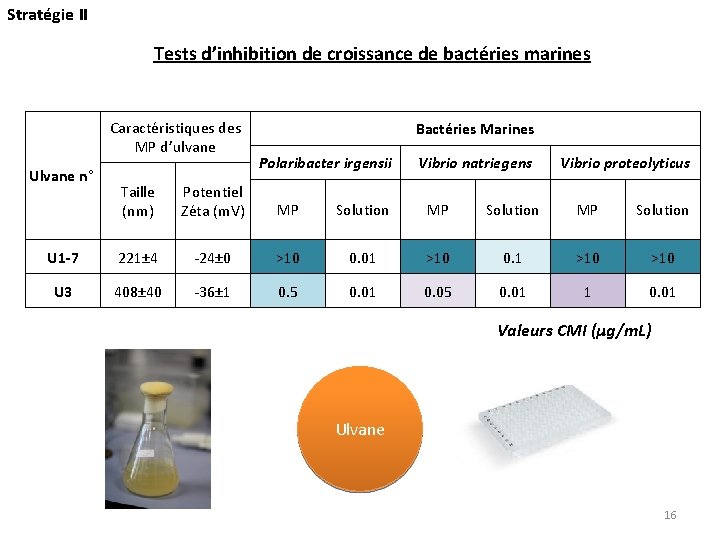
Stratégie II Tests d’inhibition de croissance de bactéries marines Caractéristiques des MP d’ulvane Ulvane n° Bactéries Marines Polaribacter irgensii Vibrio natriegens Vibrio proteolyticus Taille (nm) Potentiel Zéta (m. V) MP Solution U 1 -7 221± 4 -24± 0 >10 0. 01 >10 0. 1 >10 U 3 408± 40 -36± 1 0. 5 0. 01 0. 05 0. 01 1 0. 01 Valeurs CMI (µg/m. L) Ulvane 16

Conclusion - Elaboration et caractérisation de MP-Ulvane - Les MP sont stables dans le temps - Propriétés biocides conservées CMI MP-Ulvane > CMI Ulvane en solution Perspectives - Propriétés biocides (tests en cours) - Inhibition de croissance, inhibition d’adhésion des bactéries sur nombreuses souches bactériennes (marines + terrestres) - Inhibition de croissance de microalgues - Séquestration de principes actifs antibactériens (nisine) dans les MP Etude des propriétés biocides 17

GFP Ouest / SFGP Ouest 2013 Merci de votre attention 18
- Slides: 18