Gestasyonel trofoblastik hastalk epidemiyoloji genetik tan Prof Dr

Gestasyonel trofoblastik hastalık, epidemiyoloji, genetik tanı Prof. Dr. Hasan YÜKSEL Jinekolojik Onkoloji Bölümü, Aydın TJOD 2015

GTH, histolojik tipler 1 - Hidatidiform Mol (HM) Komplet (KM) Parsiyel (PM) Benign Premalign 2 - İnvaziv Mol (İM) 3 - Koriyokarsinom (KK) 4 - Plasental site trofoblastik tm (PSTT) ve 5 - Epiteloid trofoblastik tm (ETT) MALİGN

Gestasyonel Trofoblastik Neoplazi Tanısı 1. β-h. CG platosu (± %10), dört ölçüm veya ≥ 3 hafta sürede—günler 1, 7, 14, 21 2. β-h. CG > %10, ardışık ≥ 3 hafta ölçümlerde, ≥ 2 hafta sürede—günler 1, 7, 14 3. β-h. CG ≥ 6 ay serumda saptanabiliyorsa 4. Histolojik olarak koriyokarsinom ise
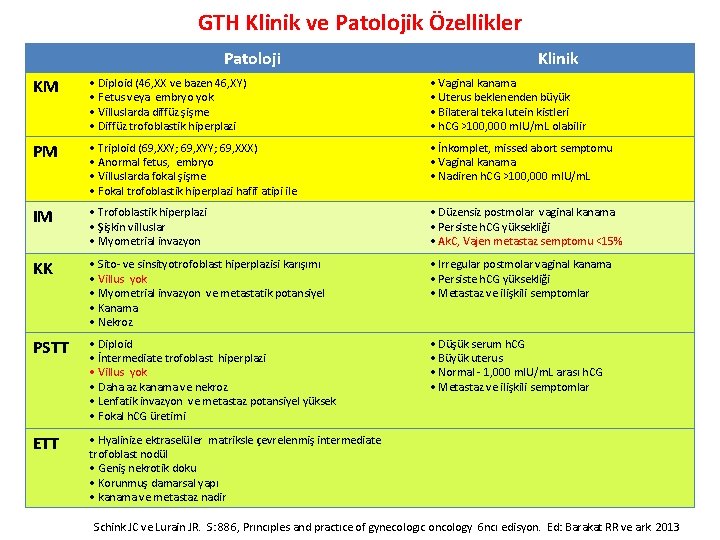
GTH Klinik ve Patolojik Özellikler Patoloji Klinik KM • Diploid (46, XX ve bazen 46, XY) • Fetus veya embryo yok • Villuslarda diffüz şişme • Diffüz trofoblastik hiperplazi • Vaginal kanama • Uterus beklenenden büyük • Bilateral teka lutein kistleri • h. CG >100, 000 m. IU/m. L olabilir PM • Triploid (69, XXY; 69, XYY; 69, XXX) • Anormal fetus, embryo • Villuslarda fokal şişme • Fokal trofoblastik hiperplazi hafif atipi ile • İnkomplet, missed abort semptomu • Vaginal kanama • Nadiren h. CG >100, 000 m. IU/m. L IM • Trofoblastik hiperplazi • Şişkin villuslar • Myometrial invazyon • Düzensiz postmolar vaginal kanama • Persiste h. CG yüksekliği • Ak. C, Vajen metastaz semptomu <15% KK • Sito- ve sinsityotrofoblast hiperplazisi karışımı • Villus yok • Myometrial invazyon ve metastatik potansiyel • Kanama • Nekroz • Irregular postmolar vaginal kanama • Persiste h. CG yüksekliği • Metastaz ve ilişkili semptomlar PSTT • Diploid • İntermediate trofoblast hiperplazi • Villus yok • Daha az kanama ve nekroz • Lenfatik invazyon ve metastaz potansiyel yüksek • Fokal h. CG üretimi • Düşük serum h. CG • Büyük uterus • Normal - 1, 000 m. IU/m. L arası h. CG • Metastaz ve ilişkili semptomlar ETT • Hyalinize ektraselüler matriksle çevrelenmiş intermediate trofoblast nodül • Geniş nekrotik doku • Korunmuş damarsal yapı • kanama ve metastaz nadir Schink JC ve Lurain JR. S: 886, Prıncıples and practıce of gynecologıc oncology 6 ncı edisyon. Ed: Barakat RR ve ark. 2013

İnsidans HM insidansı bölgelere göre farklı Kuzey Amerika, ANZ ve Avrupa'da, 1000 gebelikde 0. 6 -1. 1 Güneydoğu Asya ve Japonya 2 -3 kat yüksek (2/1000 gebe) Tayvanda 125 gebelikte 1 İrlanda da KM 2000 de 1 PM 700 de 1 Riskli popülasyonları yeterince belirlemedeki eksiklikler ve kontrol gruplarının olmaması nedeniyle GTD gelişimine katkıda bulanan risk faktörleri tanımlamak zor Atrash HK, ve ark. Am J Obstet Gynecol 1986; Palmer JR. J Reprod Med 1994; Fukunaga M, ve ark. Hum Pathol 1995; Jeffers MD, ve ark. Int J Gynecol Pathol 1993

RİSK FAKTÖRLERİ • İleri anne yaşı • Mol öyküsü

KM riski, azalmış provitamin A ( ß-karoten) ve hayvansal yağ tüketimi ile artar Berkowitz RS, ve ark. A JOG 1985 ; Parazzini F, ve rak. AJOG 1988 İnfertilite öyküsünde ve spontan abortus öyküsünde abotusu olmayana göre 2 -3 kat artmış KM ve PM artışı Fulop V, ve ark. J Reprod Med 2004; Acaia B, ve ark. Gynecol Oncol 1988; Parazzini F, ve ark. Obstet Gynecol 1991 Üreme çağı başları ve sonlarında (>40 yaş) KM artar, 5 -10 kat risk artışı Parazzini F, ve ark. BJOG 1986; Sebire NJ, ve ark. BJOG 2002 Ø 50 yaşta her 3 gebelikten 1 molar Bracken MB, BJOG 1987 Mutasyone genler biparental kökenli KM un ailesel olanlarında Murdoch S, et al. Nat Genet 2006 ; Wang CM, et al. J Med Genet 2009; Fisher RA, ve ark. J Reprod Med 2004

PM vitamin A eksikliği ile, İleri anne yaşı ile ilişkisiz; Adet düzensizliği öyküsü ve yüksek estrojenli OKS kullanımı ile ilişkilidir Berkowitz RS, et al. AJOG 1995; Acaia B, et al. Gynecol Oncol 1988

Menarşın yaşı >12 olması, adet kanamasının az olması, uzun süre OKS kullanımı KK riskini artırır*, postmolar GTN ile OKS kullanım ilişkisi açık değildir. Buckley JD, ve ark. Cancer Res. 1988*; Stone M, ve ark. BJOG 1976; Costa HL, Doyle P. Gynecol Oncol 2006 Kan grubu A olan kadınlarda KK riski artmıştır Palmer JR. J Reprod Med 1994; Palmer JR, ve ark. J Natl Cancer Inst 1999

MOL TEKRARI Histolojik tanı KM ve PM izleyen gebelikte mol: 1/60 (%1, 7) Tekrarlardaki ile aynı tipte Tüm mollerin >%98’inde obstetrik risk artışı olmayacaktır Sebire NJ, ve ark. , BJOG. 2003

İkinci kez KM 1 -2%, ki genelden 10 -20 kat fazla risk Sand PK, ve ark. Obstet Gynecol 1984; Berkowitz RS, ve ark. J Reprod Med. 1998 Üçüncü kez KM 15% - 20% Garrett LA, ve ark. J Reprod Med 2008; Sebire NJ, ve ark. BJOG 2003 Eş değişiminden bağımsız Tuncer ZS, ve ark. Gynecol Oncol 1999 Ailesel tekrarlayan HM vakalarında Kromozom #19 üzerindeki, NLRP 7 lokusta missense mutasyonu gösterilmiş Acaia B, ve ark. Gynecol Oncol 1988; Moglabey YB, ve ark. Hum Mol Genet 1999; Kou YC, ve ark. Mol Hum Reprod 2008; Wang CM, ve ark. J Med Genet 2009 >2 molar gebelikte bu mutasyon %60 var Messaed C, ve ark. J Med Genet. 2011

Molar gebelik boşaltılanların yaklaşık %15 inde Lokal IM gelişir KK, 50, 000 gebelikte 1 olur (gebelikle ilgili her durumlar dahil) KK diğer gebelik durumlarına göre molar gebeliği takiben gelişme olasılığı 1000 kat fazladır, KK’ların yarısı molar gebelik sonrası gelişir. İleri anne yaşı, ve öncesinde HM öyküsü, Asya, Amerikan yerlisi ve Afrika kökenli Amerikalılarda KK riski yüksektir Ngan S, Seckl MJ. Curr Opin Oncol 2007; Smith ve ark. Obstet Gynecol 2003

GTH MORTALİTE RİSKİ, ORANLARI

17 ülke 32 merkez toplam 26153 hasta, 14093 KM, 20. 6% GTN gelişmiş ve %5, 7 ölümlü 10230 PM bunların %6, 5 inde GTN 1, 165 tanı sınıflamasına sokulamadı. 548 post-term gebelik KK, %13, 4 ölüm 137 PSTT %16, 1 ölüm. n=2, 818 trofoblast merkezlerinde tedavi yapılan mortalite %2, 1 n=1, 854, başarısız tedavi sonrası merkeze yollanmış mortalite %8 (p < 0. 01) Kohorn EI. J Reprod Med. 2014

Mortalite Brezilya 10 merkez 2000 -2011, n=5, 250 Ölüm 3 (0. 06%) olgu boşaltmada Tedavide 26 ölüm 4 düşük-risk [0. 4%], 19 yüksek-risk [9. 5%], 3 PSTT [21. 4%]). Braga A, ve ark. J Reprod Med. 2014 Epidemiological report on the treatment of patients with gestational trophoblastic disease in 10 Brazilian referral centers: results after 12 years since International FIGO 2000 Consensus.

TÜRKİYE’ DE DURUM

Türkiye’de HM insidansı • İnsidans veren 24 yayınlar hastane kaynaklı • 0. 3 -16/1000 gebelik ve 1. 0 -24. 5/1000 doğum • 929, 323 gebelikte 2227 HM, insidans 2. 4/1000 • 884, 178 doğumda 1655 HM, insidans 1. 9 /1000 Ozalp SS ve ark. Hydatidifrom mole in Turkey from 1932 to 2000, Int J Gynaecol Obstet, 2001. Topluma dayalı çalışma (Eskişehir) - 15 -49 yaş, n=2, 032, 6, 274 gebelikte 4 HM - HM sıklığı 1, 000 canlı doğumda 0. 8 ve 1, 000 gebelikte 0. 6 Ozalp SS ve ark. Eur J Gynaecol Oncol. 2003

Üreme hayatının uçlarında insidans (TR) 1932 -2000, 222 yayın içinde 19’u (hastane kaynaklı) HM; ≤ 20 -21 yaş = %0. 3 -1. 6 HM; >39 -40 yaş = %1. 7 -23. 1 Ozalp SS ve ark. , Eur J Gynaecol Oncol. 2002

Rekürren HM (TR) HM rekürrensi: %1. 1, 6 merkez, 10 yıl, 351, 650 doğum Oge T, Ozalp SS, Güngör T, Yildirim Y, Sanci M, Dogan A, Ertas IE, Yetimalar H, Dilek S, Celik C. J Reprod Med. 2012 HM rekürrensi: %5. 5, 310 olgu sonucu; rekürrenslerin yarıya yakınında en az 2 kez HM Mungan, T et al, Int J Gynecol Obstet, 1996 HM rekürrensi: %0. 7, 701 olgu Atasü, T et al, Ülkemizde Mol hidatiform taraması. Çağdaş Hekim, 1975 GTN’de KT sonrası gebeliklerde (n= 49) %4. 6’sında HM Ayhan, A et al, J Reprod Med, 1990

Ozalp SS ve ark. 2014, Asian Pac J Cancer Prev 2003 -2013 28 Merkez, 1, 173, 235 doğum 456 GTN (364 veri) 0. 38 /1, 000 doğum median yaş: 31 (15 -59) Öncesi: Mole %54. 9, term gebelik %16. 5 352 (%96. 7) remisyon, 7 (%1. 9) persiste, 5 (%1. 4) mortalite İM; n=81 KK; n=66 PSST; n=17 Olguların %45 inde patoloji. Dx var

EPİDEMİYOLOJİDE DEĞİŞİKLİKLER Ortalama tanı haftası düşmüştür Boşaltım işleminin tekrarı azalmıştır Postmolar GTN hafif artmış (%25. 2 %30) Kemoterapi gereken GTN oranı artmıştır Median yaş değişmemiştir Asemptomatik hasta, kanama olmadan tanı oranı artmıştır (%2. 9 %13. 6) Gebelikte HT düşmüş (%22 %2. 5) Killick S, ve ark. J Reprod Med 2012 Lertkhachonsuk AA, ve ark. J Reprod Med 2013

HM’ de malign değişim KHM’ de %16 PHM’ de %0. 5 Ngan S, ve Seckl MJ. Curr Op. n Oncol, 2007

KT GEREKECEK HASTALARI BİLEBİLİR MİYİZ? PHM (n = 50) KHM 1 -spontan iyileşme (n = 50) 2 - KT gereken (n= 50). İmmünboya MLH 1, MSH 2, nm 23, TERT, p 53, EGFR, and Cerb. B 2. Morfolojik veya immunohistokimyasal özellikler KHM de sonradan KT alacak hastaları öngörememektedir. Petts G, ve ark. J Reprod Med. 2014

GENETİK • HANGİ HASTALAR PERSİSTE GTD OLACAK? • GEÇİRİLMİŞ HASTALIKTA HANGİ HASTALARDA REKÜRRENS RİSKİ YÜKSEK OLUYOR? • AİLESEL GEÇİŞLERDE DURUM NEDİR?

GTH Genetik KM %75 -85 46, XX ve kalanı 46, XY paternal * boş veya nükleusu olmayan ovum tek haploid sprem ile döllenip XX replike olur * iki haploid sperm döller XX ve XY olur PM 69 XXX, XYY, XXY iki paternal bir maternal * iki sperm * tek sperm replikasyonu
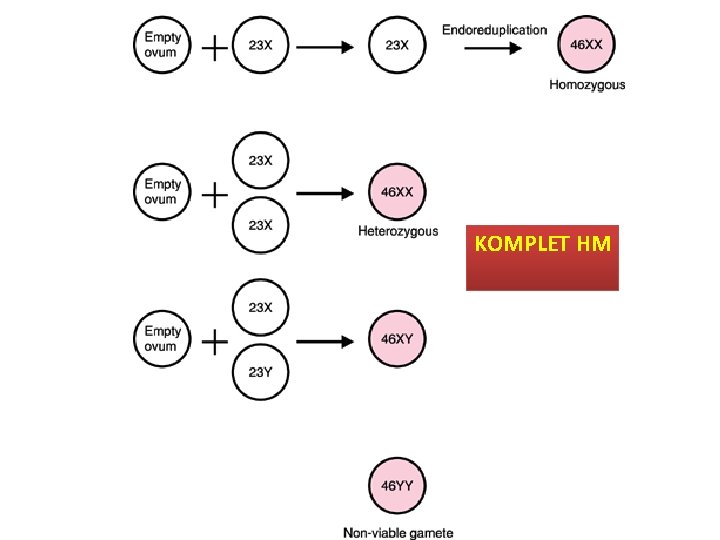
KOMPLET HM
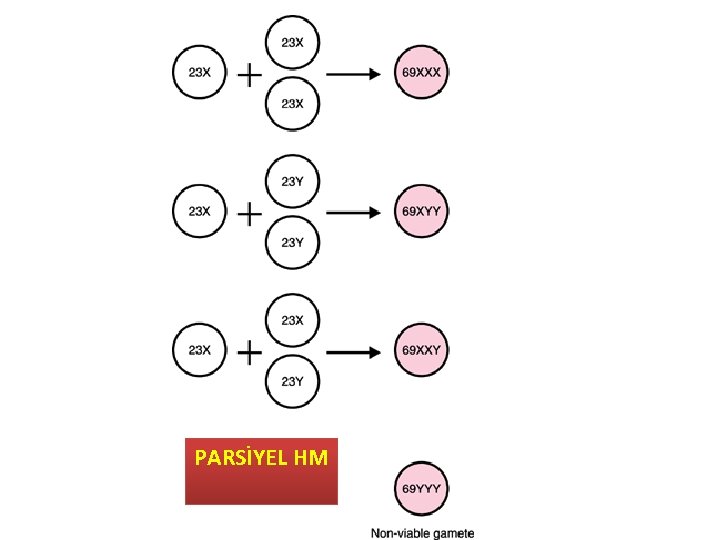
PARSİYEL HM

HM • Genetik özellikler – KM Diploid androgenetik (46, XX > 46, XY) % 80 -90 monospermik % 10 -20 dispermik diploid biparental triploid diandrik dispermik tetraploid triandrik – PM Triploid diandrik dispermik diploid biparental (diploid abortuslar, ikiz gebelikler, mozaisizm) triploid digynic triploid monospermik tetraploid triandrik Slim R, Wallace EP. Front Immunol. 2013
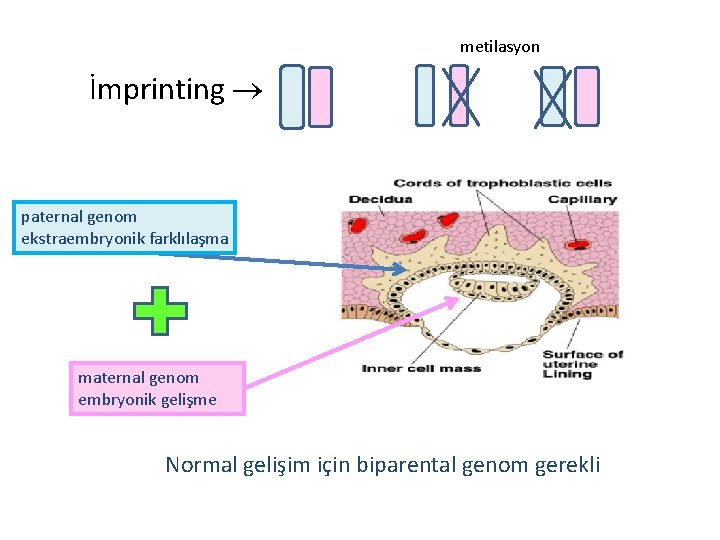
metilasyon İmprinting paternal genom ekstraembryonik farklılaşma maternal genom embryonik gelişme Normal gelişim için biparental genom gerekli
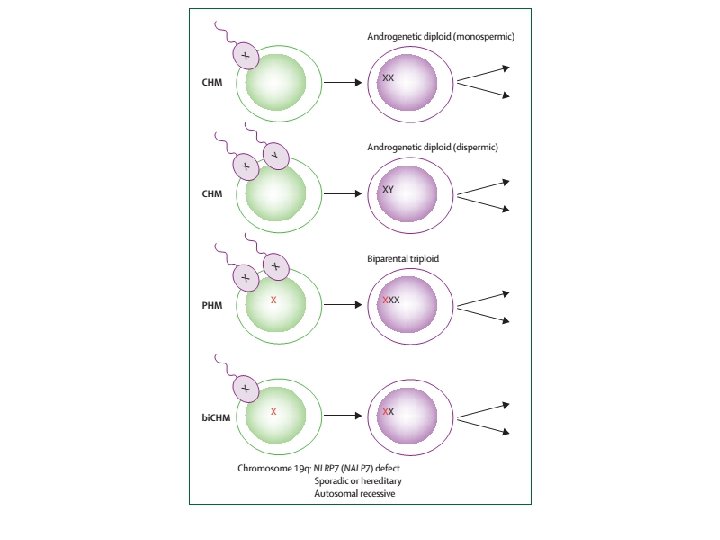

Uniparental kökenli doku insanda var ancak çok nadir Maternal kökenli Over Matür kistik Teratomu (Digynic diploid genom) Oosit maturasyonunda mayotik hata Üç embriyonel germ hücre tabakası var Paternal orjinli Androgenetik komplet HM (Androgenetik diploid genom) Koriyon villus hidrofik dejenerasyon var Embryo, kord, embriyonik membran YOK
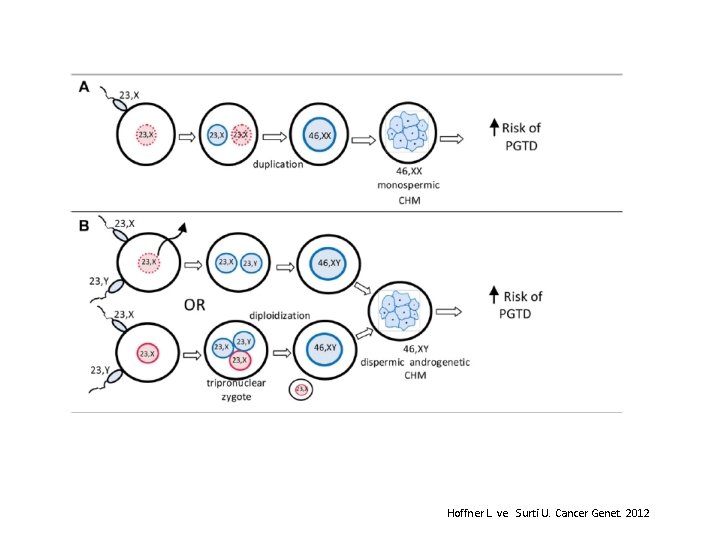
Hoffner L. ve Surti U. Cancer Genet. 2012
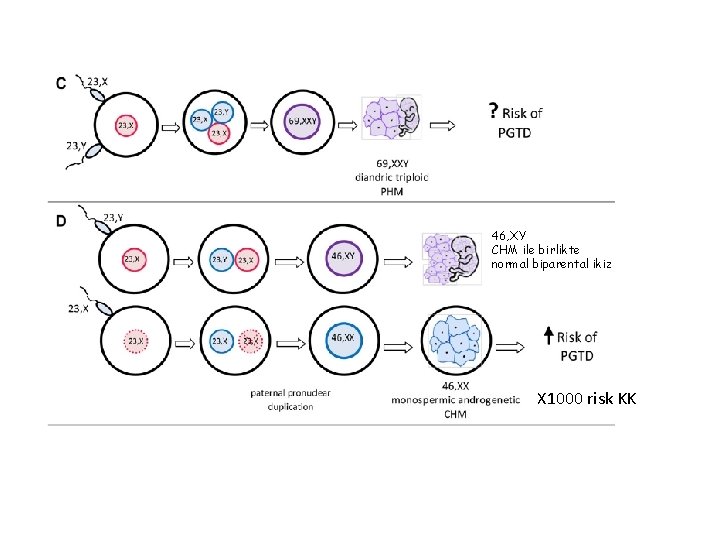
46, XY CHM ile birlikte normal biparental ikiz X 1000 risk KK
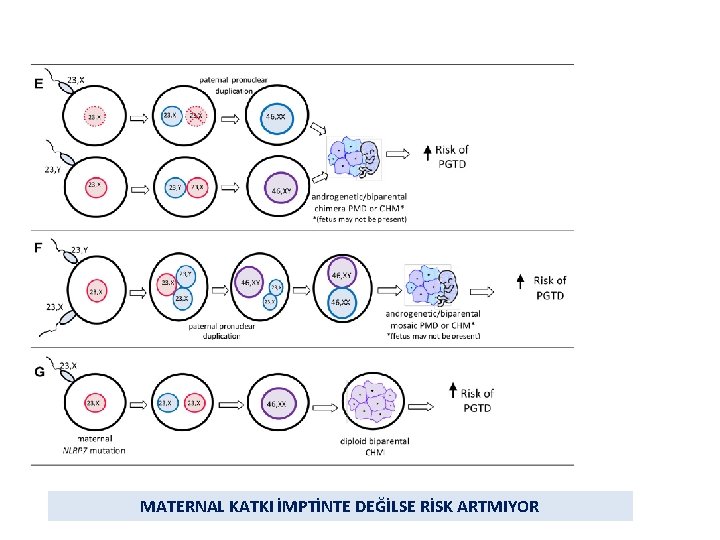
MATERNAL KATKI İMPTİNTE DEĞİLSE RİSK ARTMIYOR
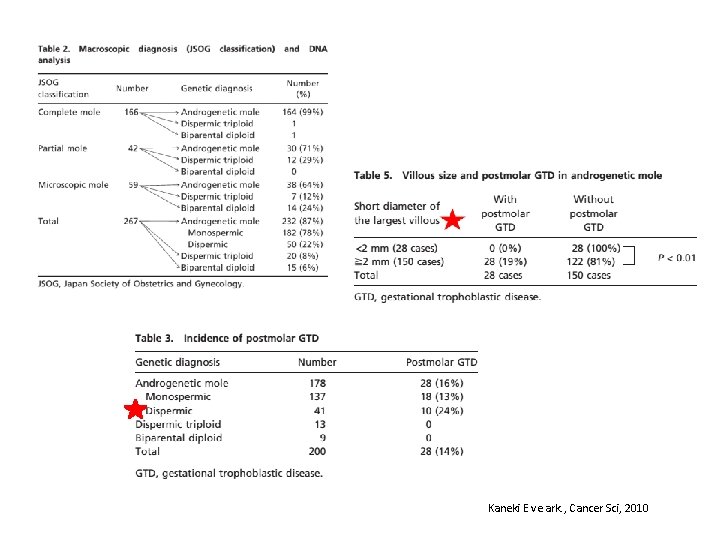
Kaneki E ve ark. , Cancer Sci, 2010
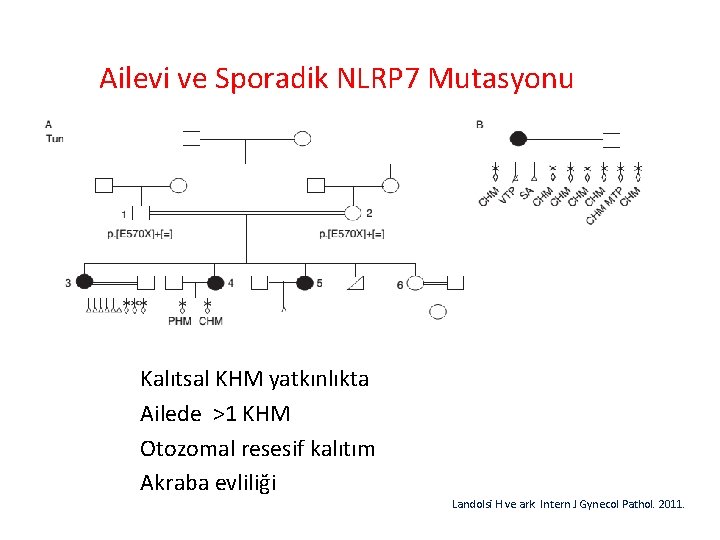
Ailevi ve Sporadik NLRP 7 Mutasyonu Kalıtsal KHM yatkınlıkta Ailede >1 KHM Otozomal resesif kalıtım Akraba evliliği Landolsi H ve ark. Intern J Gynecol Pathol. 2011.

Kalıtsal HM predispozisyonunda KHM riski % 75 >50 Bi. HM ailesi % 0 - %60 NLRP 7 mutasyon var -homozigot/ birleşik heterozigot/ heterozigot (varyant) NLRP 7 üzerinde de çok fazla mutasyon var Wang CM, ve ark. J Med Genet. 2009 Ülkemizden de FRKM de NLRP 7 mutasyonu gösterildi Ülker V, ve ark. 2013 EJOGRB
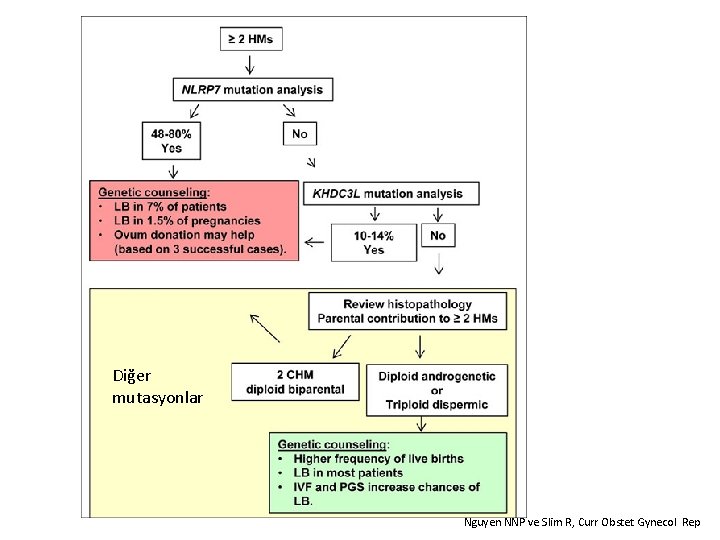
Diğer mutasyonlar Nguyen NNP ve Slim R, Curr Obstet Gynecol Rep

Genetik Çalışma Mol şüphenilen hidrofik plasentalarda genetik inceleme (Mozaik /kimerik) • HM, PMD (Plasental mezenşimal displazi) • Fetal malformasyon, çocuk gelişim bozuklukları • Androgenetik hücreler PGTD riskini artırır

SONUÇ- Epidemiyoloji • Güneydoğu Asya dışında HM insidansı 1000 gebelikte <1, (Japonya’da 2) • Ülkemizde topluma dayalı tek çalışmada insidans dünyaya benzer • Üreme çağının uçlarında ve öyküde HM varsa insidans artıyor, ileri yaşta malignite artıyor • Erken tanı ile artık daha çok asemptomatik yakalanıyor • MALİGNİTE GELİŞİM ORANI AZALMAMIŞTIR

SONUÇ-Genetik • Histopatolojik tanıya ek genetik tanı, takip ve tekrarlayan ya da ailesel vakalarda yararlı olabilir • KHM, PHM ve hidrofik abortus ayrımı PGTD riski için önemlidir • Mozaik /Kimerik ayırımı önemli olabilir • Özellikle NLRP 7 ve diğer mutasyonların tekrarlayan Biparental HM gelişimindeki rollerinin belirlenmesi (histopatoloji belirleyemez) beklenmektedir

T E Ş E K K Ü R L E R
- Slides: 42