Geometria Molecular Geometria Molecular As molculas formadas por
















- Slides: 28

Geometria Molecular

Geometria Molecular � As moléculas formadas por ligações covalentes podem apresentar de dois a milhares de átomos. � Os átomos se alinham formando formas geométricas em relação aos núcleos dos átomos. � TEORIA DA REPULSÃO DOS PARES ELETRÔNICOS DA CAMADA DE VALÊNCIA.

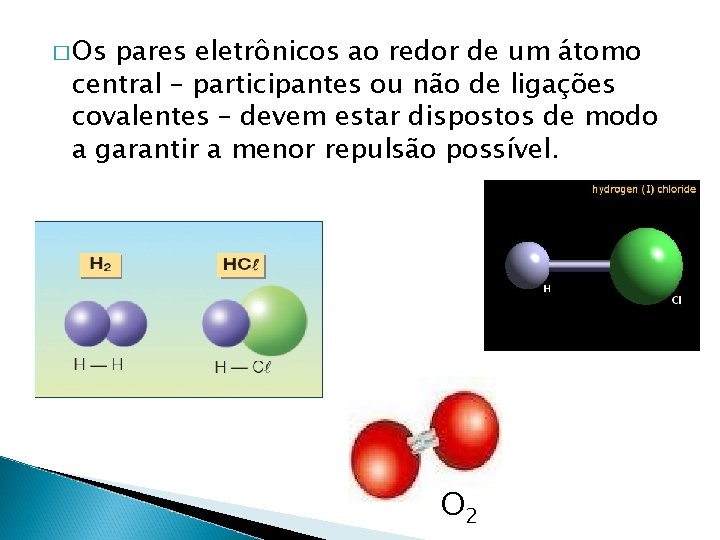
� Os pares eletrônicos ao redor de um átomo central – participantes ou não de ligações covalentes – devem estar dispostos de modo a garantir a menor repulsão possível. O 2

� Moléculas diatômicas (apenas 2 átomos) SEMPRE apresentarão geometria linear!!!!

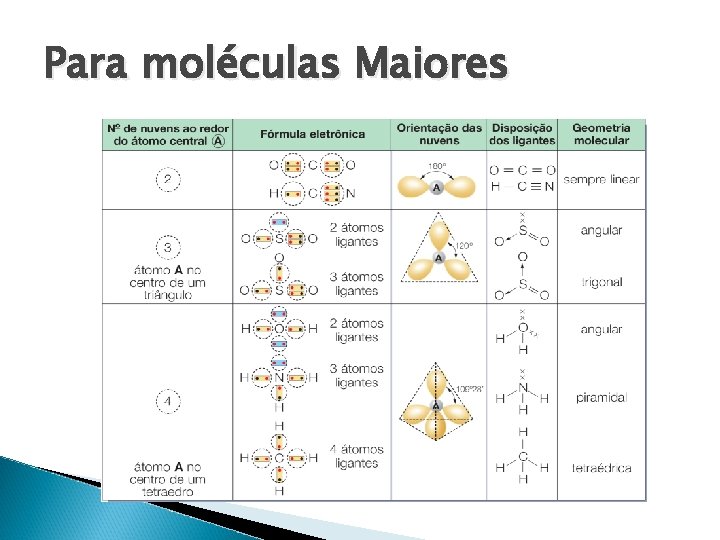
Para moléculas Maiores

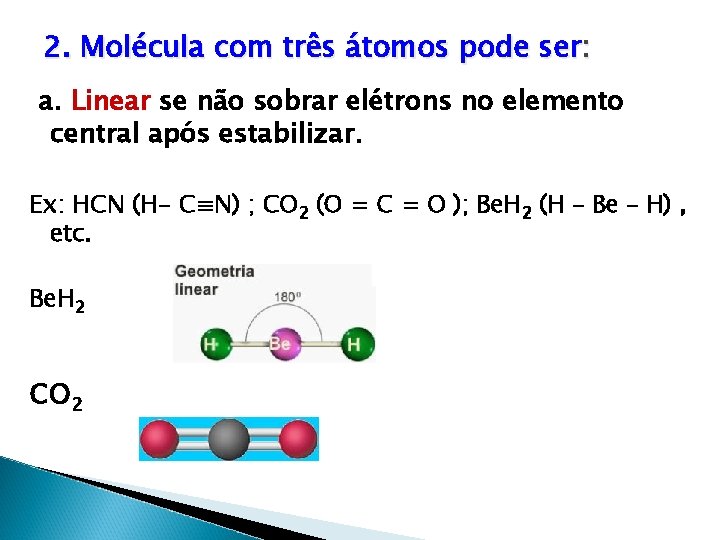
2. Molécula com três átomos pode ser: a. Linear se não sobrar elétrons no elemento central após estabilizar. Ex: HCN (H- C≡N) ; CO 2 (O = C = O ); Be. H 2 (H – Be – H) , etc. Be. H 2 CO 2

2. Molécula com três átomos pode ser: b. Angular se sobrar elétrons no elemento central após estabilizar. Ex: H 2 O; O 3; SO 2 (molécula da H 2 O) (molécula de SF 2)

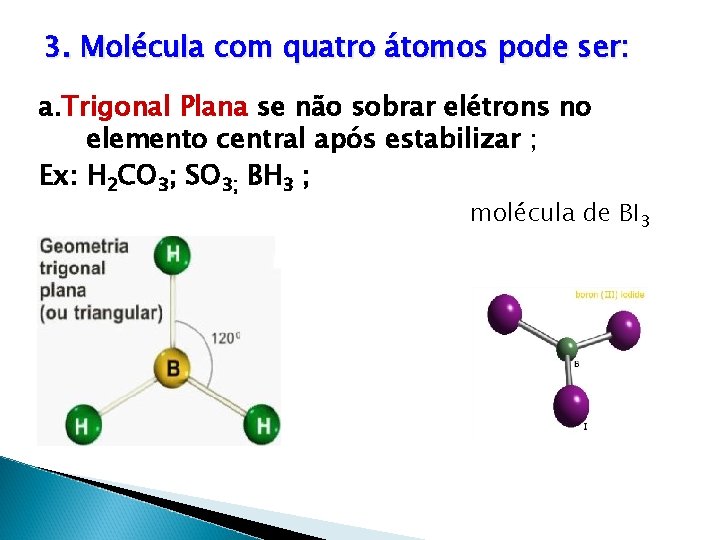
3. Molécula com quatro átomos pode ser: a. Trigonal Plana se não sobrar elétrons no elemento central após estabilizar ; Ex: H 2 CO 3; SO 3; BH 3 ; molécula de BI 3

b. Trigonal Piramidal se sobrar elétrons no elemento central após estabilizar. � Ex: NH 3; PCl 3

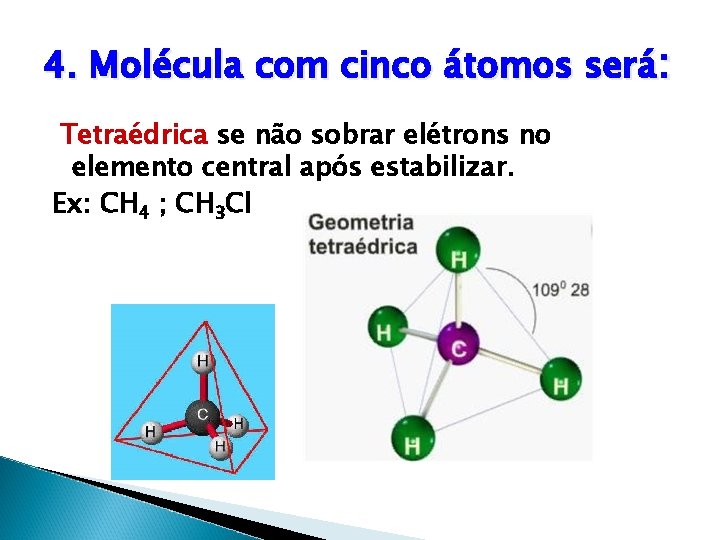
4. Molécula com cinco átomos será: Tetraédrica se não sobrar elétrons no elemento central após estabilizar. Ex: CH 4 ; CH 3 Cl

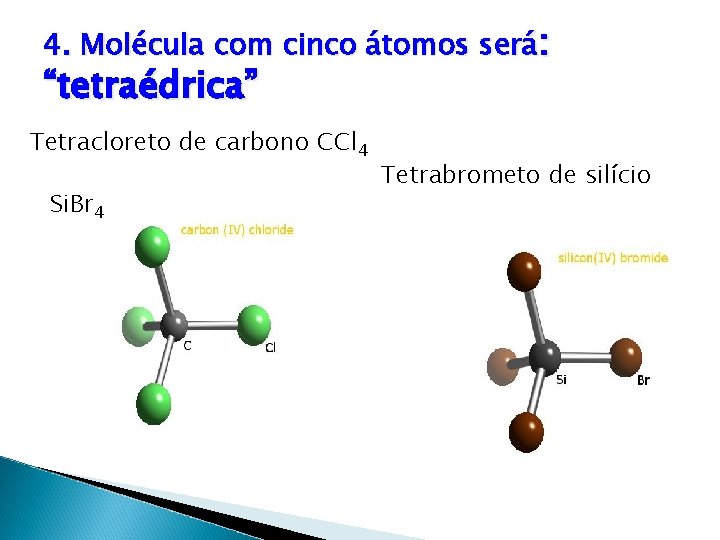
4. Molécula com cinco átomos será: “tetraédrica” Tetracloreto de carbono CCl 4 Si. Br 4 Tetrabrometo de silício

Polaridade das Ligações � POLOS: região presença de cargas em determinada � LIGAÇÔES � Toda IÔNICAS: ligação Iônica é POLAR!!! Na+ Cl- cargas (polos) reais TRANSFERÊNCIA DE ELÉTRONS

� LIGAÇÔES COVALENTES � Compartilhamento �A de pares de elétrons polaridade estará relacionada com a diferença de eletronegatividade e a consequente deformação da nuvem eletrônica.

� Para moléculas diatômicas em que não há diferença de eletronegatividade: MOLECULA APOLAR

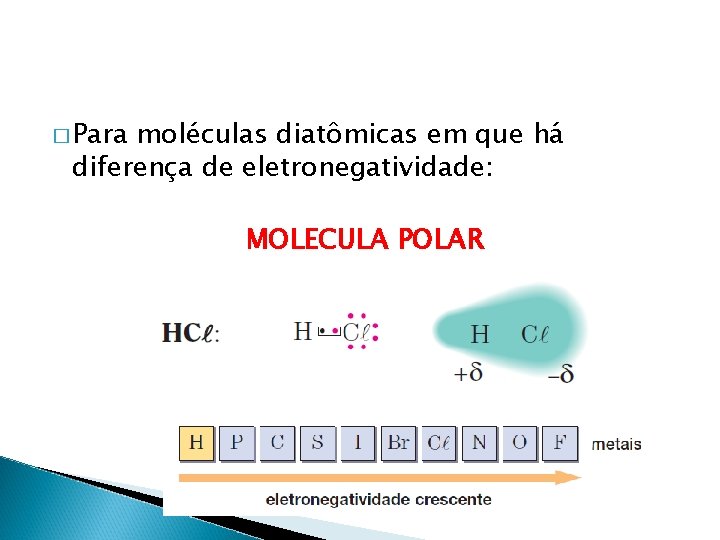
� Para moléculas diatômicas em que há diferença de eletronegatividade: MOLECULA POLAR

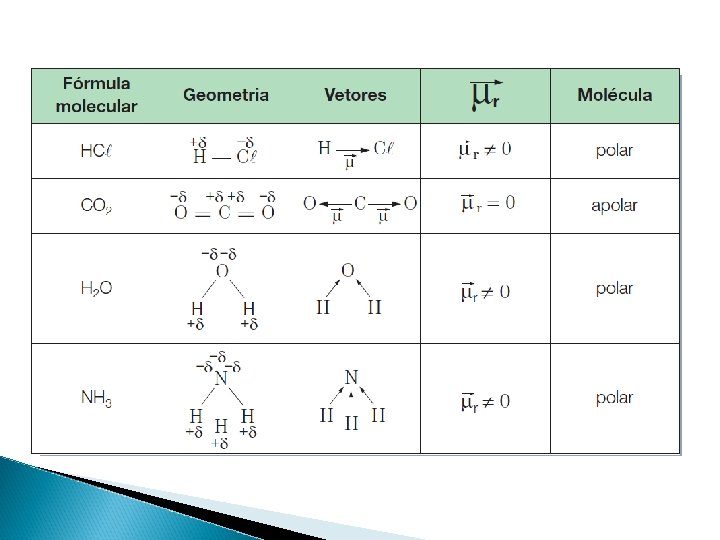
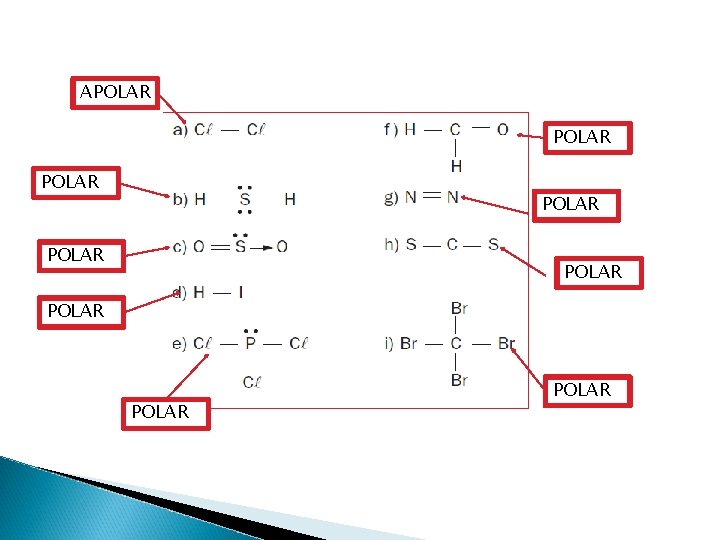
Determinação da polaridade em moléculas maiores � Pode –se determinar a polaridade de uma molécula através do vetor momento dipolar resultante


APOLAR POLAR POLAR

Polaridade e Solubilidade � Semelhante dissolve semelhante. � Soluto polar tende a dissolver bem em solvente polar. � Soluto apolar tende a dissolver bem em solvente apolar.


Força de Interação ou Ligação Intermolecular

�O que mantêm as moléculas unidas nos três estados (sólido, líquido e gasoso) são as chamadas ligações ou forças ou interações moleculares. � São três tipos de forças: � Ligação de Hidrogênio � Dipolo permanente ou dipolo-dipolo (DD) � Dipolo instantâneo (DI), força de van der Waals ou força de dispersão de London

Dipolo Induzido – Dipolo Induzido � Ocorrem em todas as substâncias apolares � F 2, Cl 2, Br 2, I 2, hidrocarbonetos

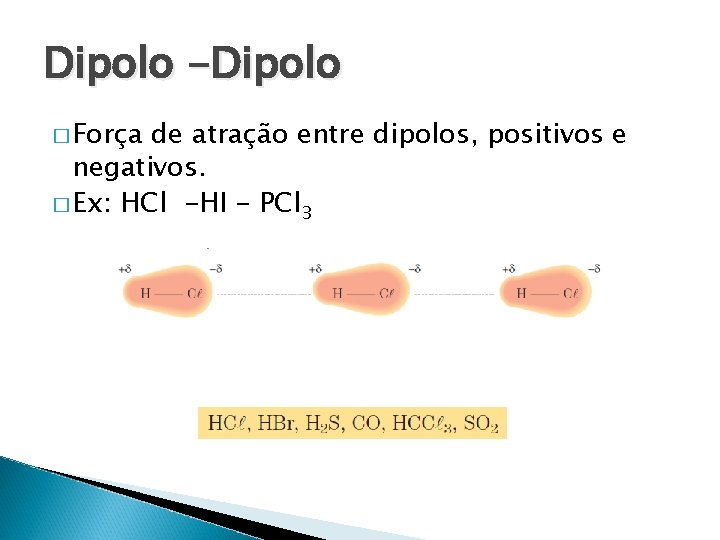
Dipolo -Dipolo � Força de atração entre dipolos, positivos e negativos. � Ex: HCl -HI - PCl 3

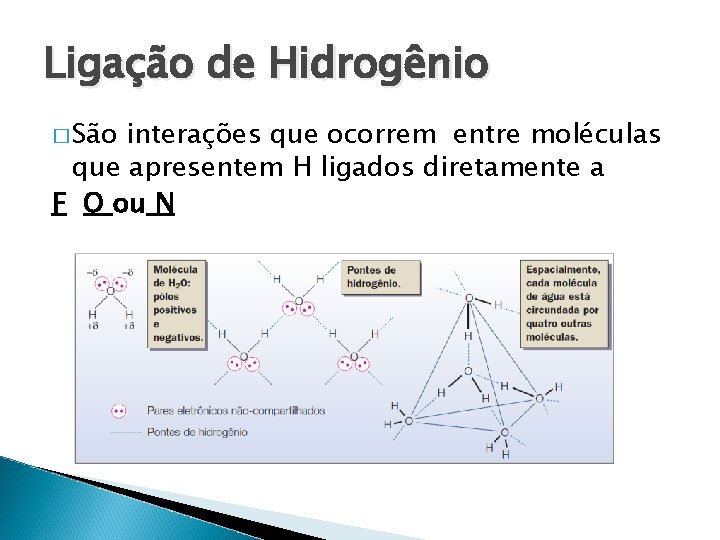
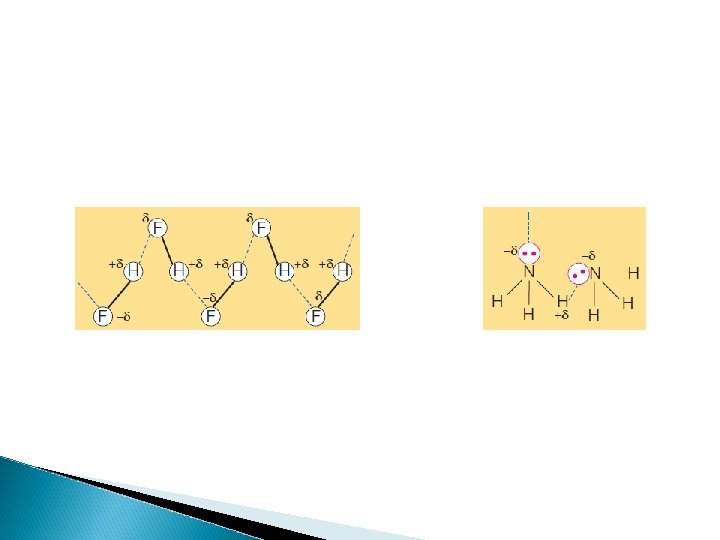
Ligação de Hidrogênio � São interações que ocorrem entre moléculas que apresentem H ligados diretamente a F O ou N



Forças Intermoleculares e Temperatura e fusão e ebulição