Geokemija elemenata u tragovima Definicija Uloga u interpretaciji







- Slides: 21

Geokemija elemenata u tragovima - Definicija - Uloga u interpretaciji geoloških podataka

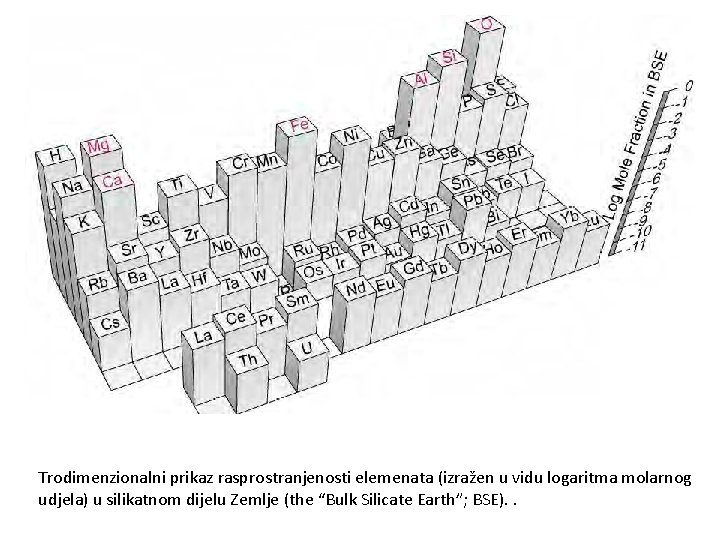
Trodimenzionalni prikaz rasprostranjenosti elemenata (izražen u vidu logaritma molarnog udjela) u silikatnom dijelu Zemlje (the “Bulk Silicate Earth”; BSE). .


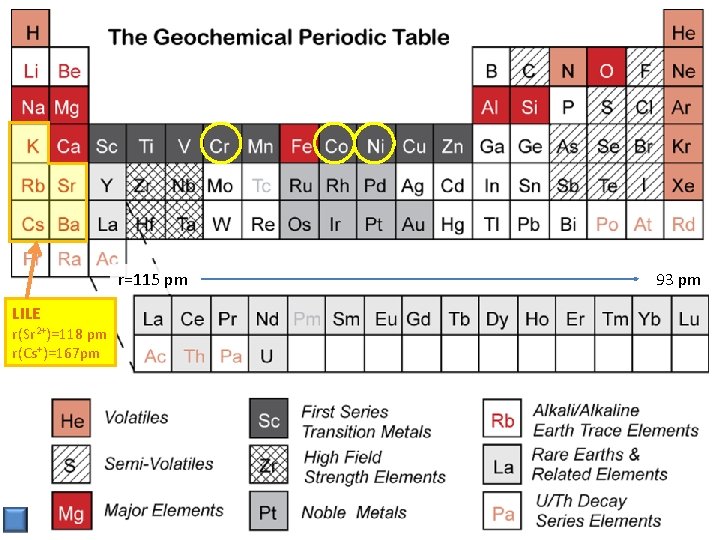
r=115 pm LILE r(Sr 2+)=118 pm r(Cs+)=167 pm 93 pm



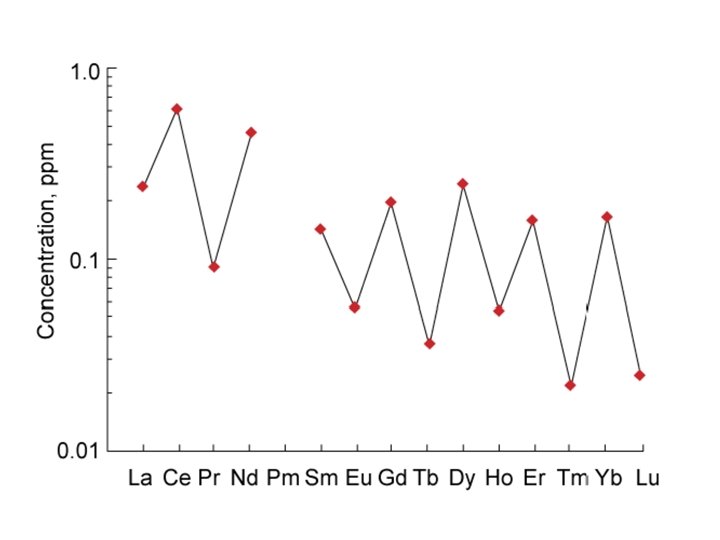
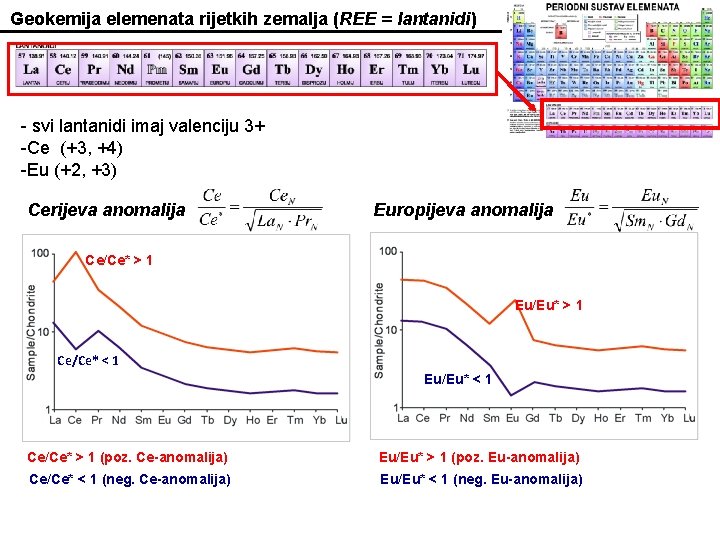
Geokemija elemenata rijetkih zemalja (REE = lantanidi) - svi lantanidi imaj valenciju 3+ -Ce (+3, +4) -Eu (+2, +3) Cerijeva anomalija Europijeva anomalija Ce/Ce* > 1 Eu/Eu* > 1 Ce/Ce* < 1 Eu/Eu* < 1 Ce/Ce* > 1 (poz. Ce-anomalija) Eu/Eu* > 1 (poz. Eu-anomalija) Ce/Ce* < 1 (neg. Ce-anomalija) Eu/Eu* < 1 (neg. Eu-anomalija)

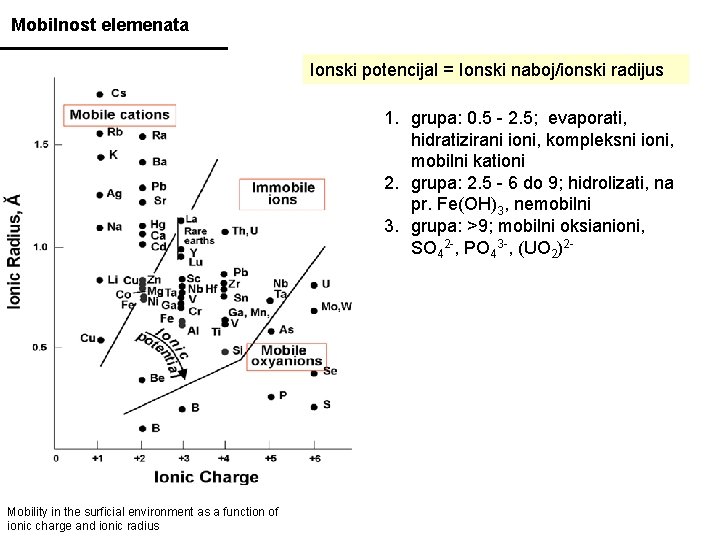
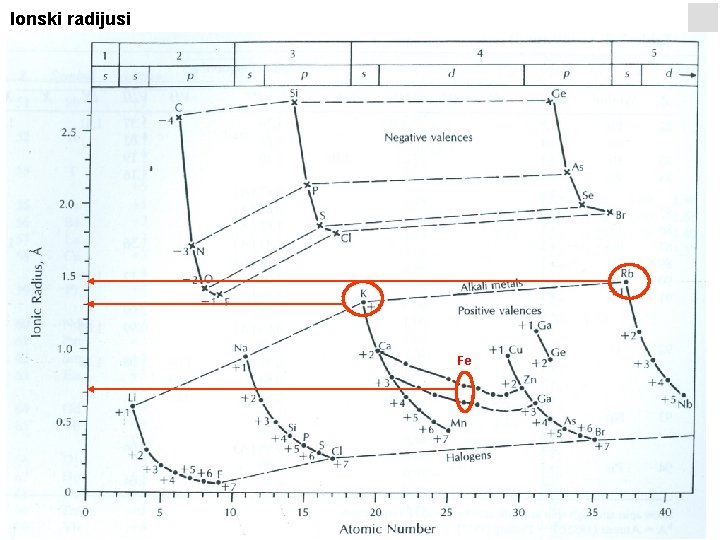
Mobilnost elemenata Ionski potencijal = Ionski naboj/ionski radijus 1. grupa: 0. 5 - 2. 5; evaporati, hidratizirani ioni, kompleksni ioni, mobilni kationi 2. grupa: 2. 5 - 6 do 9; hidrolizati, na pr. Fe(OH)3, nemobilni 3. grupa: >9; mobilni oksianioni, SO 42 -, PO 43 -, (UO 2)2 - Mobility in the surficial environment as a function of ionic charge and ionic radius

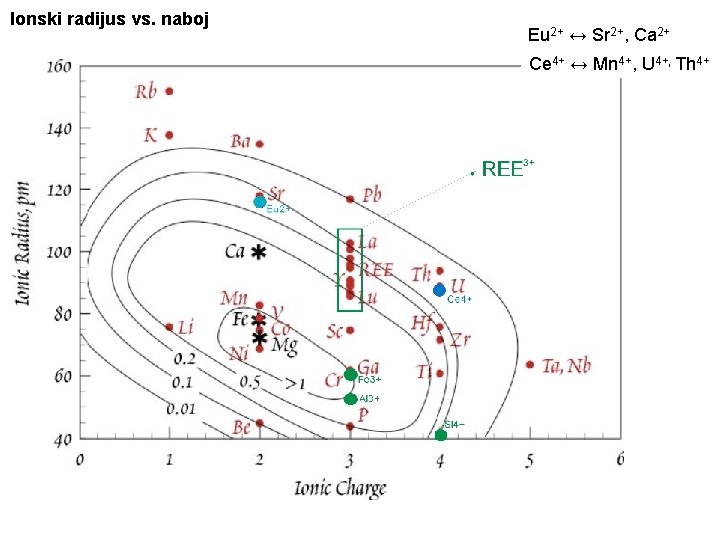
Ionski radijus vs. naboj Eu 2+ ↔ Sr 2+, Ca 2+ Ce 4+ ↔ Mn 4+, U 4+, Th 4+

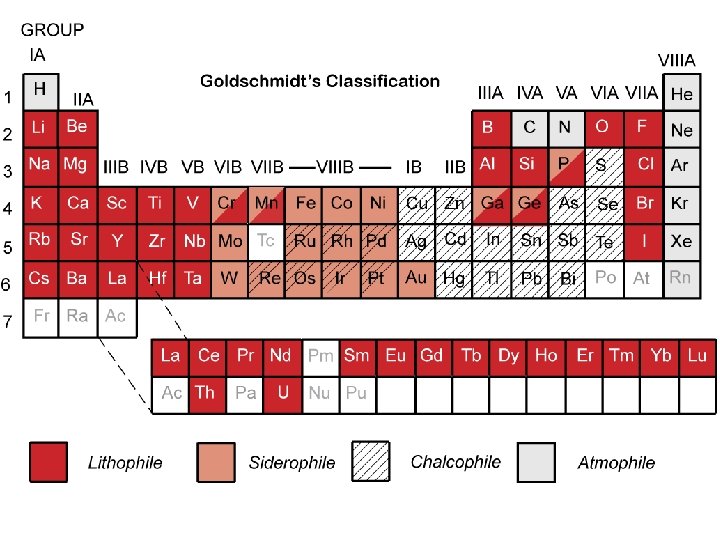
Ionske zamjene u kristalima Goldschmidtova pravila zamjene: 1. Ioni jednog elementa mogu zamijeniti ione drugog elementa u ionskim kristalima ukoliko se njihovi ionski radijusi ne razlikuju za više od 15% 2. Ioni čiji se naboji razlikuju za jednu jedinicu mogu se zamjenjivati uz uvjet da je sačuvana elektronetralnost kristala 3. Kada dva različita iona konkuriraju za isto mjesto u kristalnoj rešetci, zauzet će ga onaj s većim ionskim potencijalom (naboj/radijus) 4. Zamjena može biti znatno ograničena čak i kada su zadovoljeni kriteriji veličine i naboja iona, ali je razlika u elektronegativnosti iona koji se zamjenjuju velika. Npr. Na+ i Cu+ imaju isti naboj i slične radijuse, ali Cu ne zamjenjuje Na u Na. Cl i albitu (Na. Al. Si 3 O 8) Glavni elementi Elementi u tragovima (< 1000 ppm ili 0, 1%)

Kompatibilni vs. inkompatibilni elementi Inkompatibilni elementi: elementi koji su preveliki i/ili previsokog naboja da bi ušli u kristalnu rešetku petrogenih minerala koji kristaliziraju iz taljevine Large-ion lithophile elements (LILE): inkompatibilni zbog veličine npr. Rb+, Cs+, Sr 2+, Ba 2+, (K+), REE High-field strength elements (HFSE): inkompatibilni zbog naboja npr. Zr 4+, Hf 4+, Ta 4+, Nb 5+, Th 4+, U 4+, Mo 6+, W 6+, itd. Kompatibilni elements: Elementi koji lako ulaze u petrogene minerale npr. Cr, V, Ni, Co, Ti, itd. Na višim temperaturama kristali su tolerantniji prema stranim ionima. Npr. visokotemperaturni sfalerit (Zn. S) može sadržavati i preko 10% Fe 2+. Zn. S (Fe, Zn. S)

Ionski radijusi Fe

Tri načina razdiobe elemenata u tragovima između taljevine i krutine: 1. Kamuflaža (CAMOUFLAGE) 2. Zahvaćanje (CAPTURE) 3. Prijem (ADMISSION) 1. Kamuflaža - element u tragovima isti naboj i sličan ionski radijus kao i glavni element Npr. Zr 4+ (0, 80 Å) i Hf 4+ (0, 79 Å), Hf uglavnom ne stvara vlastite minerale nego se “kamuflira” u cirkonu (Zr. Si. O 4) 2. Zahvaćanje - element u tragovima ulazi u strukturu preferirano zbog većeg ionskog potencijala Npr. K-feldspati mogu “zahvatiti” Ba 2+ (1. 44 Å; Z/r = 1. 39) ili Sr 2+ (1. 21 Å; Z/r = 1. 65) na mjesto K+ (1. 46 Å, Z/r = 0. 68). K+ + Si 4+ Sr 2+ (Ba 2+) + Al 3+ 3. Prijem - element u tragovima ulazi u strukturu iako ima manji ionski potencijal Npr. Rb+ (1. 57 Å; Z/r = 0. 637) za K+ (1. 46 Å, Z/r = 0. 68) u K-feldspatima, Sr 2+ (1. 21 Å) za Ca 2+ (1. 08 Å) u kalcitu.

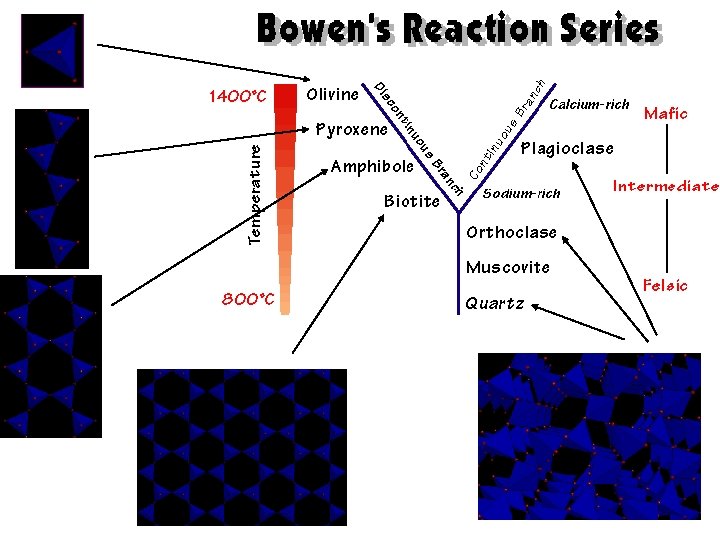
- Zašto je visokotemperaturni olivin obogaćen na forsteritnu komponentu? Forsterit Mg 2 Si. O 4 Tm = 1910°C Fajalit Fe 2 Si. O 4 Tm = 1503°C (Fe, Mg)2 Si. O 4 r (Mg 2+) = 0, 67 Å r (Fe 2+) = 0, 74 Å - Zašto su visokotemperaturni plagioklasi obogaćen na anortitnu komponentu? Anortit Ca. Al 2 Si 2 O 8 Albit Na. Al. Si 3 O 8 Peridotit r (Ca 2+) = 1, 08 Å r (Na+) = 1, 10 Å Z/r Plagioklasi


U kojoj vrsti stijena možemo očekivati beril? Be 3 Al 2(Si. O 3)6 Akvamarin Smaragd

Koeficijent distribucije elemenata Cs – koncentracija elementa u krutoj fazi Cl – koncentracija elementa u taljevini Migmatit Pegmatit

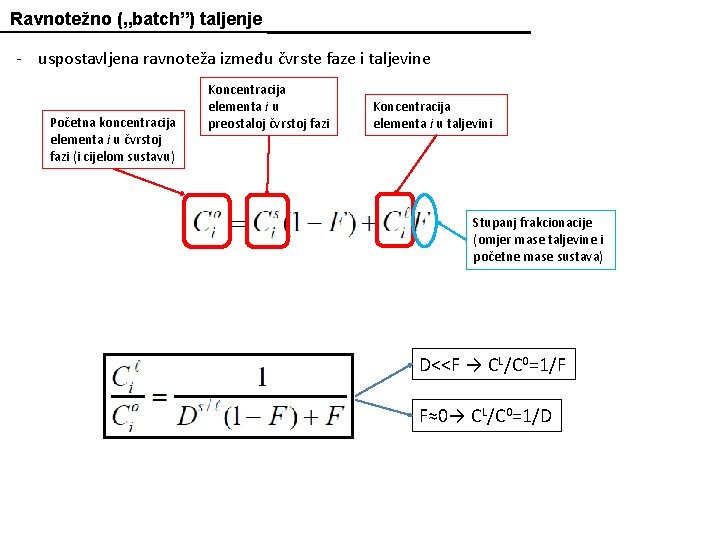
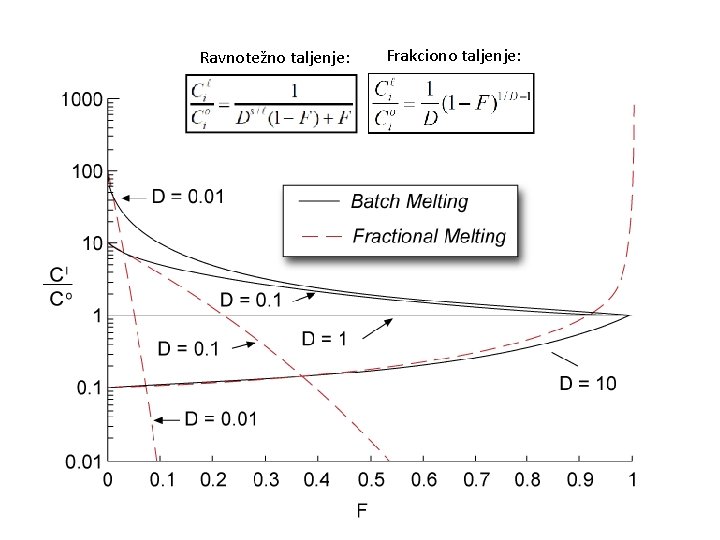
Ravnotežno („batch”) taljenje - uspostavljena ravnoteža između čvrste faze i taljevine Početna koncentracija elementa i u čvrstoj fazi (i cijelom sustavu) Koncentracija elementa i u preostaloj čvrstoj fazi Koncentracija elementa i u taljevini Stupanj frakcionacije (omjer mase taljevine i početne mase sustava) D<<F → CL/C 0=1/F F≈0→ CL/C 0=1/D

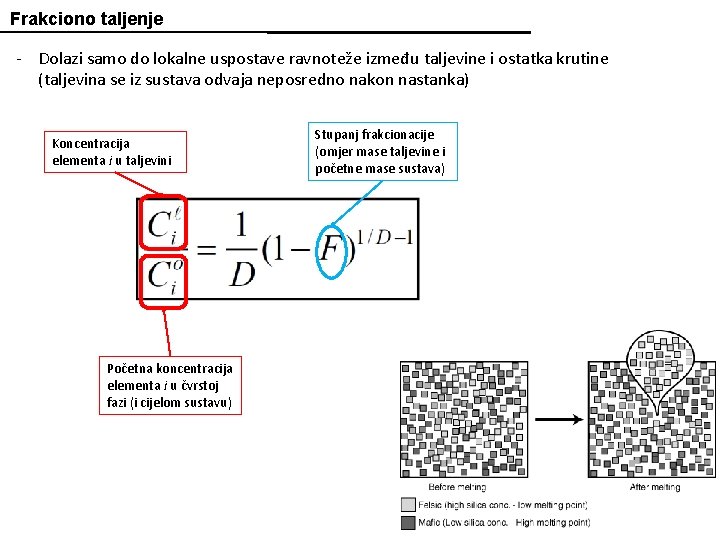
Frakciono taljenje - Dolazi samo do lokalne uspostave ravnoteže između taljevine i ostatka krutine (taljevina se iz sustava odvaja neposredno nakon nastanka) Koncentracija elementa i u taljevini Početna koncentracija elementa i u čvrstoj fazi (i cijelom sustavu) Stupanj frakcionacije (omjer mase taljevine i početne mase sustava)

Ravnotežno taljenje: Frakciono taljenje:
