GENEL KMYA II LABORATUVARI Prof Dr Baki Hazer

GENEL KİMYA II LABORATUVARI Prof. Dr. Baki Hazer Zonguldak Karaelmas Üniversitesi Fen Edebiyat Fakültesi Kimya Bölümü
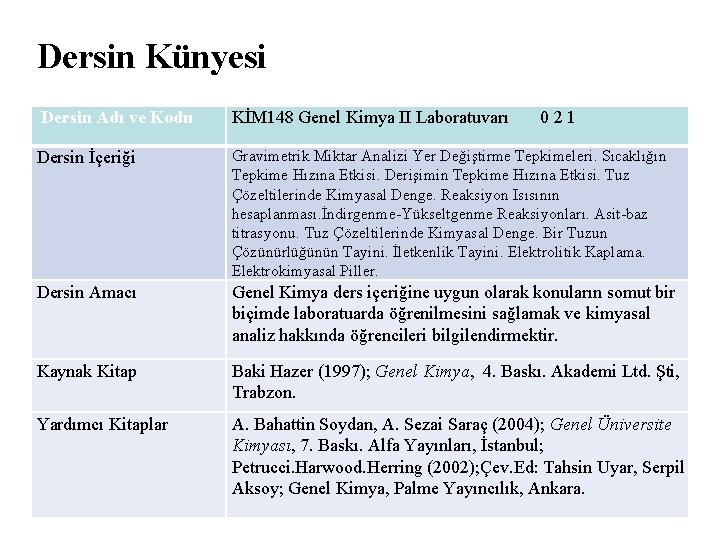
Dersin Künyesi Dersin Adı ve Kodu KİM 148 Genel Kimya II Laboratuvarı 021 Dersin İçeriği Gravimetrik Miktar Analizi Yer Değiştirme Tepkimeleri. Sıcaklığın Tepkime Hızına Etkisi. Derişimin Tepkime Hızına Etkisi. Tuz Çözeltilerinde Kimyasal Denge. Reaksiyon Isısının hesaplanması. İndirgenme-Yükseltgenme Reaksiyonları. Asit-baz titrasyonu. Tuz Çözeltilerinde Kimyasal Denge. Bir Tuzun Çözünürlüğünün Tayini. İletkenlik Tayini. Elektrolitik Kaplama. Elektrokimyasal Piller. Dersin Amacı Genel Kimya ders içeriğine uygun olarak konuların somut bir biçimde laboratuarda öğrenilmesini sağlamak ve kimyasal analiz hakkında öğrencileri bilgilendirmektir. Kaynak Kitap Baki Hazer (1997); Genel Kimya, 4. Baskı. Akademi Ltd. Şti, Trabzon. Yardımcı Kitaplar A. Bahattin Soydan, A. Sezai Saraç (2004); Genel Üniversite Kimyası, 7. Baskı. Alfa Yayınları, İstanbul; Petrucci. Harwood. Herring (2002); Çev. Ed: Tahsin Uyar, Serpil Aksoy; Genel Kimya, Palme Yayıncılık, Ankara.

BİRİNCİ HAFTA Deney No: 1 Gravimetrik Miktar Analizi

Deney No: 1 Gravimetrik Miktar Analizi Kimyasal tepkimelerde, tepkimeye giren ve tepkimede oluşan maddelerin kütleleri arasındaki ilişkilerin bulunmasına stokiyometri denir. Bu deneyde potasyum kloratın mangan dioksit katalizörü ile ısıl bozunması incelenecek ve elde edilen veriler KCl. O 3 ün stokiyometrisinin belirlenmesinde kullanılacaktır. Daha sonra potasyum klorat ve potasyum klorür karışımında ağırlıkça % değerleri belirlenecektir. Potasyum klorat Mn. O 2 ile ısıtılınca aşağıdaki tepkimeye göre ayrışır:

Deney No: 1 Deneyin Yapılışı: A) Potasyum kloratın stokiyometrisinin incelenmesi: Kuru ve temiz bir deney tüpüne bir miktar mangan dioksit koyulur ve tüple birlikte 0, 01 g duyarlılıkla tartılır. Tüpe bir miktar potasyum klorat eklenerek tekrar tartım yapılır. Tüpün çeperlerine hafifçe vurarak tüp içindeki klorat ve katalizörün iyice karışması sağlanır. Karıştırma işleminden sonra tüp bir spora yaklaşık 45 derecelik açı ile tutturularak önce yavaşça sonrasında kuvvetlice ısıtılır. Bek alevinde sıcaklığın en yüksek olduğu konum mavi alevin üst noktasıdır. Isıtma işlemine tüp kırmızılaşıncaya dek devam edilir. Bu noktada tüplerin pyrex cam olduklarından dolayı eriyebilecekleri veya sünebilecekleri unutulmamalıdır. Duruma göre ısıtma işlemine tüpü hafifçe çevirerek devam edilmelidir. Oksijenin tamamen uzaklaştığından emin olmak için tüpün açık kısmına yanık bir kibrit tutulur.

Deney No: 1 Eğer parlak bir alevle yanıyorsa hala oksijen geliyor demektir. Bu durumda ısıtma işlemine devam edilir. Deney sonucunda bek söndürülerek tüpün soğuması beklenir ve numune tartılır. Kütle farklarından stokiyometriler hesaplanır. B) Karışımda bileşenlerin yüzdelerinin belirlenmesi: A şıkkındaki deneysel sıralamanın aynısı potasyum klorat ve potasyum klorür karışımı için tekrarlanır. Tartım sonucu elde edilen verilere dayanarak karışım yüzdesi hesaplanır.

Deney No: 1 Veriler: A) Potasyum kloratın stokiyometrisinin incelenmesi: Tüp + Mn. O 2 kütlesi. . . . Tüp + Mn. O 2 + KCl. O 3 kütlesi. . . Isıtma sonunda tüp katalizör ve kalanın kütlesi. . . . . B) Karışımda bileşenlerin % lerinin belirlenmesi: Tüp + Mn. O 2 kütlesi. . . . Tüp + Mn. O 2 + karışım kütlesi. . . Isıtma sonunda tüp katalizör ve kalanın kütlesi. . . . .

Deney No: 1 Hesaplama ve Sonuçlar A) Potasyum kloratın stokiyometrisinin incelenmesi: Kaybolan oksijenin kütlesi. . . . Kaybolan oksijenin mol sayısı. . . . . . Potasyum kloratın kütlesi. . . . Cl un mol sayısı. . . . . K un mol sayısı. . . . .

Deney No: 1 B) Karışımda bileşenlerin % lerinin belirlenmesi: Karışımın kütlesi. . . . . Kaybolan oksijenin kütlesi. . . . KCl ün kütlesi. . . . . Kaybolan oksijenin mol sayısı. . . Potasyum kloratın mol sayısı. . . Bilinmeyen numunedeki KCl ün kütlesi. . . . . KCl ve KCl. O 3 ın kütlece yüzde bileşimi. . . . .

İKİNCİ HAFTA Deney No: 2 Yer Değiştirme Reaksiyonlarının İncelenmesi

Deney No: 2 Yerdeğiştirme Tepkimeleri Önce, birçok bileşiğin formülü, ismi, fiziksel hali, rengi, kokusu, kristal yapısı ve çözünürlüğü ile ilgili gözlem yapılır. Tepkimeye giren tüm katyonların anyonlarının değişmesi sonucu oluşan tepkimelere metatez tepkimeleri denir. Metatez tepkimelerinin gelişimini sistematik olarak inceleyebilmek için gözlem yapmak ve tepkime denklemlerini yazmamız gerekir. Örnek olarak aşağıdaki denklem verilebilir:

Deney No: 2 Çözeltide tepkimeye giren maddeler tepkime başlamadan önce ayrı tüplerde çözücüde çözülür. Maddelerin çözülüp çözülmediğini gözlemlenir. Çözülüyorsa iyonlar çözeltide hidratlaşmış şekilde yazılır. Tepkimenin olduğunu gösteren belirtiler aşağıdaki özellikler gözlemlenerek söylenir. 1. Çökelek oluşumu 2. Gaz çıkışı 3. Isı alış verişi 4. Renk değişimi 5. Asit-bazlıkta değişim Tepkime sonucu çözeltide oluşan ürünlerin formülleri tepkimeye giren maddeler sulu çözeltide araya gelince oluşan ürünlerin formülleri yazılır.

Deney No: 2 Çökelek oluşumu alt indis(k), iyonik halde çözeltide kalanlar alt indis (su) şeklinde gösterilir. İyonik denklem: Tepkimeye giren ve tepkime sonucu oluşan maddeler bir araya getirilir ve tepkime denklemi yazılır. Net iyonik denklem: Burada tepkimenin oluşumunda sorumlu olan iyonlar tepkime denkleminde görülür. Diğer iyonlar net tepkime denkleminde görünmez.

Deney No: 2 Deneyin Yapılışı: Deney tüpleri 1 den 11 e kadar etiketlenir. Tüplere sırayla; 1. tüpe katı Ca. CO 3 yazılır ve tüpe spatülün ucuyla katı Ca. CO 3 koyulur. 2. tüpe 3 M, 2 m. L Na. OH 4. tüpe 0, 1 M, 2 m. L Fe. Cl 3⋅6 H 2 O 5. tüpe 0, 1 M, 2 m. L Co. Cl 2⋅6 H 2 O 6. tüpe katı NH 4 Cl 7. tüpe 0, 1 M, 2 m. L Na 2 CO 3 8. tüpe 0, 1 M, 2 m. L Ni. Cl 2⋅6 H 2 O 9. tüpe 0, 1 M, 2 m. L Na 3 PO 4⋅12 H 2 O 10. tüpe 0, 1 M, 2 m. L Cu. SO 4⋅5 H 2 O 11. tüpe 0, 1 M, 2 m. L Ba. Cl 2⋅2 H 2 O

Deney No: 2 On bir adet metatez tepkimesi incelenecek, tepkimelerin denklemleri, formülleri ve çözeltideki iyonları yazılacaktır. Her kimyasal maddenin kristal özellikleri, renkleri, çözünürlükleri belirtilir. Gözlemler her tepkime için ayrı kaydedilir. Bu parametreler tepkime olduğunu gösteren renk değişimi, koku, çökelek, ısı değişimi, gaz çıkışı ve benzeri şeylerdir. Yapılacak işlem sırası aşağıdaki gibidir: 1. HCl asit çözeltisinin yarısı katı Ca. CO 3 e ilave edilir. 2. Na. OH çözeltisinin 1/3 nü HCl çözeltisine ilave edilir. 3. Na. OH çözeltisinin yarısı NH 4 Cl çözeltisine ilave edilip, tüp elin sıcaklığı ile ısıtılır ve tüpün ağzı koklanır. 4. Fe. Cl 3 çözeltisinin yarısı geri kalan Na. OH e ilave edilir. 5. Co. Cl 2 çözeltisinin yarısı Fe. Cl 3 çözeltisine ilave edilir. 6. Cu. SO 4 çözeltisinin 1/3 ünü Na 2 CO 3 çözeltisine ilave edilir. 7. Geri kalan Cu. SO 4 çözeltisinin yarısı Ba. Cl 2 çözeltisine ilave edilir.

Deney No: 2 8. Na 3 PO 4 çözeltisinin yarısı kalan Cu. SO 4 çözeltisine ilave edilir. 9. Ni. Cl 2 çözeltisinin yarısı kalan Na 3 PO 4 çözeltisine ilave edilir. Bilgi için incelenecek tepkimelerde oluşan bazı maddelerin özellikleri ve kullanım alanları aşağıda verilmiştir. • Fe(OH)3 jelatinimsi çökelek, seramikte, lastikte ve camda pigment olarak, susuz bileşikleri mücevhercilikte parlatmada kullanılır. • Cu. CO 3·Cu(OH)2 tohum iyileştirmede, boyada kullanılır. • Ni. CO 3·Ni(OH)2 seramikte renklendirici olarak kullanılır. • Ba. SO 4 fotoğraf kağıdında, betonda, radyasyon yalıtıcı olarak kullanılır. • Cu(PO 4)2 gübre, fosforik asidin paslandırma etkisinin geciktirilmesinde kullanılır. • NH 3 nitrik asit üretiminde, gübre, patlayıcı yapımında ve fiberlerde kullanılır.
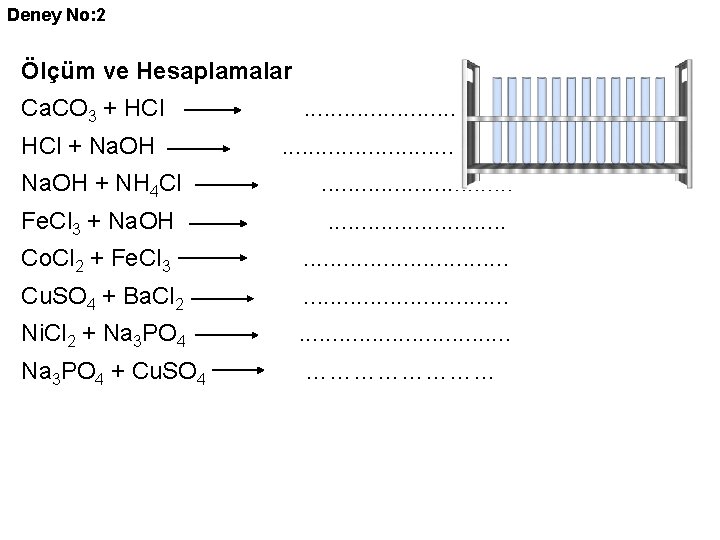
Deney No: 2 Ölçüm ve Hesaplamalar Ca. CO 3 + HCl + Na. OH . . . . Na. OH + NH 4 Cl . . . . Fe. Cl 3 + Na. OH . . . . Co. Cl 2 + Fe. Cl 3 . . . . Cu. SO 4 + Ba. Cl 2 . . . . Ni. Cl 2 + Na 3 PO 4 . . . . Na 3 PO 4 + Cu. SO 4 …………

ÜÇÜNCÜ HAFTA Deney No: 3 Sıcaklığın Tepkime Hızına Etkisi

Deney No: 3 Sıcaklığın Tepkime Hızına Etkisi Reaksiyona giren maddelerin hangi hızla ürünlere dönüştüğünü, bu dönüşümde ortaya çıkan fiziksel ve kimyasal özelikleri ve moleküllerin reaksiyona girdiklerinde birbiriyle nasıl etkileştiklerini kimyasal kinetik inceler. Bir reaksiyonun olabilmesi için reaksiyona giren atomların, moleküllerin veya iyonların birbiriyle çarpışmaları ve ayrıca çarpışan taneciklerin belli bir hıza sahip olmaları gerekir. Dolayısıyla bir reaksiyonun hızı derişime, sıcaklığa ve basınca bağlıdır. Katalizörler de ayıca reaksiyon hızını seçimi bir yönde arttırmak için kullanılır.

Deney No: 3 Arrhenius’a göre her molekül çarpışınca reaksiyon vermez, ancak aktifleşme enerjisi denen minimum enerjiye sahip olan moleküller çarpışınca reaksiyon verebilir. Reaksiyon için gerekli aktifleşme enerjisine sahip moleküllerin sayısı da sıcaklıkla artar. Dolayısıyla sıcaklıkla reaksiyon hızı artmaktadır. Deneyin Yapılışı: Bu deneyde potasyum permanganat ile okzalik asit reaksiyonu asidik ortamda yürür. Bu yüzden ortam p. H ı sülfürik asit ile düşürülmüştür. Reaksiyon sonunda permanganatın pembe renginin sıcaklığa karşın değişimi gözlemlenecektir. Reaksiyon denklemi aşağıda gösterilmiştir.

Deney No: 3 5 deney tüpünün her birine 5× 10− 4 M lık potasyum permanganat çözeltisinden 5 er m. L ve 0, 25 M’lık sülfürik asit çözeltisinden 1 er m. L konulur. Ayrıca 5 tüp daha alınır ve tüplerin her birine 2, 5× 10− 3 M lık okzalik asit çözeltisinden 9 ar m. L konulur. İçinde permanganat çözeltisi bulunan tüplerden biri ile okzalik asit bulunan tüplerden biri, içinde 25ºC de su bulunan 250 m. L’lik behere daldırılır. Bu sabit sıcaklıktaki su banyosunda tüpler 5 dk tutulur. Çabuk ve dikkatlice tüpteki okzalik asit permanganat çözeltisine aktarılır. Reaksiyon sona ermesi için geçen süre ölçülür. Bu süre içinde tüpün sıcaklığı 25ºC de tutulmalıdır. Tüpler 25ºC deki sabit sıcaklık su banyosundan çıkartılarak banyonun sıcaklığı 35ºC ye yükseltilir. Permanganat ve okzalik asit tüplerinden birer tane alınarak deney tekrarlanır.

Deney No: 3 Deney 45ºC, 55ºC ve 65ºC de yinelenir. Sonuçlar ve Değerlendirme: a) 25ºC’ da rengin kaybolması için geçen süre. . . 35ºC’ da rengin kaybolması için geçen süre. . . . 45ºC’ da rengin kaybolması için geçen süre. . . . 55ºC’ da rengin kaybolması için geçen süre. . . . 65ºC’ da rengin kaybolması için geçen süre. . . . b) sıcaklığın 10ºC artması için reaksiyon hızı hangi çarpan kadar artıyor? 25 -35ºC için. . . . . 35 -45ºC için. . . . . 45 -55ºC için. . . . . 55 -65ºC için. . . . . c) sıcaklığa karşı zamanı gösteren bir grafik çizimi.

DÖRDÜNCÜ HAFTA Deney No: 4 Derişimin Tepkime Hızına Etkisi

Deney No: 4 Derişimin Tepkime Hızına Etkisi Teori: Kimyasal reaksiyonlar, çok yavaş, oldukça hızlı veya hızlı gerçekleşebilirler. Reaksiyonların hızlarını etkileyen en temel neden, reaksiyona giren maddelerin özellikleridir (yapısal etken). Ancak reaksiyon hızları yapısal etken dışındaki kriterlerle de değişebilirler. Çeşitli dış etkenlere göre, reaksiyona giren maddelerin çarpışma sayıları, yada reaksiyona ilişkin aktivasyon enerjileri (etkinleşme enerjileri) farklılaşabilir. Buna göre reaksiyon hızlarını etkileyen başlıca faktörler:

Deney No: 4 • Yapısal Etkenler • Sıcaklık • Derişim (veya basınç) • Reaktant tanecikleri arasındaki temas yüzeyi (yüzey alanı ve karıştırma hızı) • Katalizörler Reaksiyon hızı bir reaksiyonda birim hacimde ve birim zamanda dönüşmeye uğrayan maddenin mol sayısı olarak tanımlanabilir. Hacim birimi genel olarak litre, zaman birimi de saniye, dakika, saat veya gündür. Bazı reaksiyonlar o kadar hızlı olur ki, hızlarını ölçmek pratik olarak mümkün değildir. Örneğin O 2 ve H 2 gazları bir kıvılcım yardımı ile ani olarak reaksiyona girerler.

Deney No: 4 Yine kuvvetli bir asit kuvvetli bir bazla çok hızlı olarak nötralleşme reaksiyonu verir. Bu reaksiyonlar çok hızlıdırlar ve ölçülemezler. Diğer bazı reaksiyonlar, o kadar yavaş cereyan eder ki, zamanla hiçbir dönüşme gözlenmeyeceği için bunların hızı da pratik olarak ölçülemez. Örneğin O 2 ve H 2 gazları bir kapta beraber bulunsalar, bu karışım yıllarca beklese bir reaksiyon gerçekleşmez veya reaksiyon o kadar yavaştır ki, ne harcanan gaz miktarını ne de oluşan su miktarını ölçmek mümkün değildir. Bazı inorganik reaksiyonlar vardır ki normal bir hızla olurlar ve bu reaksiyonların hızlarının ölçülmesi mümkündür. Bu tip reaksiyonlarda reaksiyona katılan maddeler tamamen harcanırlar. Reaksiyonun hızına konsantrasyon, sıcaklık, ve katalizör etki eder.

Deney No: 4 Deneyin Yapılışı A) Derişimin Reaksiyon Hızına Etkisi: Bir büret (100 m. L) 0, 2 M KI çözeltisi ile, aynı büyüklükteki diğer büret 0, 1 M (NH 4)2 S 2 O 8 çözeltisi ile doldurulur. Bu çözeltilerin her birinden ayrı tüplere dikkatli bir şekilde 20 m. L çözelti koyulur. Na 2 S 2 O 3 çözeltisinin konsantrasyonu 0, 005 M dır. Beherdeki tiyosülfat çözeltisi içine 3 damla nişasta indikatörü ilave edilir ve bir termometre beher içine daldırılır. Daha önce büretten deney tüplerine 20 m. L olarak alınmış olan I ve peroksidisülfat çözeltileri beherde karışırken kronometre ayarlanır. Çözelti karıştırılır ve çözelti sıcaklığı dikkatli bir şekilde tespit edilir. İki farklı tüpteki 20 m. L çözelti behere ilave ettikten sonra mavi renk oluşana kadar geçen zaman saptanır. Sıcaklık, mavi renk oluşması için geçen zaman ve kullanılan çözeltilerin hacmi kaydedilir.

Deney No: 4 Aynı deney tabloda verilen azaltılmış iyodür ve peroksidisülfat çözeltileri kullanarak tekrar edilir. Her deneyde tiyosülfat 10 m. L ve nişasta 3 damla alınır. Toplam hacmi sabit tutmak için KCI ve (NH 4)2 SO 4 çözeltiler kullanılır. Toplam iyon şiddetini aynı tutmak için saf su yerine KCI ve (NH 4)2 SO 4 çözeltileri tercih edilir.

Deney No: 4 Her bir deney için I, S 2 O 32− ve S 2 O 82− iyonlarının başlangıç konsantrasyonları hesaplanır. Reaksiyonun hızı şu şekilde ifade edilebilir. Ölçülen zaman 2, 5× 10− 5 mol S 2 O 82− iyonun 50 m. L de reaksiyona girmesi için gerekli zamandır. Bu nedenle reaksiyonun hızı S 2 O 82− cinsinden ifade eldir. Örneğin 2, 5× 10− 5 mol S 2 O 82− iyonunun 50 m. L çözelti içinde reaksiyona girmesi için gerekli zaman 10 dakika olsun. Bu zaman esasında Δ (S 2 O 8 2−) = -5× 10− 4 mol/L dir. Bu zaman esnasındaki ortalama hız;

Deney No: 4 Reaksiyon hızı değişen konsantrasyonlara karşı grafiğe geçirilebilir. (1, 4 ve 5 deneyler için I− iyonu ve 1, 2, 3 deneyler için S 2 O 82− iyonu). Veriler ve Sonuçlar: Reaksiyon Hızına Konsantrasyonun Etkisi:

BEŞİNCİ HAFTA Deney No: 5 Tuz Çözeltilerinde Kimyasal Dengenin İncelenmesi

Deney No: 5 Tuz Çözeltilerinde Kimyasal Denge Bir kimyasal tepkimede, dengenin konumu ortamın p. H sı ve derişimle değişebilir. Bu değişim çözeltinin renk farkından izlenebilir. Çoğu kimyasal tepkime tamamen ürüne dönüşmez. Bu deneysel teknik ve düzenlemelerin bir sonucu değil tamamen tepkimenin özelliklerinden kaynaklanmaktadır. Başlangıçta tepkime ürüne dönüşmeye başlar ama bir süre sonra tepkimeye girenlerin ve tepkimede oluşan ürünlerin derişimleri sabit kalır. Bu noktada artık tepkimeye giren maddelerin ürüne dönüşme hızı, ürünlerin tepkimeye girenlere dönüşme hızına eşittir.

Deney No: 5 Diazotetraoksitin oluşma hızı azotoksidin oluşma hızına eşittir. Tepkimede dengeye her iki taraftan da başlanarak ulaşılabilir. Dengeye dışarıdan bir etki olduğu zaman, denge bu etkiyi yok edecek şekilde davranır (Le Chatelier). Bu deneyde çeşitli dengeler incelenecektir. 1 - Kromat – Bikromat dengesi, Bir kromat tuzu suda çözünürse çözeltide hem kromat (Cr. O 42−) hem de bikromat (Cr 2 O 72−) iyonları bulunur. Kromat iyonlarının rengi sarı, bikromat iyonlarının rengi turuncudur. Bu denge tepkimesi ortamın p. H sından etkilenir.

Deney No: 5 2 - Az çözünen tuzların çözünürlük dengesi, Az çözünen tuzlar çözeltide bir dengeye kadar iyonlarına ayrışır. Ortamın p. H sı iyonlaşma dengesini etkiler. 3 - Kompleks dengeleri, Co. Cl 2 suda çözünür ve Co 2+ iyonları su ile pembe renkli oktahedral (koordinasyon sayısı altı) bir kompleks oluşturur. [Co(H 2 O)6]2+. Su yerine etilalkol çözücü olarak kullanılırsa mavi renkli tetrahedral (koordinasyon sayısı dört) olan bir kompleks oluşturur. [Co. Cl 4]2−. Alkolün içerisinde az miktarda su bulunursa çözeltide her iki kompleks de bulunur. Ortamdaki klor ve su derişimlerine bağlı olarak dengenin konumu değişebilir.

Deney No: 5 Deneyin Yapılışı: 1 - Kromat – Bikromat dengesi: İki deney tüpüne 20 şer damla 0, 3 M Na 2 Cr. O 4 çözeltisi koyulur ve çözeltilerin renklerine dikkat edilir. Tüplerden birine damla 0, 3 M Na. OH (5 damla), diğerine 0, 3 M HCl ilave edilir. Her damladan sonra tüpler çalkalanarak renk değişimleri kaydedilir. Tepkime denklemleri yazılarak dengenin değişimi açıklanır. Denklem. . . . . Değişim. . . . . 2 - Az çözünen tuzların çözünürlük dengesi: Bir deney tüpüne 20 damla 0, 3 M Na 2 Cr. O 4 çözeltisi koyulur. Bu çözeltiye 5 damla 0, 1 M Ba. Cl 2 ilave edilir. Oluşan tepkime ve reaksiyonu açıklanır. Denklem. . . . . Değişim. . . . .

Deney No: 5 Çözeltiye damla 0, 3 M HCl ilave edilir (5 damla). Oluşan tepkime ve reaksiyonu açıklanır. Denklem. . . . . Değişim. . . . . Çözeltide Ba. Cr. O 4 ü çöktürmek için çözeltiye ne ilave edilmelidir? . . . . . 3 - Kompleks dengeleri: Co. Cl 2 nin etanoldeki çözeltisinden 20 damla bir tüpe konur. Rengine dikkat edilir. Bu çözeltinin üzerine damla saf su ilave edilir. Renk değişimi gözlemlenir. Denge akua ve klor kompleksleri yönünde nasıl değişmektedir? Saf su ilave edilen tüpe yeniden çözelti mavi renge dönünceye kadar derişik HCl ilave edilir. Denge akua kompleksi yönünde ekzotermiktir. Pembe akua kompleksi buz banyosunda soğutulursa tepkimenin kloro kompleksi yönüne kaydığı görülür.

Deney No: 5 Alkoldeki kobalt kompleksine su ilave edildiğinde akua kompleksi (pembe) oluşur. Bu kompleks sıcak su banyosunda ısıtılırsa tepkimenin tetraklorokobaltat (mavi) kompleksi yönüne kaydığı görülür. Denklem. . . . . Değişim. . . . .

ALTINCI HAFTA Deney No: 6 Reaksiyon Isısının Hesaplanması

Deney No: 6 Reaksiyon Isısının Hesaplanması Teori: Deneyde reaksiyon ısısı, molar ısı kapasite, spesifik ısı ve kalorimetre kavramlarını irdelenecek ve bir reaksiyon ısısı hesaplanacaktır. Termodinamik, fiziksel ve kimyasal olaylara eşlik eden enerji değişimlerini inceler. Kimyasal termodinamiğin yasaları, belirli koşullarla belirli bir kimyasal tepkimenin kuramsal olarak oluşup oluşmayacağını önceden tahmin etmemizi sağlar. Tepkime ısısı, sabit sıcaklık ve sabit basınçta yürüyen bir kimyasal tepkimede sistem ile çevresi arasında alınıp verilen ısı miktarıdır. Tepkime ısıları deneysel olarak kalorimetre denilen ve ısı miktarını ölçen aletlerle belirlenir. Bir tepkime yalıtılmış bir sistemde gerçekleşirse yani çevresi ile madde ve enerji alışverişinde bulunmazsa, tepkime sistemin ısısal enerjisinde değişme meydana getirir ve sıcaklık artar yada azalır.

Deney No: 6 Yaratılmış bir sistemde sıcaklık artışına neden olan yada yalıtılmamış bir sistemde çevreye ısı veren bir tepkimeye ekzotermik tepkime denir. Ekzotermik bir tepkimede, tepkime ısısı negatif (qtep<0) bir büyüklüktür. Yalıtılmış bir sistemde sıcaklığın azalmasına neden olan yada yalıtılmamış bir sistemde çevreden ısı alan bir tepkimeye de endotermik tepkime denir. Bu durumda tepkime ısısı pozitif (qtep>0) bir büyüklüktür. Isı, sıcaklık farkından ileri gelen enerji alışverişidir. Sıcak bir cisimden soğuk bir cisme enerji aktarımı ısı şeklinde olur. Bir sistemin sıcaklığını bir derece değiştirmek için gerekli ısı miktarına o sistemin ısı kapasitesi denir. Sıcaklık değişimi: Burada Ts son sıcaklık, Ti ilk sıcaklıktır.

Deney No: 6 Sistemin sıcaklığı artarsa Ts>Ti dir ve ΔT pozitiftir. q nun pozitif olması ısısın soğurulduğunu, ada sistem tarafından kazanıldığını belirtir. Sistemin sıcaklığı azalırsa (Ts<Ti) ΔT negatiftir. Negatif q ısı açığa çıktığını yada ısı kaybedildiğini gösterir. Termodinamiğin birinci yasası enerjinin korunumu yasasıdır. Sistem ve çevresi arasındaki etkileşimlerde toplam enerji sabit kalır. Diğer bir deyişle evrenin toplam enerjisi sabittir. Bu yasa aşağıdaki gibi formülle edilebilir. qsistem + qçevre = 0 Buna göre, sistemin kaybettiği ısı çevresi tarafından kazanılır, çevrenin kaybettiği ısı sistem tarafından kazanılır. Yani: qsistem = - qçevre

Deney No: 6 Reaksiyon Isılarının Ölçülmesi: Isı miktarını hesaplayabilmek için ısı kapasitesinin bilinmesi gerekir. Isı kapasitesi faz geçişlerinin olmadığı sıcaklık aralıklarında iki türlü tanımlanır. 1) Molar ısı kapasitesi: Bir mol maddenin sıcaklığını 1 K veya 1ºC yükseltmek için gerekli olan ısı miktarıdır. Birimi J/Kmol dür. 2) Spesifik ısı: Bir gram maddeyi 1 K veya 1ºC yükseltmek için gerekli olan ısı miktarıdır. Birimi J/Kg dır. ΔT=Ts-Ti (1) Bu durumda bir cismin aldığı veya verdiği ısı iki farklı şekilde hesaplanabilir. Isı(q) = mol sayısı × molar ısı kapasitesi × ΔT (2) Isı(q) = kütle × spesifik ısı × ΔT (3)

Deney No: 6 Kalorimetreler: Reaksiyon ısıları ölçmek için kullanılan aletlerdir. Gerek sabit hacimde (kapalı kaplarda), gerek sabit basınçta (açık kaplarda, atmosfer basıncında) reaksiyon ısıları ölçülerek ΔE (iki halin iç enerjileri arasındaki fark) veya ΔH (entalpi değişimi) deneysel olarak hesaplanabilir. Her iki halde de önce kalorimetrenin ısı kapasitesi deneysel olarak belirlenmelidir. Kalorimetrenin kazandığı ısı: q(J) = kalorimetre ısı kapasitesi (J/K) ×ΔT(K) (4) bağıntısı kullanılarak kalorimetrenin ısı kapasitesi hesaplanır. Bu hesap yapıldıktan sonra kalorimetre ısı kapasitesi yerine konarak reaksiyon ısıları sadece kalorimetre içindeki sıcaklık yükselmesi (veya azalması) okunarak bulunur. Çözelti kalorimetre laboratuarda bir termos yada alüminyum yaprakla ağzı örtülmüş beherlerden yapılabilir.

Deney No: 6 Deneyin Yapılışı: 1. Isı kapasitesi tayini: Kalorimetrenin ısı kapasitesi tayini için beher tipi kalorimetre kullanılır. (ağzı alüminyum folyo ile kapatılmış 250 m. L’lik beher içinde beher) Önceden tartılan Cu parçası(m. Cu) 30 dakika 100ºC deki etüvde ısıtılır. 250 m. L lik behere 100 gram saf su (msu) konyulur. Bu suyun sıcaklığı bir termometre yardımı ile okunur ve kaydedilir (t 1). 30 dakika sonra bakır parçası etüvden alınır ve bakırın ısısını kaybetmemesi için hemen kalorimetre kabına yerleştirilip son sıcaklığı kaydedilir (t 2). (7) nolu bağıntıyı kullanılarak ısı kapasitesi hesaplanır. 2. Reaksiyon ısısının hesabı: 1. kısımda kullanılan beher boşaltılır ve kurutulur. Bu defa reaksiyon ısısı ölçülecek karışımlar koyulur. Behere 100 gram seyreltik HCl çözeltisi koyulur ve çözeltinin sıcaklığı okunarak kaydedilir (t 1).

Deney No: 6 Önceden tarttılan magnezyum parçası çözeltiye atılarak reaksiyon tamamlanınca sıcaklık okunur (t 2). (8) nolu bağıntı kullanılarak reaksiyon ısısı hesaplanır. Aşağıdaki reaksiyonun reaksiyon ısısı hesaplanacaktır: Hesaplamalar: 1) Termodinamiğin birinci kanununa göre kaybedilen ısı kazanılan ısıya eşit olmalıdır. Bir başka değişle kazanılan ve 2) kaybedilen ısıların toplamı sıfır olmalıdır. 3) q bakırın kaybettiği = q suyun kazandığı + q kalorimetrenin kazandığı (6) m. Cu × CCu* × (100 -t 2) = msu × Csu*(t 2 -t 1) + Isı kapasitesi*(t 2 -t 1) (7) * : CCu = 0, 385 J/Kg * : Csu = 4, 18 J/Kg

Deney No: 6 Reaksiyon ısısı = Isı kapasitesi × (t 2 -t 1) + çözeltinin kütlesi × Cçözelti × (t 2 -t 1) (8) Cçözelti = 4, 21 J/Kg Sonuçlar: Beherin ısı kapasitesi: . . . Reaksiyon ısısı: . . . .

YEDİNCİ HAFTA Deney No: 7 İndirgenme-Yükseltgenme Reaksiyonları

Deney No: 7 İndirgenme Yükseltgenme Reaksiyonları Çok sayıda tepkime indirgenme yükseltgenme tepkimeleri olarak sınıflandırılabilir. Bu tepkimeler genelde oksitlenme basamağında değişikliklerin olduğu elektron aktarım tepkimeleridir. Bu tepkimeler sırasında bazen gözle görünür bir değişiklik olmaz. Bu durumda uygun bir test kullanmak gerekir. Bilinen bazı testler aşağıda verilmiştir.
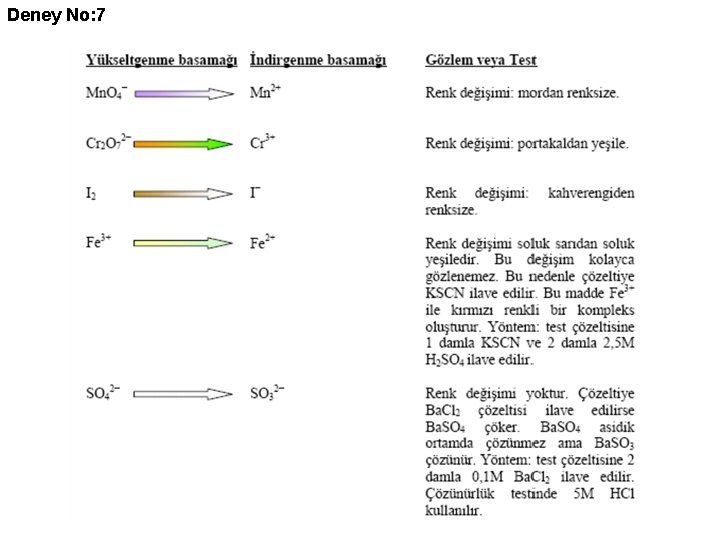
Deney No: 7

Deney No: 7 Deneyin Yapılışı: Demir(II) – Hidrojen peroksit İki tane temiz test tüpüne 5 damla 0, 1 M Fe. SO 4 ve 2 damla 2, 5 M H 2 SO 4 koyulur. Bu test tüplerinden birine 5 damla H 2 O 2 çözeltisi diğerine ise 5 damla saf su damlatılır. Çözeltiler su banyosunda ısıtılır ve değişiklikler gözlenir, tepkime denklemi yazılır. Fe 2+ , H 2 O 2, H+ /. . . . Fe 2+ , H 2 O, H+ /. . . . . İyot – Hidrojen peroksit İki tane temiz test tüpüne 2 damla 2, 5 M H 2 SO 4 ve 5 damla 0, 5 M KI koyulur. Bu test tüplerinden birine 5 damla H 2 O 2 çözeltisi diğerine ise 5 damla saf su damlatılır. Çözeltiler su banyosunda ısıtılır ve değişiklikler gözlenir, tepkime denklemi yazılır. I−, H 2 O 2, H+ /. . . . I−, H O, H+ /. . . . .

Deney No: 7 Permanganat – Mangan(II) Üç tane temiz test tüpüne 5 damla 0, 1 M KMn. O 4 çözeltisi koyulur. Bu test tüpleri 2 şer damla derişik H 2 SO 4 ile asidik hale getirilir. Bu çözeltilerden birine 5 damla 0, 1 M Fe. SO 4 damlatılır. Diğer çözeltiye 5 damla H 2 O 2 çözeltisi ilave edilir. Son tüpe ise 5 damla 0, 1 M Na 2 SO 3 eklenir. Değişiklikler gözlenir ve tepkime denklemi yazılır. KMn. O 4, H 2 O 2, H+ /. . . . KMn. O 4, Fe. SO 4, H+ /. . . . Dikromat – Krom(III) İki tane temiz test tüpüne 5 damla 0, 1 M K 2 Cr 2 O 7 çözeltisi koyulur. Bu test tüpleri derişik H 2 SO 4 ile asidik hale getirilir. Tüplerin birine 5 damla 0, 1 M Fe. SO 4 , diğerine 0, 5 M KI çözeltisinden 2 damlatılır. Değişiklikler gözlenir, tepkime denklemi yazılır. Fe. SO 4, K 2 Cr 2 O 7, H+ /. . . . K 2 Cr 2 O 7, KI, H+ /. . . .

SEKİZİNCİ HAFTA Deney No: 8 Bazı Tuzların Asitlerle Reaksiyonu

Deney No: 8 Bazı Tuzların Asitlerle Reaksiyonu Hidrojen, H 2 Renksiz ve kokusuzdur. Hava ile patlayıcı bir karışım oluşturur. Test tüpünün ağzına yanan bir kibrit yaklaştırılırsa farklı bir ses duyulur. Karbondioksit, CO 2 Renksiz ve kokusuzdur. Gaz Ca(OH)2 çözeltisinden geçirilirse Ca. CO 3 çökeltisi oluşur. Bu durum berrak çözeltinin bulanıklaşması şeklinde gözlenir. Azot dioksit, NO 2 Renksiz, çok ağır kokulu ve zehirli bir gazdır. Bir kağıda emdirilmiş dikromat çözeltisi SO 2 ile etkileşirse portakal renkli kağıdın rengi yeşile (Cr. III) döner Azot oksit, NO renksiz bir gazdır. Hava ile temas edince rengi kahverengiye döner.

Deney No: 8 Hidrojen sülfür, H 2 S çürük yumurta kokulu, renksiz ve zehirli bir gazdır. Kurşun asetat kağıdını siyaha çevirir. Oksijen, O 2 Renksiz ve kokusuz bir gazdır. Amonyak, NH 3 Keskin kokulu, renksiz bir gazdır. Turnusol kağıdının rengini maviye çevirir. Azot, N 2 Renksiz ve kokusuz bir gazdır. Varlığını tanımlamak zordur. Deneyin Yapılışı: Deney tüpünün içerisine az bir miktar katı tuz konulur. Bu tuzun üzerine 2, 5 M H 2 SO 4 çözeltisinden 2 damla ilave edilir. Karbonatı test ederken seyreltik HCl kullanılır. Eğer tepkime soğukta oluyorsa deney tüpü su banyosunda ısıtılarak değişiklikler gözlenir. Tepkimelere ait reaksiyonlar yazılır. Aşağıdaki tepkimelerin bazılarında gaz çıkışı olmayabilir.

Deney No: 8 Nitrit: . . . . . Karbonat: . . . . Nitrat: . . . . . Sülfit: . . . . . Kükürt: . . . . . Klorat: . . . . .

DOKUZUNCU HAFTA Deney No: 9 Asit Baz Titrasyonu

Deney No: 9 Asit Baz Titrasyonu p. H bir çözeltinin asitlik özelliğinin göstergesi olup, hidrojen iyonunun aktivitesinin eksi logaritmasına eşittir. p. H = – log [H+] p. H değeri iki farklı ölçüm prensibi ile hesaplanır. Bunlardan birincisi p. H kağıdı kullanılarak uygulanana kolorometrik yöntemdir. Bir diğer yöntem olan elektrometrik metot bir standart hidrojen elektrodu ve bir referans elektrodu kullanan potansiyometrik ölçümle, hidrojen iyonları aktivitesinin belirlenmesidir.

Deney No: 9 Çeşitli maddelerin p. H değerleri: Madde adı. . . . p. H Pil asidi. . . . 1. 0 Mide öz suyu. . . 1. 4 Limon suyu. . . 2. 1 Portakal suyu. . . 2. 8 Kola. . . . 3. 0 Domates suyu. . . 4. 1 Express kahve. . . 5. 0 İdrar. . . . 6. 0 Süt. . . . 6. 8 Distile su. . . . 7. 0 Kan. . . . 7. 3 Sodyum bikarbonat (Na. HCO 3). . . . . 8. 5 Amonyak (NH 3). . . 11. 9
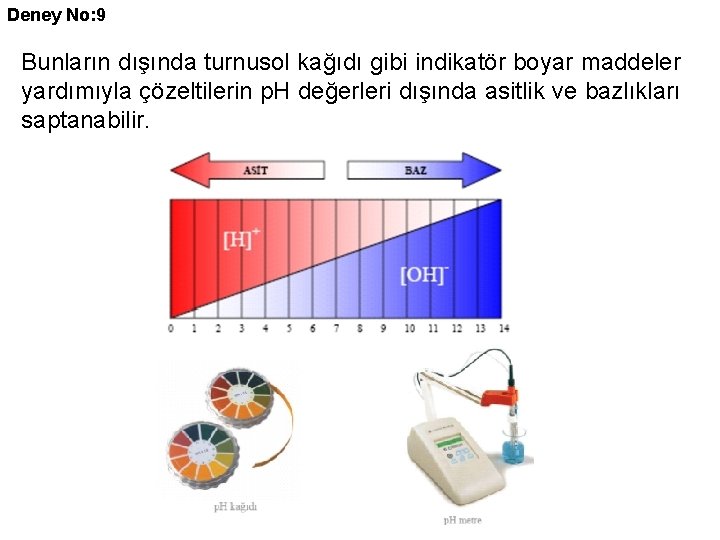
Deney No: 9 Bunların dışında turnusol kağıdı gibi indikatör boyar maddeler yardımıyla çözeltilerin p. H değerleri dışında asitlik ve bazlıkları saptanabilir.

Deney No: 9 Deneyin Yapılışı: 0, 1 M Na. OH ve 0, 1 M Mg(OH)2 bazları 1 er m. L deney tüplerine koyulur. Bu bazların turnusol kağıdına verdikleri renk kaydedilir. Üzerlerine 1 er damla fenolftaleinden damlatılır. 0, 1 M HCl bazların üzerine damla ilave edilir. Her ilaveden sonra renk kayboluncaya kadar tüp çalkalanır. Nötralleşme için gerekli damla sayısı bulunur. Sonra asitleri (0, 1 M HNO 3, 0, 1 M H 2 SO 4) turnusol kağıdına verdiği renk kaydedilerek deney tüplerine koyulur. 1 er damla fenolftalein damlatılır. 0, 1 M Na. OH damla ilave edilerek nötralleşme olduğu anda damla sayısı bulunur. Reaksiyon denklemleri yazılır.
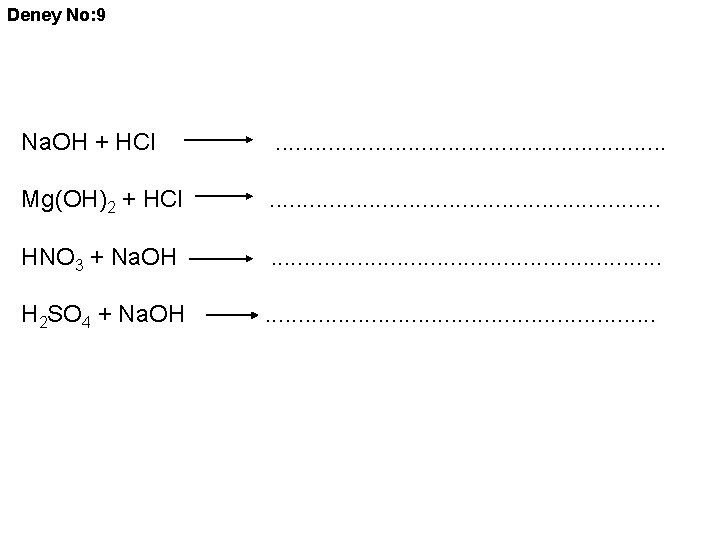
Deney No: 9 Na. OH + HCl . . . . Mg(OH)2 + HCl . . . . HNO 3 + Na. OH . . . . H 2 SO 4 + Na. OH . . . .

ONUNCU HAFTA Deney No: 10 Tuz Çözeltilerinde Kimyasal Denge

Deney No: 10 Tuz Çözeltilerinde Kimyasal Denge Bir kimyasal tepkimede, dengenin konumu ortamın p. H sı ve derişimle değişebilir. Bu değişim çözeltinin renk farkından izlenebilir. Çoğu kimyasal tepkime tamamen ürüne dönüşmez. Bu deneysel teknik ve düzenlemelerin bir sonucu değil tamamen tepkimenin özelliklerinden kaynaklanmaktadır. Başlangıçta tepkime ürüne dönüşmeye başlar ama bir süre sonra tepkimeye girenlerin ve tepkimede oluşan ürünlerin derişimleri sabit kalır. Bu noktada artık tepkimeye giren maddelerin ürüne dönüşme hızı, ürünlerin tepkimeye girenlere dönüşme hızına eşittir.

Deney No: 10 Diazotetraoksitin oluşma hızı azotoksidin oluşma hızına eşittir. Tepkimede dengeye her iki taraftan da başlanarak ulaşılabilir. Dengeye dışarıdan bir etki olduğu zaman, denge bu etkiyi yok edecek şekilde davranır (Le Chatelier). Bu deneyde çeşitli dengeler incelenecektir. 1 - Kromat – Bikromat dengesi, Bir kromat tuzu suda çözünürse çözeltide hem kromat (Cr. O 42−) hem de bikromat (Cr 2 O 72−) iyonları bulunur. Kromat iyonlarının rengi sarı, bikromat iyonlarının rengi turuncudur. Bu denge tepkimesi ortamın p. H sından etkilenir.

Deney No: 10 2 - Az çözünen tuzların çözünürlük dengesi, Az çözünen tuzlar çözeltide bir dengeye kadar iyonlarına ayrışır. Ortamın p. H sı iyonlaşma dengesini etkiler. 3 - Kompleks dengeleri, Co. Cl 2 suda çözünür ve Co 2+ iyonları su ile pembe renkli oktahedral (koordinasyon sayısı altı) bir kompleks oluşturur. [Co(H 2 O)6]2+. Su yerine etilalkol çözücü olarak kullanılırsa mavi renkli tetrahedral (koordinasyon sayısı dört) olan bir kompleks oluşturur. [Co. Cl 4]2−. Alkolün içerisinde az miktarda su bulunursa çözeltide her iki kompleks de bulunur. Ortamdaki klor ve su derişimlerine bağlı olarak dengenin konumu değişebilir.

Deney No: 10 Deneyin Yapılışı: 1 - Kromat – Bikromat dengesi: İki deney tüpüne 20 şer damla 0, 3 M Na 2 Cr. O 4 çözeltisi koyulur ve çözeltilerin renklerine dikkat edilir. Tüplerden birine damla 0, 3 M Na. OH (5 damla), diğerine 0, 3 M HCl ilave edilir. Her damladan sonra tüpler çalkalanarak renk değişimleri kaydedilir. Tepkime denklemleri yazılarak dengenin değişimi açıklanır. Denklem. . . . . Değişim. . . . . 2 - Az çözünen tuzların çözünürlük dengesi: Bir deney tüpüne 20 damla 0, 3 M Na 2 Cr. O 4 çözeltisi koyulur. Bu çözeltiye 5 damla 0, 1 M Ba. Cl 2 ilave edilir. Oluşan tepkime ve reaksiyonu açıklanır. Denklem. . . . . Değişim. . . . .

Deney No: 10 Çözeltiye damla 0, 3 M HCl ilave edilir (5 damla). Oluşan tepkime ve reaksiyonu açıklanır. Denklem. . . . . . Değişim. . . . . Çözeltide Ba. Cr. O 4 ü çöktürmek için çözeltiye ne ilave edilmelidir? . . . . . 3 - Kompleks dengeleri: Co. Cl 2 nin etanoldeki çözeltisinden 20 damla bir tüpe konur. Rengine dikkat edilir. Bu çözeltinin üzerine damla saf su ilave edilir. Renk değişimi gözlemlenir. Denge akua ve klor kompleksleri yönünde nasıl değişmektedir? Saf su ilave edilen tüpe yeniden çözelti mavi renge dönünceye kadar derişik HCl ilave edilir. Denge akua kompleksi yönünde ekzotermiktir. Pembe akua kompleksi buz banyosunda soğutulursa tepkimenin kloro kompleksi yönüne kaydığı görülür.

Deney No: 10 Alkoldeki kobalt kompleksine su ilave edildiğinde akua kompleksi (pembe) oluşur. Bu kompleks sıcak su banyosunda ısıtılırsa tepkimenin tetraklorokobaltat (mavi) kompleksi yönüne kaydığı görülür. Denklem. . . . . Değişim. . . . .

ONBİRİNCİ HAFTA Deney No: 11 Bir Tuzun Çözünürlüğünün Tayini

Deney No: 11 Bir Tuzun Çözünürlüğünün Tayini Teorik Bilgi: Bir tuzun çözünürlüğü, genel olarak belli bir ağırlıktaki çözücüde (genel olarak 100 g) ve belli bir sıcaklıkta kaç gram çözüldüğü dikkate alınarak hesaplanır. Çözünürlüğü etkileyen faktörlerin başında sıcaklık gelir. Doygun bir çözeltinin sıcaklığını azaltmak veya arttırmak, çözücü-çözünen arasındaki dengede bir stres yaratır ve Le Chatelier İlkesine göre dengenin yönü bu stresi azaltıcı doğrultuda kayar. Bu nedenle sıcaklık arttırılınca denge, endotermik yöne; aksine sıcaklık düşürülünce, ekzotermik yöne kayma eğilimi gösterir. İyonik bileşiklerin çoğu sıcaklık artışına paralel bir çözünürlük artışı gösterirler. Zira doygun bir çözeltide daha fazla maddenin çözünmesi, genellikle ek enerji (ısı) girdisi ve yüksek sıcaklık gerektiren endotermik bir süreçtir Sıcaklıkla çözünürlük değişimini bir grafik halinde göstermek daha uygundur.

Deney No: 11 Deneyin Yapılışı: Tuzlardan biri seçilir, Seçtiğiniz tuzdan yaklaşık 8 gr havanda iyice toz haline getirilir. Diğer taraftan, büyük bir deney tüpü (20 cm) uygun 2 delikli bir tıpa ile kapatılır. Deliklerden birine 110°C lik bir termometre geçirilir. Termometrenin ucunun tüpün tabanına değmemesine dikkat edilir. İkinci deliğe bir ucu tüpün içinde kalacak büyüklükte halka yapılmış bakır tel geçirilir. Bakır telin halkası mantar tıpa dışında kalan ucu kullanarak elle kolaylıkla aşağı yukarı hareket ettirilebilmelidir. Bu şekilde hazırlanan deney tüpü tıpası çıkarılarak 0, 01 gr hassasiyetle bir analitik terazide tartılır. İçine toz haline getirilen, çözünürlüğü tayin edilecek kuru maddeden yaklaşık 5 gr kadar koyulur ve analitik terazide hassas olarak yeniden tartılır. Üzerine bir pipet ile dikkatlice 3 m. L saf su ilave edilir ve tüpün tıpası kapatılır. Bu şekilde hazırlanan tüp 400 m. L beher içinde kaynayan suya daldırılır.

Deney No: 11 Tüpün içindeki çözelti su banyosunun içinde kalacak şekilde tüp bir kıskaç ile spora tutturulur ve bütün tuz çözünene kadar tüp içindeki halkalı çubukla karıştırılır. Bu işlem yapılırken termometrenin kırılmamasına dikkat edilir. Kaynayan suyun içindeki tüpte bulunan tuz birkaç dakika içinde tam olarak çözünmezse 1 m. L daha su ilave edilir. Gerekirse her defasında 1 m. L olmak üzere tuz tam olarak çözünene kadar saf su ilavesine devam edilir. Gereğinden fazla su ilave edilmemelidir çünkü çözeltinin doygunluk derecesine çok yakın olması istenir. Tüp kaynayan su içinde gerektiğinden fazla tutulmaz. Bu suretle buharlaşma ile fazla su kaybı engellenmiş olur. Tüpteki tuz tam olarak çözündükten sonra tüp sıcak sudan çıkarılır. Tüpün soğuması sırasında kristallenmenin başlayacağı an dikkatli bir şekilde gözlenir ve kristallenmenin başladığı andaki sıcaklığı tespit edilir.

Deney No: 11 Bu sıcaklık, çözeltinin doygunluk sıcaklığıdır. Doğru bir doygunluk sıcaklığı elde etmek için bu ısıtma, soğutma ve kristallenme sıcaklığının tespiti işlemi birkaç defa tekrarlanmalıdır. Sonrasında tüpe büretten 1 m. L saf su ilave edilir. Tekrar tüp içindeki bütün kristal çözünene kadar kaynayan suyun içinde tutulur. Çözünme işi tamamlanınca tüp sıcak sudan çıkarılır. Devamlı karıştırılarak soğutulur. Yukarıda yaptığımız gibi soğuma esnasında kristalin oluşmaya başladığı sıcaklık doğru bir şekilde tespit edilir. Bu durumda doğru bir doygunluk sıcaklığı elde etmek için ısıtma ve soğutma işlemi birkaç defa tekrarlanır. Bu işlem (1 m. L saf ilavesini) geniş bir sıcaklık aralığını kaplayan en az 5 veya 6 doygunluk sıcaklığı elde edene kadar tekrarlanır. Yani 1 m. L saf su ilave ederek farklı doygunluk sıcaklığı elde etme deneyimi 5– 6 defa yapılır.

Deney No: 11 Eğer 1 m. L saf su ilave ettiğimiz zaman doygunluk sıcaklığı çok düşük bir değer gösterirse diğer deneyleri 1 m. L saf su yerine 0, 5 m. L saf su ilave ederek tekrarlanabilir. Tersine 1 m. L saf su ilavesi doygunluk sıcaklığını çok az düşürmüş ise 1 m. L saf su yerine 2 veya 3 m. L saf su ilave ederek deneyler tekrarlanabilir.

Deney No: 11 Sonuç: Deneyin sonuçlarından yararlanarak ve 1 m. L su ağırlığını 1 gr kabul ederek her doygunluk sıcaklığı için 100 gr suda çözünen tuz miktarı hesaplanır. Çözünürlüğünü tespit ettiğimiz tuz için, bir çözünürlük - sıcaklık grafiği çizilir. Grafikte düşey eksenini 100 g sudaki çözünürlük için, yatay ekseni de doygunluk sıcaklıkları için kullanılır.

ONİKİNCİ HAFTA Deney No: 12 İletkenlik Tayini

Deney No: 12 İletkenlik Tayini İletkenlik, bir çözeltinin elektrik taşıyabilme özelliğinin sayısal ifadesidir. İletkenlik, çözeltideki iyonik türlerin derişimlerine, değerliklerine, taşınırlıklarına, bağıl derişimlerine ve ölçüm sıcaklığına bağlı olarak değişir. İnorganik bileşikler iyi iletkenlik gösterirken, organik bileşikler çok zayıf bir akım geçirir. İletkenlik ölçümü genelde tersi olan direnç ile ohm veya megaohm olarak ölçülür. Bir iletkenin direnci, iletken kesit alanı ile ters orantılı ve uzunluğu ile de doğru orantılıdır. Su örenklerinde ölçülen direnç büyüklüğü de buna benzer şekilde iletkenlik kabı özelliklerine bağlıdır ve bu kaba ait özelliklerin hesaba katılması olmaksızın hiç bir sonuca varılamaz. "İletkenlik" birimi genel olarak μohm/cm dir. Bazen de milisiemens olarak m. S/m şeklinde ifade edilir. Burada, 1 m. S/m = 10 μohm/cm

Deney No: 12 E eşittir. Yeni distile edilmiş su için iletkenlik değeri 0, 5 ila 2 μohm/cm dir. Eğer saf su birkaç hafta bekletilirse iletkenlik değerinin 2 ila 4 μmho/cm e yükseldiği gözlenir. Bu artışa ortamda bulunan CO 2'nin distile suya absorblanması ile açıklanır. İçme suları genelde 50 ila 1500 μohm/cm aralığında özgül iletkenlik değerlerine sahiptir. Elektrolitik iletkenlik her 1ºC derecede %1, 9 mertebesinde değişir. Her iyon sıcaklığa bağlı olarak iletkenlik değerini değiştirir ve bu nedenle, sıcaklığın çok hassas olarak ölçülmesi gerekir. Deneyin Yapılışı a. Kap sabiti tayini: İletkenlik kabı 0, 01 M KCl ile en az üç kere yıkandıktan sonra 0, 01 M KCl ile doldurulur ve sıcaklığı 25, 0 ± 0, 1ºC hassasiyetinde ayarlanır. Direnç değeri (RKCl) ve sıcaklık (tölçülen) kaydedilir ve aşağıdaki formül yardımı ile kap sabitini (C) hesaplanır.

Deney No: 12 b. Özgül iletkenlik ölçümü: İletkenlik kabını numune ile birkaç kez yıkadıktan sonra kabı numune ile doldurulup direnç ve sıcaklık ölçümleri kaydedilir. Hesaplamalar: İletkenlik değeri; formülü ile hesaplanır. Bulunan iletkenlik değeri ayrıca m. S/m cinsinden de ifade edilir. 1 m. S/m = 10 μohm/cm dir

ONÜÇÜNCÜ HAFTA Deney No: 13 Elektrolitik Kaplama
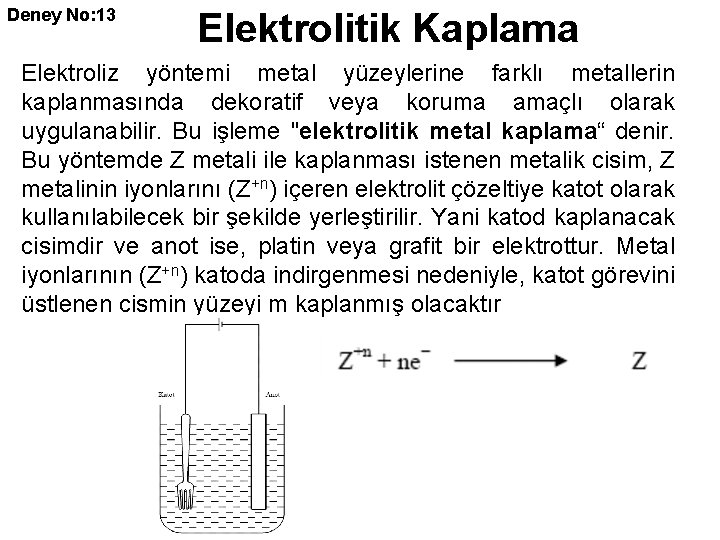
Deney No: 13 Elektrolitik Kaplama Elektroliz yöntemi metal yüzeylerine farklı metallerin kaplanmasında dekoratif veya koruma amaçlı olarak uygulanabilir. Bu işleme "elektrolitik metal kaplama“ denir. Bu yöntemde Z metali ile kaplanması istenen metalik cisim, Z metalinin iyonlarını (Z+n) içeren elektrolit çözeltiye katot olarak kullanılabilecek bir şekilde yerleştirilir. Yani katod kaplanacak cisimdir ve anot ise, platin veya grafit bir elektrottur. Metal iyonlarının (Z+n) katoda indirgenmesi nedeniyle, katot görevini üstlenen cismin yüzeyi m kaplanmış olacaktır

Deney No: 13 Gümüş Kaplama Deneyin Yapılışı Şekildeki deneysel düzenek hazırlanarak, 200 m. L gümüş iyodür kompleks çözeltisi gözenekli kaba aktarılır. Gözenekli kap gümüş kaplama çözeltisini kaplama işlemi sırasında oluşabilen istenmeyen ürünlerden korur. Kaplanacak metalin yüzeyi temizledikten sonra, güç kaynağının eksi kutbuna bir tel aracılığı ile bağlanır. Platin veya grafit elektrot anoda bağladıktan sonra, elektroliz işlemi gerçekleştirilir. Metalin yüzeyinde gümüş kaplanması gözlemlenir.
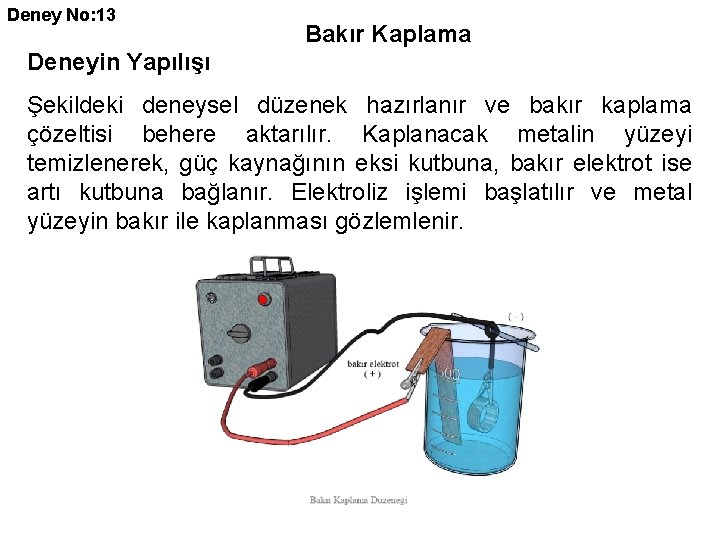
Deney No: 13 Bakır Kaplama Deneyin Yapılışı Şekildeki deneysel düzenek hazırlanır ve bakır kaplama çözeltisi behere aktarılır. Kaplanacak metalin yüzeyi temizlenerek, güç kaynağının eksi kutbuna, bakır elektrot ise artı kutbuna bağlanır. Elektroliz işlemi başlatılır ve metal yüzeyin bakır ile kaplanması gözlemlenir.

ONDÖRDÜNCÜ HAFTA Deney No: 14 Elektrokimyasal Piller

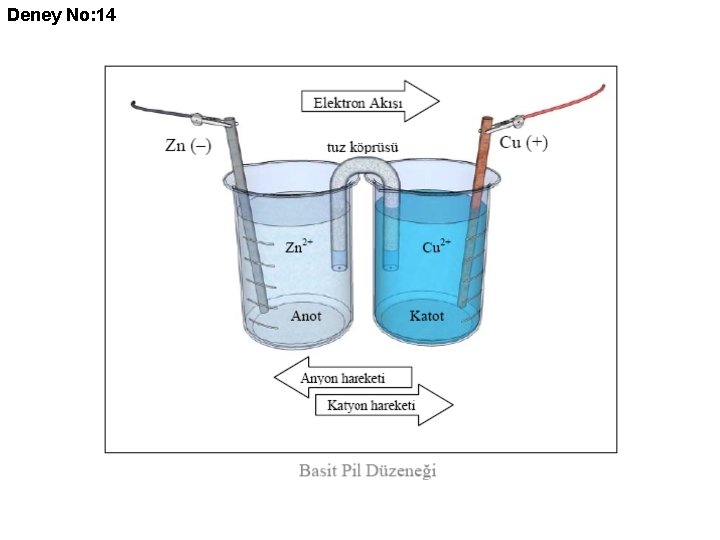
Deney No: 14 Elektrokimyasal Piller İndirgenme-Yükseltgenme tepkimelerinde yükseltgen madde ile indirgen madde birbirleri ile temas halinde aynı kabın içerisindedir ve bu durum indirgen maddeden yükseltgen maddeye doğru elektron aktarımına yol açar. Kimyasal enerjinin elektrik enerjisine dönüştürülmesinde yükseltgenme indirgenme tepkimelerinden yararlanılabilir. Bu tür özel düzeneklere “elektrokimyasal pil” adı verilir ve indirgen madde ile yükseltgen madde iki ayrı kapta bulunur. Alessendro Volta ve Luigi Galvani tarafından geliştirilmiş olan bu türler piller Voltaik veya Galvanik piller olarak adlandırılır. Elektrokimyasal pillerle ilgili temeller şu şekilde sıralanabilir. • İndirgenme yarı reaksiyonu ile yükseltgenme yarı reaksiyonu iki ayrı kapta yürütülür.

Deney No: 14 • Pil düzeneğinde elektrolit çözeltiye batırılan iletken çubuklar (elektrotlar) farklı isimlerle ayırtedilir. İndirgenme yarı tepkimesinin gerçekleştiği elektroda "katot" yükseltgenme yarı tepkimesinin gerçekleştiği elektroda "anot" denir. • Pil düzeneğinde iki elektrotun bir telle bağlanmasından “elektrik akımı”, iki elektrolit çözeltinin bir tuz köprüsü ile bağlanması ile “iyon akımı” gerçekleştirilmiş olur. • Anot ve katod elektrodlarını birbirine bağlayan tele gerilim-akım ölçer (galvanometre) bağlanırsa gerilim farkı veya geçen akımın şiddeti ölçülebilir. • Anot ve katotta gerçekleşen yarı reaksiyonlar toplandığında "pil reaksiyonu" elde edilir.

Deney No: 14 • Eğer pil reaksiyonu standart koşullarda (25°C, 1 atm, 1 M) gerçekleştirilirse ölçülen pil gerilimi "standart pil gerilimi" dir. Katotta oluşan yarı tepkimesine ilişkin standart indirgenme gerilimi (E°K) ile anotta oluşan yarı tepkimeye ilişkin standart indirgenme geriliminin (EºA) farkı ile bir pilin standart gerilimi (ΔE°AH) bulunabilir. Standart pil gerilimi (ΔE°pil) sıfırdan büyük ise pil reaksiyonu kendiliğinden gerçekleşiyor demektir. Örneğin Cu 2+ ile Zn arasındaki pil tepkimesine ait standart gerilimi:

Deney No: 14 Standart pil gerilimini hesaplamak için, hem katot hem de anotta gerçekleşen yarı tepkimelere ait indirgenme gerilimlerinin farkı alınmalıdır. Buna göre anotta gerçekleşen yarı tepkime de indirgenme olarak yazılırsa, (indirgenme gerilimi) olur ve standart pil gerilimi, olarak bulunur.
Deney No: 14

Deney No: 14 Deneyin Yapılışı Dört behere sırasıyla, 1 M Cu. SO 4, 1 M Zn. SO 4, 0, 5 M Cu. SO 4 ve 0, 5 M Zn. SO 4 ile doldurulur. Her bir çözeltini sıcaklıkları kaydedilir. Tuz köprüsü oluşturmak için bir U boru içerisine Doymuş KCl ve agar-agar doldurulur ve uçları cam pamuğu ile kapatılır. Bakır elektrot 1 M Cu. SO 4 çözeltisine ve çinko elektrot 1 M Zn. SO 4 çözeltisine daldırılarak şekildeki düzenek hazırlanır. Akım-gerilim ölçer (avometre) ile değer okunur. Veriler:
- Slides: 90