Genel Kimya 2 lkeler ve Modern Uygulamalar Petrucci










![Çözünürlük ve p. H Örnek sorular ÖRNEK 19 -6 A Deniz suyunda [Ca 2+]≈0, Çözünürlük ve p. H Örnek sorular ÖRNEK 19 -6 A Deniz suyunda [Ca 2+]≈0,](https://slidetodoc.com/presentation_image/2870a21d96663a61330e7fd094b1b2f0/image-14.jpg)










![Bakır(II) Üzerine Bir Test [Cu(H 2 O)4]2+(aq) + 4 NH 3(aq) → [Cu(NH 3)4]2+(aq) Bakır(II) Üzerine Bir Test [Cu(H 2 O)4]2+(aq) + 4 NH 3(aq) → [Cu(NH 3)4]2+(aq)](https://slidetodoc.com/presentation_image/2870a21d96663a61330e7fd094b1b2f0/image-27.jpg)


- Slides: 29

Genel Kimya 2 İlkeler ve Modern Uygulamalar Petrucci • Harwood • Herring 8. Baskı Konu 19: Çözünürlük ve Kompleks-İyon Dengeleri Philip Dutton University of Windsor, Canada N 9 B 3 P 4 Prentice-Hall © 2002 ⇄ ⇌ ‾ + ÷ ↑↓ ↕ | ǁ |│║ │∫∑ √ ∛ ∜ ≤ ≥ ~ ∞ ≡ ≈ Δ δ π σ υ λ α β γ ψ μ t τ ζ Ψ Ω θ Χ ε φ ω η ō Ō ½ ¼ ¾ ΔGo , ΔSo , ΔHo 1 /29

The Periodic table Alkaline Earths Halogens Noble Gases Main Group Transition Metals Main Group Lanthanides and Actinides 2

Konu 19: Çözünürlük ve Kompleks-İyon Dengeleri İÇİNDEKİLER 749 19 -1 19 -2 19 -3 19 -4 19 -5 19 -6 19 -7 19 -8 19 -9 Çözünürlük Çarpımı Sabiti, Kçç 750 Çözünürlük ve Kçç Arasındaki İlişki 751 Çözünürlük Dengelerinde Ortak-İyon Etkisi 753 Kçç Kavramında Kısıtlamalar 755 Çökelme ve Tam Çökmenin Ölçütleri 757 Ayrımsal Çöktürme 759 Çözünürlük ve p. H 761 Kompleks İyonları İçeren Dengeler 763 Nitel Katyon Analizi 768 Özel Konu Kabuklar, Dişler ve Fosiller 772 Konu 19 Sorular 3 /29

19 -1 Çözünürlük Çarpımı Sabiti, Kçç 750 • Kçç = Çözünürlük Çarpımı Sabiti, katı ve az çözünen maddelerin doymuş çözeltilerdeki iyonlar arasındaki dengeyi gösteren sabittir. Ca. SO 4(k) ⇄ Ca 2+(aq) + SO 42 -(aq) ➨ Kçç=[Ca 2+][SO 42 -]=9, 1 x 10 -6 (SŞ) ➨p. Kç=5, 041 4

19 -2 Kçç , p. Kçç, s = Molar Çözünürlük, %ç , ppm-ç 751 Am. Bn(k) ⇄m. An+(aq)+ n. Bm-(aq) ➪ KççAm. Bn=[An+]m. [Bm-]n =(ms)m. (ns)n ➪ p. Kçç= - log. Kçç Molar Çözünürlük = s = Az çözünen bileşiğin Doymuş sulu çözeltisindeki molaritesidir. Yüzde ÇÖZÜNÜRLÜK = %ç (g Ba. SO 4 /100 m. L aq) ppm-ÇÖZÜNÜRLÜK = ppm-ç ( mg Ba. SO 4/L aq) ÖRNEK: p. Kç=9, 96 olan Ba. SO 4 (233 g/mol)’ın s=? , %ç=? , ppm-ç=? ÇÖZÜM : p. Kç=9, 96 ➪Kçç Ba. SO 4 =1, 1 x 10 -10=[Ba 2+]. [SO 42 -]=s 2 ➪ s=√ 1, 1 x 10 -10 =1, 05. 10 -5 mol. Ba. SO 4/L ➪ %ç=1, 05. 10 -5 mol. Ba. SO 4/L aq*233 g/mol*0, 1=2, 45. 10 -4 = ➪ ppm-ç =2, 45 mg/L aq ÖRNEK 19 -2: p. Kç=5, 041 olan Ca. SO 4’ın %ç=? ÇÖZÜM: p. Kç=5, 041 ➨Kçç= 9, 1 x 10 -6= [Ca 2+][SO 42 -]= s 2 s =√ 9, 1 x 10 -6 =3. 10 -3 mol/L ➪%ç= 3. 10 -3 mol/L*136 g/mol*0, 1= 0, 041 g/100 m. L ➪ 0, 41 g/L ➪ ppm-ç=410 ÖRNEK 19 -2 A-Ag. CNO (150)’ın ppm çözünürlüğü 70 dir p. Kçç=? ÇÖZÜM s=70 g/L: (1000 g/Lx 150 g/mol )=4, 67. 10 -4 ➪ Kçç=s 2=(4, 67. 10 -4)2=2, 18. 10 -7➪ p. Kçç=6, 66 ÖRNEK 19 -2 B-Li 3 PO 4 (116 g/mol)’ın çözünürlüğü 340 ppm. dir p. Kçç=? ÇÖZÜM s=340 mg/L/(1000 g/Lx 116 g/mol )=2, 93. 10 -3➪ Kçç=27 s 4=27(2, 93. 10 -3)4=1, 99. 10 -9➪ p. Kçç=8, 7 ÖRNEK 19 -3 A -Fe(OH)3 (107 g/mol)’ın p. Kçç=37, 4 dür, ppm çözünürlüğü nedir? ÇÖZÜM p. Kçç=37, 4 ➪ Kçç=27 s 4= 4. 10 -38 ➪Suda s=1, 96. 10 -10 mol/Lx 107 g/mol x (1000 g/L )=2, 1. 10 -5 ppm 5

19 -2 Kçç , p. Kçç, s = Molar Çözünürlük, %ç , ppm-ç 751 • ÖRNEK : p. Kçç = 11, 62 olan Ag 2 Cr. O 4 (332 g/n) ‘ın s=? %ç=? ppm-ç=? • ÇÖZÜM : Ag 2 Cr. O 4 ⇄ 2 Ag+ + Cr. O 4= ➪ Kçç Ag 2 Cr. O 4 = [Ag+]2[Cr. O 4=] = (2 s)2. s = 4 s 3 ➪ Kçç = 10 -11, 62 = 2, 4. 10 -12 ➪ s= ∛Kçç: 4 = ∛ 2, 4. 10 -12 : 4 = 8, 43. 10 -5 M ➪ %ç = 8, 43. 10 -5 mol/L*332 g/mol * 0, 1= 0, 0028 g/100 m. L ➪ = 0, 028 g/L ➪ ppm-ç=28 mg/L • ÖRNEK : p. Kçç = 32, 89 olan Al(OH)3( 78 g/n)’in s=? %ç=? ppm-ç=? • ÇÖZÜM : Al(OH)3 ⇄ Al 3+ + 3 OH- ➪ Kçç Al(OH)3 = [Al 3+][OH-] = (3 s)3. s = 27 s 4 ➪ Kçç = 10 -32, 89 = 1, 3. 10 -33 ➪ s= ∜Kçç: 27 = ∜ 1, 3. 10 -33 : 27 = 2, 63. 10 -9 M ➪ %ç = 2, 63. 10 -9 mol/L*78 g/mol * 0, 1= 2, 1. 10 -8 g/100 m. L ➪ 2, 1. 10 -7 g/L ➪ ppm-ç= 2, 1. 10 -4 mg/L • ÖRNEK : p. Kçç = 97 olan Bi 2 S 3( 514 g/n)’in s=? %ç=? • ÇÖZÜM : Bi 2 S 3 ⇄ 2 Bi 3+ + 3 S= ➪ Kçç Bi 2 S 3 = [Bi 3+]2. [S=]3 = (2 s)2. (3 s)3 = 108 s 5 ➪ Kçç = 10 - 97 ➪ s= (Kçç: 108)1/5 = 1, 56. 10 -20 M ➪ %ç =1, 56. 10 -20 mol/L*514 g/mol * 0, 1= 8, 02. 10 -19 g/100 m. L 6

19 -3 Çözünürlük Dengelerinde Ortak-İyon Etkisi 753 Pb. I 2(k) ⇄ Pb 2+(aq) + 2 I-(aq) Dengesinde ortama I-(aq) eklenirse Le Chatelier’e göre denge geri ⇦ döner çözünürlük azalır. Buna Ortak İyon etkisi denir. ÖRNEK 19 -4 - Pb. I 2(k) ’ın p. Kçç=8, 15’dir. Suda ve 0, 1 M KI(aq)’daki Molar çözünürlüğü nedir? ÇÖZÜM Kçç=4 s 3=7, 1. 10 -9 ➪ Suda ➪ s’≈7, 1. 10 -7 M s=1, 21. 10 -3 M ➪ 0, 1 M KI(aq) de s’. (0, 1+2 s’)2=7, 1. 10 -9 ÖRNEK 19 -4 A- Pb. I 2(k) ’ın Kçç=7, 1. 10 -9 dir. Suda ve 0, 1 M Pb 2+(aq)’daki x=Molar çözünürlüğü nedir? ÇÖZÜM Kçç=4 x 3=7, 1. 10 -9 ➪ Suda s=1, 21. 10 -3 M ➪ 0, 1 M Pb 2+(aq) de (0, 1+s’). (2 s’)2=7, 1. 10 -9 ➪ s’≈1, 3. 10 -4 M ÖRNEK 19 -3 A/4 B-Fe(OH)3’ın Kçç=4. 10 -38 p. H=8, 2 olan aq’de s=molar çözünürlük=? ÇÖZÜM p. OH=14 -8, 2=5, 8 Kçç=s. (1, 58. 10 -6)3=4. 10 -38 ➪ s =1. 10 -20 M bulunur. 7

19 -4 Kçç Kavramında Kısıtlamalar 755 • Kçç genellikle az çözünen bileşikler için kullanılır. Çok çözünenler bileşikler için iyon etkinlikleri (aktivite) önemlidir. • a = aktif konsantrasyon (Etkinlik = etkin derişim), ölçülen derişimlerden daha küçük olur. • Tuz Etkisi (veya Yabancı-Farklı İyon Etkisi) Çözeltinin toplam iyon derişimi arttıkça, iyonlar arası çekim önemlidir. Az çözünen bir bileşiğin çözünürlüğü, fazla yabancı-iyon içeren çözücülerde artar. 8

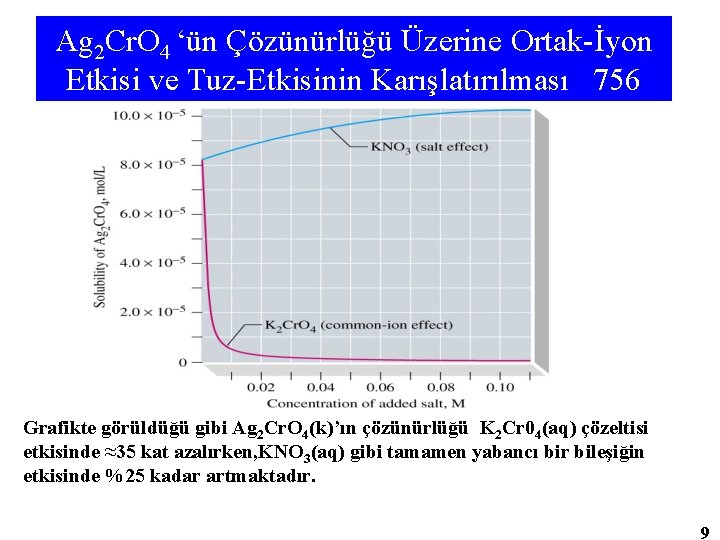
Ag 2 Cr. O 4 ‘ün Çözünürlüğü Üzerine Ortak-İyon Etkisi ve Tuz-Etkisinin Karışlatırılması 756 Grafikte görüldüğü gibi Ag 2 Cr. O 4(k)’ın çözünürlüğü K 2 Cr 04(aq) çözeltisi etkisinde ≈35 kat azalırken, KNO 3(aq) gibi tamamen yabancı bir bileşiğin etkisinde %25 kadar artmaktadır. 9

Çözünenin İyonlara Tam Ayrışamaması ve İyon Çiftleri oluşması • Çözeltideki tüm iyonların ayrıştığı, oluşan iyonların birbirinden bağımsız hareketi geçerli değildir. Bu iyonlarda yüklerine ve aralarındaki elektrostatik çekimin gücüne göre İYON ÇİFTLERİ oluşturabilirler. Buda çözeltideki iyon derişimini azaltır fakat Kçç eşitliğinin sağlanması için ise çözünürlüğün arttığı gözlenir. Yani, Çözünen iyonların bir kısmı çözelti de İYON ÇİFTİ • olan molekül haline geçer. Karşılıklı elektrostatik çekim arttıkça • artan iyon çifti oluşumu nedeniyle çözünürlüğün arttığı gözlenir. çözünürlükten hesaplanırsa Kçç (Ca. SO 4) = 2, 3 x 10 -4 bulunur. Çizelge 19. 1’de: Kçç (Ca. SO 4) = 9, 1 x 10 -6 dır ve bu değer iyon çifti oluşumu göz önüne alınmadan bulunmuştur. Arada 25 kat fark vardır. oluşan iyon çiftleri çözünürlüğü 10 -100 kat kadar artırabilmektedir. • Etkinliklerde iyon çifti oluşumu göz önüne alınır ve kullanılır. • Çözeltide farklı dengeler de olabilir. Örneğin Ksu Dengeyi etkiliyorlarsa onun da hesaba katılması gerekir. 10 /29

19 -5 Çökelme ve Tam Çökmenin Şartları 757 Ag. I(s) ⇄ Ag+(aq) + I-(aq) Kçç = [Ag+][Cl-] = 8. 5 x 10 -17 SORU Ag. NO 3(aq) ve KI(aq) karıştırılarak 0. 010 M Ag+ ve 0. 015 M Iiçeren bir karışım oluşturulmuştur. Bu oluşan karışım çözelti doymamış, doymuş, veya aşırı doymuş mudur ? sorusunun cevabı için Qçç=İYON ÇARPIMI bulunur. Qçç=İYON ÇARPIMI = [Ag+][Cl-] = (0. 010)(0. 015) = 1. 5 x 10 -4 > Kçç dir. Qçç > Kçç ise çökelme var sistemde doymuş çözelti ve katı madde 2 fazlı karışımdır Qçç = Kçç ise çözelti tam doymuş çözelti olup ve denge halidir ve 1 fazlıdır. Qçç < Kçç ise çökelme yoktur. Sistem doymamış çözeltidir ve tek fazlıdır. 11

Örnek 19 -5 Az Çözünen Bir Bileşiğin Çökme Şartı Üç damla 0, 20 M KI, 100. 0 m. L 0. 010 M Pb(NO 3)2’ye ekleniyor. Kurşun iyodür çökeleği oluşur mu? (1 damla = 0. 05 m. L) Pb. I 2(s) ⇄ Pb 2+(aq) + 2 I-(aq) Kçç= 7, 1 x 10 -9 I- iyonun miktarını hesaplayalım: n. I- = 3 damla 0. 05 m. L 1 L 1 damla 1000 m. L I- yeni derişimini [I-] = 0. 20 mol KI 1 mol I- 1 L 1 mol KI 3 x 10 -5 mol I 0. 1000 L = 3 x 10 -5 mol/0, 1 L I- = 3 x 10 -4 M I- Çökme Şartı Q = [Pb 2+][I-]2 = (0, 010)(3 x 10 -4)2 = 9 x 10 -10 < Kçç = 7. 1 x 10 -9 olduğu için henüz çökme yoktur. 12

19 -6 Çözünürlük ve p. H 761 ÖRNEK 19 -6 - Deniz suyundan Mg eldesi için deniz suyu sönmüş kireç ile doyurulur. Deniz suyunda [Mg 2+]≈0, 06 dir. Deniz suyu sönmüş kireç ile doyurulunca p. H≈11, 3 olmaktadır. Bu durumda Mg 2+ çökmesi tam mıdır? p. H=11, 3 ➪ p. OH=2, 7 ➪ [OH -] =10 -2, 7=2. 10 -3 Mg(OH)2 (k) ⇄ Mg 2+(aq) + 2 OH-(aq) Kçç=1, 8 x 10 -11 CEVAP) Q= İYON ÇARPIMI=[Mg 2+][OH-]2 = Q=(0, 06). (2, 10 -3)2 =2, 4. 10 -7 > Kçç Çökme var. Q=Kçç olduğunda çökme durur. Bu anda ➪ Kçç=[Mg 2+] (2, 10 -3)2 = 1, 8 x 10 -11 ortamda çökmeden kalan➪[Mg 2+] =4, 5. 10 -6 M olup %= 100 x (4, 5. 10 -6/0, 06) =% 0, 0075 < %0, 1 bu halde çökmenin tam olduğu kabul edilir. 13
![Çözünürlük ve p H Örnek sorular ÖRNEK 19 6 A Deniz suyunda Ca 20 Çözünürlük ve p. H Örnek sorular ÖRNEK 19 -6 A Deniz suyunda [Ca 2+]≈0,](https://slidetodoc.com/presentation_image/2870a21d96663a61330e7fd094b1b2f0/image-14.jpg)
Çözünürlük ve p. H Örnek sorular ÖRNEK 19 -6 A Deniz suyunda [Ca 2+]≈0, 01 dir. p. H≈12, 6 olan ortamda Ca 2+ çökmesi tam mıdır? p. H=12, 6 ➪ p. OH=1, 4 ➪ [OH -] =10 -1, 4 = 0, 04 Kçç = 5, 5 x 10 -6 ÇÖZÜM) Kçç=[Ca 2+][OH-]= [Ca 2+]. (0, 04)2 =5, 5. 10 -6 ➪ [Ca 2+]=3, 4. 10 -3 % çöken 34 olup çökme tam değildir. ÖRNEK 19 -8 - 0, 01 M Mg. Cl 2 ve 0, 1 M NH 3 içeren çözeltide çökme olur mu? KNH 3=1, 8. 10 -5 ➪ 11 Q= İYON ÇARPIMI=[Mg 2+][OH-]= (0, 01). (1, 3. 10 -3)2=1, 7. 10 -8>1, 8. 10=Kçç ÇÖKME OLUR. ÖRNEK 19 -9 - 0, 01 M Mg. Cl 2 ve 0, 1 M NH 3 içeren çözeltide çökme olmaması için [NH 4+]=? Çz. Kçç=[Mg 2+][OH-]2= (0, 01). [OH]2=1, 8. 10 -11➪[OH-]=4, 2. 10 -5 ➪ KNH 3=1, 8. 10 -5=[NH 4+]. 4, 2. 10 -5: 0, 1 ➪ [NH 4+]=/>0, 043 M olduğu zaman Mg 2+ çökmesi önlenmiş olur.

19 -6 Ayrımsal Çöktürme 759 Bir çözeltide iki veya daha çok iyonun aynı çöktürücü iyonla çökelek verebildiği durumlarda kullanılan bir tekniktir. Çözeltilerde gözle görülebilen farklılıklar elde etmek gereklidir. ÖRNEK 19 -7 0, 01 M Cr. O 4= ve 0, 01 M Br- içeren çözeltiye Ag. NO 3(aq) damla katıldığında önce ne çöker 2. Madde ne zaman çökmeye başlar. 2. Madde çökmeye başladığında 1. maddenin çökmeyen %=? Bu tam bir çöktürme midir? Kçç Ag Cr. O =1, 1. 10 -12 Kçç Ag. Br= 2 4 ÇÖZÜM : Ag 2 Cr. O 4 çökmesi için 5. 10 -13 [Ag+]2. (0, 01) =1, 1. 10 -12 ➪ [Ag+]=1. 10 -5 Ag. Br çökmesi için [Ag+]. (0, 01) =5. 10 -13 ➪ [Ag+]=5. 10 -11 çökmesi için daha az reaktif gereken önce çöker 1. çöken Ag. Br olup 2. Ag 2 Cr. O 4 çökmesi başladığında Kçç Ag. Br=5. 10 -13=(1. 10 -5). [Br-] ➪ [Br-] =5. 10 -8 bu miktar çözeltide kalan çökmeyen madde derişimidir. Ohalde 1. maddenin çökmeyen %= 100*(5. 10 -8/0, 01) = 5. 10 -4 < % 0, 1 olup bu çökmenin tam olduğunu gösterir. 15

19 -6 Ayrımsal Çöktürme 759 • ÖRNEK : 0, 1 M Zn 2+ ve 0, 1 M Fe 2+ karışımı çözeltiden H 2 S gazı geçirilirse a) Önce hangi madde çöker ? b) 2. çöken madde ne zaman çöker? c) Çökme tam mıdır? p. KççFe. S=19, p. KççZn. S=23, 4 • ÇÖZÜM)Fe. S çökmesi için KççFe. S=10 -19= (0, 1)[S=] ➪[S=]=10 -18 • Zn. S çökmesi için KççZn. S=10 -23, 4=3, 98. 10 -24= (0, 1)[S=] ➪[S=]=3, 98. 10 -23 a) Daha az reaktif gerektiren Zn. S önce çöker. b) 2. madde Fe. S çökmesi için [S=]=10 -18 olması gerektiğinden KççZn. S=3, 98. 10 -24=[Zn 2+]. (10 -18) ➪[Zn 2+]=3, 98. 10 -6 kaldığında Fe. S çökmesi başlar. c)Çökmeyen Zn 2+ % =100* 3, 98. 10 -6 / 0, 1 = 3, 98. 10 -3 < % 0, 1 olup çökme tamdır. veya Çöken Zn 2+ % =100*0, 1 -3, 98. 10 -6 / 0, 1 = 99, 996 olup çökme tamdır. 16

AYRIMSAL ÇÖKTÜRME SORU: 0, 2 M KCl ve 0, 2 M K 2 Cr. O 4 eşit hacımda karıştırıp karışıma Ag. NO 3(aq) damla ilave edilirse önce ne çöker? 2. Madde ne zaman çöker? Çökme tam mıdır? p. KççAg. Cl=10 , p. KççAg 2 Cr. O 4=11, 62 CEVAP: Önce Ag. Cl çöker. Ag 2 Cr. O 4 çökmesi [Ag+]= 4, 9. 10 -6 M veya [Cl-]=2, 04. 10 -5 M olunca başlar. Çökme tamdır. SORU: 0, 1 M Ba. Cl 2 ve 0, 1 M Sr. Cl 2 karışıma Na. SO 4(aq) damla ilave edilirse önce ne çöker? 2. Madde ne zaman çöker? Çökme tam mıdır? p. KççBa. SO 4=10 , p. KççSr. SO 4=6, 6 CEVAP: Önce Ba. SO 4 çöker. SO 4 çökmesi [Ba 2+]= 3, 9. 10 -5 olunca başlar. Çökme tamdır.

19 -8 Kompleks İyonlar İçeren Dengeler Ag. Cl(s) + 2 NH 3(aq) → [Ag(NH 3)2]+(aq) + Cl-(aq) Koordinasyon Bileşikleri. Kompleks iyonları içeren maddeler. Kompleks iyonlar. Çok atomlu anyon ve katyonlar: Merkezi metal iyonu. Ligand Ag+(aq) + 2 NH 3(aq) → [Ag(NH 3)2]+(aq) Kol = [Ag(NH 3)2]+ [Ag+][NH 3] 7 = 1. 6 x 10 2 18

Table 19. 2 Formation Constants for Some Complex Ions 19

ÖRNEK 19 -11 Kompleks İyonları Oluşturan Bir Çözeltiden Çökelek Oluşması. 0. 10 mol Ag. NO 3, 1. 00 L 1. 00 M NH 3 içinde çözünüyor. Bu çözeltiye 0. 010 mol Na. Cl eklenirse, Ag. Cl(s) çöker mi? Kol değerinin çok büyük olduğunu varsayarsak: Ag+(aq) + 2 NH 3(aq) → [Ag(NH 3)2]+(aq) İlk Derişim 0. 10 M 1. 00 M 0 M Değişme -0. 10 M -0. 20 M +0. 10 M Denge Hali. (≈0) M 0. 80 M 0. 10 M [Ag+] çok küçüktür ama sıfır değildir, Kol değeri [Ag+]’yi hesaplamada kullanılır: İlk Durum 0 M 0. 80 M 0. 10 M Değişmeler +x M +2 x M -x M Denge Hali x. M 0. 80 + 2 x M 0. 10 - x M Kol = [Ag(NH 3)2]+ [Ag+] [NH 3]2 = 0. 10 -x x(0. 80 + 2 x)2 ≈ 0. 10 x(0. 80)2 = 1. 6 107 x = [Ag+] = 9. 8 10 -9 M Qçç < Kçç Ag. Cl çökelmeyecektir. Kçç = 1. 8 x 10 -10 20 /29

The Periodic table Alkaline Earths Halogens Noble Gases Main Group Transition Metals Main Group Lanthanides and Actinides 21

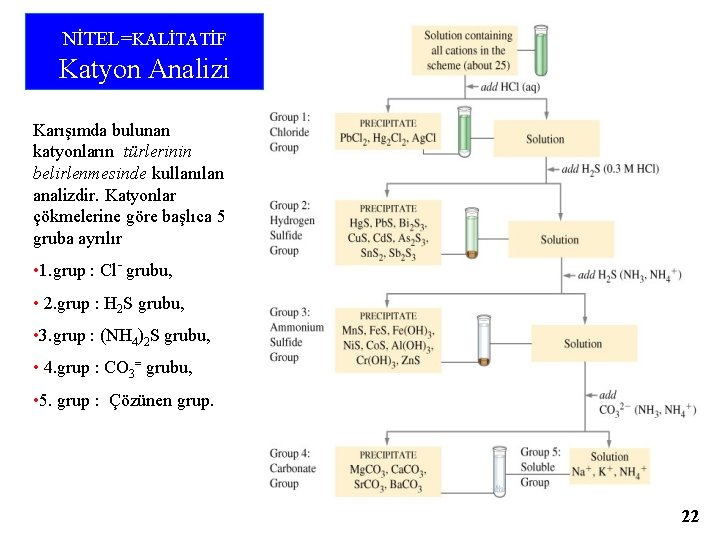
NİTEL=KALİTATİF Katyon Analizi Karışımda bulunan katyonların türlerinin belirlenmesinde kullanılan analizdir. Katyonlar çökmelerine göre başlıca 5 gruba ayrılır • 1. grup : Cl- grubu, • 2. grup : H 2 S grubu, • 3. grup : (NH 4)2 S grubu, • 4. grup : CO 3= grubu, • 5. grup : Çözünen grup. 22

ALEV RENKLENMESİ a) Hidrojen lambası b) Helyum Lambası c-d-e Alkali metal Tuzlarının Bunzen beki alevinin renklenmesi c) Lityum / Stronsyum (Karmen Kırmızısı) d) Sodyum (parlak sarı) e)Potasyum (Menekşe) [Bakır (Mavi-Yeşil), Baryum (Fıstık Yeşili), Kalsiyum (Kiremit Kırmızısı)] 23

1. grup - Klorür Grubu Ayrılması Numuneye % 20 HCl(aq) çözeltisi ilavesinde 1. grup katyonları Pb. Cl 2, Ag. Cl, ve Hg 2 Cl 2 beyaz çökelek oluşturur. Ayrılan çökelek sıcak suyla muamele edilirse bir miktar Pb. Cl 2 çözünerek çözeltiye geçer. Çözünen Pb 2+ (aq) I- (aq) veya, Cr. O 42 - (aq) eklenerek sarı kristalize çökme olup olmadığı test edilir. Pb 2+(aq) + Cr. O 42 -(aq) → Pb. Cr. O 4(k) Pb 2+(aq) + I-(aq) → Pb. I 2(k) Geri kalan çökelek, amonyak ile test edilir. Ag. Cl(k) + 2 NH 3(aq) → [Ag(NH 3)2]+ (aq) + Cl-(aq) çözeltiye geçer Hg 2 Cl 2(k) + 2 NH 3 → Hg(s) + Hg. NH 2 Cl(s) + NH 4+(aq) + Cl-(aq) üstte kalan çökelek sıvı Hg ayrılması dolayısıyla siyahlaşır. Alt geçen [Ag(NH 3)2]+ (aq) ne HNO 3 damlatılırsa Ag. Cl beyaz çökeleği yeniden oluşacaktır. [Ag(NH 3)2]Cl (aq) + HNO 3 Ag. Cl(k) + NH 4 NO 3(aq) 24

Pb. S Çözünürlük Denge Eşitliği Pb. S(s) + H 2 O(l) Pb 2+(aq) + HS-(aq) + OH-(aq) Ksp = 3 x 10 -28 H 3 O+(aq) + HS-(aq) H 2 S(aq) + H 2 O(aq) 1/Ka 1 = 1. 0/1. 0 x 10 -7 H 3 O+(aq) + OH-(aq) H 2 O(l) + H 2 O(l) 1/Kw = 1. 0/1. 0 x 10 -14 Pb. S(s) + 2 H 3 O(l) Pb 2+(aq) + H 2 S(aq) + 2 H 2 O(l) Kçça = Kçç Ka 1 x Ksu = 3 x 10 -28 -7 = 3 x 10 -14 1. 0 x 10 -7 x 1. 0 x 10 25

Metal Sülfürlerin Çözünmesi • Metal sülfürleri çözmek için bazı yöntemler bulunur. – Bir Asitle reaksiyona sokmak. • Fe. S güçlü asidik çözeltilerde çözünürler ancak Pb. S ve Hg. S gibileri Kçç değerli düşük olduğundan çözünmezler. – Bir Yükseltgen ile tepkimeye sokmak. 3 Cu. S(aq) + 8 H+(aq) + 2 NO 3 -(aq) → 3 Cu 2+(aq) + 3 S(s) + 2 NO(g) + 4 H 2 O(l) 26
![BakırII Üzerine Bir Test CuH 2 O42aq 4 NH 3aq CuNH 342aq Bakır(II) Üzerine Bir Test [Cu(H 2 O)4]2+(aq) + 4 NH 3(aq) → [Cu(NH 3)4]2+(aq)](https://slidetodoc.com/presentation_image/2870a21d96663a61330e7fd094b1b2f0/image-27.jpg)
Bakır(II) Üzerine Bir Test [Cu(H 2 O)4]2+(aq) + 4 NH 3(aq) → [Cu(NH 3)4]2+(aq) + 4 H 2 O(l) 27

Özel Konu: Deniz Kabukları, Dişler ve Fosiller Kalsit Ca 2+(aq) + 2 HCO 3 -(aq) → Ca. CO 3(s) + H 2 O(l) + CO 2(g) Hidroksiapatit Florapatit Ca 5(PO 4)3 OH(s) Ca 5(PO 4)3 F(s) Ca 5(PO 4)3 OH(s) + 4 H 3 O+(aq) → 5 Ca 2+(s) + 5 H 2 O(l) + 3 HPO 42 -(aq) 28

Öncelikle konu içinde verilmiş olan 1 adedi çözülmüş 2 adedi çözülecek örnek sorular üzerinde titizlikle durulması tavsiye edilir. Sınav soruları genellikle onlardan seçilecektir. • Konunun daha iyi anlaşılması açısından konunun sonunda yer alan aşağıdaki sorulara da bakılırsa iyi olur. • 9 -12 -14 -17 -19 -31 -35 -39 -4145 -49 -51 -57 -61 -65 -69 -7173 -75 - 83 -105 -106 29 /29