GDP rakendamine Inge Me Maris Dubova Ravimiamet 02

GDP rakendamine Inge Mäe Maris Dubova Ravimiamet 02. 12. 2015

Head turustamistavad Good Distribution Practice (GDP) • Suunised on kehtestatud Euroopa Ühenduse tasandil • Uuendatud suunised avaldati märtsis 2013 • Jõustusid septembris 2013, parandatud versioon novembris 2013 • On kohustuslikud täitmiseks Eestis (Rav. S § 26 lg 81) inimtervishoius kasutatavate ravimite ja toimeainete hulgimüük ning ravimite vahendamine peavad vastama Euroopa. . . direktiivi 2001/83/EÜ. . . alusel koostatud headele turustamistavadele • RA veebilehel leitav: http: //www. ravimiamet. ee/inimtervishoius-kasutatavateravimite-hea-turustamistava-0

• Kehtivad kõikidele hulgimüüjatele, sõltumata sellest, kas tegemist kõiki või mõnda hulgimüügitoimingut tegeva ettevõttega • GDP suuniste järgimine peaks tagama kontrolli turustusahela üle ja säilitama seega ravimite kvaliteedi ja muutumatuse tootjalt tarbijani • Vastavust GDP nõuetele kinnitab GDP sertifikaat – väljastatakse hulgimüüjale pärast inspektsiooni 90 päeva jooksul • Tänaseks väljastatud Eestis 10 GDP sertifikaati 3

Kvaliteedisüsteem Kvaliteedikäsiraamat või muu sarnane dokument (nt tööeeskirjad), kus on kajastatud - organisatsiooni struktuur - vastutus - ressursid - riskihalduse põhimõtted - tegevused ravimite kvaliteedi säilimiseks - seadusliku tarneahela tagamine 4

- protsessid, tegevused - tellimus-/teenustööd (GDP: „allhanketegevused“), heakskiitmine - kõrvalekallete haldus - muutuste haldus (protsessid, dokumendid) - perioodiline ülevaatus - juhtkonnapoolne ülevaatus Kvaliteedisüsteem ei saa kunagi valmis – muutub ja täieneb pidevalt 5

Riskihaldus / riskijuhtimine • Süstemaatiline protsess / tegevus - ravimi kvaliteeti mõjutavate riskide hindamiseks - riskide kontrolli all hoidmiseks - teabevahetuseks - riskide ülevaatamiseks • Riskide hindamine - ennetav - tagantjärele (nt kõrvalekalde juhtumis) • Määrata kindlaks, millise seadme kvalifitseerimine ja/või olulise protsessi valideerimine on vajalik • Riskihindamiste dokumenteerimine

Kvalifitseerimine ja valideerimine – seadmed, protsessid • Teha kindlaks - millise olulise seadme kvalifitseerimine ja/või olulise protsessi valideerimine on vajalik, et tagada korrektne paigaldus/toimimine • Valideerimine/kvalifitseerimine enne kasutuselevõtmist ja pärast olulisi muudatusi • Valideerimisaruanded – tulemused, kõrvalekalded, meetmed (ennetavad ja korrigeerivad tegevused) • Valideerimine/kvalifitseerimine tuleb heaks kiita 7

Kõrvalekalded • Säilitamistingimustes (nt temperatuur, niiskus, häiresüsteemid, külmaahela katkemine) • Käitlemistoimingutes (nt noppevead, vead kauba vastuvõtul, transport, kliendi rahulolematus, arvestus) • Dokumenteerimine • Analüüs • Järeldused 8

Muudatused. Muudatuste haldus. • Peab olema kehtestatud süsteem muudatuste halduseks - olulisemate muudatuste juhtumid - tööeeskirjade uued versioonid • Õigusaktide muutmise järgselt, ettevõtte enda algatusel, inspektsioonide tulemusel vm • Kui tehakse olulisi muutusi töökorralduses vm: - muudatuse sisu, kirjeldus - planeerimine - kvalifitseerimine-valideerimine - heakskiitmine - järeldused (nt vajalik teha muutus kvaliteedisüsteemis) • Iga muudatuse kohta dokumentatsioon (muudatuse haldus) 9

Tarnijate kvalifitseerimine Eesmärk – et võltsitud ravimid ei satuks seaduslikku tarneahelasse • Ravimid hangitakse hulgimüügi või tootmisloa omajatelt, soovi korral kasutades registreeritud vahendajaid • Tarnijate kvalifitseerimine ja heakskiitmine enne ravimite hankimist • Kvalifitseerimine on dokumenteeritud ning perioodiliselt kontrollitud • Uute tarnijate taustakontroll 10

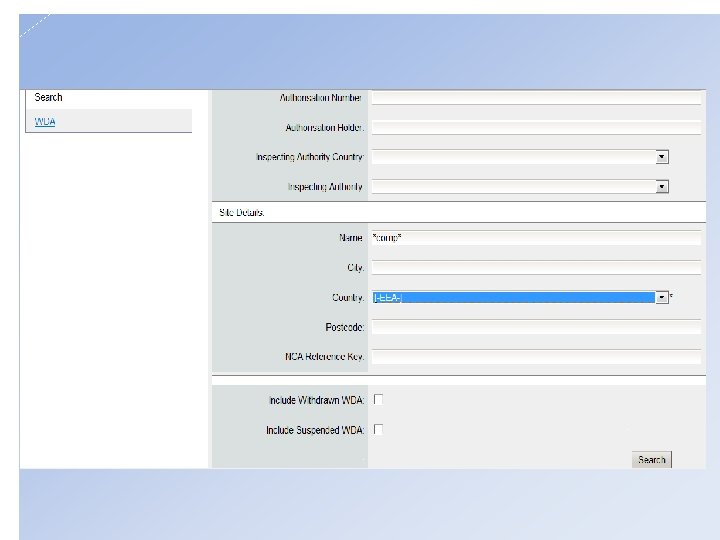
Ühenduse andmebaas, Eudra. GMDP http: //eudragmdp. ema. europa. eu täidavad riikide ravimiametid haldab EMA

WDA Wholesale Distribution Authorisation Hulgimüügi tegevusluba GDP sertifikaadid GDP-le mittevastavused

Klientide kvalifitseerimine • Tagatud, et ravimeid väljastatakse ainult hulgimüügiluba omavatele isikutele või isikutele, kellel on luba või õigus väljastada ravimeid üldsusele • Kontrollida vastavaid lubasid – küsida tegevusloa koopia, andmed pädeva asutuse veebilehel • Kontrollimine kirjeldatud tööeeskirjades ja dokumenteeritud • Müügipiirangute kehtestamine klientidele, kellel ei ole ravimite hankimise õigust, sh nt narkootiliste ja psühhotroopsete ainete käitlemise õigust • Ebakorrapärased tellimused – kirjeldus, RA teavitamine 14

Tellimus-/teenustööd (GDP: allhanked) Töö tellija vastutab tellimustööna tehtava tegevuse eest • Kirjalik leping • Tellimuse täitja sobivuse hindamine • Poolte vastutus • Auditid - sagedus - võimalik teostada igal ajal - tellimuse täitja kompetentsus • Tellimuse täitja ei või tööd (osa tööst) edasi anda kolmandale isikule, kui see pole töö Tellija poolt heaks kiidetud. 15

Töötajad • Individuaalset vastutust omavad töötajad - pädev isik „responsible person“ = üldvastutusega isik, kes saab delegeerida ülesandeid, kuid mitte vastutust; peab olema pidevalt kättesaadav - vastutav ja asendav isik iga toimingu osas - teised töötajad oma ülesannete osas • Igal töötajal ametijuhend - tööülesanded ja vastutusalad • Koolituskava - esmased ja jätkukoolitused, sh GDP alane koolitus ja erikoolitused (ohtlikud ravimid, kuritarvitatavad ravimid, külmaravimid, võltsitud ravimite jne) 16

Ruumid • Oma ruumid või ruumide kasutamise leping • Juurdepääsuõigused • Vastuvõtmise-, väljastamise- ja säilitamisala; karantiin • Säilitamistingimused (temperatuur, niiskus, valgustus, ventilatsioon, puhtus, signalisatsioon) • Koristamine vastavalt koristuskavale, vajadusel kahjurite tõrje

Seadmed • • • Hoolduskava Igal seadmel hoolduse protokollid Kalibreerimine Häiresüsteemid (sh regulaarne kontroll) Temperatuuri- ja keskkonnakontroll - temperatuuride esmane kaardistamine - kaardistamine erinevates tingimustes 18

Arvutisüsteemid peavad tagama andmete kättesaadavuse ja turvalise säilimise • Süsteemi kirjeldus (+skeemid) • Valideerimine või verifitseerimine (sobivuse tõendamine) • Andmete sisestamise, muutmise ja vaatamise õigused määratud • Arvutisüsteem vs dokumentide haldus arvutis • Varukoopiate tegemine ja hiljem andmete kättesaadavus • Tööeeskiri rikete ja katkestuste korral 19

Säilitamine FIFO (first in, first out ), FEFO (first expired, first out ) • Ravimid tegevusloal märgitud laos • Füüsiline ja/või elektrooniline eraldamine • Ravimid füüsiliselt eraldi toodetest, mis võivad mõjutada nende kvaliteeti • Kõlblikkusaja lõpule lähenevad ravimid - kriteeriumid laost kõrvaldamiseks - kõlblikkusaeg alla 2 kuu – kuidas eraldatud (vajalik kirjalik nõusolek) • Inventuur 20

Kõlbmatud ravimid • Säilitada füüsiliselt eraldi • Vastavalt märgistada • Ohtlikud jäätmed - jäätmekäitlusettevõttesse - erisused - hävitamine http: //www. ravimiamet. ee/ravimite-havitamine 21

Ravimite vastuvõtmine • Vastuvõtukontroll - kauba vastavus saatedokumentidele - eritingimusi nõudev kaup - eriluba-turustamisluba - kvaliteeti tõendavad dokumendid, vaktsiinidel OCABR sertifikaat • Karantiin 22

Väljastamine • • Klientide kvalifitseerimine Õige komplekteerimise tagamine Lühikese kõlblikkusajaga ravimid Temperatuuritundlikud ravimid - termopakendid (valideeritud) - termopakendite komplekteerimine (juhend) - külmaelemendid: külmutatud, jahutatud - mittetäielikult külmutatud/jahutatud – peab olema tagatud, et ei võeta kasutusse 23

Transport Hulgimüüja vastutab transporditingimuste eest • Lepingud • Eeskirjad • Sõidukid ja seadmed - konteineri valik ja märgistus - hooldus • Transpordimarsruudi riskide hindamine - peale- ja mahalaadimised - kus ja millal vaja temperatuure kontrollida - vaheladudes säilitamine - kõrvalekallete haldus 24

• Temp tundlike toodete transport - kaardistamine (suvel, talvel) - temp jälgimise seadmed (sõidukis ja/või konteineris) - teave kliendile • Autojuhtide koolitus • Kauba jõudmine õige kliendini • Kolmandate osapoolte kasutamine – peab olema tellija heakskiit • Transporditingimuste, vaheladude ja mahalaadimiskohtade auditeerimine ja heakskiitmine 25

Tagastatud ravimid • Riskide hindamine tagastamisel • Määratud tagastuse aeg • Tagastamise tingimused (pakend avamata, kõlblik, klient tõendanud säilitamistingimuste täitmist, sh temperatuuritundlike ravimite korral) • Hinnangu annab pädev isik või selleks määratud isik • Lõpliku heakskiidu annab pädev isik (võib väljastuslattu panna) • Väljastuslattu paigutamine 26

Kaebused Kaebus on tagasiside, mis annab võimaluse areneda ja kvaliteeti tõsta • Eristada ravimi ja teenuse kohta esitatud kaebused • Iga kaebuse menetlus dokumenteerida - juhtumi menetlemise andmed leitavad - millised järelmeetmed on vajalikud? - keda ja kuidas teavitatakse? • Perioodiline ülevaatus 27

Väljastamispiiranguga ravimid • • Väljastamispiirangu toiming teostatav igal ajahetkel 24/7 kättesaadav isik Kuidas leitavad klientide andmed Iga töötaja teab, kuidas toimida Toimingute dokumenteerimine Lõpparuanne Kogu teave pädevale isikule Tegutsemise tõhususe hindamine 28

Siseaudit Eeskirjade ja GDP põhimõtete järgimine, parendusettepanekute tegemine • Ajakava (Kes? Mida? Millal? ) • Läbiviijad on kompetentsed ja koolitatud • Dokumenteerida aruandena, kus on välja toodud: – auditeeritud toimingud – leitud puudused ja kõrvalekalded – rakendatavad ennetavad tegevused • Aruanne edastatakse juhtkonnale ülevaatuseks 29

Aitäh! inge. mae@ravimiamet. ee maris. dubova@ravimiamet. ee www. ravimiamet. ee
- Slides: 30