Gases nobles Son los elementos menos reactivos por

Gases nobles • Son los elementos menos reactivos, por lo tanto forman un número reducido de compuestos. • Todos los elementos del grupo 18, son gases monoatómicos a temperatura ambiente. • En la fase líquida, se forman dímeros en bajas concentraciones que se mantienen unidos por fuerzas de dispersión.
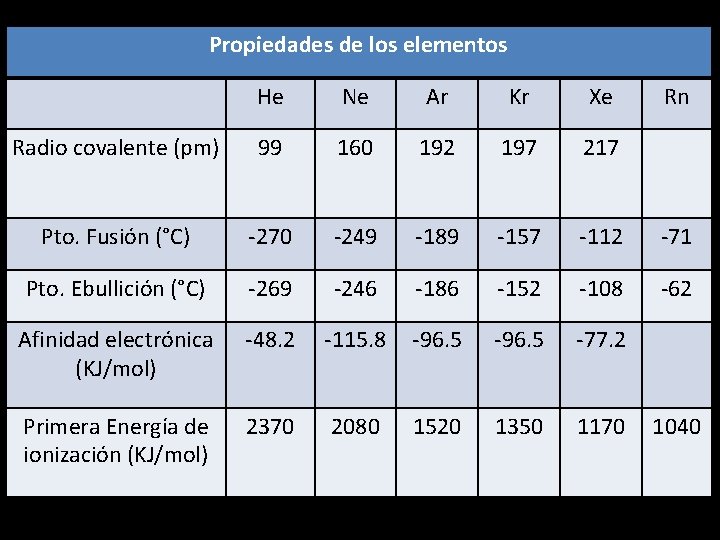
Propiedades de los elementos He Ne Ar Kr Xe Rn Radio covalente (pm) 99 160 192 197 217 Pto. Fusión (°C) -270 -249 -189 -157 -112 -71 Pto. Ebullición (°C) -269 -246 -186 -152 -108 -62 Afinidad electrónica (KJ/mol) -48. 2 -115. 8 -96. 5 -77. 2 Primera Energía de ionización (KJ/mol) 2370 2080 1520 1350 1170 1040
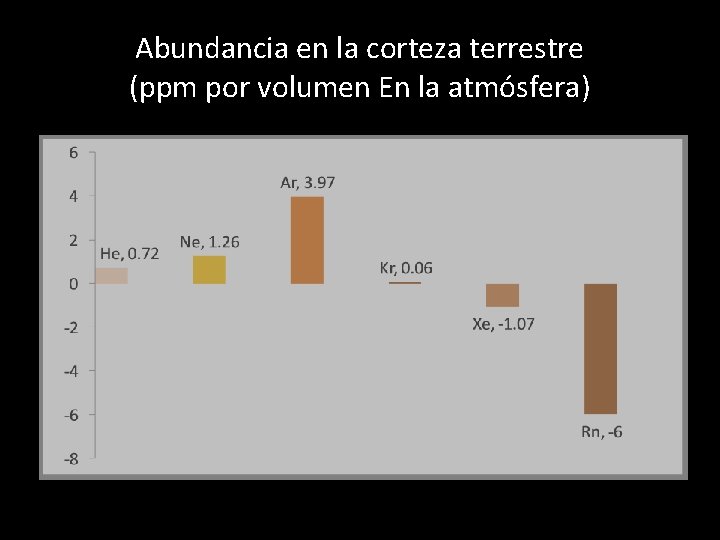
Abundancia en la corteza terrestre (ppm por volumen En la atmósfera)

Helio • • • Forma el 23% en masa del universo y del sol, y es el segundo elemento más abundante después del hidrógeno. Los átomos de helio son demasiado ligeros como para ser retenidos por el campo gravitacional de la Tierra. La mayor parte del helio en este planeta (5 ppm por volumen), proviene de las emisiones α que se originan en el decaimiento de los elementos radiactivos. Un pequeño porcentaje proviene de las partículas α del viento solar. Cuando se enfría por debajo de 2. 178 K, sufre una transición de fase a una segunda fase líquida conocida como He II. El helio sólido sólo se puede formar a alta presión.

Usos • Para inflar globos y zeppelines, a causa de su baja densidad y su naturaleza no combustible. • Por su bajo punto de ebullición se utiliza en tecnología criogénica y como refrigerante de muy baja temperatura. Es el refrigerante de los imanes superconductores usados tanto en la espectroscopía de RMN como en IRN (Imagenología por Resonancia Magnética). • Proporciona una atmósfera inerte adecuada para el crecimiento de cristales de materiales semiconductores como el Silicio. • Mezclado con O₂ en proporción 4: 1, se usa para generar una atmósfera artificial para los buzos.

• Es un gas incoloro e inodoro. • Se obtiene por destilación del aire líquido a baja temperatura. • Se han observado complejos endoédricos de fulereno para C+60, contenido como ión o átomo huésped el Neón.

• Es empleado comúnmente en diversas fuentes luminosas, como luces de neón y láser (He. Ne). Éstas fuentes luminosas funcionan cuando una descarga eléctrica pasa a través del gas, ioniza algunos de los átomos y promueve que tanto iones como átomos neutros pasen a estados excitados, emitiendo radiación electromagnética cuando regresan a su estado energético más bajo. • También se utiliza como refrigerante criogénico. Láser He. Ne

Argón • • • Serie química de Gases nobles Grupo 18 Periodo 3, bloque p Densidad 1, 784 Apariencia Incoloro

Obtención El gas se obtiene por medio de la destilación fraccionada del aire licuado, se encuentra en una proporción de aproximadamente el 0, 94%. • Casi todo el argón proviene de la desintegración radiactiva del isótopo del potasio K-40. • En la atmósfera terrestre, el Ar-39 se genera por bombardeo de rayos cósmicos a partir del Ar-40. • Los principales isótopos de argón presentes en la Tierra son Ar-40 (99, 6%), Ar-36 y Ar-38

Usos • Se usa en relleno de bombillas (impide la vaporización del wolframio y crea una atmósfera inerte para que el wolframio no reaccione químicamente). • Argón junto a vapor de mercurio, se utilizan para llenar lámparas fluorescentes. • Argón, mezclado con algo de neón, se emplea para llenado de tubos fluorescentes de descarga eléctrica, empleados en letreros de propaganda. Con el argón se obtiene un color azul o verde, en lugar del rojo del neón.

Y más usos… • En el buceo técnico, se emplea argón para el inflado de trajes secos • El láser de argón tiene usos médicos en odontología y oftalmología. Soldadura por arco y soldadura a gas.


Xenón Isótopos de 124 Xe a 126 Xe Grupo 18 Periodo 5, bloque p Densidad 5. 894 g/L Apariencia: Incoloro, inodoro Estado de oxidación: 0 0. 087 ppm en la atmósfera terrestre. (en menor proporción en algunos manantiales) • En tubos de gas, emite brillo azul cuando se aplica carga eléctrica. • •

Obtención y usos Es extraído comercialmente conjuntamente con nitrógeno e hidrógeno de la destilación de aire licuado. • Se usa en lámparas de láser de rubí, bactericidas y estroboscópicas, flashes fotográficos, faros de automóviles. • Puede ser usado como anestésico general. • Los perexenatos son usados como agentes oxidantes.

Reacciones • Xe + F 2 → Xe. F 2. • Ba 2 Xe. O 6 (s) + 2 H 2 SO 4 (aq) → H 4 Xe. O 6 (aq) + 2 Ba. SO 4 (s).

Reacciones • Xe + F 2 → Xe. F 2.
- Slides: 16