Gas ideal sebagai standar pembanding bagi sifatsifat gas


Gas ideal : sebagai standar pembanding bagi sifat-sifat gas nyata Larutan ideal : sebagai standar pembanding bagi sifat-sifat larutan nyata Pers. (3. 23): (3. 23) Larutan ideal didefinisikan sebagai larutan dengan: (4. 1)

Untuk besaran termodinamika yang lain, hubungannya mengikuti apa yang sudah diturunkan pada Bab 3. Dengan mengingat bahwa: maka (4. 2) Dengan cara yang sama: (4. 3)

Karena maka substitusi ers. (4. 1) dan (4. 2) akan menghasilkan: (4. 4) Summability relation, pers. (3. 11), jika diterapkan pada larutan ideal:

Jika diterapkan pada pers. (4. 1) sampai (4. 4): (4. 5) (4. 6) (4. 7) (4. 8)

ATURAN LEWIS/RANDALL Persamaan (3. 42): Untuk kasus khusus berupa larutan ideal: (4. 9) Jika persamaan (4. 1) dimasukkan ke pers. (4. 9): Selanjutnta persamaan (3. 27): (3. 27)

dimasukkan ke persamaan terakhir: (4. 10) Persamaan ini disebut ATURAN LEWIS-RANDALL Jika kedua sisi pers. (4. 10) dibagi dengan P xi, maka: (4. 11)

Definisi: (4. 12) (4. 13) Definisi ME analog dengan definisi MR ME – MR = – (Mid – Mig) Karena campuran gas ideal juga merupakan larutan gas ideal, maka pers. (4. 5) – (4. 8) juga berlaku untuk gas ideal:

(4. 14) (4. 15) (4. 16) (4. 17) Sehingga: Jika digabung dengan pers. Di slide sebelumnya: (4. 18)

Hubungan partial property analog dengan pers. (3. 45): (4. 19) Fundamental excess property relation: (4. 20)

ENERGI GIBBS EKSES DAN KOEFISIEN AKTIFITAS Persamaan (3. 42): (3. 42) Persamaan (4. 9): (4. 9) Jika pers. (4. 10): disubstitusikan ke pers. (4. 9) maka akan diperoleh: (4. 9 a)
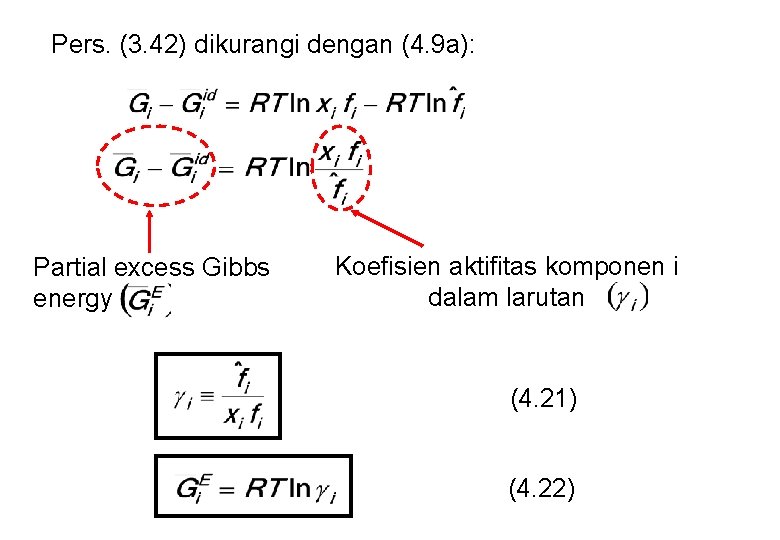
Pers. (3. 42) dikurangi dengan (4. 9 a): Partial excess Gibbs energy Koefisien aktifitas komponen i dalam larutan (4. 21) (4. 22)

Jika pers. (4. 22) dimasukkan ke (4. 20): (4. 23) (4. 24) (4. 25) (4. 26)
Pers. (4. 24– 4. 26) analog dengan pers. (3. 53– 3. 55) Dapat dihubungkan langsung dengan data PVT dan persamaan keadaan VE, HE, dan i dapat diukur dalam eksperimen • i dari data keseimbangan uapcair • VE dan HE dari data pencampuran

Diferensiasi pers. (4. 26) terhadap P: (4. 27)

Dengan cara yang sama akan diperoleh: (4. 28) Berdasarkan pers. (4. 26): ln i merupakan partial molar property, sehingga mengikuti aturan summability relation: (4. 29) Untuk sistem yang terdiri dari n mol, pers. (4. 29) menjadi:

Jika dideferensialkan: Pada T dan P konstan, menurut pers. (4. 23) berlaku: Jika kedua persamaan terakhir digabung akan diperoleh: (T dan P konstan) (4. 30)

Definisi koefisien aktifitas menurut pers. (4. 21): (4. 21) Untuk cairan, fugasitas komponen i murni fi didefinisikan dalam persamaan (3. 41): (3. 41)

Kriteria keseimbangan untuk sistem 2 fasa (uap-cair) multi komponen adalah kesamaan T, P, dan: (4. 31) Jika pers. (3. 48), pers. (4. 21), dan pers. (3. 41) dimasukkan ke pers. (4. 31) maka akan diperoleh: (4. 32) Atau: (4. 33)

Menurut persamaan (4. 22): (4. 22) merupakan partial molar property, sehingga: Atau: (4. 34) Untuk larutan biner, korelasi untuk energi bebas Gibbs berupa persamaan empiris.

MODEL SIMETRIS (4. 35) Definisi koefisien aktivitas menurut pers. (4. 26): (4. 26) GE merupakan fungsi x, bukan n ? ?

Untuk sistem biner: (4. 37) Definisi dari partial molar property:

Jika pers. (4. 37) dimasukkan ke pers. terakhir: (4. 38) Dengan cara yang sama: (4. 39)
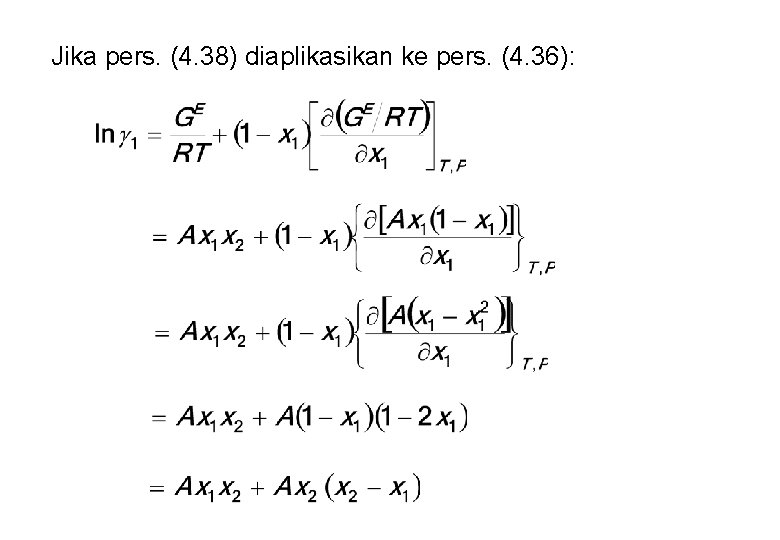
Jika pers. (4. 38) diaplikasikan ke pers. (4. 36):

(4. 40) Dengan cara yang sama akan diperoleh: (4. 41)

MODEL MARGULES (4. 42) (4. 43) (4. 44)

MODEL VAN LAAR (4. 45) (4. 46) (4. 47)

MODEL WILSON (4. 48) (4. 49) (4. 50) Vi. L : volume molar komponen cairan i murni
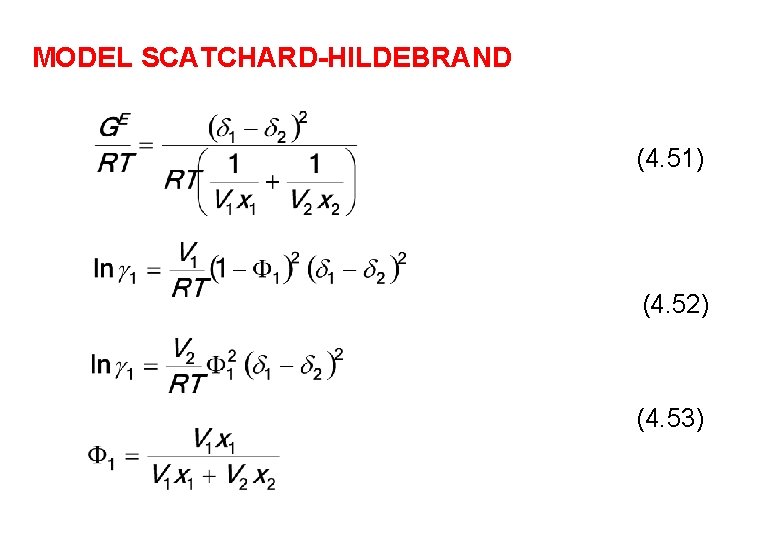
MODEL SCATCHARD-HILDEBRAND (4. 51) (4. 52) (4. 53)

INFINITE DILUTION MODEL SIMETRIS Pada konsentrasi = 0 atau pengenceran tak terhingga: x 1 0, maka x 2 1, sehingga pers. (4. 40) menjadi: Demikian juga untuk x 2 0, maka x 1 1, sehingga pers. (4. 41) menjadi: sehingga (4. 54)

MODEL VAN LAAR DAN MARGULES (4. 55) (4. 56) MODEL SCATCHARD-HILDEBRAND (4. 57) (4. 58)
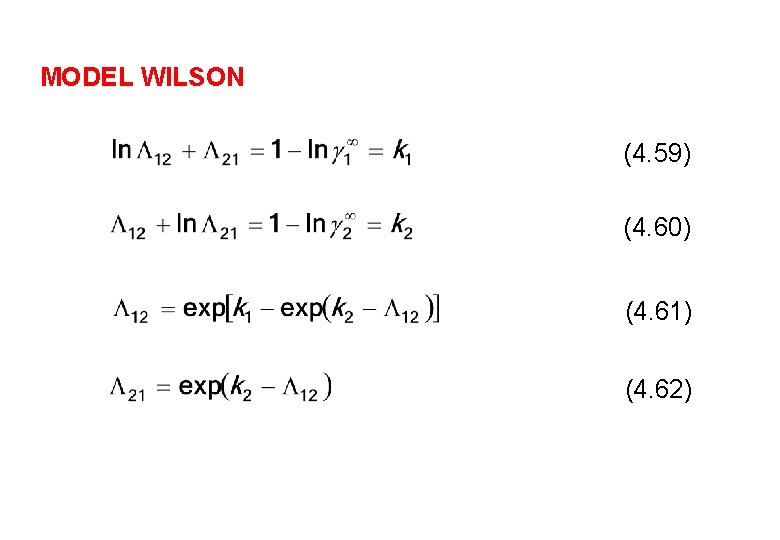
MODEL WILSON (4. 59) (4. 60) (4. 61) (4. 62)
- Slides: 32