FUNES QUMICAS Definio grupos de substncias com propriedades

FUNÇÕES QUÍMICAS Definição: grupos de substâncias com propriedades químicas semelhantes. Classificação Geral: Funções Inorgânicas Funções Orgânicas
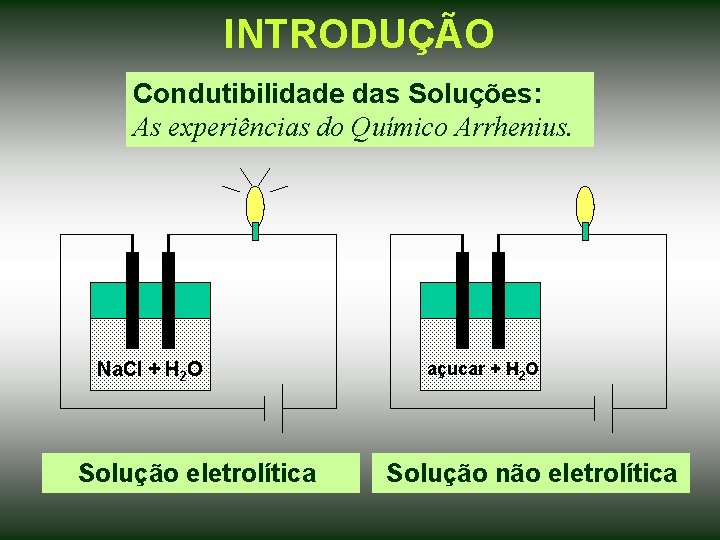
INTRODUÇÃO Condutibilidade das Soluções: As experiências do Químico Arrhenius. Na. Cl + H 2 O Solução eletrolítica açucar + H 2 O Solução não eletrolítica

FUNÇÕES INORG NICAS CLASSIFICAÇÃO: ÁCIDOS ÓXIDOS HIDRETOS SAIS BASES

Conceitos de Arrhenius: Ácidos, Hidretos e Bases Ácidos: substâncias que em meio aquoso se ionizam originando apenas cátions H+ (H 3 O+). Ex. : HCl + H 2 O H+ (H 3 O+). + Cl. Hidretos: compostos binários de hidrogênio. Ex. : HCl, KH, NH 3, etc. Bases: Compostos iônicos que em meio aquoso se dissociam liberando exclusivamente ânions OH-. Ex. : Na. OH Na+ + OH-

Conceitos de Arrhenius: Óxidos e Sais Óxidos: compostos binários onde o elemento mais eletronegativo é o oxigênio. Ex. : Fe 2 O 3, SO 3, Na 2 O, N 2 O, etc. Sais: compostos iônicos que em meio aquoso se dissociam liberando pelo menos um cátion diferente do H+ ou um ânion diferente do OH-. Ex. : Na. Cl, K 2 Cr 2 O 7, Na. H 2 PO 4, etc.

Definições Importantes Soluções iônicas – conduzem corrente elétrica. Soluções não iônicas – não conduzem corrente elétrica. Dissociação iônica – processo pelo qual a água separa os íons já existentes. Solvatação – envolvimento dos íons do soluto iônico pelas moléculas de água. Ionização – processo de formação de íons que não existiam por reação com a água. Dissolução – processo de separação de componentes não eletrolíticos por ação da água.

Definições Importantes Grau de dissociação iônica ( ) – relação entre o n° de unidades dissociadas ou ionizadas na solução pelo número de unidades inicial da substância. = n / N ou em porcentagem = n / N x 100 Eletrólito forte – 50% ( 0, 5) Eletrólito semiforte – 5% 50% (0, 05 0, 5) Eletrólito fraco – 5% ( 0, 05)

Exercícios de fixação: 1. Os compostos abaixo são, respectivamente: Ag. NO 3 NH 4 OH HCl. O 4 a) ácido, base, sal b) base, sal, base c) sal, base, ácido d) ácido, sal, ácido e) sal, base 2. (UCSal) Considere a apaparelhagem desenhada abaixo, empregada para teste de condutibilidade elétrica. O teste de condutibilidade elétrica deu resultado positivo com um dos líquidos abaixo. Qual deve ter sido? a) Oxigênio liquefeito. b) Nitrogênio liquefeito. c) Hélio liquefeito. d) água do mar. e) Gasolina.

Exercícios de fixação: 3. Assinale as proposições verdadeira: (01) Todo eletrólito é um composto iônico. (02) A equação HBr + H 2 O H 3 O + Br- representa a dissolução do HBr. (04) O açúcar (C 12 H 22 O 11) ao ser adicionado à água, sofre dissociação. (08) O HCl liquefeito conduz corrente elétrica. (16) O Na. OH emágua forma uma solução eletrolítica.

NOMENCLATURA DAS FUNÇÕES: ÓXIDOS, BASES E HIDRETOS

ÓXIDOS: Nomenclatura Ø Óxidos de metais com Nox fixo: lê-se óxido seguido do nome do elemento. Ex. : Na 2 O – óxido de sódio / Zn. O – óxido de zinco. Ø Óxidos de metais ou ametais com Nox variável: lêse óxido seguido do nome do elemento e do Nox escrito em algarismo romano. Ex. : Fe. O – óxido de ferro II. Au 2 O 3 – óxido de ouro III. SO 2 – óxido de enxofre IV.

Óxidos: Nomenclatura Ø Observações: 1) Óxidos de metais com dois Nox utiliza-se as terminações oso ou ico no cátion de menor e maior Nox, respectivamente. Ex. : Fe. O – óxido ferroso Au 2 O 3 – óxido áurico. Pb. O 2 – óxido plumbico.

Óxidos: Nomenclatura 2) A nomenclatura dos óxidos também pode ser feita indicando-se prefixos (mono, di, tri, etc. ) para o número de átomos de cada elemento: Ex. : Cl 2 O 5 pentóxido de dicloro. 3) Nox dos principais metais: Fe, Co e Ni + 2 e +3 Hg e Cu +1 e +2 Pb e Pt +2 e +4 Au +1 e +3

Óxidos: Nomenclatura 4) Os óxidos ácidos são chamados de anidridos e ganham terminações em função do Nox, vide tabela. Terminação Per ico oso Hipo oso Nox +7 (+3 + 4) +5 e +6 +3 e +4 +1 e +2 (+3) ico apenas para o boro - B (+4) ico apenas para o carbono - C Ex. : SO 3 anidrido sulfúrico / CO 2 anidrido carbônico Cl 2 O anidrido hipocloroso / Cl 2 O 5 anidrido clórico Mn 2 O 7 anidrido permangânico, etc.

BASES: Nomenclatura Ø Bases de metais com Nox fixo: lê-se hidróxido seguido do nome do metal. Ex. : Na. OH – hidróxido de sódio Ø Bases de metais com dois Nox: lê-se hidróxido seguido do nome do elemento e do Nox escrito em romano. Ex. : Fe(OH)2 – hidróxido de ferro II. Ø Observação: Hidróxidos de metais com dois Nox utilizase as terminações oso e ico no cátion de menor e maior Nox, respectivamente. Ex. : Fe(OH)3 – hidróxido férrico.

HIDRETOS: Nomenclatura Ø Hidretos de metais com Nox fixo: lê-se hidreto seguido do nome do metal. Ex. : Ca. H 2 – hidreto de cálcio. Ø Hidretos de metais com dois Nox: lê-se hidreto seguido do nome do elemento e do Nox escrito em romano. Ex. : Cu. H 2 – hidreto de cobre II. Ø Observação: hidretos de metais com dois Nox utiliza-se as terminações oso e ico no cátion de menor e maior Nox, respectivamente. Ex. : Ni. H 2 – hidreto niqueloso.

Exercícios de fixação: Dê o nome ou fórmula , para os seguintes compostos: 1. Mg. O 2. Pb 3 O 4 3. Ca(OH)2 4. Cu. H 5. Fe(OH)3 6. Óxido de alumínio 7. Óxido de potássio 8. Óxido de ferro III 9. Óxido plumboso 10. Óxido estânico 11. Hidreto de lítio 12. Hidróxido de zinco 13. Hidróxido ferroso 14. Hidreto de fósforo

CLASSIFICAÇÃO & REAÇÕES DAS FUNÇÕES: ÓXIDOS, BASES E HIDRETOS

ÓXIDOS: Classificação Geral Óxidos básicos fortes: alcalinos e alcalinos terrosos. Óxidos ácidos: ametais Exceção: Be. O (anfótero) Óxidos neutros: CO, N 2 O e NO (exceções) Óxidos básicos fracos: Nox = +1 e +2 Óxidos ácidos: Nox > +4 Óxidos anfóteros: Nox = +3 ou +4 Exceções: Zn. O e Pb. O (anfóteros) Água Óxidos básicos fortes Óxidos básicos fracos, ácidos ou anfóteros Óxidos ácidos ou neutros Não formam óxidos

ÓXIDOS: Regras de Classificação 1) Identificar o elemento combinado com o oxigênio se é: metal, ametal / semimetal. 2) Ametal: provavelmente óxido ácido, exceção para os óxidos neutros (NO, N 2 O e CO). O N 2 O é o gás hilariante. 3) Metal de Nox = + 8/3 (fórmula Me 3 O 4) - óxido salino. 4) Metal com Nox = +1 e +2 – óxido básico, exceção para o Be. O, Pb. O e Zn. O (anfóteros). Atenção para os peróxidos Nox do O = -1 e superóxidos Nox do O = - ½. 5) Metal com Nox > +4 – óxido ácido. 6) Metal com Nox = +3 e +4 – óxido anfótero

Óxidos: Classificação Química Ø Óxidos básicos: óxidos iônicos que reagem com água formando uma base ou com ácido formando sal e água. Reações: 1) Na 2 O + H 2 O 2 Na. OH 2) Fe. O + 2 HCl Fe. Cl 2 + H 2 O Ø Peróxidos: óxidos iônicos de caráter básico em que o oxigênio apresenta Nox = -1. Ø Reações: 1) Ca. O 2 + 2 H 2 O Ca(OH)2 + H 2 O 2 2) Ca. O 2 + 2 HNO 3 Ca(NO 3)2 + H 2 O 2

Óxidos: Classificação Química Ø Superóxidos: óxidos iônicos de caráter básico em que o oxigênio apresenta Nox = -1/2. Reações: 1) Ca. O 4 + 2 H 2 O Ca(OH)2 + H 2 O 2 + O 2 2) Ca. O 2 + 2 HNO 3 Ca(NO 3)2 + H 2 O 2 + O 2 Ø Óxidos ácidos: óxidos moleculares que reagem com água formando um ácido. Reações: 1) SO 3 + H 2 O H 2 SO 4 2) Mn 2 O 7 + 2 Na. OH 2 Na. Mn. O 4 + H 2 O 3) SO 3 + Mg. O Mg. SO 4 4) NO 2 + H 2 O HNO 2 + HNO 3

Óxidos: Classificação Química Ø Óxidos anfóteros: óxidos metálicos com caráter ácido e básico. Reações: 1) Zn. O + 2 HCl Zn. Cl 2 + H 2 O 2) Zn. O + Na. OH Na 2 Zn. O 2 + H 2 O Ø Óxidos neutros ou indiferentes: óxidos moleculares que não reagem com água nem com ácido ou base: CO, NO e N 2 O. Ø Óxidos duplos, mistos ou salinos: óxidos metálicos de fórmula geral Me 3 O 4, corresponde a soma de dois óxidos do elemento. Exemplos: Fe 2 O 3 + Fe. O = Fe 3 O 4 / Pb. O 2 + 2 Pb. O = Pb 3 O 4 Reações: 1) Fe 3 O 4 + 8 HCl 2 Fe. Cl 3 + Fe. Cl 2 + 4 H 2 O Fe 2 O 3 + 6 HCl 2 Fe. Cl 3 + 3 H 2 O Fe. O + 2 HCl Fe. Cl 2 + H 2 O

Bases: Classificação 1) Quanto ao número de hidroxila (OH-): Monobase, ex. : Na. OH / Dibase, ex. : Ba(OH)2 Tribase, ex. : Al(OH)3 / Tetrabase, ex. : Pb(OH)4 2) Quanto a solubilidade: Solúveis: bases do grupo 1 A e NH 4 OH Pouco solúveis: a maioria das bases do grupo 2 A Insolúveis: as demais, incluem Be(OH)2 e Mg(OH)2

Bases: Classificação 3) Quanto ao grau de dissociação: Fortes: bases dos grupos 1 A e 2 A. Fracas: as demais, inclue NH 4 OH 4) Quanto a volatilidade: Voláteis: NH 4 OH Fixas: as demais.

BASES: Reações 1) Reações com óxidos ácidos: 2 Na. OH + 2 NO 2 Na. NO 3 + Na. NO 2 + H 2 O 2) Reações de neutralização: Na. OH + HCl Na. Cl + H 2 O 3) Reações com sais: 2 Na. OH + Cu. Cl 2 Cu(OH)2 + 2 Na. Cl Na. OH + NH 4 Cl 2 2 Na. Cl + NH 3 + H 2 O Obs. Na primeira reação há a preciptação do Cu(OH)2, na segunda liberação do gás NH 3.

Hidretos: Classificação 1) Hidretos Iônicos: Nox do hidrogênio – 1 Ex. : Na. H, Ca. H 2 2) Hidretos Moleculares: Nox do hidrogênio +1 Ex. : Be. H 2, NH 3

NOMENCLATURA, CLASSIFICAÇÃO & REAÇÕES DAS FUNÇÕES: ÁCIDOS E SAIS

ÁCIDOS: Nomenclatura Ø Ácidos não Oxigenados ou Hidrácidos: lê-se ácido seguido do nome do elemento com a terminação ídrico. Ex. : HCl – ácido clorídrico. H 2 S – ácido sulfídrico. HCN – ácido cianídrico (caso especial). Ø Ácidos Oxigenados: lê-se ácido seguido do nome do elemento com prefixos e terminações especiais de acordo com o nome do anidrido que lhe deu origem. Ex. : H 2 SO 4 – ácido sulfúrico (origem SO 3 Nox do S = +6). HCl. O 4 – ácido perclórico ( origem Cl 2 O 5 Nox do Cl = +7)

ÁCIDOS: Nomenclatura especial Ø Ácidos originados de anidridos elementos P, Sb e As: reagem com um número variável de moleculas de água. Ganham os prefixos: orto - 3 H 2 O / piro - 2 H 2 O / meta - 1 H 2 O. Ex. : H 3 PO 4 - ácido ortofosfórico (P 2 O 5 + 3 H 2 O 2 H 3 PO 4) Ø Ácidos originados do B: reage com 3 ou 1 moléculas de água. Ganham os prefixos: orto - 3 H 2 O / meta - 1 H 2 O. HBO 2 – ácido metabórico (B 2 O 3 + H 2 O HBO 2) Ø Ácidos originados do Si: pode reagir com 2 ou 1 moléculas de água. Ganham os prefixos: piro - 2 H 2 O / meta - 1 H 2 O. H 4 Si. O 4 – ácido silícico (Si. O 2 + 2 H 2 O H 4 Si. O 4 ) Ø Ácidos originados do Cr: pode reagir com 1 ou duas moléculas do óxido crômico com uma de água formando os ácidos crômico e dicromico, H 2 Cr. O 4 e H 2 Cr 2 O 7, respectivamente.

Exercícios de fixação: Dê o nome ou fórmula, para os seguintes compostos: 1. HF 2. H 2 SO 3 3. H 2 S 4. HNO 3 5. H 2 Cr 2 O 7 6. H 3 PO 4 7. HNC 8. Ácido bromídrico 9. Ácido carbônico 10. Ácido permangânico 11. Ácido hiposulfuroso 12. Ácido brômico 13. Ácido cloroso 14. Ácido pirofosfórico
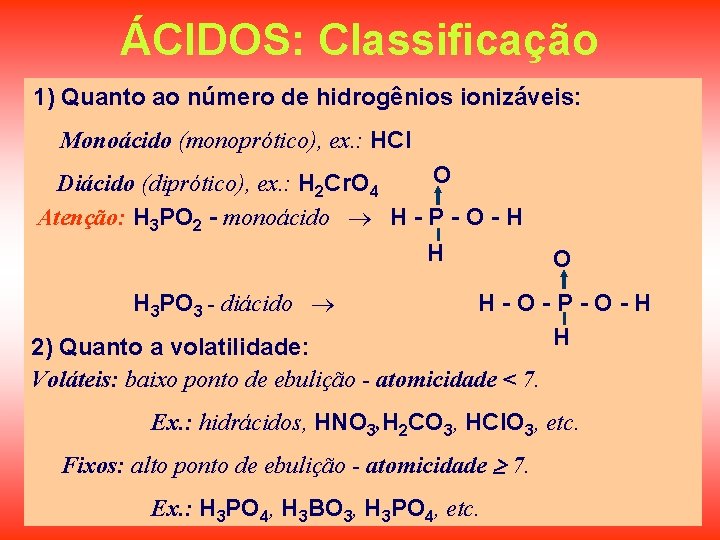
ÁCIDOS: Classificação 1) Quanto ao número de hidrogênios ionizáveis: Monoácido (monoprótico), ex. : HCl O Diácido (diprótico), ex. : H 2 Cr. O 4 Atenção: H 3 PO 2 - monoácido H - P - O - H H H 3 PO 3 - diácido O H-O-P-O-H H 2) Quanto a volatilidade: Voláteis: baixo ponto de ebulição - atomicidade < 7. Ex. : hidrácidos, HNO 3, H 2 CO 3, HCl. O 3, etc. Fixos: alto ponto de ebulição - atomicidade 7. Ex. : H 3 PO 4, H 3 BO 3, H 3 PO 4, etc.

Ácidos: Classificação 3) Quanto ao grau de dissociação ( ) Ácido fraco: < 0, 05 ( 5%) Ácido médio: 0, 05 0, 5 (5 - 50 %) Ácido forte: > 0, 5 (50%) Ø Hidrácidos: Fortes: HCl, HBr e HI / Médio: HF / Fracos: demais Ø Oxiácidos: depende da relação entre o número de H ionizavel e o número de O da molécula: Hx. Ez. Oy (y - x) / z > 1 - forte (y - x) / z = 1 - médio (y - x) / z < 1 - fraco Exceção: H 2 CO 3 - fraco ( = 0, 18%)

ÁCIDOS: Reações 1) Reações com metais: depende da reatividade, metais nobres não deslocam o Hidrogênio (Cu, Hg, Ag, Pt e Au) HCl + Cu não reage (metal nobre) HCl + Zn Zn. Cl 2 + H 2 2) Reações especiais: Cu + H 2 SO 4 Cu. SO 4 + 2 H 2 O + SO 2 Cu + 4 HNO 3 Cu(NO 3)2 + 2 H 2 O + 2 NO 2 Cu + 8 HNO 3 3 Cu(NO 3)2 + 4 H 2 O + 2 NO * Estas reações acontecem também com Ag e Hg / Au só reage com água régia, HCl + HNO 3, / Pt não reage.

Ácidos: Reações 3) Desidratação dos oxiácidos: H 2 SO 4 SO 3 + H 2 O 4) Reações de neutralização: HCl + Na. OH Na. Cl + H 2 O H 2 SO 4 + 2 Na. OH Na 2 SO 4 + 2 H 2 O

SAIS: Nomenclatura x Classificação Ø Os sais são obtidos da reação de um ácido com uma base dando origem a diversos tipos de sais: 1) Reação dos hidrácidos com monobases: HCl + Na. OH Na. Cl + H 2 O Nomenclatura: ídrico êto – cloreto de sódio (normal - halóide) 2) Reação dos oxiácidos com monobases: H 2 SO 4 + Na. OH Na 2 SO 4 + 2 H 2 O Nomenclatura: ico ato – sulfato de sódio (normal – oxi-sal) H 2 SO 3 + Na. OH Na 2 SO 3 + 2 H 2 O Nomenclatura: oso ito – sulfito de sódio (normal – oxi-sal)

SAIS: Nomenclatura x Classificação H 2 SO 4 + Na. OH Na. HSO 4 + H 2 O Nomenclatura: hidrogeno sulfato de sódio, sulfato ácido de sódio ou bisulfato de sódio (sal ácido ou hidrogeno sal – oxi-sal) 3) Reação dos hidrácidos ou oxiácidos com polibases: HCl + Ca(OH)2 Ca. OHCl + H 2 O Nomenclatura: hidróxi cloreto de cálcio ou cloreto básico de cálcio (hidroxi sal ou sal básico) Obs. O caráter ácido ou básico do sal depende do ácido ou base que lhe deram origem e não da presença do H+ e OH- no sal. Ø Cu. SO 4 + 5 H 2 O Cu. SO 4. 5 H 2 O Nomenclatura: sulfato de cobre II pentahidratado ou sulfato cúprico pentahidratado (oxi-sal hidratado).

SAIS: Fórmula x Nomenclatura Ø A obtenção da fórmula de sais a partir do nome do sal segue a mesma seqüência da obtenção da fórmula dos ácidos: Ex. 1: Sulfato de ferro II Ato Nox do enxofre = 6+ SO 3 + H 2 O H 2 SO 4 Fe. SO 4 Ex. 2: Hipoclorito de sódio Ito Nox do cloro = 1+ Cl 2 O + H 2 O 2 HCl. O Na. Cl. O Obs. A carga do ânion corresponde ao n° de H ionizável do ácido.

Exercícios de fixação: Dê o nome ou fórmula , para os seguintes compostos: 1. KF 2. Na 2 SO 3 3. Zn. S 4. Na. NO 3 5. K 2 Cr 2 O 7 6. Rb. H 2 PO 4 7. NH 4 NC 8. Brometo de lítio 9. Hidróxi carbonato de cálcio 10. Permanganato de cálcio 11. Hiposulfito de sódio 12. Metaborato de potássio 13. Perclorato de bário 14. Hidrogenosulfato de potássio
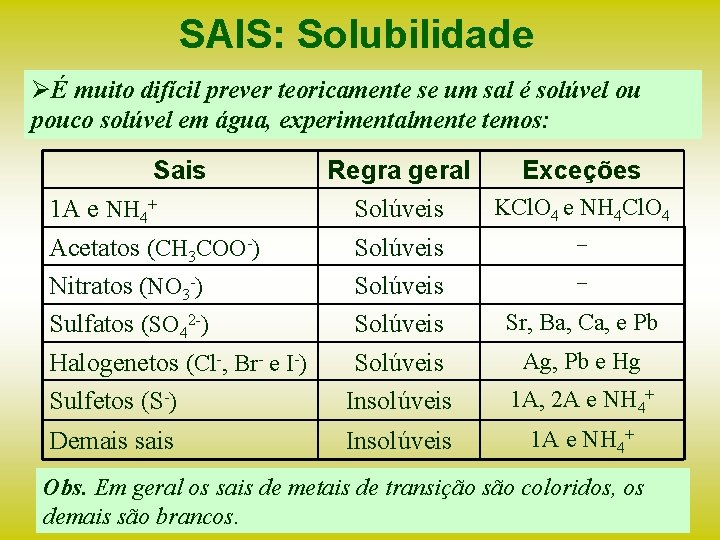
SAIS: Solubilidade ØÉ muito difícil prever teoricamente se um sal é solúvel ou pouco solúvel em água, experimentalmente temos: Sais Regra geral Exceções KCl. O 4 e NH 4 Cl. O 4 1 A e NH 4+ Solúveis – Acetatos (CH 3 COO-) Solúveis – Nitratos (NO 3 -) Solúveis Sr, Ba, Ca, e Pb Sulfatos (SO 42 -) Solúveis Ag, Pb e Hg Halogenetos (Cl-, Br- e I-) Solúveis 1 A, 2 A e NH 4+ Sulfetos (S-) Insolúveis Demais sais Insolúveis 1 A e NH 4+ Obs. Em geral os sais de metais de transição são coloridos, os demais são brancos.

SAIS: Reações Ø Sal + metal – depende da ordem de reatividade dos metais envolvidos na reação. Ex. : Cu. SO 4 + Zn Zn. SO 4 + Cu Ø Sal + ácido – ocorrem em três hipóteses: 1) Formação de um ácido mais fraco: Fe(CN)2 + 2 HNO 3 Fe(NO 3)2 + 2 HCN 2) Formação de um ácido volátil: 2 Na. Cl + H 2 SO 4 Na 2 SO 4 + 2 HCl 3) Formação de um sal insolúvel: Ba. Cl 2 + H 2 SO 4 Ba. SO 4 + 2 HCl

SAIS: Reações Ø Sal + base – ocorrem em três hipóteses: 1) Formação de um sal ou base insolúvel: 2 Na. OH + Cu. SO 4 Cu(OH)2 + Na 2 SO 4 2) Formação de uma base mais fraca: 2 Na. OH + Ca(NO 3)2 2 Na. NO 3 + Ca(OH)2 3) Formação de uma base volátil: Na. OH + NH 4 Cl Na. Cl + NH 4 OH (NH 3 + H 2 O) Ø Sal 1 + Sal 2 –formação de um sal insolúvel: KCl + Ag. NO 3 Ag. Cl + KNO 3

Exercícios de fixação: 1. A única alternativa incorreta é: a) Fe 3 O 4 é um óxido salino. b) N 2 O é um óxido neutro. c) Ca. O é um óxido anfótero. d) Cl 2 O 7 é um óxido ácido. e) H 2 O 2 é um peróxido. 2. Com relação às bases é incorreto afirmar: a) As bases ou hidróxidos têm fórmula geral M(OH)x, onde M é um metal ou íon NH 4+. b) As dibases têm fórmula geral M(OH)2. c) As bases alcalinas são fortes. d) O NH 4 OH é praticamente insolúvel em água. e) Todas as bases de metais de transição pode ser classificada em fraca e insolúvel.

Exercícios de fixação: 3. O ácido que corresponde à classificação monoácido e ternário é: a) HNO 3 b) H 2 SO 4 c) H 3 PO 4 d) HCl e) HCNO 4. Dentre os ácidos abaixo, o de maior grau de ionização é: a) H 4 P 2 O 7 b) H 2 SO 3 c) HNO 2 d) HCl. O 4 e) H 3 BO 3 5. Os seguintes sais são solúveis em água: a) KCl e Ba. CO 3 b) Ag. Cl e Na. NO 3 c) K 2 Cr 2 O 7 e KMn. O 4 d) KCl. O 4 e Ni. S e) Na. HCO 3 e Ca. CO 3

NOVOS CONCEITOS DE ÁCIDOS E BASES

Complemento do Conceito de Arrhenius Ácidos – Conceito original: substâncias que em meio aquoso se ionizam originando apenas cátions H+. aq Ex. : HCl H+ + ClÁcidos – Conceito atual: substâncias que reagem com água originando íons hidroxônio – H 3 O+. Ex. : HCl + H 2 O H 3 O+ + Cl. Bases – mantido o mesmo conceito.

Limitações do Conceito de Arrhenius Restrito a soluções aquosas. Outros solventes também ionizam ácidos e dissociam bases. Incapaz de prever o caráter de ácidos não hidrogenados ou bases sem hidroxilas.
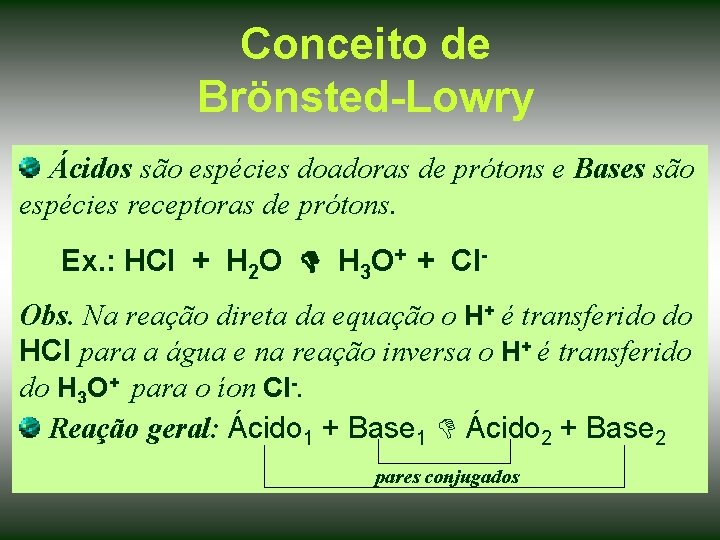
Conceito de Brönsted-Lowry Ácidos são espécies doadoras de prótons e Bases são espécies receptoras de prótons. Ex. : HCl + H 2 O H 3 O+ + Cl. Obs. Na reação direta da equação o H+ é transferido do HCl para a água e na reação inversa o H+ é transferido do H 3 O+ para o íon Cl-. Reação geral: Ácido 1 + Base 1 Ácido 2 + Base 2 pares conjugados
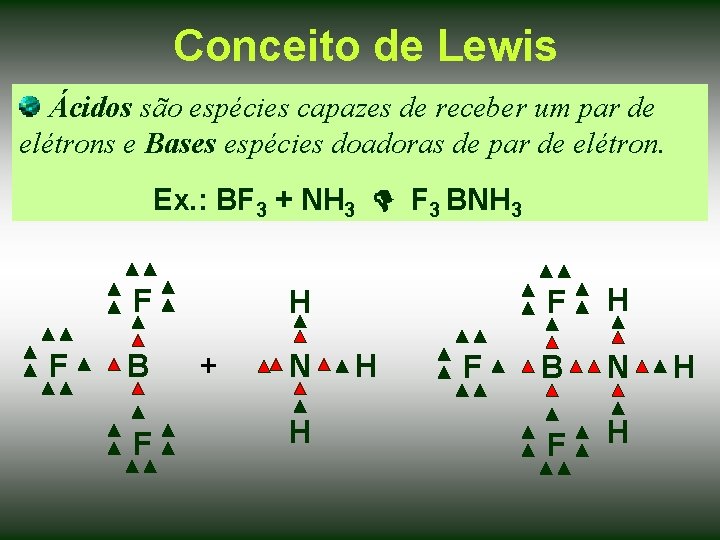
Conceito de Lewis Ácidos são espécies capazes de receber um par de elétrons e Bases espécies doadoras de par de elétron. Ex. : BF 3 + NH 3 F 3 BNH 3 F F B F H + N H H F F H B N F H H

Exercícios de fixação: 1. (FUC-MT) No equilíbrio HCl + NH 3 NH 4+ + Cl-, podemos afirmar que de acordo com o conceito de ácido e base de Brösted-Lowry: a) NH 4+ atua como base. b) NH 3 atua como base. c) HCl atua como base. d) Cl- atua como ácido. e) NH 3 atua como ácido. 2. Julgue as proposições: (01) Na reação HCl + NH 3 NH 4+ + Cl-, o HCl funciona como ácido segundo Arrhenius. (02) Na reação HCl + HF H 2 F + + Cl-, os pares conjugados são: HCl/Cl- e HF/ H 2 F +. (04)Na reação Co+3 + 6 NH 3 [Co(NH 3 )6 ]+3 o cátion cobalto (Co+3) funciona como ácido de Lewis. (08) As bases de Lewis são também bases de Brösted-Lowry. (16) Os ácidos de Arrhenius são também ácidos segundo Lewis.
- Slides: 50