Fundamentos de Espectrometra de Masa Biolgica Matas Mller

Fundamentos de Espectrometría de Masa Biológica Matías Möller 3 de mayo de 2013 Lab. Fisicoquímica Biológica Instituto de Química Biológica Facultad de Ciencias Universidad de la República 1

Bibliografía recomendada: Physical Biochemistry, Van Holde, 2006, 2 nd Ed. Cap. 15. J. Chem. Ed. , Vestling, 2003, Vol. 80, p. 122. Introduction to proteomics, Liebler, 2002. 2

Espectrometría de masa 1 - Generalidades 2 - MALDI-TOF 3 - ESI-Q 4 - Peptide Mass Fingerprinting y tandem MS 3

Espectrometría de masa 1 - Generalidades 4

Espectrometría de masa Técnica que permite la separación y determinación de la relación masa/carga de iones gaseosos 5

Espectrometría de masa Espectrometría ≠ Espectroscopía (Medición de un rango) (implica absorción o emisión de energía radiante) 6

Espectrometría de masa de Biomoléculas Determinación de masa y/o composición: v Péptidos, Proteínas, Complejos Supramoleculares v Polisacáridos, oligosacáridos v Lípidos Lipidoma v Fragmentos de ácidos nucleicos Técnica muy sensible: puede analizar mg-ng (y menos) de material 7

Espectrometría de masa de Proteínas v Determinación de masa y/o composición v Identificación por comparación con bases de datos (peptide mass fingerprint) y secuenciación de péptidos v Modificaciones postraduccionales v Complejos Supramoleculares: Interacción entre proteínas Interacción compuestos de bajo PM v Plegamiento v Niveles de expresión/modificación posttraduccional 8

Gel 2 D de hígado humano http: //ca. expasy. org/swiss-2 dpage/ 9
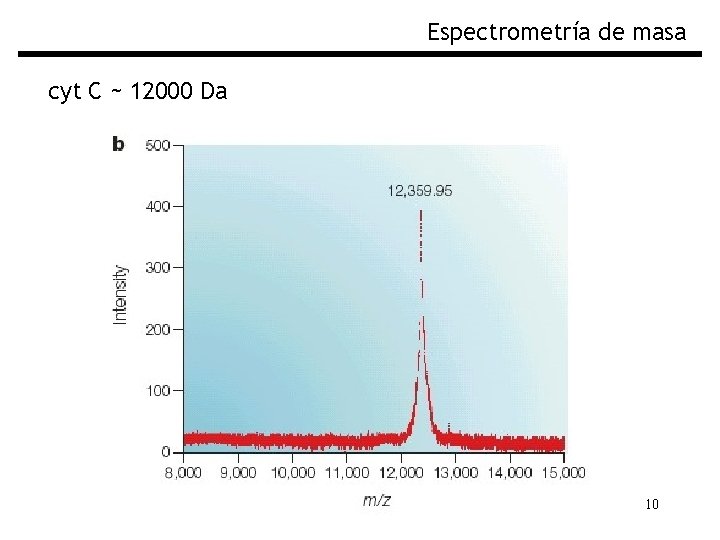
Espectrometría de masa cyt C ~ 12000 Da 10
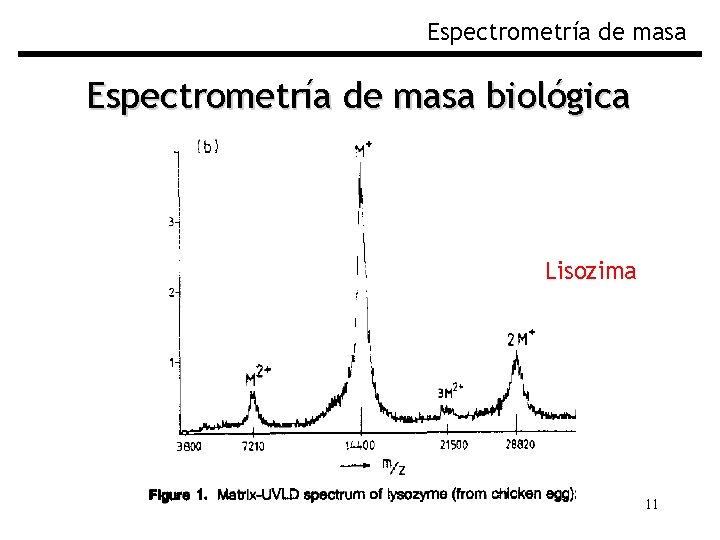
Espectrometría de masa biológica Lisozima 11

Espectrometría de masa Los Iones son importantes En el proceso de Ionización se forman diferentes tipos de iones cambios en m/z: [M+H]+ o [M-H]De la protonación o deprotonación de aminas, carboxilos, fenoles, fosfatos, sulfatos (pueden ser [M+2 H]2+, [M+n. H]n+) [M+Na]+, [M+K]+, [M+NH 4]+, [M+Cl]- De la unión de iones especialmente a moléculas que contienen oxígeno (Na = 23 Da; K = 39 Da) [M]*+, [M]*(oxidación o reducción monoelectrónica-no muy común) 12
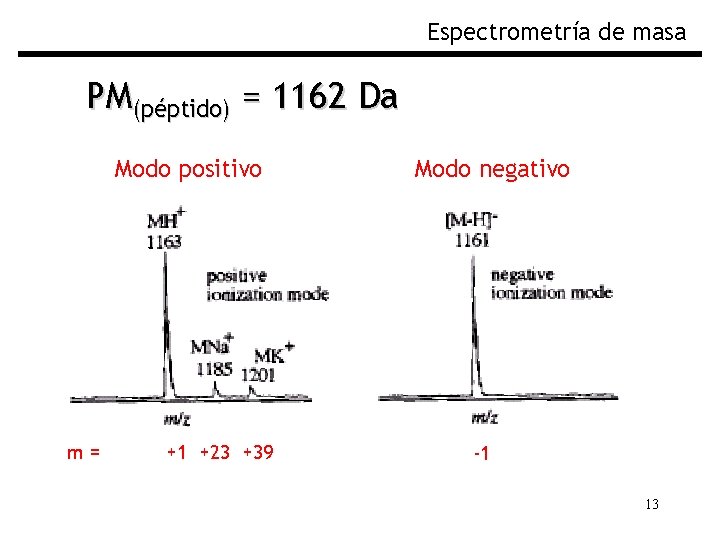
Espectrometría de masa PM(péptido) = 1162 Da Modo positivo m= +1 +23 +39 Modo negativo -1 13
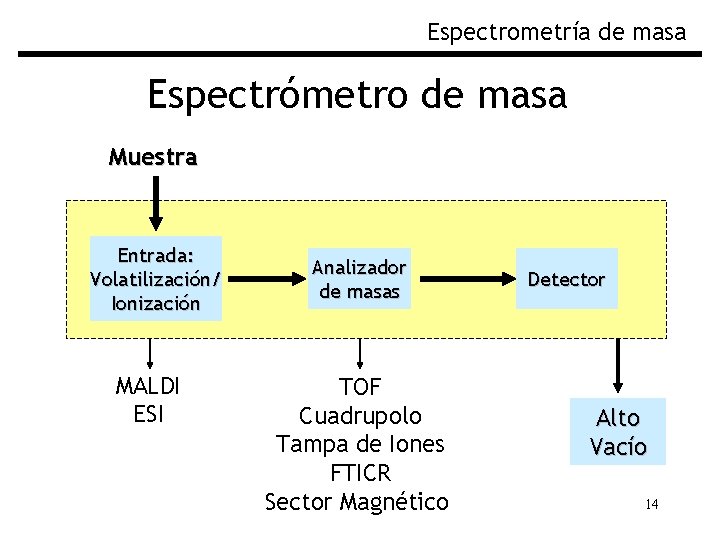
Espectrometría de masa Espectrómetro de masa Muestra Entrada: Volatilización/ Ionización MALDI ESI Analizador de masas TOF Cuadrupolo Tampa de Iones FTICR Sector Magnético Detector Alto Vacío 14

Espectrometría de masa ¿Cómo volatilizar una proteína? Premio Nobel de Química 2002 Fenn (1988)- ESI: Electrospray Ionization Tanaka (1988)- LDI: Laser Desorption/Ionization Sin Premio: Karas y Hillenkamp (1988)- MALDI: Matrix Assisted LDI (como se usa ahora, pero Tanaka hizo volar una proteína antes) 15

Espectrometría de masa Espectrómetros de masa (configuraciones para grandes biomoléculas) MALDI-TOF: Matriz Assisted Laser Desorption/Ionization. Time of Flight ESI-Q: Electro. Spray Ionization-Quadrupole ESI-IT: Electro. Spray Ionization-Ion Trap FT-MS: FT-MS Fourier-Transform Ion Cyclotron Resonance 16

Espectrometría de masa 2 - MALDI-TOF 17

Espectrometría de masa Ionización por MALDI: (Matrix assisted Laser desorption/ionization) Las Biomoléculas se mezclan con una matriz que absorbe energía de un laser y al disiparla produce la coevaporación de la muestra: La energía agregada hace que la matriz “explote”, llevando la proteína cargada hacia la entrada del analizador. El proceso de desorción está asociado con una transferencia de H+. Las proteínas cargadas son dirigidas al analizador mediante un campo eléctrico 18
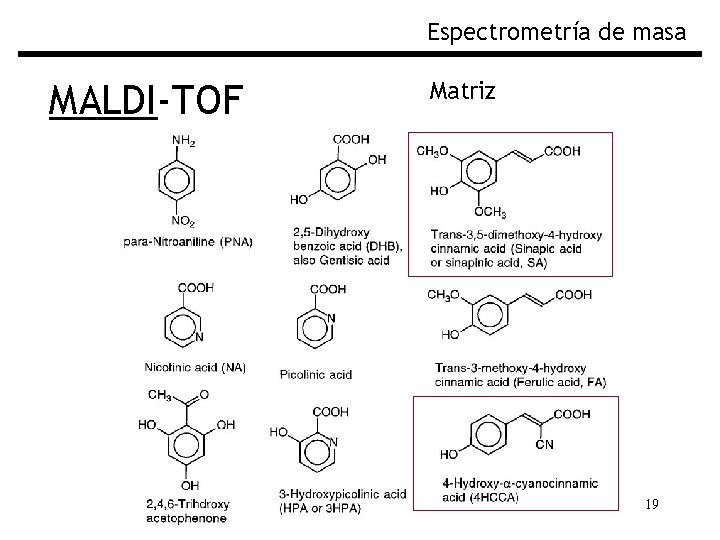
Espectrometría de masa MALDI-TOF Matriz 19
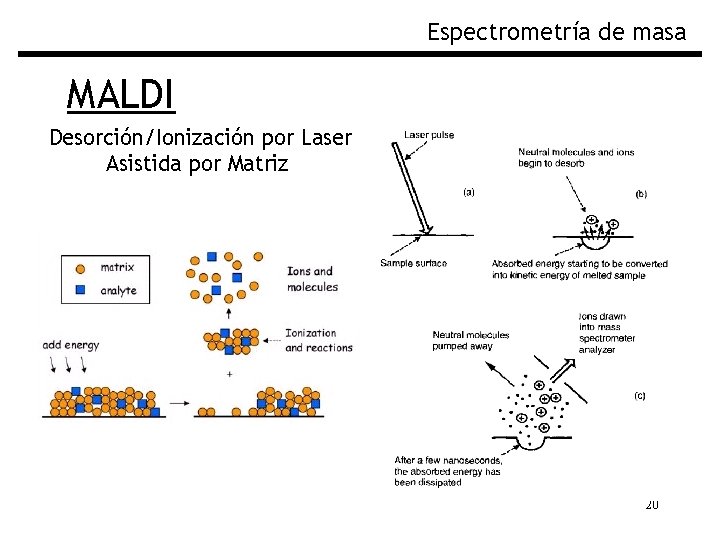
Espectrometría de masa MALDI Desorción/Ionización por Laser Asistida por Matriz 20

Espectrometría de masa MALDI-TOF Se determina la masa de las moléculas cargadas de acuerdo a su “tiempo de vuelo”(t). t (m/z)1/2 las partículas con menor m/z llegan antes al detector No tienen muy buena resolución, pero son robustos, simples y tienen un virtualmente ilimitado rango de masas (300 k. Da) 21

Espectrometría de masa MALDI-TOF Los iones positivos generados en la fuente por MALDI son acelerados por un campo eléctrico E, que le imparte una energía cinética: Ek = ze. Es donde s es la distancia de la región de la fuente. Entonces entran a una región (tubo) sobre la que no actúa ningún campo. los iones con igual carga tienen la misma Ek, ½mv 2 = ze. Es v = (2 ze. Es/m)½ t = D/v = (m/2 ze. Es)½D m/z = 2 e. Es(t/D)2 22
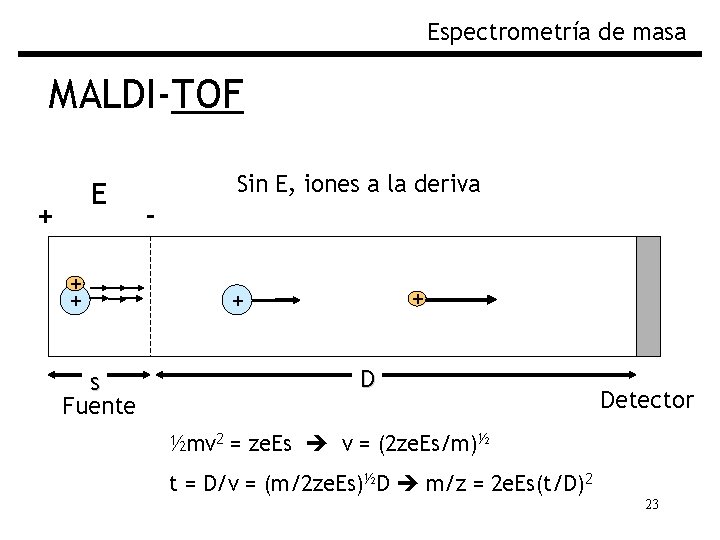
Espectrometría de masa MALDI-TOF E + Sin E, iones a la deriva Fig. Separación por TOF + + s Fuente + + D Detector ½mv 2 = ze. Es v = (2 ze. Es/m)½ t = D/v = (m/2 ze. Es)½D m/z = 2 e. Es(t/D)2 23
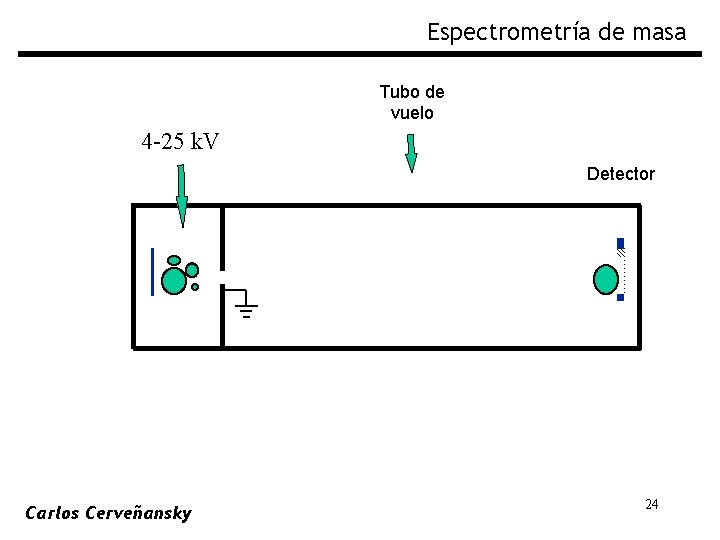
Espectrometría de masa Tubo de vuelo 4 -25 k. V Detector Carlos Cerveñansky 24
Espectrometría de masa Tubo de vuelo 4 -25 k. V Detector Carlos Cerveñansky 25
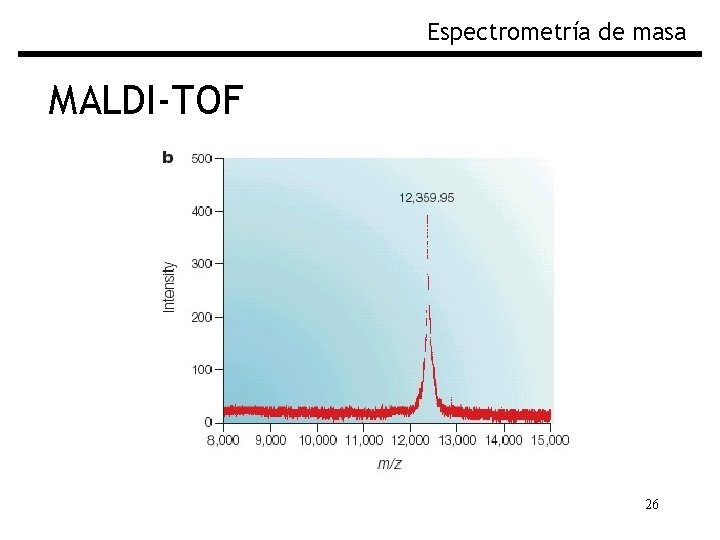
Espectrometría de masa MALDI-TOF 26
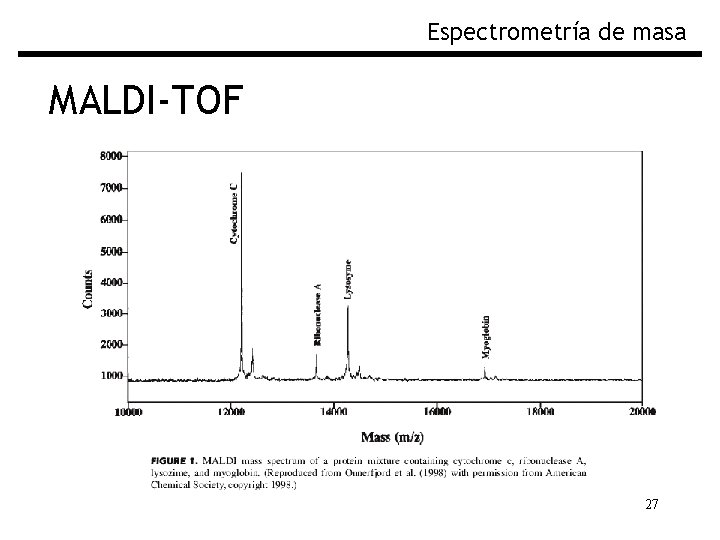
Espectrometría de masa MALDI-TOF Fig. Espectro de masas por MALDI-TOF 27
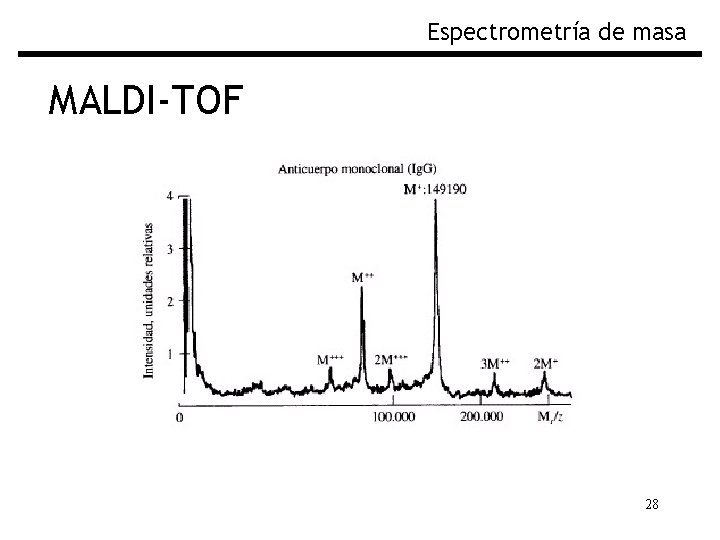
Espectrometría de masa MALDI-TOF 28
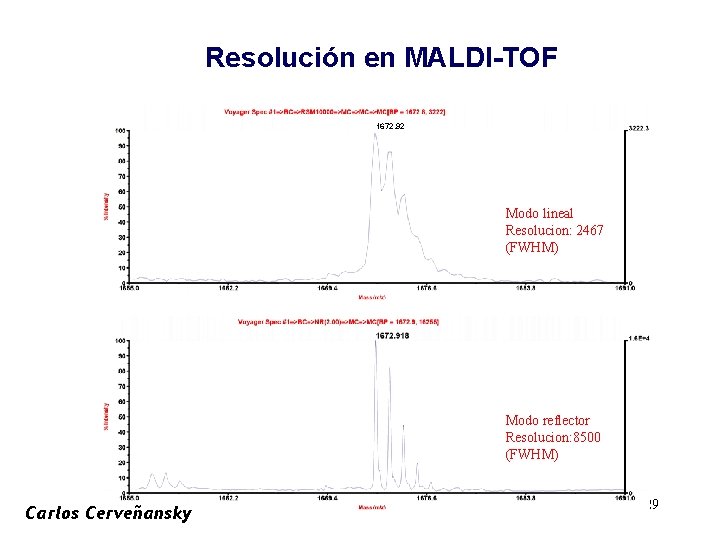
Resolución en MALDI-TOF 1672. 92 Modo lineal Resolucion: 2467 (FWHM) Modo reflector Resolucion: 8500 (FWHM) Carlos Cerveñansky 29

Espectrometría de masa Los Isótopos son importantes Los espectrómetros de masa diferencian entre isótopos Pesos moleculares: Unidades de masa atómica (amu), se basa en una escala relativa al 126 C = 12 amu 1 amu = 1 dalton = 1. 66054 x 10 -24 g Abundancia isotópica: 12 C 13 C 12. 0000 13. 0034 98. 90 % 1. 10 % 30
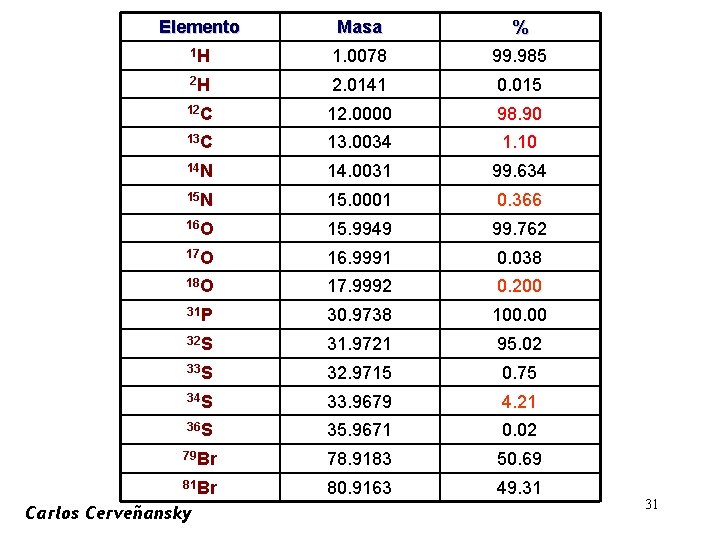
Elemento Masa % 1 H 1. 0078 99. 985 2 H 2. 0141 0. 015 12 C 12. 0000 98. 90 13 C 13. 0034 1. 10 14 N 14. 0031 99. 634 15 N 15. 0001 0. 366 16 O 15. 9949 99. 762 17 O 16. 9991 0. 038 18 O 17. 9992 0. 200 31 P 30. 9738 100. 00 32 S 31. 9721 95. 02 33 S 32. 9715 0. 75 34 S 33. 9679 4. 21 36 S 35. 9671 0. 02 79 Br 78. 9183 50. 69 81 Br 80. 9163 49. 31 Carlos Cerveñansky 31

Carlos Cerveñansky 32
![Voyager Spec #1=>MC[BP = 2469. 5, 12005] 2 x. C 13 100 90 2093 Voyager Spec #1=>MC[BP = 2469. 5, 12005] 2 x. C 13 100 90 2093](http://slidetodoc.com/presentation_image_h/85fd178fa81a96c7233960fd8117f334/image-33.jpg)
Voyager Spec #1=>MC[BP = 2469. 5, 12005] 2 x. C 13 100 90 2093 C 13 80 % Intensity 70 60 50 40 C 12 30 20 10 0 5725 5729 5733 Mass (m/z) 5737 5741 5745 Espectro de masa con resolución isotópica de insulina bovina. (aprox. 0. 15 pmoles, 0. 8 ng, en 1 ml de muestra; matriz: CHCA; R= 13800 FWHM) Carlos Cerveñansky 33 0
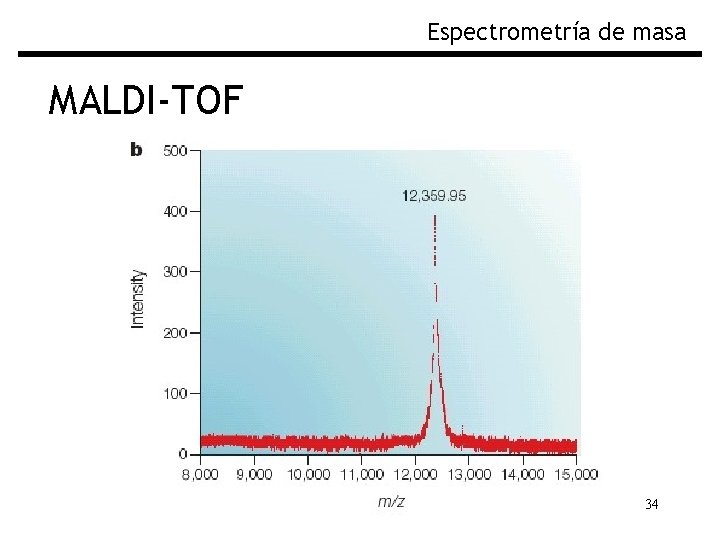
Espectrometría de masa MALDI-TOF 34

Espectrometría de masa 3 - ESI-MS 35

Espectrometría de masa ESI-Q Electro. Spray Ionization - Quadrupole Las Proteínas se introducen al analizador por un capilar sometido a un fuerte voltaje, rodeado por un flujo de N 2 (gas secante). El fuerte voltaje hace que se formen gotas muy pequeñas cargadas (spray), donde el solvente termina de evaporarse y las proteínas cargadas viajan hacia el analizador El Analizador es un “filtro de masa” cuadrupolo 36
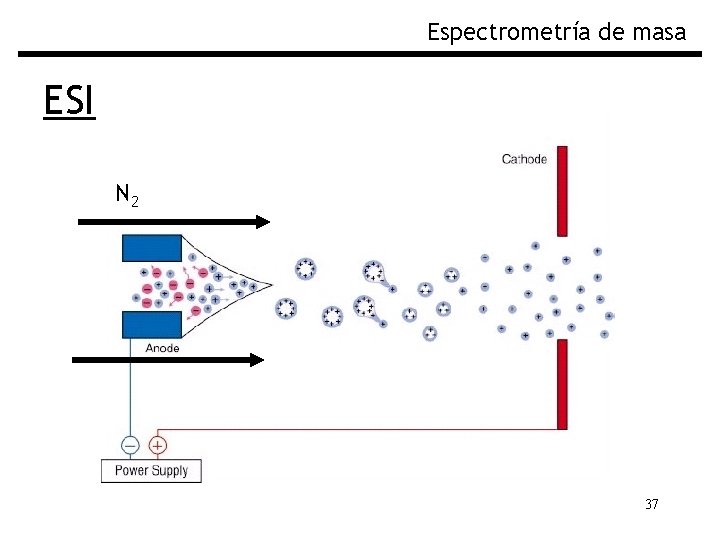
Espectrometría de masa ESI N 2 37
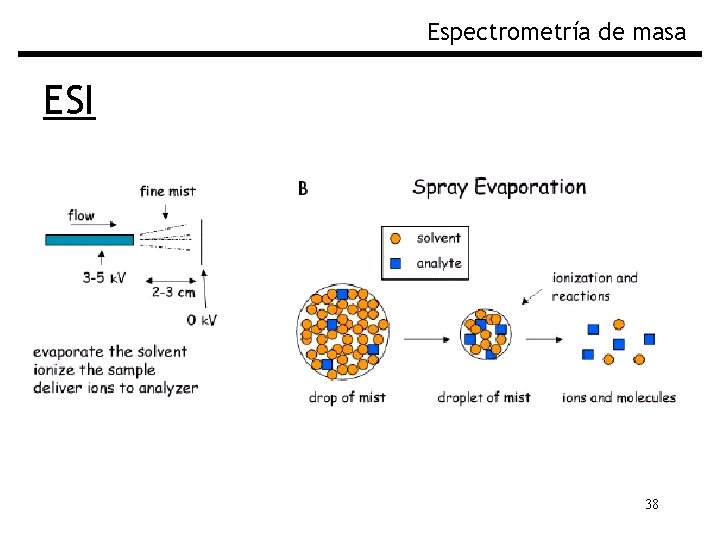
Espectrometría de masa ESI 38

Espectrometría de masa ESI-Q Al analizador de masas de Cuadrupolo se le llama “Filtro de Masas” porque normalmente transmite iones de un pequeño rango de m/z, todos los otros iones son neutralizados y eliminados. Variando las señales eléctricas de un cuadrupolo es posible variar la m/z y realizar un barrido espectral Consiste en cuatro barras cilíndricas metálicas que sirven de electrodos del filtro de masas Robustos, baratos y tienen tiempos de barrido breves, no tienen muy buena resolución y el rango de m/z llega hasta 3000 39
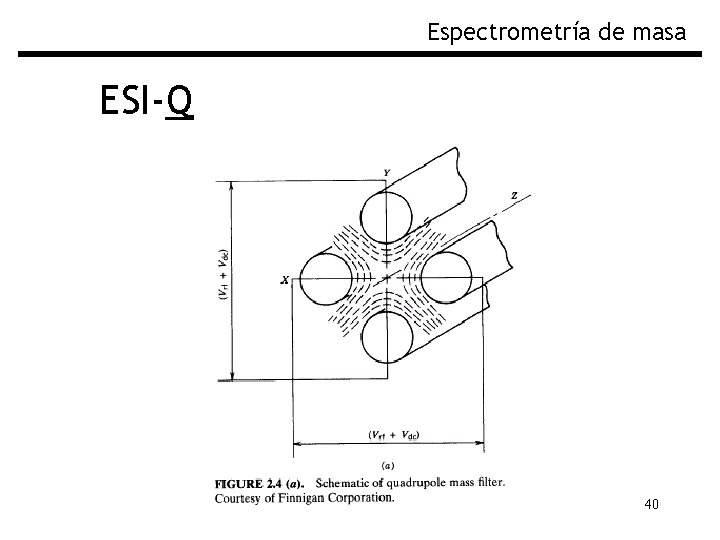
Espectrometría de masa ESI-Q 40
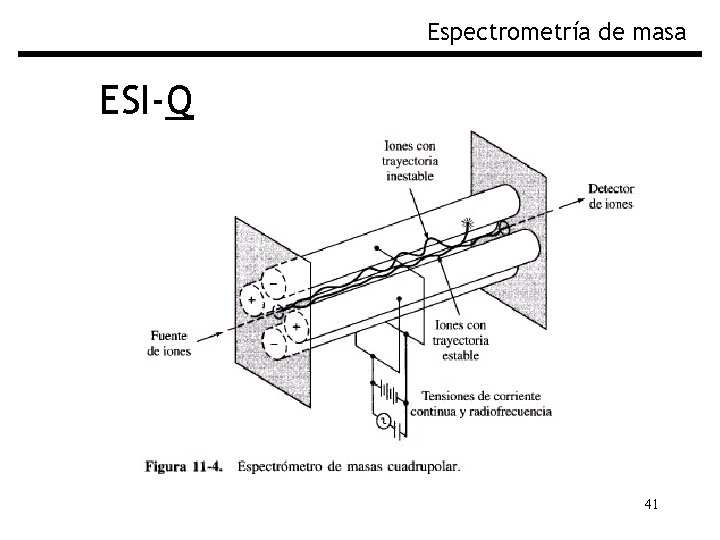
Espectrometría de masa ESI-Q 41
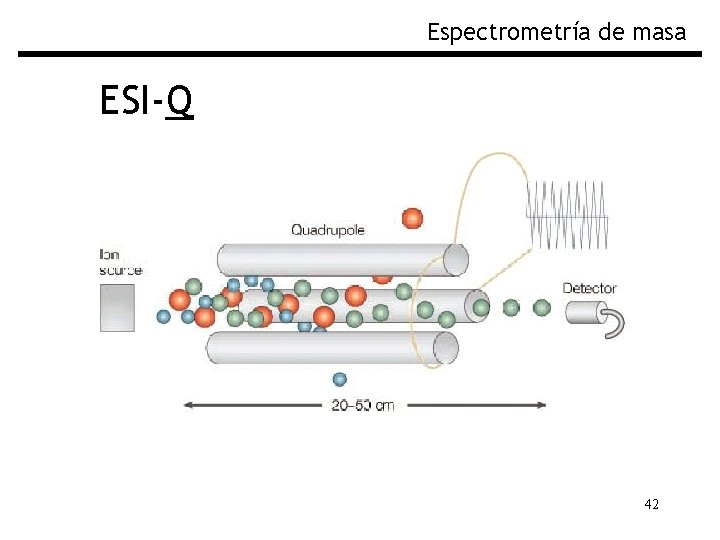
Espectrometría de masa ESI-Q 42
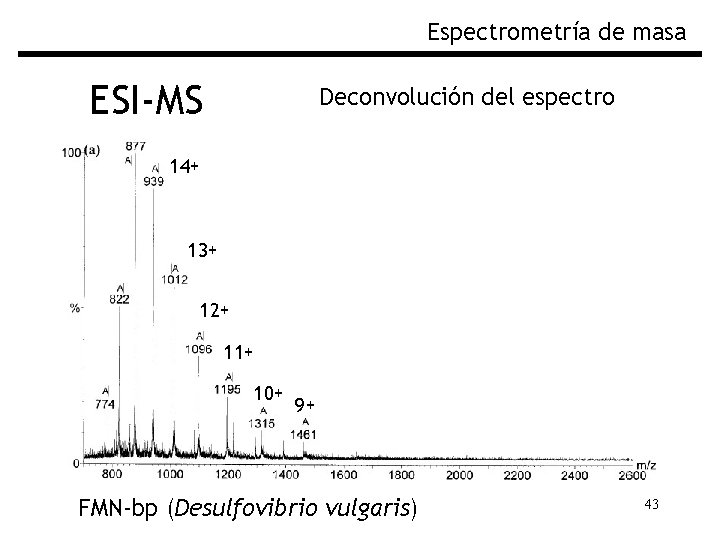
Espectrometría de masa ESI-MS Deconvolución del espectro 14+ 13+ 12+ 11+ 10+ 9+ FMN-bp (Desulfovibrio vulgaris) 43
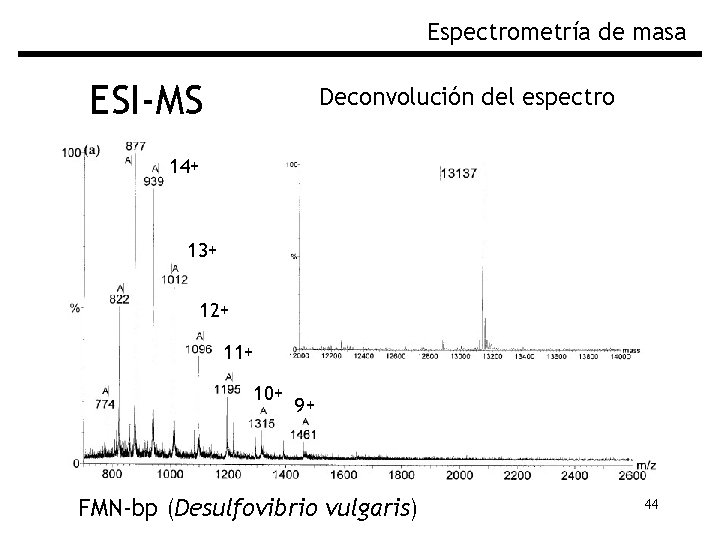
Espectrometría de masa ESI-MS Deconvolución del espectro 14+ 13+ 12+ 11+ 10+ 9+ FMN-bp (Desulfovibrio vulgaris) 44
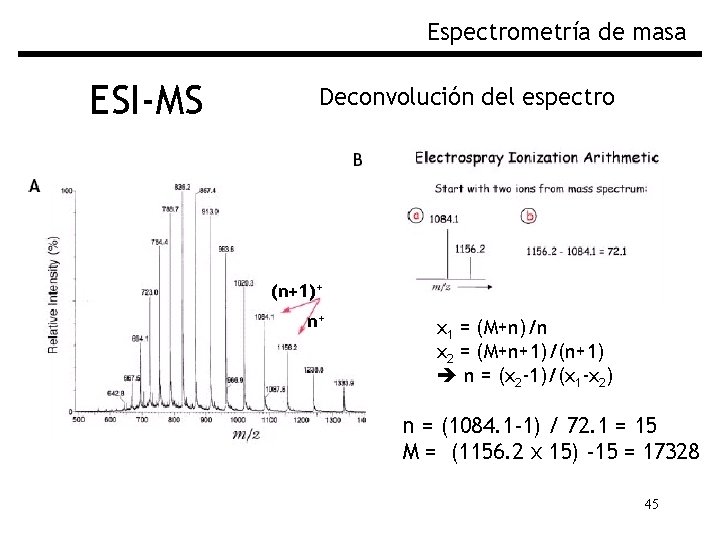
Espectrometría de masa ESI-MS Deconvolución del espectro (n+1)+ n+ x 1 = (M+n)/n x 2 = (M+n+1)/(n+1) n = (x 2 -1)/(x 1 -x 2) n = (1084. 1 -1) / 72. 1 = 15 M = (1156. 2 x 15) -15 = 17328 45
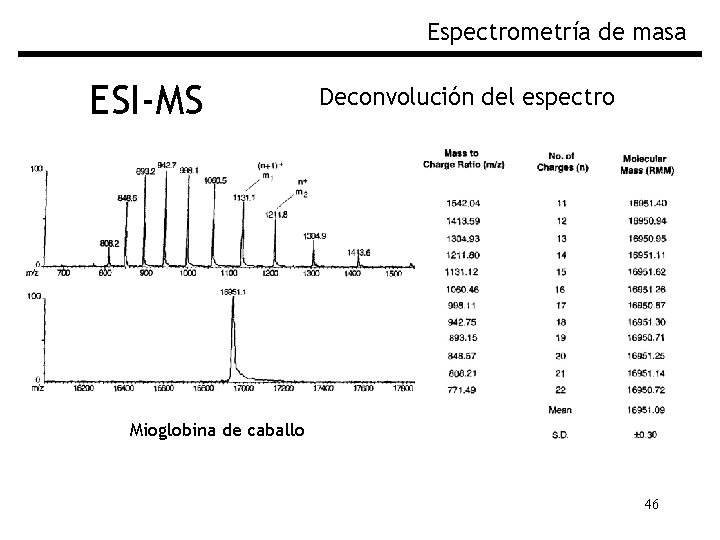
Espectrometría de masa ESI-MS Deconvolución del espectro Mioglobina de caballo 46
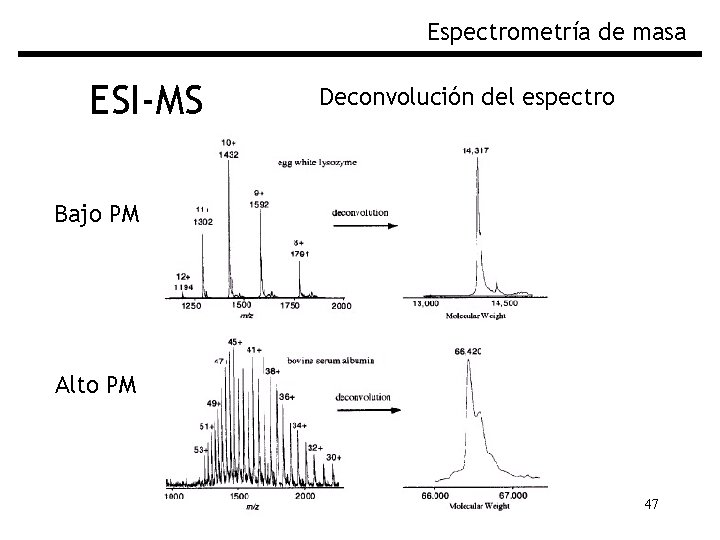
Espectrometría de masa ESI-MS Deconvolución del espectro Bajo PM Alto PM 47
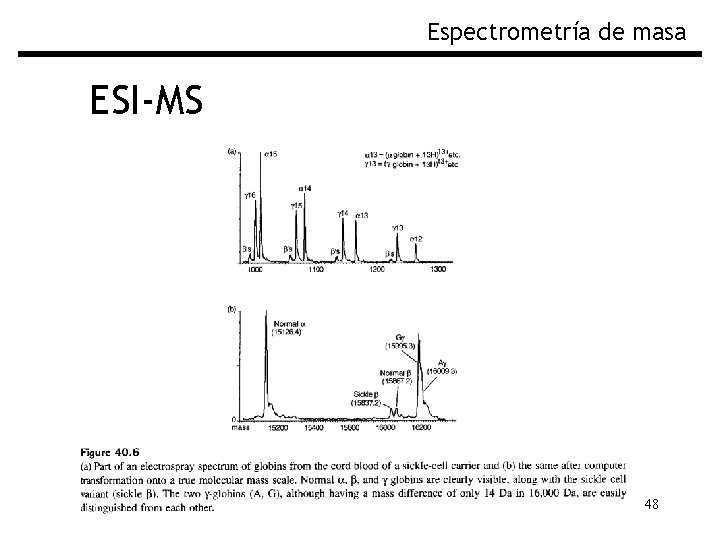
Espectrometría de masa ESI-MS 48
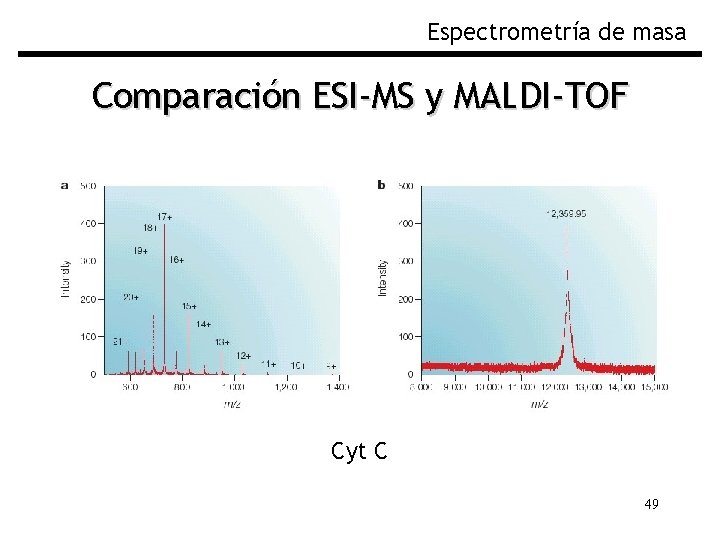
Espectrometría de masa Comparación ESI-MS y MALDI-TOF Cyt C 49
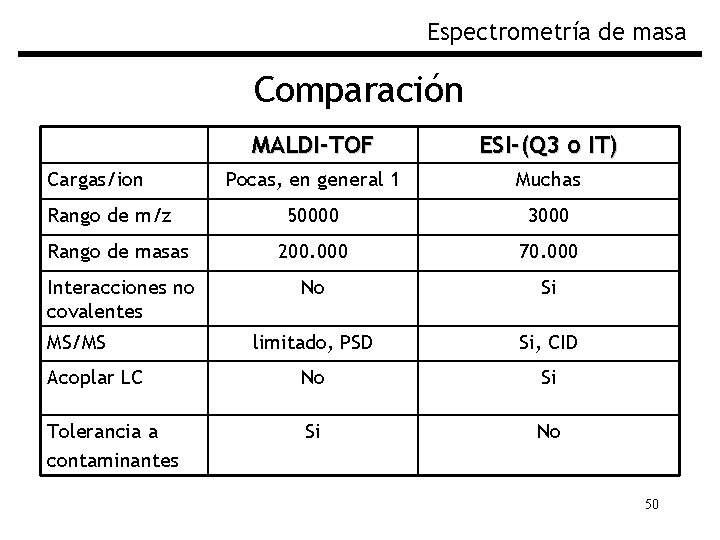
Espectrometría de masa Comparación MALDI-TOF ESI-(Q 3 o IT) Pocas, en general 1 Muchas 50000 3000 Rango de masas 200. 000 70. 000 Interacciones no covalentes No Si limitado, PSD Si, CID Acoplar LC No Si Tolerancia a contaminantes Si No Cargas/ion Rango de m/z MS/MS 50

51
- Slides: 51