FUNCIONES QUIMICA INORGANICAS NOMENCLATURA y Conceptos Bsicos FUNCIONES

FUNCIONES QUIMICA INORGANICAS

NOMENCLATURA y Conceptos Básicos
FUNCIONES QUÍMICAS base l sa Las principales funciones son: óxido, base, ácido y sal. óxido “Es un conjunto de propiedades comunes que caracterizan a un grupo de sustancias, distinguiéndolas demás”. ácido ¿Qué es una función Química?
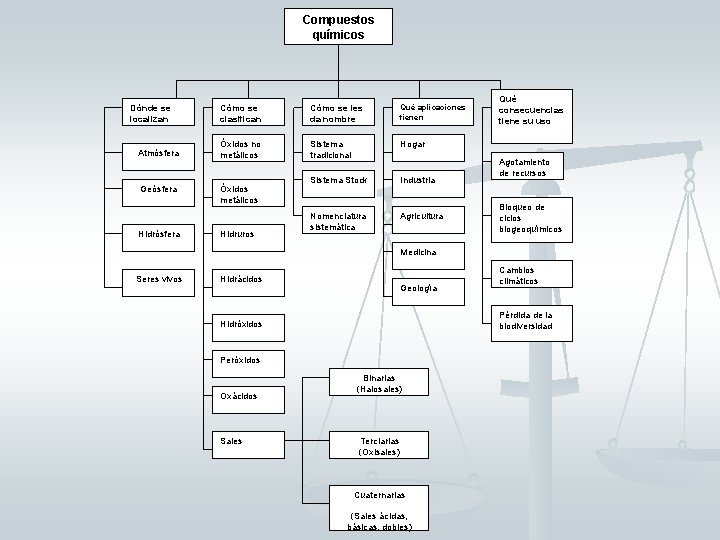
Compuestos químicos Dónde se localizan Atmósfera Geósfera Hidrósfera Cómo se clasifican Cómo se les da nombre Qué aplicaciones tienen Óxidos no metálicos Sistema tradicional Hogar Sistema Stock Industria Nomenclatura sistemática Agricultura Óxidos metálicos Hidruros Qué consecuencias tiene su uso Agotamiento de recursos Bloqueo de ciclos biogeoquímicos Medicina Seres vivos Hidrácidos Geología Pérdida de la biodiversidad Hidróxidos Peróxidos Oxácidos Sales Cambios climáticos Binarias (Halosales) Terciarias (Oxisales) Cuaternarias (Sales ácidas, básicas, dobles)
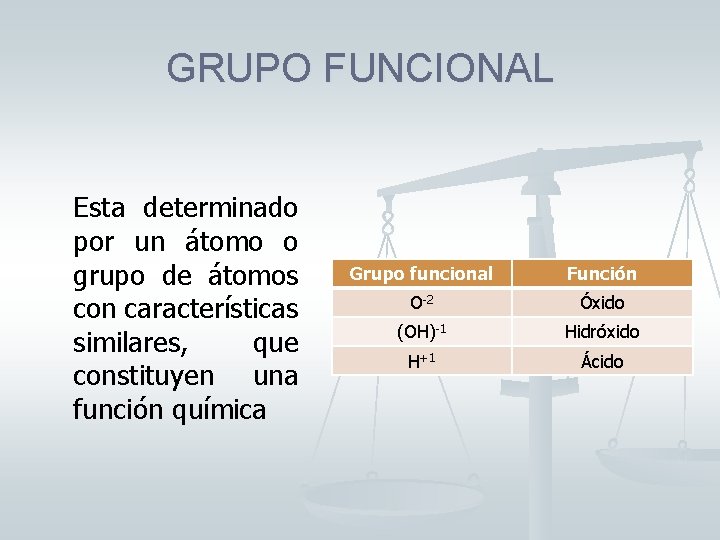
GRUPO FUNCIONAL Esta determinado por un átomo o grupo de átomos con características similares, que constituyen una función química Grupo funcional Función O-2 Óxido (OH)-1 Hidróxido H+1 Ácido
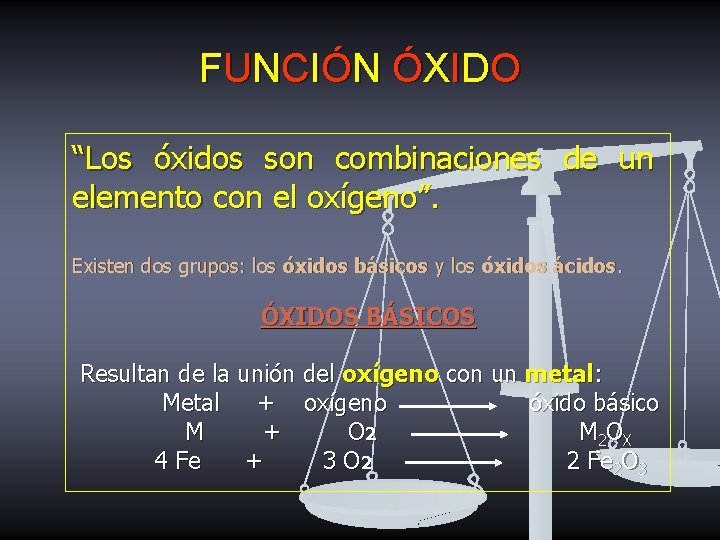
F UNCI Ó N Ó X I DO “Los óxidos son combinaciones de un elemento con el oxígeno”. Existen dos grupos: los óxidos básicos y los óxidos ácidos. ÓXIDOS BÁSICOS Resultan de la unión del oxígeno con un metal: Metal + oxígeno óxido básico M + O 2 M 2 OX 4 Fe + 3 O 2 2 Fe 2 O 3

F UNCI Ó N Ó X I DO “Los óxidos son combinaciones de un elemento con el oxígeno”. Existen dos grupos: los óxidos básicos y los óxidos ácidos. ÓXIDOS ÁCIDOS o ANHÍDRIDOS Resultan de la unión del oxígeno con un no metal: No Metal + No. M + C + oxígeno O 2 óxido ácido (No. M 2)OX C 2 O 4 CO 2

F UNCI Ó N HI DRÓ X I DO n n “Un óxido básico al combinarse con el agua forma las bases o hidróxidos”. Se caracterizan por: n n n Poner azul el papel tornasol rojo Enrojecer la fenolftaleína Son cáusticos y de sabor amargo Óxido básico M 2 OX Na 2 O + + + agua H 2 O Hidróxido M(OH)X 2 Na(OH)
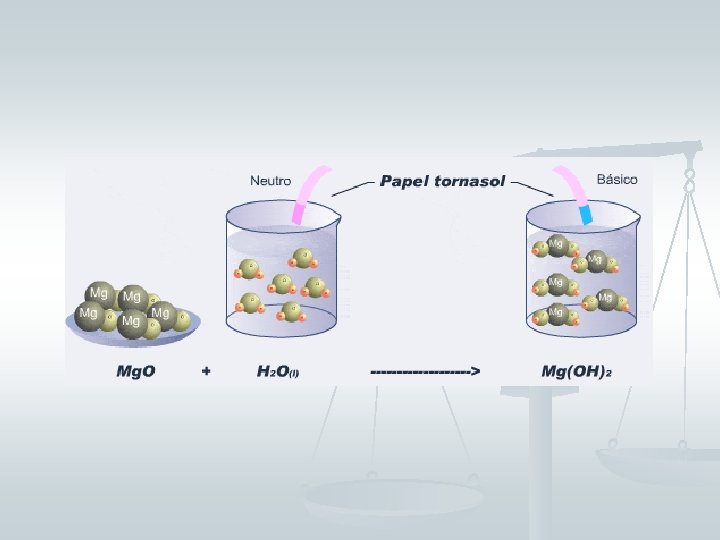

FUNCIÓN ÁCIDO n n Se caracterizan por: n Enrojecer el papel tornasol azul n La fenolftaleína permanece incolora n Presentar agrio, picante (los ácidos no se deben saborear por ser muchos de ellos tóxicos) Las sustancias ácidas pueden agruparse en dos clases: hidrácidos y oxácidos.

FUNCIÓN HIDRURO “La combinación del Hidrógeno con un metal forma los Hidruros”. En este caso el H presenta estado de oxidación : -1 Metal + 2 Na + Fe + H 2 H 2 MHX 2 Na. H Fe. H 2
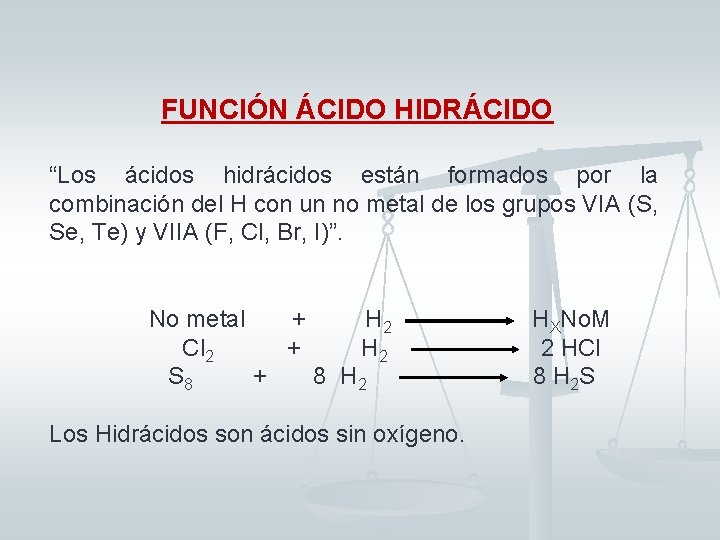
FUNCIÓN ÁCIDO HIDRÁCIDO “Los ácidos hidrácidos están formados por la combinación del H con un no metal de los grupos VIA (S, Se, Te) y VIIA (F, Cl, Br, I)”. No metal + H 2 Cl 2 + H 2 S 8 + 8 H 2 Los Hidrácidos son ácidos sin oxígeno. HXNo. M 2 HCl 8 H 2 S

FUNCIÓN ÁCIDO OXÁCIDO n “Un óxido ácido o anhídrido al reaccionar con el agua forma los ácidos oxácidos”. Óxido ácido No M 2 OX CO 2 + + + agua H 2 O Ácido oxoácido Ha(No. M)b. Oc H 2 CO 3 ácido carbónico

FUNCIÓN SAL “La combinación entre un hidróxido y un ácido (hidrácido u oxoácido) da una sal más agua”. Hidróxido + Ácido Sal + Agua n n n Se clasifican en: SALES HALOIDEAS: (No. M M) “Resultan de la combinación de un hidróxido y un ácido hidrácido (ácido sin oxígeno)”. OXISALES o SALES OXOÁCIDAS: (No. M M O) “Resultan de la combinación de un hidróxido y un ácido oxácido (ácido con oxígeno)”.
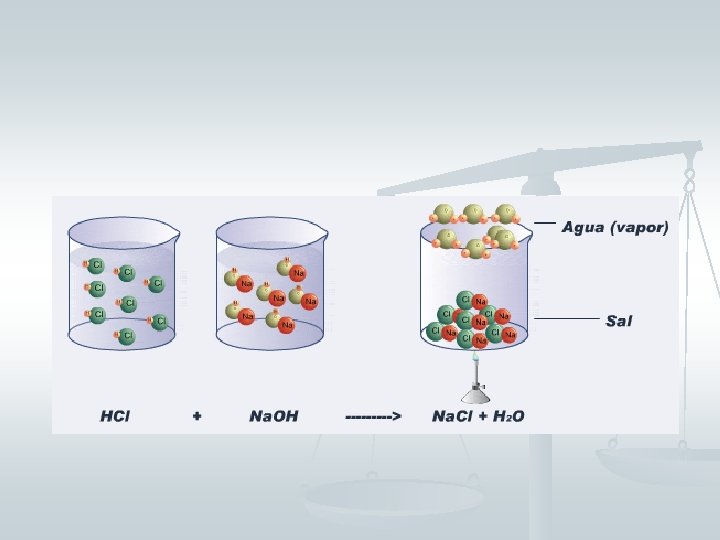
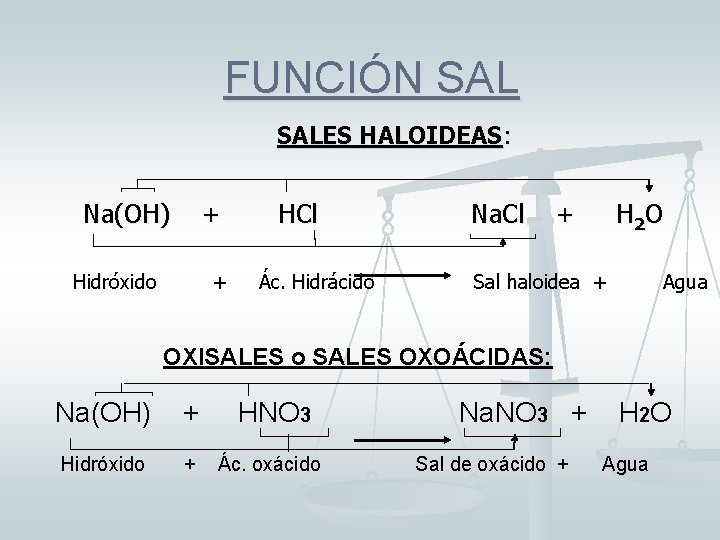
FUNCIÓN SALES HALOIDEAS: Na(OH) + Hidróxido + HCl Ác. Hidrácido Na. Cl + H 2 O Sal haloidea + Agua OXISALES o SALES OXOÁCIDAS: Na(OH) + HNO 3 Hidróxido + Ác. oxácido Na. NO 3 + Sal de oxácido + H 2 O Agua
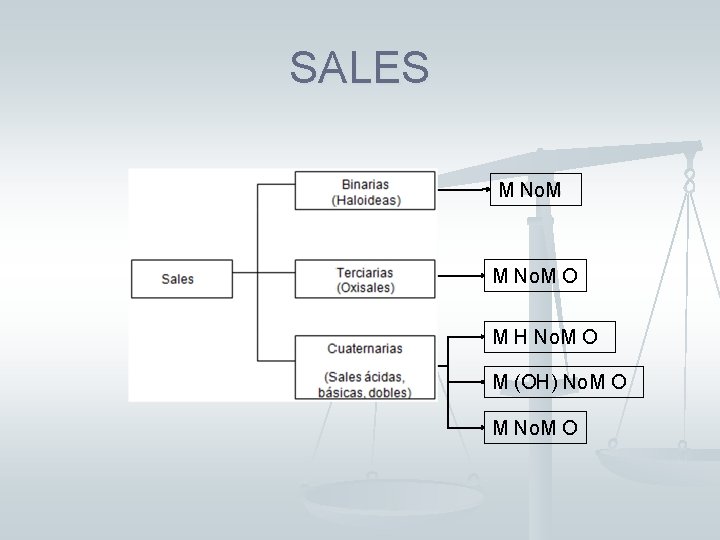
SALES M No. M O M H No. M O M (OH) No. M O M No. M O
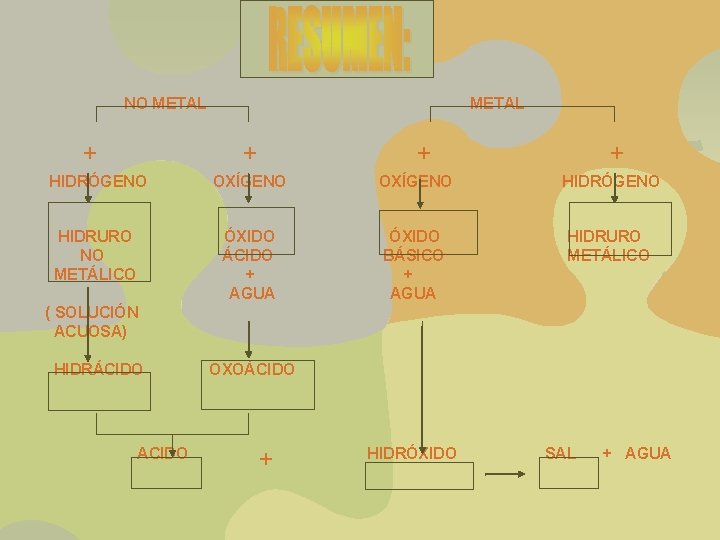
NO METAL + + + HIDRÓGENO OXÍGENO HIDRÓGENO HIDRURO NO METÁLICO ÓXIDO ÁCIDO + AGUA ÓXIDO BÁSICO + AGUA HIDRURO METÁLICO ( SOLUCIÓN ACUOSA) HIDRÁCIDO ACIDO OXOÁCIDO + HIDRÓXIDO SAL + AGUA

VALENCIA Es la capacidad que posee un elemento de combinarse con otro Como el hidrógeno se toma como referencia (valencia I), se define también como el número de átomos de hidrógenos que se puede combinar con un elemento HCl: la valencia del Cl es I H 2 S: la valencia del S es II NH 3: la valencia del N es III CH 4: la valencia del C es IV

NÚMERO DE OXIDACIÓN Es el nº de electrones que un átomo puede captar o ceder (total o parcialmente) al formar un compuesto El nº de oxidación no tiene porqué coincidir con la valenciade un elemento: CH 4: la valencia del C es IV; el nº oxidación es -4 CH 3 Cl: la valencia del C es IV; el nº oxidación es -2 CH 2 Cl 2: la valencia del C es IV; el nº oxidación es 0 CCl 4: la valencia del C es IV; el nº oxidación es +4

LAS REGLAS DE ASIGNACIÓN DEL NÚMERO DE OXIDACIÓN SON: 1. El n. o. de todos los elementos libres es cero, en cualquiera de las formas en que se presenten: Ca metálico, He, N 2 , P 4 , etc. 2. El n. o. de un ión simple coincide con su carga: Así, los n. o. del S 2–, Cl– y Zn 2+ son, respectivamente, – 2, – 1, +2 3. El n. o. del H en sus compuestos es +1, excepto en los hidruros metálicos, que es – 1, H 2 S, Ca. H 2 4. El n. o. del O en sus compuestos es – 2, excepto en los peróxidos, que es – 1, K 2 O, H 2 O 2 5. El n. o. más probable para los elementos de los grupos I, II y III A esta dado por el número del grupo, Mg. O, Li 2 O 6. El n. o. más probable para los elementos de los grupos V, VI y VII A se encuentra restándole a 8 el número del grupo, SO 3, CO 2, Cu. Br 2 7. La suma algebraica de los n. o. de los átomos de una molécula es cero, y si se trata de un ión, igual a la carga del ión

CUADRO DE N. O. DE LOS ELEMENTOS MÁS FRECUENTES: No metales: Elemento Nº de oxidación H -1; +1 F Cl, Br, I -1 -1; +1, +3, +5, +7 O S, Se, Te -2 -2; +2, +4, +6 N P As, Sb, Bi -3; +1, +2, +3, +4, +5 -3; +1, +3, +5 -3; +3, +5 B -3; +3 C Si -4; +2, +4 -4; +4
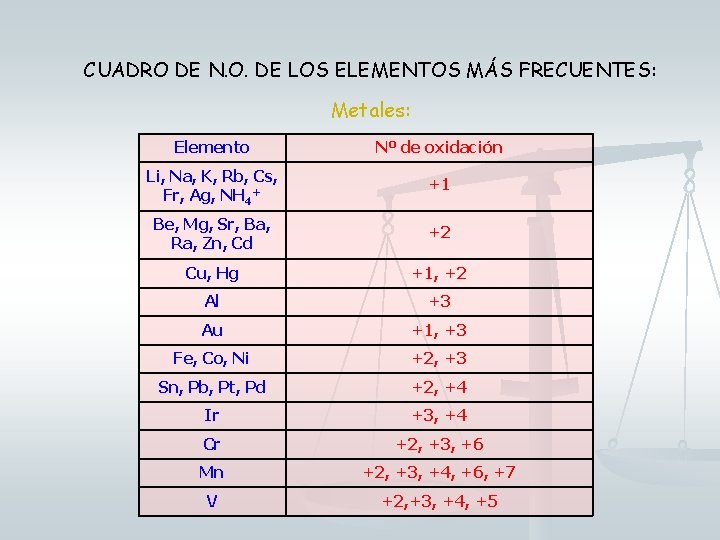
CUADRO DE N. O. DE LOS ELEMENTOS MÁS FRECUENTES: Metales: Elemento Nº de oxidación Li, Na, K, Rb, Cs, Fr, Ag, NH 4+ +1 Be, Mg, Sr, Ba, Ra, Zn, Cd +2 Cu, Hg +1, +2 Al +3 Au +1, +3 Fe, Co, Ni +2, +3 Sn, Pb, Pt, Pd +2, +4 Ir +3, +4 Cr +2, +3, +6 Mn +2, +3, +4, +6, +7 V +2, +3, +4, +5
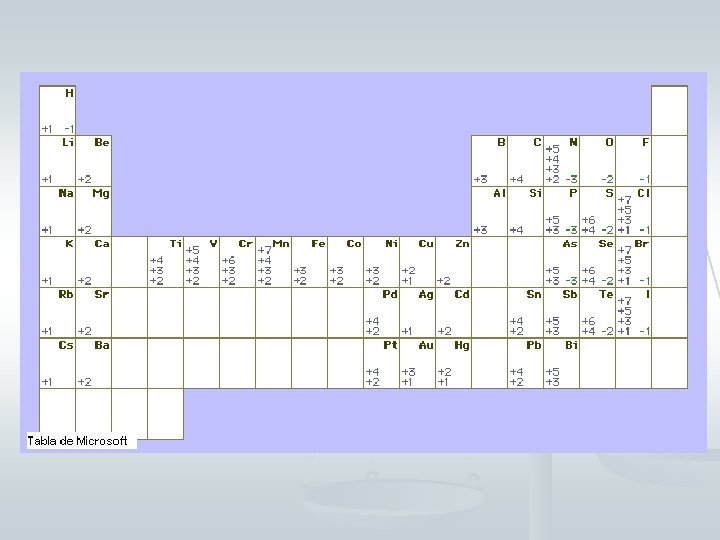

FORMULACIÓN: n ÁCIDOS OXOÁCIDOS: n Son aquellos que están formados por el hidrógeno, un no metal y oxígeno. MÉTODO MECÁNICO: Se escriben los elementos en el siguiente orden: 1º) HIDROGENO; 2º) NO METAL; 3º) OXÍGENO HCO HSO HNO H Cl O
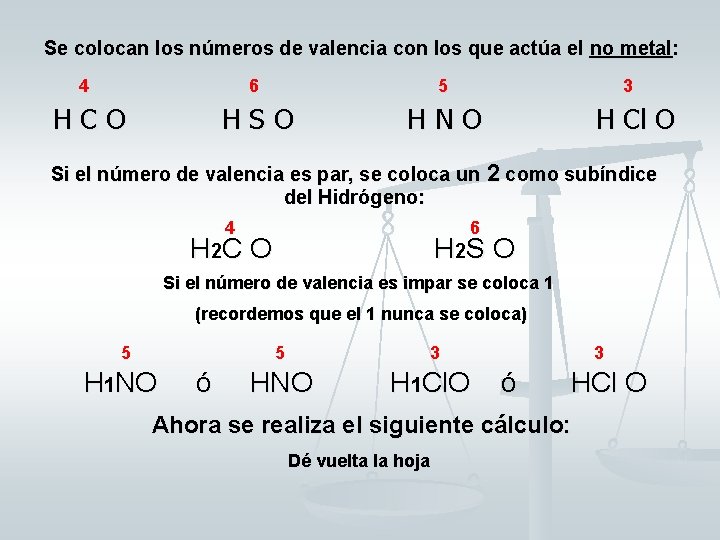
Se colocan los números de valencia con los que actúa el no metal: 4 6 5 3 HCO HSO HNO H Cl O Si el número de valencia es par, se coloca un 2 como subíndice del Hidrógeno: 4 6 H 2 C O H 2 S O Si el número de valencia es impar se coloca 1 (recordemos que el 1 nunca se coloca) 5 H 1 NO ó 5 3 HNO H 1 Cl. O 3 ó HCl O Ahora se realiza el siguiente cálculo: Dé vuelta la hoja
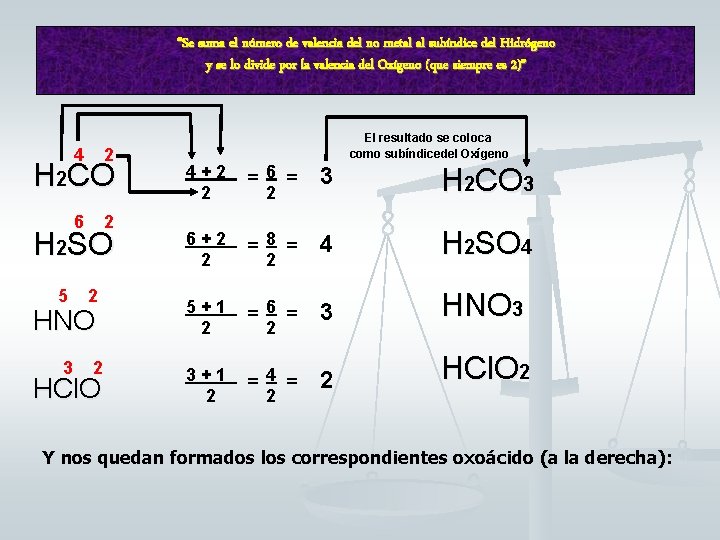
“Se suma el número de valencia del no metal al subíndice del Hidrógeno y se lo divide por la valencia del Oxígeno (que siempre es 2)” 4 2 H 2 CO El resultado se coloca como subíndicedel Oxígeno 4+2 2 =6 = 3 H 2 CO 3 6+2 2 =8 = 4 H 2 SO 4 HNO 5+1 2 =6 = 3 HNO 3 3 3+1 2 =4 = 2 HCl. O 2 6 2 H 2 SO 5 2 2 HCl. O 2 2 Y nos quedan formados los correspondientes oxoácido (a la derecha):

H 2 CO 3 H 2 SO 4 HNO 3 HCl. O 2 ECUACIONES DE FORMACIÓN: Óxido Ácido + Agua Ácido Óxoácido Para formarlos se escriben los elementos en el orden dados en el punto anterior. Ejemplo: CO 2 + H 2 O HCO A continuación se coloca a cada elemento un subíndice que es igual al número total de átomos del elemento que se encuentra del lado izquierdo (reactivos): CO 2 + H 2 O Y nos queda formado el compuesto (recordemos que el 1 no se coloca): H 2 C 1 O 3 H 2 CO 3

Para continuar Pero hay que estudiar
- Slides: 29