FSICA I GRADO Ingeniera Mecnica M 2 Prof














- Slides: 25

FÍSICA I GRADO Ingeniería Mecánica (M 2) Prof. Norge Cruz Hernández Examen parcial (M 2): 12 -12 -2019 Aula: 2. 4 19: 30 CINEMÁTICA DE LA PARTÍCULA. DINÁMICA DE LOS SISTEMAS DE PARTÍCULAS. SÓLIDO RÍGIDO.

FÍSICA I GRADO Ingeniería Mecánica Tema 7. Termodinámica: Primer principio Prof. Norge Cruz Hernández

Tema 7. Termodinámica: Primer principio (3 h) 7. 1 Introducción 7. 1 Conceptos básicos. Sistemas, estados y transformaciones termodinámicas. 7. 2 Equilibrio térmico y temperatura. Principio cero. 7. 3 Termometría: propiedades termométricas. Escalas de temperatura. 7. 4 Concepto de calor. Capacidades caloríficas y calores latentes. 7. 5 Gas ideal 7. 6 Trabajo termodinámico. Trabajo en procesos cuasiestáticos. 7. 7 Primer principio de la termodinámica. Energía interna.

Bibliografía Clases de teoría: - Física Universitaria, Sears, Zemansky, Young, Freedman ISBN: 970 -26 -0511 -3, Ed. 9 y 11. Clases de problemas: -Problemas de Física General, I. E. Irodov -Problemas de Física General, V. Volkenshtein - Problemas de Física, S. Kósel -Problemas seleccionados de la Física Elemental, B. B. Bújovtsev, V. D. Krívchenkov, G. Ya. Miákishev, I. M. Saráeva. Libros de consulta: -Problemas de Física, Burbano, Gracia. - Resolución de problemas de física, V. M. Kirílov.

Termodinámica: Es la rama de la ciencia que se dedica al estudio de las transformaciones de energía en las que intervienen: el calor, el trabajo mecánico y otros aspectos de la energía, así como la relación entre estas transformaciones y las propiedades de la materia. La Termodinámica: No hace hipótesis sobre la estructura interna de la materia. Toma en consideración sólo magnitudes medibles y definidas a una escala macroscópica. Deriva sus leyes de la experiencia, no de primeros principios. Estas leyes se expresan en forma de ecuaciones matemáticas.

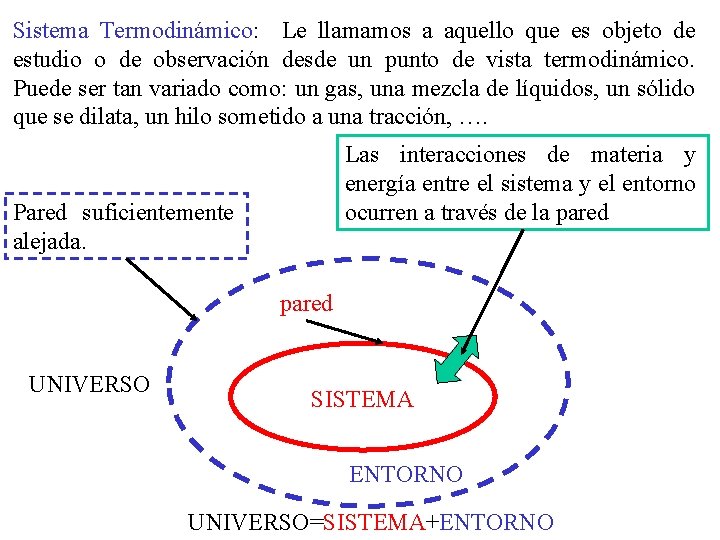
Sistema Termodinámico: Le llamamos a aquello que es objeto de estudio o de observación desde un punto de vista termodinámico. Puede ser tan variado como: un gas, una mezcla de líquidos, un sólido que se dilata, un hilo sometido a una tracción, …. Las interacciones de materia y energía entre el sistema y el entorno ocurren a través de la pared Pared suficientemente alejada. pared UNIVERSO SISTEMA ENTORNO UNIVERSO=SISTEMA+ENTORNO

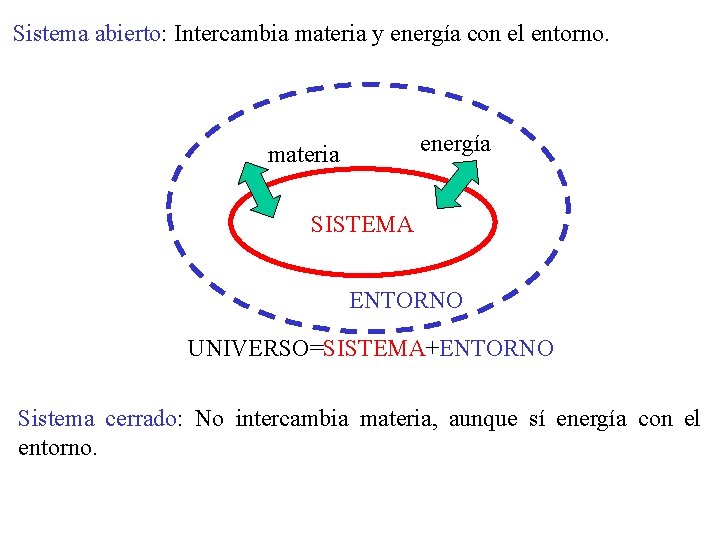
Sistema abierto: Intercambia materia y energía con el entorno. energía materia SISTEMA ENTORNO UNIVERSO=SISTEMA+ENTORNO Sistema cerrado: No intercambia materia, aunque sí energía con el entorno.

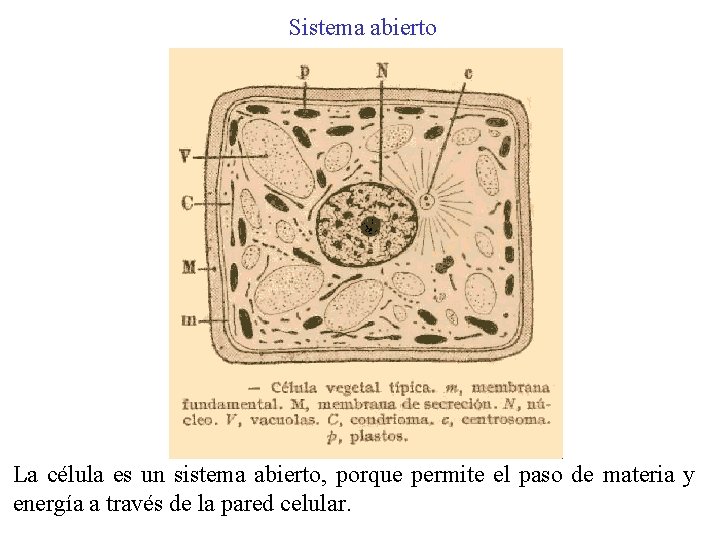
Sistema abierto La célula es un sistema abierto, porque permite el paso de materia y energía a través de la pared celular.

Sistema cerrado Las cápsulas espaciales no intercambian materia con el espacio exterior, pero sí intercambian energía. A través de sus paneles solares, transforman la energía del sol en energía eléctrica.

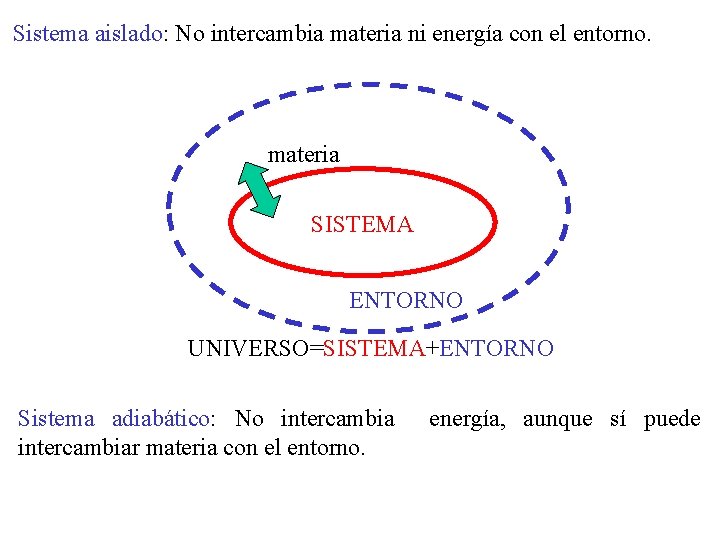
Sistema aislado: No intercambia materia ni energía con el entorno. materia SISTEMA ENTORNO UNIVERSO=SISTEMA+ENTORNO Sistema adiabático: No intercambiar materia con el entorno. energía, aunque sí puede

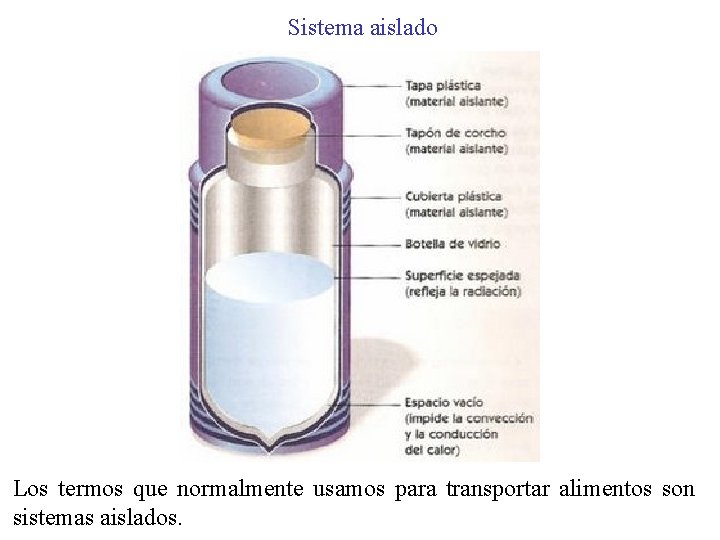
Sistema aislado Los termos que normalmente usamos para transportar alimentos son sistemas aislados.

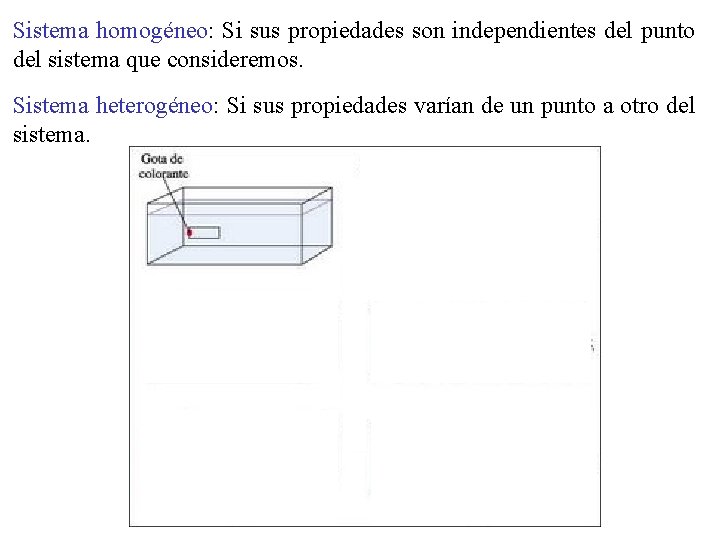
Sistema homogéneo: Si sus propiedades son independientes del punto del sistema que consideremos. Sistema heterogéneo: Si sus propiedades varían de un punto a otro del sistema.

Variables de estado: Se le llama a una serie de magnitudes macroscópicas que determinan al sistema, por ejemplo: P, V, T, la densidad, la energía del sistema, …. Grado de libertad del sistema: Se le llama al número máximo de variables de estado independientes que describen un sistema. Equilibrio termodinámico: Se le llama al estado del sistema donde las variables termodinámicas se mantienen constantes en el tiempo, sin sufrir ninguna variación espontánea. Equilibrio químico: Es aquel en el que las concentraciones de reaccionantes y productos se mantienen constantes en el tiempo. Equilibrio mecánico: Se alcanza cuando tanto en el interior de un sistema, como entre él y el medio que lo rodea, no se ejercen fuerzas netas. Equilibrio térmico: …….

Ecuaciones de Estado Variables de estado: Se le llama a una serie de magnitudes macroscópicas que determinan al sistema, por ejemplo: P, V, T, la densidad, la energía del sistema, …. Normalmente, no podemos variar una de estas variables sin alterar la otra, es decir, no son independientes totalmente. Ecuación de estado: Se le llama a la relación que existe entre las variables que definen un estado. caso simple caso complicado

Cambios diferenciales de Estado Suponemos conocida la ecuación de estado de un determinado sistema, de forma que podemos expresar: Un cambio infinitesimal del volumen lo podemos expresar como: De forma general, debemos tener en cuenta que:

Estas derivadas parciales tienen un significado físico muy importante: Coeficiente de dilatación cúbica: La experiencia demuestra que es prácticamente independiente de P y que varía ligeramente con T. Así, dentro de un pequeño intervalo de temperatura puede tomarse como constante: Coeficiente de compresibilidad cúbica: Es una función prácticamente independiente de P y T.

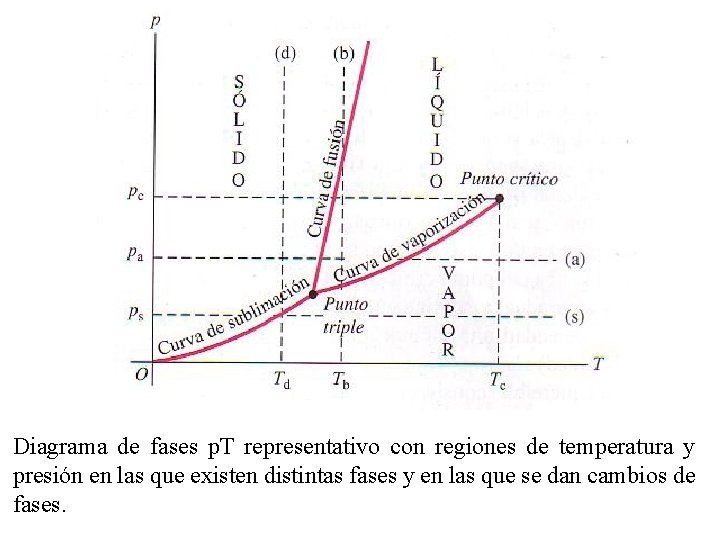
Diagrama de fases p. T representativo con regiones de temperatura y presión en las que existen distintas fases y en las que se dan cambios de fases.

Sistema Termodinámico en Equilibrio (Termodinámica Clásica) La termodinámica clásica considera procesos, es decir, cambios de un sistema desde el estado inicial a un estado final. La termodinámica clásica supone que este proceso transcurre tan lentamente que el sistema tiene tiempo de alcanzar el equilibrio después de un cambio infinitesimal, de tal forma que todos los estados intermedios son estados de equilibrio con sus coordenadas termodinámicas bien definidas. A este proceso se le llama : cuasiestático.

Temperatura: Nos transmite una idea de “frio” o “calor” según nuestra orientación del tacto. La temperatura puede estar relacionada con propiedades como: Energía cinética de las moléculas de un material. Longitud de una barra de metal. La presión de vapor de una caldera. La capacidad de un alambre para conducir corriente eléctrica. El color de un objeto brillante muy caliente.

Sistema cuya temperatura se especifica con el valor de la longitud L. termómetros Sistema cuya temperatura está dada por el valor de la presión p.

Si queremos medir la temperatura de nuestro café del desayuno introducimos el termómetro en nuestra taza de café. Al interactuar entre los dos, el termómetro se calienta y el café se enfría un poco. El líquido del termómetro comienza a subir hasta que se estabiliza y entonces podemos leer la temperatura. El estado en el cual el termómetro no cambia de medida le llamamos estado de equilibrio térmico. Aislante “ideal”: Se le llama al material que no permite la interacción entre dos sistemas, es decir, evitan que se alcance el equilibrio térmico entre dos sistemas.

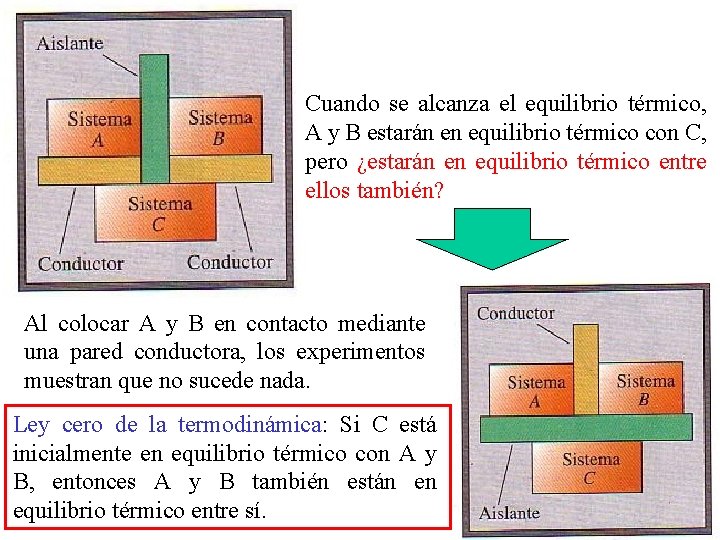
Cuando se alcanza el equilibrio térmico, A y B estarán en equilibrio térmico con C, pero ¿estarán en equilibrio térmico entre ellos también? Al colocar A y B en contacto mediante una pared conductora, los experimentos muestran que no sucede nada. Ley cero de la termodinámica: Si C está inicialmente en equilibrio térmico con A y B, entonces A y B también están en equilibrio térmico entre sí.

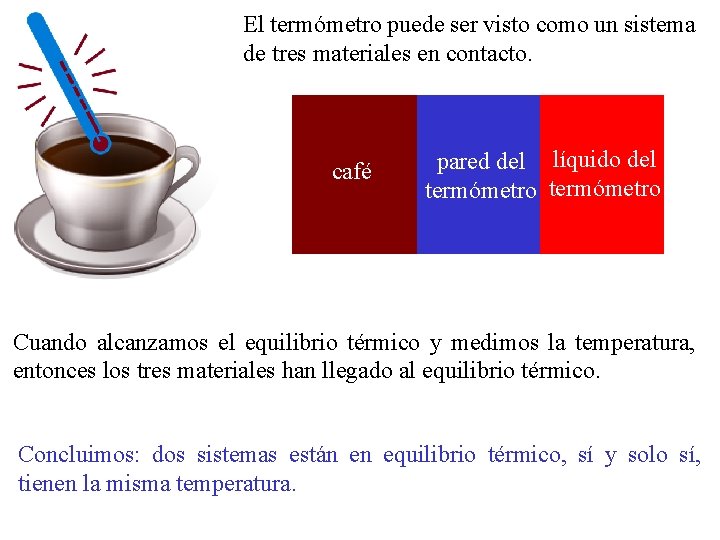
El termómetro puede ser visto como un sistema de tres materiales en contacto. café pared del líquido del termómetro Cuando alcanzamos el equilibrio térmico y medimos la temperatura, entonces los tres materiales han llegado al equilibrio térmico. Concluimos: dos sistemas están en equilibrio térmico, sí y solo sí, tienen la misma temperatura.

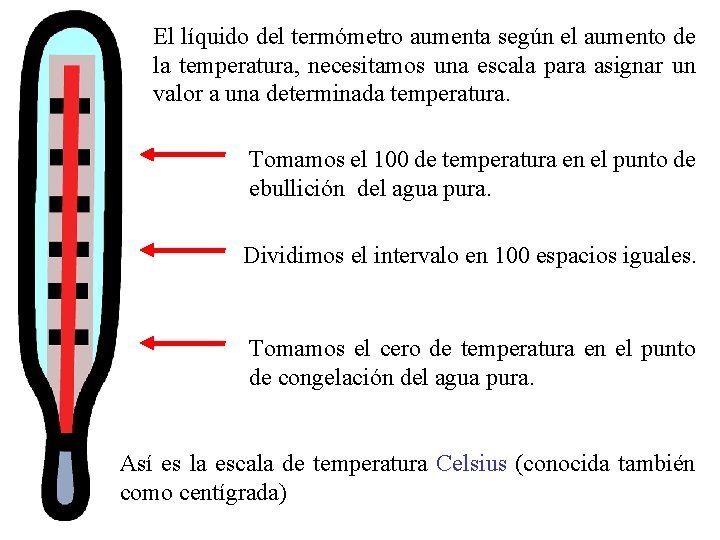
El líquido del termómetro aumenta según el aumento de la temperatura, necesitamos una escala para asignar un valor a una determinada temperatura. Tomamos el 100 de temperatura en el punto de ebullición del agua pura. Dividimos el intervalo en 100 espacios iguales. Tomamos el cero de temperatura en el punto de congelación del agua pura. Así es la escala de temperatura Celsius (conocida también como centígrada)

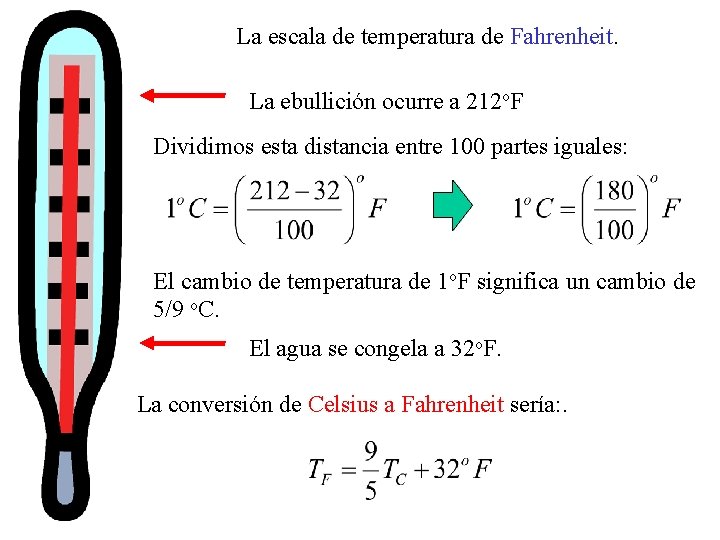
La escala de temperatura de Fahrenheit. La ebullición ocurre a 212 o. F Dividimos esta distancia entre 100 partes iguales: El cambio de temperatura de 1 o. F significa un cambio de 5/9 o. C. El agua se congela a 32 o. F. La conversión de Celsius a Fahrenheit sería: .